10.1.3 Médico: pacientes neonatales y pediátricos con enfermedad de células falciformes (SCD) – efecto de la transfusión de GR sobre los desenlaces de los pacientes
Antecedentes
La enfermedad de células falciformes (SCD por sus siglas en inglés) es causada por la herencia homocigótica del alelo de HbS o la herencia heterocigótica compuesta de ese alelo con otra anormalidad del gen de la globina beta, tal como HbC o ß talasemia.
Las manifestaciones clínicas importantes de la SCD en pacientes pediátricos incluyen secuestro esplénico, hemólisis, crisis aplásticas, priapismo, infección, infarto y episodios recurrentes dolorosos vaso-oclusivos como la dactilitis y el síndrome torácico agudo.
La mayoría de los niños con SCD en los países desarrollados sobrevivirán hasta la edad adulta; sin embargo, la esperanza de vida puede ser reducida.
Las transfusiones de GR son una importante estrategia de tratamiento en el manejo de las complicaciones agudas de la SCD y en la prevención de complicaciones de larga duración como el infarto. Durante la infancia, por lo menos el 20% de los niños con SCD tendrán lesiones isquémicas silenciosas que son visibles en la resonancia magnética (RM), y estas lesiones se asocian con una mayor incidencia de infarto clínico (36-37).
La transfusión regular de glóbulos rojos suele conducir a una sobrecarga de hierro, que suele tratarse con quelación de hierro. Los pacientes con SCD también están en riesgo significativo de reacciones de transfusión hemolítica y aloinmunización de GR.
Los altos índices de aloinmunización se observan en los pacientes con SCD que reciben transfusiones crónicas. Debido a las altas tasas de transfusión en estos pacientes, y las diferencias antigénicas entre los donantes y poblaciones receptoras.
Transfusión de GR versus no transfusión (o diferente dosis de GR) en pacientes pediátricos con SCD
Dos revisiones sistemáticas de buena calidad examinaron el efecto de la transfusión de GR en pacientes pediátricos con SCD (38-39).
Estas revisiones incluyeron dos estudios de buena calidad nivel II: el ensayo de prevención del infarto en la anemia falciforme (STOP) (34), con edades comprendidas entre 2 y 16 años) con alto riesgo de sufrir un infarto basándose en la detección con Doppler transcraneal (DTC) ya sea a transfusión de GR o tratamiento estándar (sin transfusión); y el ensayo STOP 2 (40), que asignó al azar a los niños (de edades comprendidas entre los 2 y los 16 años) un alto riesgo de infarto a las transfusiones continuas de GR o a la cesación de la terapia transfusional después de 30 meses de transfusiones (grupo de detención de las transfusiones).
En la revisión de la literatura se identificaron dos estudios adicionales nivel II de calidad moderada a baja (41).
El ensayo SIT (Silent Cerebral InfaECA Multi-Center Clinical Trial) comparó el efecto de las transfusiones de GR con la no transfusión sobre el infarto cerebral entre pacientes pediátricos (5-15 años) con SCD y al menos una lesión similar a un infarto detectada por resonancia magnética. El segundo ensayo informó la incidencia de infarto y los datos de infarto silencioso de la cohorte STOP a los 36 meses (41).
Mortalidad
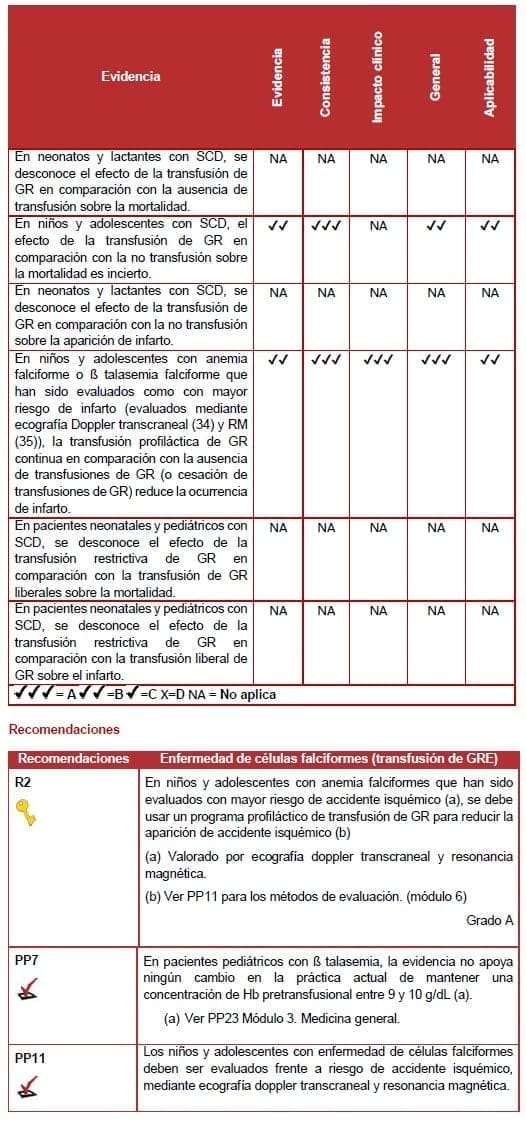
Tres estudios nivel II informaron mortalidad y no encontraron diferencias significativas entre los grupos de tratamiento (33-34, 40). Sin embargo, los estudios fueron insuficientes para este resultado.
(Lea También: Pacientes Neonatales y Pediátricos con ß Talasemia)
Infarto
Dos revisiones sistemáticas (38-39) y los dos ECA (35, 41) examinaron el efecto de las transfusiones de GR sobre la incidencia de infarto. No se realizó un meta análisis para la incidencia de infarto debido a las diferencias en las poblaciones de pacientes y el diseño del estudio.
El ensayo STOP demostró un riesgo significativamente reducido de infarto en niños con SCD y velocidades anormales de DTC que iniciaron transfusiones sanguíneas regulares en comparación con aquellos que no recibieron transfusión (34).
El ensayo STOP 2 se cerró temprano debido a las preocupaciones sobre el aumento del riesgo de infarto en el grupo que suspendió la transfusión (40). Se reportaron más infartos en el grupo que suspendió la transfusión, aunque esto no alcanzó significación estadística. Sin embargo, en el grupo que suspendió la transfusión, el número de pacientes que revierten a velocidades anormales de DTC aumentó. Lo que implica un mayor riesgo de infarto.
El estudio de seguimiento de 36 meses de la cohorte STOP original encontró que la terapia de transfusión a largo plazo continuaba reduciendo el riesgo de infarto (41).
En los niños con SCD e infartos silenciosos conocidos en el ensayo SIT, la transfusión regular de GR comparada con el cuidado estándar (sin transfusión) redujo la tasa de eventos neurológicos. Incluyendo el infarto cerebral y los ataques isquémicos transitorios.
Efectos adversos graves relacionados con la transfusión
Un estudio nivel I (38) y el ensayo de SIT (35) informaron la incidencia de eventos adversos graves relacionados con la transfusión, incluyendo la aloinmunización de GR y las reacciones transfusionales. Como era de esperar, las reacciones adversas graves a la transfusión. Incluyendo la aloinmunización, y las reacciones de transfusión febril y no febril fueron mucho mayores en los grupos expuestos a más transfusiones.
Medidas funcionales o de rendimiento
Ningún estudio informó medidas funcionales o de rendimiento.
Comentario clínico – efecto de la transfusión de GR en pacientes pediátricos con SCD
Los niños y adolescentes con SCD con alto riesgo de infarto deben comenzar un programa de transfusión crónica a largo plazo para reducir su riesgo de aparición de un infarto (ver R2). Esta recomendación está de acuerdo con las recientes directrices del National Institutes of Health (National Institutes of Health, NIH) sobre el manejo de la SCD (42). Las cuales recomiendan que los niños con talasemia HbSS o HbS/B0 y DTC elevada sean referidos para terapia de transfusión crónica.
Los pacientes pediátricos con SCD deben ser evaluados para su riesgo de infarto por DTC y RM (ver PP11).
La RM se incluye debido al alto número de niños con evidencia de isquemia cerebral silenciosa sin síntomas clínicos incluidos en el ensayo SIT. Ese ensayo examinó 1074 participantes elegibles (de 5 a 15 años) con RM, y encontró que 379 niños y adolescentes (35%) tenían evidencia de infarto silencioso sin síntomas clínicos.
Las pautas actuales de los NIH no recomiendan el tamizaje de pacientes con genotipos HbS/B + talasemia o HbSC, o tamización de niños asintomáticos con RM. Sin embargo, las pautas de los NIH se basaron en una revisión de la literatura hasta julio de 2014, que no captó la publicación de ensayos SIT (35).
El ensayo fase III del DTC con transfusiones que cambian a hidroxiurea (TWiTCH). (43)
Es un ensayo de no inferioridad que compara la transfusión de GR con hidroxiurea en pacientes pediátricos con SCD. El ensayo se detuvo tempranamente, porque se descubrió que la hidroxiurea era tan eficaz como las transfusiones para reducir la velocidad media de DTC del flujo sanguíneo. Los datos completos. Tncluyendo el resultado secundario del infarto primario, aún no están disponibles.
En vista del aumento de la aloinmunización de GR en pacientes con SCD que se someten a una transfusión a largo plazo, los pacientes deben tener un fenotipo GR extendido antes de su primera transfusión.