Una Nueva Herramienta para el Urólogo
Dr. Juan Carlos Castaño Botero.
Urólogo Hospital Pablo Tobón Uribe.
Medellín – Colombia
Resumen
En la actualidad son 7 tipos de toxina los que se han logrado aislar del Clostridium Botulinum, de ellos la A y B tienen aplicaciones clínicas vigentes, su mecanismo de acción básico es el bloqueo de la exocitosis de los neurotransmisores.
El caso de la acetilcolina cuando se buscan efectos motores y las ultimas teorías hablan del bloqueo de la exocitosis de la sustancia P, glutamato y péptido relacionado con el gen de la calcitonina cuando se buscan efectos analgésicos.
En Urología desde 1988 se viene empleando para el manejo de la disinergia detrusor esfinteriana, mas recientemente en la hiperactividad del detrusor y nuevas indicaciones se viene explorando en el tratamiento de otras patologías del piso pélvico, próstata y síndromes dolorosos del tracto urinario.
Año tras año la literatura acumula mas datos clínicos relacionados con la efectividad de su aplicación convirtiéndose en una nueva opción terapéutica en aquellos casos refractarios a los tratamientos tradicionales o en los que la pobre adherencia a los mismos es la causa del fracaso.
Introducción
La intoxicación botulínica con alimentos contaminados acompaña al hombre probablemente desde sus inicios históricos, sin embargo son escasos los datos que se poseen acerca de intoxicaciones alimentarías antes del siglo XIX.
A finales del siglo XVIII a raíz de una serie de intoxicaciones en la población de Würrttenberg al Sudeste de Alemania, la investigación relacionada con el botulismo es iniciada. Justinus Kerner (1786-1862) describió con detalle los síntomas de la intoxicación por la “salsa venenosa”, y fue el primero en proponer una aplicación terapéutica a este “veneno”, 80 años después Pierre Van Ermengen un biólogo alemán logra aislar el Clostridium Botulinum, germen productor de la toxina después de analizar un caso de intoxicación masivo1 .
Estructura Molecular de la Toxina Botulínica
El Clostridium Botulinum produce siete neurotoxinas antigénicamente distintas, denominadas desde la A, B, C, D, E, F y G, todas comparten secuencias en sus cadenas y tienen funciones similares.
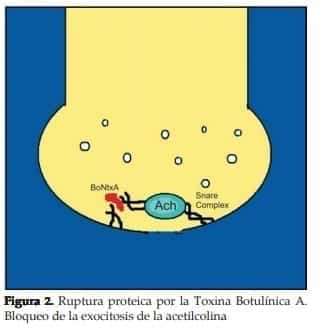
Las neurotoxinas botulínicas están formadas por dos cadenas, una cadena pesada -C Terminal (100 kDa), y una cadena ligera –N Terminal (50 kDa)2 , ambas cadenas tienen funciones diferentes, la cadena pesada es fundamental en el proceso de unión de la toxina a los re ceptores de membrana en la terminación nerviosa, y la cadena ligera ejerce su acción a nivel de las proteínas encargadas del proceso de fusión entre las vesículas que contienen los neurotransmisores y la membrana celular necesarias para la exocitosis que llevará a la transmisión del impulso nervioso, siendo así el bloqueo de la exocitosis el mecanismo de acción principal de la toxina botulínica3,4.
Mecanismos de Acción de la Toxina Butolínica
Son cuatro pasos los que se requieren para la neuromodulación producida por la toxina botulínica:
- Unión de la cadena pesada de la toxina al receptor de membrana en la terminación nerviosa
- Endocitosis mediada por receptor
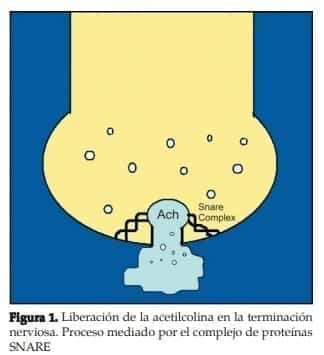
- Separación de las cadenas ligera y pesada, translocación de la cadena ligera y clivaje de las proteínas responsables de la liberación de las vesículas que contienen los neurotransmisores hacia la unión neuromuscular (ver figuras 1 y 2).
- Retorno de la función neural basal tras el brote axonal y la formación de nuevas sinapsis que finalmente hacen regresión para permitir la función de la terminación nerviosa inicial.
Todas las proteínas sobre las que ejercen su acción las diferentes toxinas hacen parte de un complejo denominado SNARE (Nethylmaleimide–sensitive factor attachment protein receptor), y cada uno de las toxinas ejerce su acción en una u otra de ellas4 .

 |
 |
Presentaciones Farmacológicas de la Toxina Botulínica
Cuatro tipos de toxina botulínica se encuentran disponible en el mercado actualmente, Botox, toxina botulínica A, producida por Allergan, que se presenta en viales de 100 MU. Dysport, toxina botulínica A, producida por Ipsen presentada en viales de 500 MU Neurobloc/Myobloc, toxina botulínica B, producido por laboratorios Elan Pharma, sus viales tienen presentaciones de 2.500 – 10.000 MU. La mas recientemente aprobada (en 2005) Xeomin, sus viales contienen100 MU de toxina botulínica A
El serotipo mas importante, el A, fue el primero aislado y purificado, en 1920 por Hermann Sommer en la universidad de California5 . Su uso clínico fue introducido por el oftalmólogo Alan Scott para el tratamiento del estrabismo6 . En 1989 fue aprobado por la FDA para el tratamiento del blefaoespasmo, estrabismo y distonía hemifacial7 . Actualmente las indicaciones urológicas de la toxina botulínica no están aprobadas por la FDA y los estudios dirigidos a esto se encuentran en fase II y III.
Las técnicas de producción y purificación de cada una de las presentaciones comerciales son diferentes entre si, y esto hace que sus dosis sean diferentes, de igual manera su potencial de difusión tisular varia entre una y otra.
Aplicaciones Urológicas de la Toxina Botulínica
Las principales indicaciones de inyección de toxina botulínica en la especialidad de la urología es la hiperactividad del detrusor tanto de origen neurogénico como idiopático, sin embargo son mas los usos que podemos dar a esta toxina, de hecho las primeras experien cias obtenidas fueron las que se realizaron a nivel del esfínter uretral.
A continuación haré mención de cada una de estas indicaciones y las principales publicaciones que soportan su uso.
(Lea También: Tratamiento de la Disfunción del Tracto Urinario Inferior)
Disinergia Detrusor-Esfinter
Desde 1988 se ha venido estudiando la aplicación de toxina botulínica en el tratamiento de la disinergia detrusor esfínter8,9. En pacientes con daño medular de origen médico o traumático con niveles de lesión por encima de los centros sacros (S2-S4) se producen contracciones vesicales en simultáneo con las contracciones esfinterianas lo que conduce a altos residuos postmiccionales, altas presiones de vaciado vesical, reflujo vesicoureteral y daño renal.
La toxina botulínica inyectada directamente en el esfínter uretral externo busca disminuir la resistencia del esfínter con el fín de conseguir micciones a baja presión vesical, los diferentes estudios emplean técnicas similares entre las cuales se describen la inyección endoscopica aplicada en 4 puntos para el hombre, periureteral con y sin guía electromiográfica en la mujer y técnica de inyección perineal con guía electormiográfica también en ambos sexos las dosis empleadas en los diferentes estudios fluctúan entre las 20 – 240 MU de Botox y de 150 – a 250 MU de Dysport. (Tabla 1.)

Los resultados son variables pero en general la disminución significativa de los residuos postmiccionales y la supresión de los cateterismos se logró conseguir en al menos el 50% de los pacientes de la mayoría de estudios publicados.
El empleo de diferentes técnicas de inyección, dosis, presentaciones del medicamento y parámetros de éxito entre los diferentes estudios hacen que el análisis de la información y comparación de los resultados sea difícil.
Hiperactividad Vesical Neurogénica y No- Neurogénica
La literatura relacionada con la aplicación de toxina botulínica inyectada en el detrusor para el tratamiento de la hiperactividad del detrusor idiopática o neurogénica viene en aumento.
En un reciente estudio retrospectivo se analizan los resultados de 200 pacientes con incontinencia secundaria a hiperactividad neurogénica. Fueron inyectadas entre 200-300 MU de Botox, tras 12 semanas se logro demostrara un significativo incremento en la capacidad vesical, residuo postmiccional y compliance vesical.
La mayoría de los pacientes lograron disminuir o suprimir por completo las dosis de anticolinergicos. En 99 pacientes se logro obtener información a las 36 semanas en la cual se demostró persistencia del efecto por medio de estudios urodinamicos14.
En el estudio de Schurch, se demostró disminución de la hiperactividad del detrusor, con un incremento promedio de la capacidad vesical de 261 ml a 490 ml, sin reporte de eventos adversos15. Grosse encontró resultados favorables en aproximadamente el 85% de los pacientes tratados, los cuales duraron hasta 1 año.
El número de inyecciones en el detrusor es de 20-30 sitios, en algunos casos el trígono es respetado por el riesgo de reflujo, aunque esto no ha sido demostrado en ninguna de las series. Las dosis por sitio varían de 2.5 a 10 MU de Botox y entre 10 a 40 MU de Dysport, La duración de la acción puede ir de 4 a 6 meses y en algunos casos hasta 1 año15. Los estudios disponibles sugieren que la mayoría de pacientes requieren entre 200-300 MU de Botox y de 700 a 1200 MU de Dysport por sesión.
MU BOTOX or 700 MU to 1200 MU Disport per
Los estudios de Schulte-Baukloh16 valoran la aplicación de toxina botulínica en 17 niños (edades promedio de 10.8 años) con hiperreflexia vesical, aplicando entre 85 MU a 300 MU de Botox en 30 a 40 sitios. El volumen reflejo medio, la máxima capacidad vesical y la compliance vesical incrementaron con una significativa disminución de la presión del detrusor.
Después de publicados numerosos estudios en hiperactividad neurogenica la pregunta de que efectos podría surtir en aquellos pacientes con hiperactividad idiopática finalmente surge. Aunque los primeros reportes fueron presentados en 200317,18, las primeras publicaciones se dieron en en 200419,20.
De igual manera que en los pacientes neurológicos la mayoría de vairables mostraron gran mejoría en lo relacionado a urgencia, frecuencia, continencia y parámetros urodinamicos. El primer estudio placebo controlado fue publicado por Sahai21, quien inyectó 30 pacientes con hiperactividad idiopática, 15 con 200 MU de Botox y 15 con placebo.
Midiendo las variaciones al inicio, a las 4, 12 y 24 semanas después de la inyección, en el grupo tratado la máxima capacidad cistomanometrica aumento de 193 a 333, 270 y 321 ml respectivamente, mientras que la máxima presión del detrusor disminuyo desde 90 a 39, 49 y 59 cm. H2O. Los episodios de frecuencia, urgencia y urge incontinencia mejoraron significativamente en el grupo control al compararlo con el grupo placebo. Ningún cambio significativo en los anteriores parámetros mencionados se reportó en el grupo placebo.
La gran diferencia entre los pacientes con hiperactividad neurogenica comparados con los de hiperactividad idiopática:
Es que los primeros generalmente se encuentran en un programa de cateterismos y es por esto que el riesgo de retención urinaria toma importancia en los segundos, esto se puede presentar entre el 0 al 45% de los casos y generalmente precisaran de 1 a 2 cateterismos temporalmente (en promedio 3 semanas).
Indicaciones Emergentes
Un número importante de nuevas indicaciones se vienen estudiando para la toxina botulínica.
Entre estas se encuentra el tratamiento de patologías vesicales como los síndromes de vejiga dolorosa (incluyendo la cistitis intersticial y la prostatitis crónica), sobre la teoría de que a toxina botulínica puede bloquear no solo la liberación de acetil colina sino también la de otros neurotransmisores relacionados con las vías del dolor como la sustancia P, el glutamato y péptido relacionado con el gen de la calcitonina, se ha inyectado toxina botulínica en pacientes con cistitis intersticial.
Dos pequeños estudios descriptivos han sido publicados al respecto con 13 y 10 pacientes, inyectando o instilando 200 MU de Botox, el primero de ellos encontró mejoría tanto objetiva como subjetiva de los síntomas es segundo no tuvo resultados satisfactorios22,23.
Entre otras nuevas indicaciones en desarrollo encontramos el tratamiento del síndrome de micción no coordinada, disfunciones del piso pélvico, anismo, vaginismo y uretroespasmo1 .
Actualmente se están llevando a cabo estudios comparativos, prospectivos y controlados que arrojaran nueva información sobre aquellos puntos que aún son controversiales en el manejo de esta nueva herramienta que se nos pone a disposición, cual es la dosis ideal según la patología y según la presentación comercial que estamos manejando?, cuales son los sitios ideales de inyección?.
La técnica de dilución que empleamos actual mente es la mejor y mas segura?. Lo que si se ha logrado demostrar a lo largo del desarrollo de esta técnica de tratamiento es que es un método seguro, útil en aquellos pacientes refractarios o con poca adherencia al tratamiento convencional (menos del 18% de pacientes continúan los anticolinericos al cabo de 6 meses) y con pocas contraindicaciones para su uso (infección urinaria activa, miastenia gravis, síndrome de Eaton Lambert y embarazo).
Bibliografía
- 1. Erbguth, Frank J. Historical Notes on Botulism, Clostridium botulinum, Botulinum Toxin, and the Idea of the Therapeutic Use of the Toxin. Movement Disorders
- 2. Vol. 19, Suppl. 8, 2004, pp. S2–S6. Brin MF. Botulinum toxin: chemistry, pharmacology, toxicity, and immunology Muscle Nerve 1997; 20:S146–68.
- 3. Montecucco C, Schiavo G, Tugnoli V, et al. Botulinum neurotoxins: mechanism of action and therapeutic applications. Mol Med Today 1996;2:418–24.
- 4. Frenkl, T. Rackley, R. Injectable Neuromodulatory Agents:Botulinum Toxin therapy. Urol Clin N Am 32 (2005) 89–99
- 5. Naumann M, Toyka KV, Moore P.History and current applications of botulinum toxin – from poison to remedy. In Handbook of Botulinum Toxin Treatment. Oxford: Blackwell Science, 2003: 3–8.
- 6 Scott AB. Botulinum toxin injection of eye muscles to correct strabismus. Trans Am Ophthalmol Soc 1981; 79: 734–70.
- 7. Jankovic J, Brin MF. Botulinum toxin: historical perspective and potential new indications. Muscle Nerve Suppl 1997; 6: S129–45.
- 8. Dykstra DD, Sidi AA, Scott AB, Pagel JM, Goldish GD. Effects of botulinum A toxin on detrusor-sphincter dyssynergia in spinal cord injury patients. J Urol 1988;139:912–922.
- 9. Dykstra DD, Sidi AA. Treatment of detrusor-sphincter dyssynergia with botulinum A toxin: a double-blind study. Arch Phys Med Rehabil 1990;71:24 –26.
- 10. Schurch B, Hauri D, Rodic B, Curt A, Meyer M, Rossier AB. Botulinum-A toxin as a treatment of detrusorsphincter dyssynergia: a prospective study in 24 spinal cord injury patients. J Urol 1996;155:1023–1029.
- 11. Petit H, Wiart L, Gaujard E, Le Breton F, Ferrie‘re JM, Lagueny A, Joseph PA, Barat M. Botulinum A toxin treatment for detrusorsphincter dyssynergia in spinal cord disease. Spinal Cord 1998;36: 91–94.
Referencias
- 12. Jost WH. Treatment of detrusor sphincter dyssynergia with botulinum toxin. J Neurol 1999;246:I/89.
- 13. Phelan MW, Franks M, Somogyi GT, Yokoyama T, Fraser MO, Lavelle JP, Yoshimura N, Chancellor MB. Botu linum toxin urethral sphincter injection to restore bladder emptying in men and women with voiding dysfunction. J Urol 2001;165:1107–1110.
- 14. Reitz A, Stohrer M, Kramer G, et al. European experience of 200 cases treated with botulinum-a toxin injection into the detrusor muscle for urinary incontinence due to neurogenic detrusor overactivity. Eur Urol 2004;45:510– 5.
- 15. Schurch B, Sto¨hrer M, Kramer G, Schmid DM, Gaul G, Hauri D. Botulinum A toxin for treating detrusor hyperreflexia in spinal cord injured patients :a new alternative to anticholinergic drugs ? Preliminary results. J Urol 2000;164:692– 697.
- 16. Schulte-Baukloh H, Michael T, Schobert J, Stolze T, Knispel HH. Efficacy of botulinum-A toxin in children with detrusor hyperreflexia due to myelomeningocele. Urology 2002;59:325–327.
- 17. Schulte-Baukloh H, Schobert J, Weiss C et al. Botulinum toxin type A as an alternative in the treatment of hyperactive bladder dysfunction: what do patients think? Urologe A 2003; 1: 42, A4.8
- 18. Chancellor M, O’Leary M, Erickson J et al. Successful use of bladder botulinum toxin injection to treat refractory overactive bladder. J Urol 2003; 169: 351, Abstract.
- 19. Rapp DE, Lucioni A, Katz EE, O’Connor RC, Gerber GS, Bales GT. Use of botulinum-A toxin for the treatment ofrefractory overactive bladder symptoms: an initial experience. Urology 2004; 63:1071–5
- 20. Kuo HC. Urodynamic evidence of effectiveness of botulinum A toxin injection in treatment of detrusor overactivity refractory to anticholinergic agents. Urology 2004; 63: 868–72
Lecturas Recomendadas
- 21. Sahai A, Khan S, Dasgupta P. Botulinum toxin A is safe and effective in the treatment of patients with overactive bladder and idiopathic detrusor overactivity: results from a randomised, double-blind, placebo-controlled trial. Eur Urol 2006; 5: 118, A381.
- 22. Smith CP, Chancellor MB. Emerging role of botulinum toxin in the management of voiding dysfunction. J Urol 2004; 171 (6 Pt 1):2128–2137.
- 23. Rackley R, Abdelmalak J. Urologic applications of botulinum toxin therapy for voiding dysfunction. Curr Urol Rep 2004; 5:381–388.