PREMIO “MAX MEYER” 2005
AL MEJOR TRABAJO EN ENDOUROLOGÍA Y LAPAROSCOPIA
Drs. Gaviria F, Uribe C, Escobar F, Castellanos R, Aramburo D, Rodríguez M, Correa JJ.
Instituto de Cirugía Mínimamente invasiva (Medlap), Hospital Pablo Tobón Uribe, Medellín Colombia.
Resumen
Objetivo:
Mostrar la utilidad de un modelo animal en el entrenamiento para nefrectomía laparoscópica.
Se describe la utilización de un modelo experimental para entrenamiento en laparoscopia, describiendo los aspectos éticos y legales, la técnica anestésica, la técnica quirúrgica y las ventajas que ofrece sobre los demás modelos utilizados para este fin.
Conclusiones:
Consideramos que el bovino (Ternero Holstein), es un excelente modelo para el entrenamiento en nefrectomía laparoscópica, ya que ofrece ventajas importantes frente a los otros modelos
Introducción
Una de las grandes dificultades que existe durante la curva de aprendizaje de la cirugía laparoscópica es la posibilidad de realizarla en un modelo experimental antes de llevarla a la práctica en humanos. El modelo experimental más utilizado a nivel mundial ha sido el cerdo, sin embargo, en nuestro medio es un modelo de alto costo. El otro modelo potencial es el canino, con las dificultades para conseguir los animales y con una anatomía diferente a la del humano. Es por esto que se requiere un modelo experimental económico y que represente los hallazgos anatómicos similares durante la nefrectomía laparoscópica.
Objetivo General
– Describir la utilización de un modelo animal (Ternero Holstein) para la realización de nefrectomía laparoscópica.
Objetivos Específicos
– Evaluar los aspectos económicos y de disponibilidad del recurso, comparándolo con otros modelos animales.
– Determinar las consideraciones anestésicas para el manejo del ternero durante el procedimiento quirúrgico.
– Establecer las características anatómicas renales y vasculares del modelo y compararlas con las del ser humano.
– Describir detalladamente la técnica quirúrgica utilizada.
– Establecer los parámetros éticos y legales para la utilización de animales en experimentación médica.
Descripción del Procedimiento
Consideraciones Anestésicas
El protocolo utilizado de anestesia fue el uso combinado de Ketamina, Xilacina y Gliceril guayacol como se describe a continuación:
El Periodo preanestésico incluye una serie de fármacos que se administran minutos antes de la inducción anestésica y cuyo fin primordial es facilitar el manejo y, básicamente elevar las condiciones de seguridad para el paciente y para el anestesista. Se trata de conseguir cierto grado de tranquilización y de analgesia, así como un control adecuado de los reflejos autónomos18.
Particularmente la Xilacina es usada en combinación con la Ketamina por sus propiedades miorelajantes ayudando a reducir la rigidez causada por los agentes disociativos.
Esta combinación ha sido probada y usada con éxito en la premedicación anestésica en grandes animales incluyendo el bovino16,17,19.
En el ternero, la administración de Xilacina (0.04mg/Kg.) permite realizar procedimientos quirúrgicos de corta duración (14). .
Se obtienen buenos resultados con la administración de 2 a 5 mg de Ketamina intravenosa9.
Los terneros pueden ser premedicados con Xilacina 0.04 mg/Kg., vía intramuscular profunda entre los músculos semitendinoso y semimembranoso; luego del periodo de tiempo en que los terneros se demoran en tomar la posición de decúbito lateral, se canaliza una de las venas yugulares con un angiocateter No. 18 o 20 y se realiza inducción intra venosa con Ketamina a razón de 5 Mg/kg, se alcanza el máximo nivel de relajación muscular con la administración intravenosa de gliceril guayacol 1Mg/Kg16,18,19.
El estudio permitió demostrar, la inducción anestésica fue suave y libre de excitación.
El tiempo de inducción fue rápido aproximadamente (10-30seg.) Lo cual se atribuye a la rápida distribución de la Ketamina en el organismo, primero al cerebro y tejidos altamente perfundidos y posteriormente a otros menos irrigados. La xilacina provee una rápida inducción a la anestesia general con o sin el uso de medicamentos preanestesicos12.
La técnica utilizada no requiere intubación del animal.
Luego de terminada la cirugía, se Sacrifican los terneros bajo efectos de la anestesia con una inyección intra cardiaca de cloruro de potasio.
Consideraciones técnicas del procedimiento
La posición recomendada para la nefrectomía en el ternero es el decúbito lateral con extensión del miembro inferior del lado en el cual vamos a trabajar. Se le da una inclinación céfalo caudal de aproximadamente 20 grados.
Una vez el animal esta anestesiado (previamente descrita), se realiza el neumoperitoneo con una técnica cerrada de insuflación utilizando la aguja de Veress. La aguja se coloca 2 cms por encima del ombligo a nivel de la línea media para evitar el ligamento umbilical medio (prominente en este modelo).
La presión intra abdominal se preselecciona en 12 mmHg durante todo el procedimiento.
Tres puertos de 10 mm son suficientes para realizar la nefrectomía. El puerto para el lente se coloca 2 a 3 cm por debajo del ombligo a nivel de la línea media. El segundo puerto se localiza 5 a 6 cm por encima del ombligo y a 2 o 3 cm por fuera de la línea media. El último puerto se localiza en el tercio inferior del abdomen del animal cerca del pliegue del miembro inferior con la cavidad abdominal.
La disección se inicia con el rechazo del estómago y de las asas intestinales.
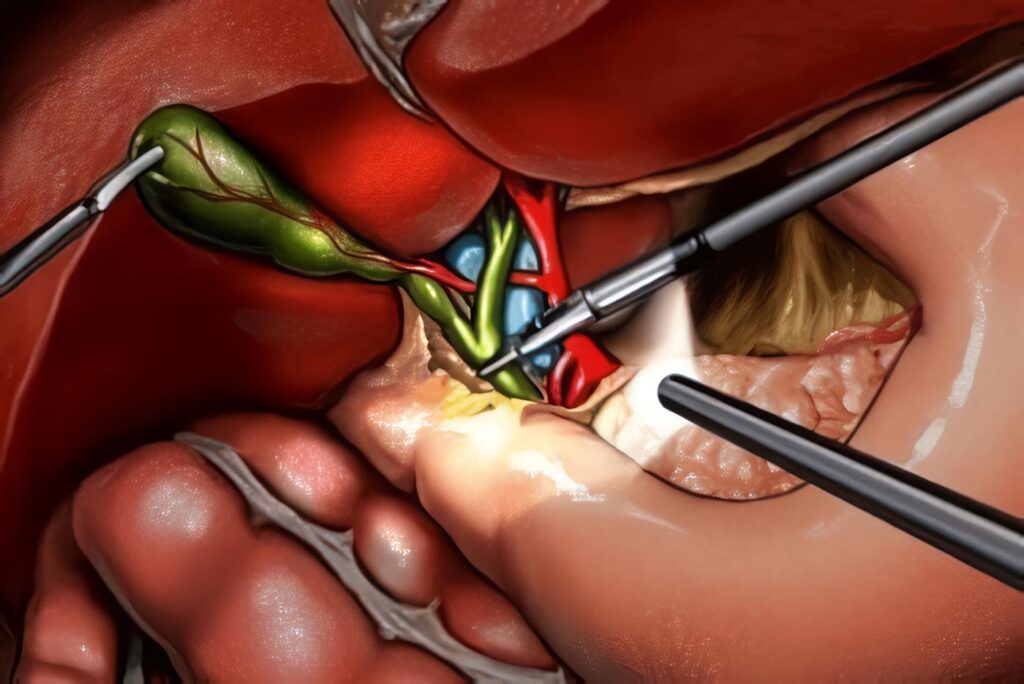
Luego de identificar el riñón se realiza una leve tracción lateral de este para facilitar la disección de los grandes vasos. Se utiliza un disector curvo para evitar la lesión vascular. La vena renal es la primera en identificarse ya que se encuentra anterior a la arteria renal (igual que en el humano). Una vez liberada la vena renal, se realiza la disección de la arteria renal que se encuentra inferior y posterior a la vena.
Una vez libre la arteria, se liga con clips como se hace en el humano. EL diámetro de la vena es muy similar a la del humano, por lo cual para su ligadura es indispensable haber reducido el flujo totalmente y utilizar clips largos o una grapadora vascular.
Una vez controlados los grandes vasos se termina la disección del riñón utilizando el bisturí armónico o el electrocauterio. El uréter de este modelo es delgado y en ocasiones no se visualiza durante la cirugía.
| Costos por Cirugía | |
| Ternero: 1.1 ml Xilacina: 3 ml Ketamina: 40 ml Gliceril guayacol Catéter: 500 ml Solución salina: Venoclisis: Jeringas: |
$ 40.000 $ 2.200 $ 6.120 $ 800 $ 1.700 $ 2.300 $ 1.600 $ 1.000 |
| Costo de medicamentos | |
| Fco Xilacina 10 ml Fco Ketamina 10 ml Fco Guayacolato 500 cm |
$ 20.000 20.400 $ 10.000 |
Consideraciones Éticas y Legales
La experimentación con animales ha permitido avances de los conocimientos biológicos y del bienestar del hombre, en particular lo que concierne al tratamiento y prevención de enfermedades. Hasta el momento, no es posible prescindir de animales en la experimentación para el progreso de las ciencias biomédicas y el beneficio de la salud humana y animal. Sin embargo, hay que aceptar también que el uso de animales en la investigación requiere de ciertos principios que la comunidad científica debe aceptar.
Es así como se han establecido normas para la utilización de animales con fines de investigación.
Russel y Burch, dos investigadores del Reino Unido crearon el concepto de las tres R en investigación animal: reducir, refinar y reemplazar. La reducción y el refinamiento se logran planeando el trabajo de forma detallada y realizando revisión bibliográfica para evitar repeticiones y reducir al máximo el número de animales utilizados. La sustitución se logra utilizando métodos alternativos como simuladores de laparoscopia (pelvi-training) y programas de realidad virtual.
Cuando es imprescindible utilizar animales debe tenerse en cuenta:
– Tratarlos con el respeto que merecen los seres vivos.
– Mantenerlos en buenas condiciones.
– No someterlos a dolor y sufrimiento innecesario.
– Calmar el dolor y el discomfort con medidas adecuadas.
– Sacrificar humanitariamente a quienes no queden en condiciones de vivir adecuadamente.
– No utilizar especies en riesgo de extinción.
Se tuvieron en cuenta las consideraciones legales, de acuerdo a los artículos 88 y 89 de la resolución número 008430 de 1993 del ministerio de salud de la República de Colombia, los cuales aceptan el uso de animales en investigación médica solamente cuando contribuyan al desarrollo de mejores medios para la protección de la salud y el bienestar tanto del hombre como del animal y reservar los estudios en animales para cuando se hayan agotado otras alternativas, según los principios de Rusell-Burch8,9,10.
Para su ejecución, la metodología y manejo de los bovinos utilizados en esta investigación en cuanto a macro y microambiente, procedimientos y criterios de selección de punto final, se contó con la aprobación del Comité de Ética para la Experimentación con Animales de la Universidad de Antioquia.
Discusión
Es un hecho que la cirugía laparoscópica está reemplazando la cirugía abierta en muchos procedimientos urológicos, pues ofrece una baja morbilidad, mejores resultados cosméticos, hospitalización más corta, menor dolor postquirúrgico y un regreso más rápido a las actividades cotidianas.
La nefrectomía laparoscópica, es un procedimiento que requiere un adecuado entrenamiento pues, aunque la visualización anatómica es mejor mediante éste método, la información táctil se disminuye y la percepción visual se limita a dos dimensiones. Es por esto que el urólogo en formación en laparoscopia, debe tener la posibilidad de practicar inicialmente en el “pelvi-trainer” para adquirir la coordinación y orientación óptica y luego es necesario familiarizarse con la utilización del instrumental y practicar los diferentes pasos del procedimiento como disección del riñón, ligadura de los vasos etc., lo cual idealmente debe hacerse en un modelo animal. El reto es optimizar el entrenamiento con el fin de hacer las curvas de aprendizaje de cirugía en humanos lo más cortas posibles.
La mejor forma actualmente de adquirir habilidad fuera del quirófano son una variedad de modelos de entrenamiento, donde se cuenta con modelos in Vitro y animales vivos.
Para el entrenamiento laparoscópico, es fundamental la utilización de modelos vivos que no pueden ser reemplazados por modelos in Vitro con relación a pulsación de los vasos, sangrado y control del sangrado (7).
En la revisión de la literatura solo encontramos un artículo donde se reporta la utilización del ternero como modelo para trombectomía laparoscópica de vena cava inferior y aurícula derecha simulando un trombo tumoral de cáncer renal nivel III o IV utilizando hipotermia11. Sin embargo, no existe ningún reporte en la literatura revisada que indique la utilización de éste para entrenamiento en nefrectomía laparoscópica.
Obtuvimos varios reportes donde se preconiza la utilización del cerdo como modelo para nefrectomía laparoscópica1,4,5.
El cerdo, tiene tal vez la mayor similitud anatómica al humano, sin embargo, en nuestro medio es un modelo costoso.
El conejo es uno de los animales utilizados como modelo en nefrectomía laparoscópica7, una dificultad con éste es el campo reducido en relación al tamaño del instrumental y un riñón que difiere en tamaño con el del ser humano.
Conclusión
El modelo bovino (Ternero Holstein) para nefrectomía laparoscópica, es un modelo ideal pues ofrece las ventajas de ser anatómicamente similar al humano, es económico. Esto lo hace un modelo de entrenamiento excelente en la curva de aprendizaje de esta técnica quirúrgica.
Bibliografía
- 1. Rassweiler JJ, Henkel TO, Potempa DM, Frede T, Stock C, Gunther M, Alken P. [Laparoscopic training in urology. An essential principle of laparoscopic interventions in the retroperitoneum]. Urology A. 1993 Sep;32(5):393-402.
- 2. Yoder B, Wolf JS Jr. Canine model of surgical stress response comparing standard laparoscopic, microlaparoscopic, and hand-assisted laparoscopic nephrectomy. Urology. 2005 Mar;65(3):600-3.
- 3. Traxer O, Gettman MT, Napper CA, Scott DJ.; Jones, DB, Roehrborn CG, Pearle MS.; Cadeddu JA. THE IMPACT OF INTENSE LAPAROSCOPIC SKILLS TRAINING ON THE OPERATIVE PERFORMANCE OF UROLOGY RESIDENTS. J Urol. 2001 Nov; 166(5):1658-61.
- 4. Valdivia Uria JG, Viloria González A, Rodríguez Gómez J, Martínez Sanudo MJ, Whyte Orozco A, Valle Gerhold J, Sever Bermejo JR. [Laparoscopic nephrectomy: experimental surgical model]. Actas Urol Esp. 1992 Feb;16(2):169-74.
- 5. Chiu AW, Chen MT, Huang WJ, Young ST, Cheng C, Huang SW, Chu CL, Chang LS. Laparoscopic nephrectomy in a porcine model.Eur Urol. 1992;22(3):250-4.
- 6. Allendorf JD, Bessler M, Whelan RL. A murine model of laparoscopic-assisted intervention. Surg Endosc. 1997 Jun;11(6):622-4.
- 7. Molinas CR, Binda MM, Mailova K, Koninckx PR. The rabbit nephrectomy model for training in laparoscopic surgery. Hum Reprod. 2004 Jan;19(1):185-90.
- 8. N. López Moratalla y G. Herranz. Experimentación en animales. Fecha de acceso: Marzo 21/2005.Disponible en: http://www.unav.es/cdb/medicinainvani.html.
- 9. República de Colombia. Ministerio de Salud, resolución No. 008430 de 1993 (4 de octubre de 1993). Acceso: febrero 13/2005. Disponible en: http://www.ins.gov.co/pdf_admon/juridica/ei/ei_1993_res_ms_8430.PDF
Referencias
- 10. Blanco Restrepo JH, Maya Mejía JM. Fundamentos de Salud Pública, Epidemiología Básica y Principios de Investigación Tomo III. Cap. 12, pag 125-132. 1ª Edición. Corporación Para Investigaciones Biológicas, 1999.
- 11. Meraney AM, Gill IS, Desai MM, Harasaki H, Sato M, Goel M, Farouk A, Ponsky L, Kaouk J, Kopchek M, Sung GT.
- 12 Laparoscopic inferior vena cava and right atrial thrombectomy utilizing deep hypothermic circulatory arrest. J Endourol. 2003 Jun;17(5):275-82.
- 13. Muir W. Manual de Anestesia Veterinaria. 2a ed. Madrid. Mobsy. 1997
- 14. SUMANO-OCAMPO, Farmacología Veterinaria. 2a ed. Mc Graw Hill interamericana. México. 2001.
- 15. Botana LM. Landoni F. Jiménez T. Farmacología y terapéutica veterinaria. Madrid. Mc Graw Hill interamericana. 2002.
- 16. Gavin M.A Anestesia y analgesia veterinaria. 2a ed. Zaragoza – España. Acribia.1970
- 17. GOODMAN & GILMAN, Las bases farmacológicas de la terapéutica. 9na ed. México. Mc Graw Hill interamericana. Vol 1. 1996.
- 18. Padrid P. Small animal practice, respiratory Medicine and surgery.The Veterinary clinics of North America. 2000. Vol. 30, No 6. 17. Gaviria E. Restrepo J. Tintinago L. Marin J. Aramburo D, et al. Evaluación del Propofol como anestésico en la cirugía de trasplante de traquea en cerdos. (Artículo de revista en prensa). 2004
- 19. Halc L.W; Clarke K.W. Veterinary Anesthesia. 9na ed. Londres. Bailliere Tindall. 1991