4.
4.1 Inhibidores de la acetilcolinesterasa
Myriam del Carmen Gutiérrez. Médica Magister en Toxicología Universidad Nacional de Colombia Profesional de Apoyo OPS/OMS -Ministerio de Salud y Protección Social Consultora FAO Regional /Naciones Unidas
Generalidades
Dentro de los plaguicidas inhibidores de la acetilcolinesterasa se encuentran los organofosforados y carbamatos.
Organofosforados (OF): son sustancias clasificadas químicamente como esteres, derivados del ácido fosfórico y ácido fosfónico utilizadas como plaguicidas para el control de insectos; son biodegradables, poco solubles en agua y muy liposolubles, su presentación más frecuente es en forma líquida.
Hay que recordar que estos productos comerciales pueden contener en algunas presentaciones líquidas solventes derivados de hidrocarburos, los cuales pueden por si mismos generar intoxicación. Además, existen armas químicas que pertenecen al grupo de los organofosforados extremadamente tóxicos, como por ejemplo el gas sarín.
Carbamatos: estos compuestos son derivados del ácido carbámico. El cuadro clínico tóxico es similar al estudiado en los organofosforados. En relación al tratamiento, es básicamente igual a los organofosforados, con la salvedad de no utilizar oximas reactivadoras en varios de ellos, pues van a formar compuestos carbamilados que pueden potenciar los efectos del inhibidor.
Toxicocinética y toxicodinamia
Los inhibidores de la colinesterasa se pueden absorber por todas las vías: oral (en intentos de suicidio principalmente y accidental usualmente en niños), inhalatoria (en trabajadores agrícolas, fumigadores), dérmica (en trabajadores agrícolas y niños). También puede entrar por vía conjuntival, vaginal y rectal.
Se metabolizan a nivel hepático mediante distintos procesos químicos, que en oportunidades aumentan la actividad tóxica del compuesto, como es el caso de parathion, malathion, diazinon y chlorpyriphos los cuales sufren un proceso de oxidación, formando compuestos más tóxicos para humanos y seres vivos, tipo oxon.
Sus metabolitos pueden almacenarse principalmente en tejidos adiposo, riñón, hígado y glándulas salivares; su excreción se realiza principalmente por vía renal.
Tienen como acción principal la inhibición de la enzima acetil-colinesterasa tanto la colinesterasa eritrocitíca o verdadera como la plasmática o pseudocolinesterasa.
Los organofosforados actúan por fosforilización enzimática originando una unión muy estable que se considera “irreversible”, mientras que los carbamatos actúan por carbamilación de la enzima siendo esa unión más débil e inestable, lo que la hace reversible.
Ambos causan pérdida de la actividad de la enzima acetilcolinesterasa necesaria en el organismo para la hidrólisis de la acetilcolina, permitiendo la acumulación de acetilcolina en la hendidura sináptica y estimulando excesivamente el SNC, los receptores muscarínicos de las células efectoras parasimpáticas, los receptores nicotínicos presentes en la placa neuromuscular y en los ganglios autónomos traducido clínicamente en un síndrome colinérgico.
La dosis tóxica depende de la potencia del organofosforado o carbamato y de muchos otros factores como la vía y el tiempo de exposición.
Es importante conocer la categoría toxicológica del compuesto involucrado para determinar junto con la cantidad ingerida o absorbida por las diferentes vías, la severidad del cuadro clínico y por lo tanto tomar las medidas terapéuticas adecuadas.
Manifestaciones clínicas
Los signos y síntomas pueden presentarse dentro de pocos minutos hasta 1 a 2 horas posteriores a la exposición.
Se presenta un deterioro progresivo estableciéndose el cuadro clínico de síndrome colinérgico agudo cuyas manifestaciones pueden ser de tres tipos:
muscarínicas, nicotínicas o de sistema nervioso central. Los síntomas nicotínicos tienden a ser los primeros en aparecer.
-
Síndrome muscarínico:
Visión borrosa, miosis puntiforme que puede llegar a paralítica, es un signo característico en intoxicaciones por organofosforados o carbamatos pero puede presentarse inicialmente midriasis en la fase primaria de la intoxicación, ocasionada por una liberación de adrenalina endógena, o en la fase final de la intoxicación por acción nicotínica o parálisis muscular la cual es premonitoria de muerte. Además, lagrimeo, sialorrea, diaforesis, broncorrea, broncoespasmo, disnea, vómito, dolor abdominal tipo cólico, diarrea, disuria, falla respiratoria, bradicardia.
-
Síndrome neurológico:
Ansiedad, ataxia, confusión mental, convulsiones, colapso, coma, depresión cardio-respiratoria central.
-
Síndrome nicotínico:
Midriasis inicial, calambres, mialgias, fasciculaciones musculares que se evidencian en los grupos musculares de la región palpebral, músculos faciales y dedos, llegando a generalizarse y persistir aún después de la muerte durante unos minutos debido a la acumulación de acetil colina en las placas neuromusculares.
-
Síndrome intermedio:
En 1974 Wadia describe un nuevo síndrome, el intermedio, que aparece entre las 24 y 96 horas de iniciada la intoxicación y que se caracteriza por una parálisis proximal que involucra pares craneanos, músculos flexores de nuca y músculos de la respiración, originando gran dificultad respiratoria y llevando a la muerte al paciente si no se proporciona soporte ventilatorio. Se han enunciado como posibles responsables a los plaguicidas fenthion, dimethoate, monocrotophos, methamidofphos. Se ha descrito como “recaída del tercer día” y se cree que ello se debe a varios factores:
-
La liposolubilidad del fosforado:
Que le permite almacenarse por algunas horas o días en el tejido graso del paciente.
-
La prolongada sobre-estimulación de la acetilcolina:
En los receptores nicotínicos postsinápticos de la unión neuromuscular que causa agotamiento y deterioro de dichos receptores.
-
La persistencia del tóxico.
A cualquier nivel de organismo probablemente a nivel del tracto digestivo (especialmente intestinal), tracto que por la “atropinización” se somete a parálisis y se ha observado que en el tiempo que se presenta la “recaída” (tercer día), se coincide con la reducción de la atropinización y el reinicio del peristaltismo intestinal, con lo cual se facilitaría que el material tóxico remanente intestinal se ponga en contacto con nuevas partes de mucosa y se produzca “reintoxicación”.
La medicación adecuada y oportuna, y sobre todo la “exhaustiva descontaminación”, especialmente de intestino, de piel, cuero cabelludo, uñas, conducto auditivo externo, disminución de la reabsorción de metabolitos excretados por sudor o secreciones que persisten en contacto con el paciente, permiten que la incidencia de esta complicación disminuya.
Algunos efectos cardiacos incluyen bloqueo A-V, cambios en el segmento ST, prolongación del QT y arritmias ventriculares. La hipersecreción bronquial, broncoconstricción y depresión respiratoria sobrevienen en casos severos lo que puede llevar a falla respiratoria y muerte.
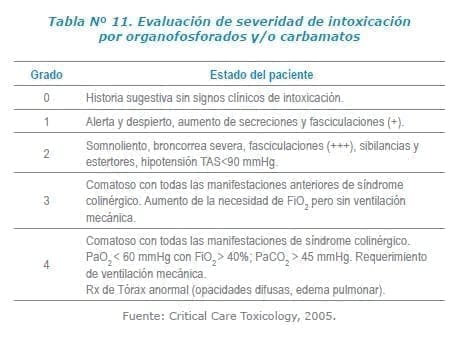
Se proponen 5 grados para clasificar clínicamente la severidad de la intoxicación y de esta manera orientar el tratamiento. Todo paciente con grado 2 o más debe ser tratado en una UCI por el riesgo de empeoramiento progresivo o aún súbito del cuadro clínico.
Diagnóstico
- Anamnesis que incluirá exposición a plaguicidas del grupo de inhibidores de colinesterasa.
- El cuadro clínico que presenta signos y síntomas claves como son: miosis, sialorrea, bradicardia, diaforesis, piel fría, dificultad respiratoria y aún convulsiones.
- Medición de niveles de actividad de colinesterasa en plasma y glóbulos rojos.
- Determinación del tóxico en contenido gástrico o heces.
- Hallazgo del plaguicida o de sus metabolismos en orina.
La determinación de la actividad de la acetil colinesterasa es muy importante y fundamental en casos de intoxicación aguda. Esta prueba nos permite saber si el individuo ha estado en contacto con plaguicidas organofosforados y/o carbamatos y a su vez la intensidad de impacto que ha ejercido sobre el paciente en estudio.
La actividad enzimática varía entre personas; sin embargo, se considera significativa una disminución de más del 25 % de la actividad tomando como referencia el límite inferior de normalidad que nos proporciona el laboratorio de Toxicología que realice el análisis.
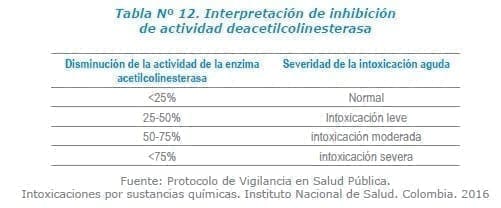
Se debe tener en cuenta que la colinesterasa eritrocítica puede estar inhibida en casos de anemia perniciosa, en hemoglobinopatías, tratamientos antimaláricos, toma en tubos de ensayo que contengas oxalatos, entre otros casos.
La colinesterasa plasmática está disminuida en pacientes con deficiencia hereditaria de la enzima, malnutrición, enfermedad hepática o debilitante crónica, estados anémicos, embarazo, periodos menstruales, ayuno prolongado entre otros.
Los resultados de colinesterasas se deben correlacionar siempre con la clínica del paciente. En casos forenses o cuando se requiera identificar el(los) plaguicida(s) responsable(s) del caso, se usa la prueba de oro que es la Cromatografía de Gases o Líquida. El costo es más alto, pero el resultado es preciso y cuantitativo.
Diagnóstico diferencial
- Los cuadros epilépticos tienen gran similitud y en estos casos se insiste sobre la importancia de apreciar el olor “aliáceo” de los insecticidas o el olor de solventes en la boca, la piel o en la ropa del enfermo. Igualmente importante es el tono muscular el cual está ausente en los casos de intoxicación. Tiene gran importancia la anamnesis dada por el paciente o la información de sus acompañantes.
- Los comas hiper o hipoglicémicos metabólicos, pero se debe tener cuidado al diferenciarlos como diagnóstico ya que los inhibidores de la colinesterasa también puede causar alteración en páncreas y trastornos metabólicos.
- Intoxicaciones con otras sustancias tóxicas como fluoracetato de sodio, hidrocarburos clorados, depresores del sistema nervioso central (barbitúricos, opiáceos, benzodiazepínicos, alcoholes etílico y metílico).
- Finalmente, episodios agudos de obstrucción de vías respiratorias, pueden tener sintomatología similar.
Tratamiento general
Mantenimiento de vía aérea con limpieza y aspiración de secreciones.
Oxigenoterapia y observación permanentemente de la actividad de los músculos respiratorios ya que puede presentar falla respiratoria aguda. En casos severos se requiere intubación orotraqueal y ventilación asistida.
Remover la ropa contaminada y realizar baño con agua y jabón en las zonas expuestas. Será preferible una segunda limpieza con agua alcalinizada (agua más bicarbonato de sodio en polvo), si la intoxicación fue por vía dérmica ya que el medio alcalino hidroliza el tóxico.
No inducir vómito por el riesgo de broncoaspiración. Además, las presentaciones líquidas de los plaguicidas muy frecuentemente contienen hidrocarburos tipo kerosene que aumenta el riesgo de producir neumonitis química durante la emesis.
Vigilancia estricta de signos vitales y estado neurológico.
Lavado gástrico con abundante suero fisiológico o solución salina, si la ingesta fue hace menos de 1 hora, protegiendo la vía aérea en caso de que el paciente tenga disminución del estado de conciencia. Administrar carbón activado 1g/kg de peso si se dispone de éste.
La administración de catártico salino no es recomendada ya que puede exacerbar la gastroenteritis causada por los organofosforados o carbamatos. Además, el cuadro colinérgico a su vez se acompaña de diarrea.
Control y manejo de equilibrio ácido-básico y electrolitos del paciente. Administrar bicarbonato de sodio según requerimientos observados en los gases arteriales.
Control de perfil hepático, renal, glicemia y amilasas.
Monitoreo cardiaco permanente y control electrocardiográfico cada 6 horas durante las primeras 24 horas. Los pacientes con prolongación del QTc (corregido) o extrasístoles ventriculares tienen mayor mortalidad y son más propensos a desarrollar falla respiratoria que los que tienen QTc normal.
Si se presenta arritmia del tipo taquicardia ventricular polimorfa (puntas torcidas), se debe administrar Sulfato de Magnesio 2-4 g (1 -2 ampollas) disueltos en 100 ml de SSN para pasar en una hora (niños 50 mg/kg) y el manejo debe ser conjunto con médico intensivista y/o pediatra.
En caso de agitación o convulsiones dar tratamiento con Diazepam.
Tratamiento específico
Atropina
Es una amina terciaria por lo que atraviesa la barrera hemato-encefálica. Es la droga base para el tratamiento y su mecanismo de acción es ser antagonista competitivo con la acetilcolina principalmente en los receptores muscarínicos. La atropina tiene poco efecto en los receptores nicotínicos por tanto no antagoniza el síndrome nicotínico.
Inicialmente se debe buscar “atropinizar” el paciente; los signos recomendados para vigilar la “atropinización” son: disminución de secreciones y aumento de frecuencia cardiaca. Es muy importante que el paciente reciba oxigenación previamente para que la fibra cardiaca pueda responder al efecto de la atropina. La miosis puede persistir aún con el paciente bien atropinizado, así que no es un buen parámetro de control.
Dosis inicial: 1-2 mg de atropina intravenosa de forma rápida (en bolo por vena periférica), luego cada 5 minutos aplicar el doble de la dosis anterior hasta control de síntomas y lograr atropinización (disminución de secreciones y aumento de frecuencia cardiaca por encima de 80 l/m).
En intoxicación grave se puede iniciar esquema con dosis de 3 a 5 mg intravenosos directos e ir duplicando dosis cada 5 minutos hasta control de síntomas y lograr de igual manera la atropinización del paciente.
Dosis de mantenimiento: una vez alcanzada la atropinización, se continúa con 1 mg. IV cada media hora durante 3-4 horas pasándose posteriormente, según respuesta del paciente a 1 mg cada 6 horas; la atropina debe mantenerse por el tiempo que lo requiera el paciente y hasta que cedan totalmente los síntomas.
Dosis pediátrica: 0.02 – 0.1 mg/ Kg IV dosis.
(Lea También: Piretrinas y Piretroides)
Pralidoxima
Es utilizada junto con la atropina en el manejo de pacientes con intoxicación severa por organofosforados. Su acción es reactivar la enzima acetilcolinesterasa fosforilada principalmente a nivel de receptores nicotínicos, mejorando la contractilidad muscular, dentro de los primeros 10 a 40 minutos después de su administración; presenta además sinergismo con la atropina en los receptores muscarínicos, por lo que siempre deben administrarse de manera conjunta.
Su eficacia está en relación directa con la precocidad de su administración (primeras 24 horas), pues el “envejecimiento” de la fosforilización aumenta la estabilidad del complejo enzima-fosforado.
Durante su administración el paciente preferiblemente debe estar bajo monitorización en una Unidad de Cuidados Intensivos. La evidencia actual de la efectividad de su uso es gran motivo de controversia a favor y en contra de su efectividad y riesgo.
Se puede aplicar intramuscular o intravenoso.
Dosis:
- Niños: dosis de carga de 20-50 mg/k (no exceder 2 gr/dosis), administradas de 15-30 minutos y continuar con infusión 10-20 mg/kg/h.
- Adultos: dosis inicial de 30 mg/kg administradas en 15-30 minutos y continuar en infusión a 8 mg/kg/h o administrar 30 mg/kg cada 4 horas.
Con dosis terapéuticas en humanos, los efectos adversos son mínimos. Con niveles mayores de 400 mg/ml de Pralidoxima se ha documentado visión borrosa, elevación de la presión diastólica, diplopía, cefalea, náuseas estupor, hiperventilación, hipotensión, taquicardia, dolor muscular, mioclonías y agitación. La administración rápida intravenosa (>200 mg/minuto) puede causar paro cardiaco y respiratorio.
Se debe administrar por personal experto y en UCI preferiblemente.
Difenhidramina
Se utiliza como coadyuvante en el tratamiento de intoxicación por organofosforados y carbamatos. Su uso reduce las cantidades necesarias de atropina en pacientes intoxicados y es de utilidad en el tratamiento de las fasciculaciones musculares, sobre las que no actúa la atropina, por ser de efecto nicotínico. Se administra concomitantemente con atropina. Dosis: 50 mg (o 1 mg/ kg de peso vía oral) en jarabe por SNG con buenos resultados cada 8 horas en adultos y cada 12 horas en niños.
No se debe dar de alta al paciente hasta que cumpla 48 horas asintomático y sale con recomendaciones al familiar o acudiente sobre observación del estado respiratorio y muscular.
En caso de intento de suicidio se debe vigilar al paciente en el Servicio de Urgencias por el riesgo suicida y siempre debe ser valorado por el médico especialista en Psiquiatría.
Valoración por toxicología clínica para continuar manejo especializado y consideración de otras medidas terapéuticas útiles en situación clínica grave.
Criterios de remisión y criterios de UCI
- Convulsiones y broncoaspiración
- Deterioro hemodinámico
- Arritmia o ECG con QTc > 500 mseg
- Necesidad de reanimación cardio-cerebro-pulmonar (RCCP)
- Signos de Síndrome Intermedio
- Hipoxemia progresiva con SatO2 < 93%
- Amilasa > de 360 UI/L
- Intoxicación Iatrogénica por atropina.
Referencias
- Barelli A, Soave PM, Del Vicario M, Barelli R. New experimental Oximes in the management of organophosphorus pesticides poisoning. Minerva Anestesiol. 2011; 77(12):1197-203.
- Buckley NA, Eddleston M, Li Y, Bevan M, Robertson J. Oximes for acute organophosphate pesticide poisoning. Cochrane Database Syst Rev. 2011(2): Cd005085.
- Castaño PA. Intoxicación por inhibidores de colinesterasas. En Peña LM, Zuluaga AF. Protocolos de Manejo del Paciente Intoxicado. Universidad de Antioquia. 1ª. Ed. Colombia. 2012. p. 66-75.
- Eddleston M, Buckley NA, Eyer P, Dawson AH. Management of acute organophosphorus pesticide poisoning. The Lancet. Vol 371. February 16, 2008. p. 597-607.
- Eddleston M, Eyer P, Worek F., et al. Pralidoxime in Acute organophosphorus insecticide poisoning – A rabdomised Controlled Trial. 2009 PLoS Med 6 (6): e1000104. doi: 101371/journal.pmed 1000104.
- King AM, Aaron CK. Organophosphate and carbamate poisoning. Emerg Med Clin North Am. 2015; 33(1):133-51.
- Worek F, Thiermann H. The value of novel oximes for treatment of poisoning by organophosphorus compounds. Pharmacol Ther. 2013; 139(2):249-59.