Revisión de 20 Años de Experiencia
Dra. Doris Salgado
Dr. César Alberto Panqueba
Dr. Jairo Antonio Rodríguez R.
Universidad Surcolombiana.
Hospital Departamental
“Hernando Monsaleano Perdomo”
Neiva, Huila, Colombia.
Resumen:
El desarrollo de la biología molecular y la respuesta inmune en la última década, nos ha permitido comprender mejor algunos procesos fisiopatogénicos de una enfermedad que afecta nuestra región de forma endémica, con una incidencia de 3 casos y una mortalidad de 7%.
El presente trabajo muestra la experiencia acumulada en los últimos 20 años sobre leishmaniasis visceral en niños del Huila, haciendo especial énfasis en aspectos clínicos. Epidemiológicos y en el tratamiento. Para el efecto, se realizó un estudio descriptivo-retrospectivo, revisando las historias clínicas de los niños con diagnóstico de leishmaniasis visceral en el Hospital General de Neiva desde 1978 hasta 1997. El 85% de los casos se presentaron en menores de 2 años e inclusive en niños de 3 meses de edad. El compromiso del estado nutricional se debe interpretar cuidadosamente, porque puede ser causa o consecuencia de una enfermedad crónica que se asocia a infecciones de origen bactetiano, como bronconeumonía y diarrea.
En la explicación de estos resultados, puede incidir la inmadurez inmunológica propia de la edad como menor expresión del CD21, receptor del linfocito B y de la célula dendrítica en el bazo, la cual interviene en la síntesis de anticuerpos específicos por la interacción con la proteína Ced del complemento.
Palabras clave: Leishmaniasis visceral, respuesta inmune, infecciones tropicales.
Summary:
In the decade the development in molecular biology and inmunology has been an important fact in order to understand fisiopatogenic events in patients affected by visceral leishmaniasis wich has an endemic behavior in our region with incidnece of 3 cases and a mortality rate of 7%.
This article shows our accumulated experience in the last 20 years about visceral leishmaniasis in children; we put special emphasis in some epidemiological and treatment issues. We have reviewed charts from 1978 to 1997 in order to find children who suffered of visceral leishmaniasis and assisted at the “Hospital General de Neiva”. 85% of affected patients were children younger than 2 years of age, moreover, children 3 months old were reported. The results about nutritional status are controversial since they can appeared as cause or consecuence of this chronic disease which is associated to bacterial infections i.e bronoconeumonia or diaorrhea.
These results can be explained by inmunologic immaturity which is represented by a decreased expression of CD21 o B lymphocytes and dendritic cells at spleen both important in the production of specific antibodies, due to its interaction with complement protein C3d.
Introducción:
La leishmaniasis visceral o kala-azar (Fiebre negra) se conoce desde los albores del siglo XX. En 1900 Sir William Leishman descubrió el parásito en el bazo de un soldado muerto en el Africa por la llamada fiebre Dum-Dum1,2.
La primera publicación de la entidad data de 1903 cuando Donovan descubrió el parásito en un aspirado esplénico. En nuestro continente aparece referida en 1913 por Migone quien diagnosticó un paciente en el Brasil1,3,4.
En Colombia el primer casi fue descrito por Gast-Galvis en 1944 como hallazgo de material de viscerotomía en Santander; en 1964 Gómez-Vargas informa nuevos casos en la misma área, pero sólo en 1968 empieza a reportarse la enfermedad en otras áreas.
Corredor y Ronderos, quienes insisten sobre la presencia de la entidad, muestran su real incidencia y presentan las características para reconocerla como un problema de salud pública. La enfermedad es más frecuente en regiones como el valle del alto Magdalena, Tolima, Huila, Cundinamarca, Santander y en áreas aisladas de Sucre1,5.
El kala-azar es una clásica zoonosis producida por un microorganismo unicelular leishmania donovani, el cual es un parásito intracelular obligado de células presentadoras de antígeno como macrófagos y células dendríticas, capaz de trasnmitirse de un individuo a otro por artrópodos6,7.
El kala-azar es una enfermedad de países tropicales y subtropicales que poseen condiciones propicias tales como alturas entre 800 y 1200 metros, clima seco, vegetación boscosa y ubicada entre 19 y 29 grados de latitud norte y sur respectivamente. Estos hechos favorecen el desarrollo del vector es decir, la Lutzomia que por sus características domicialiarias y antropofílicas promueven la enfermedad8.
La L donovani puede afectar varios huéspedes vertebrados como los cánidos, roedores e inclusive al hombre2,9. El ciclo de vida del parásito incluye:
- La forma intracelular llamada amastigote, es pequeña de 2-3 mm de diámetro, con un núcelo céntrico y ovalado que posee un cinetoplasto. Tiene una gran capacidad de multiplciación que realiza a través de fisión binaria, generando fácilmente la desintegración de la célula infectada, liberando así nuevos amastigotes que parasitan otras células perpetuando el proceso9.
- La forma promastigota que se encuentra en el vector es más grande y posee un flagelo que le permite migrar al tubo digestivo del mosquito para infectar a los huéspedes9.
Las características clínicas de esta entidad de curso crónico, dependerán de la severidad del compromiso de los órganos que contienen las células permisivas a la multiplicación del parásito como el hígado, bazo y médula ósea, los que resultan frecuentemente afectados. Lo anterior explica la hepatoesplenomegalia y la disfunción medular observadas en los pacientes con leishmaniasis visceral. Las alteraciones causadas a la médula ósea facilitan la aparición de complicaciones secundarias como anemia e inmunosupresión, lo que conlleva a sobreinfecciones en piel, tracto respiratorio o digestivo2,8,10.
Es importante destacar que no todos los individuos que entran en contacto con la leishmania desarrollarán la enfermedad, lo cual actualmente puede explicarse por factores genéticos, que incluyen al complejo mayor de histocompatibilidad u otros genes como el generador de la síntesis de la proteína asociada con la resistencia natural dle macrófago (NRAMP1), cuyo locus se ubica en el cromosoma 2 humano11-14.
Materiales y Métodos:
Hemos revisado los últimos 20 años de infección visceral en el Departamento del Huila, en donde la enfermedad persiste afectando la población pediátrica. Desarrollamos el trabajo de forma descriptiva-retrospectiva.
Pacientes: Se revisaron las historias clínicas de los pacientes que asistieron al servicio de pediatría del Hospital Departamental “Hernando Moncaleano Perdomo” en los últimos 20 años y se establecieron las características clínicas más relevantes.
Se obtuvo un total de 56 casos de leishmaniasis visceral en los niños que consultaron a nuestro hospital.
Diagnóstico: Para realizar el diagnóstico de la entidad se tuvo en cuenta el resultado de aspirado medular, el cual además, en algunos pacientes se realizó al finalizar el tratamiento, para confirmar el control de la infección. En el último año se inició la toma de muestra esplénica para la confirmación parasitológica15.
Tratamiento: Se utilizaron antimoniales pentavalentes específicamente N-metil glucamina en ciclos de 10 a 14 días en dosis de 100 mg de la sal por kilogramo de peso y por día, vía parenteral (IM)4.
Resultados:
Sexo: No hubo diferencia significativa en el sexo de la población afectada. De los 56 casos, 32 (57%) pertenecen al sexo masculino y 24 (43%) al femenino.
Edad: Como se observa en la Tabla No. 1 la mayoría de los casos se presentaron en los primeros dos años de edad.
Tabla No. 1. Distribución etárea 1977 – 1996.

Estado nutricional: Tabla No. 2. Aunque el estudio no permite concluir si el estado nutricional de los niños se asocia o no favorablemente con el curso de la enfermedad, se conoce que la entidad induce un aumento en los requerimientos proteico calóricos con el fin de controlar la infección, po lo cual puede afirmarse que los cursos más severos de la entidd se correlacionan con una progresiva pérdida de peso que se evidencia en el 53,6% de los casos que presentaron por lo menos desnutrición grado l.
Tabla No. 2. Estado nutricional de los casos de leishmaniasis visceral en los útlimos 20 años en el Hospital Departamental “Hernando Moncaleano Perdomo”.

Evolución y tratamiento: Por su cronicidad, la leishmaniasis visceral se constituye en una entidad costosa, pues por lo menos el 50% de los pacientes tuvieron una evolución de más de 1 mes de la enfermedad. El 41% de los pacientes requirió más de 15 días continuos de estancia hospitalaria, lo que aumentó aún más los costos generados por es ta patología. La mortalidad fue del 7.1%, lo que indica que el tratamiento es efectivo, sin embrago, en los últimos años han comenzado a describirse cepas resistentes al glucantime, lo cual aumentaría aún más los gastos y generaría mayor morbimortalidad. El 20% de los casos requirieron dos o más ciclos de la droga para obtener una respuesta favorable.
Discusión:
La leishmaniasis visceral persiste como problema infeccioso crónico en los niños de la región del Huila. La mayoría de los pacientes provienen de la ribera del río Magdalena, probablemente por las características áridas de la región lo que favorece el crecimiento del mosquito vector de la especie Phlebotomus.
La hembra del mosquito al picar al hombre introduce el germen en la forma de promastigote, así el parásito alcanza bien las células dendríticas o los macrófagos dentro de las cuales encuentra condiciones adecuadas para su desarrollo. Una vez en el interior del fagocito, el parásito pasa de promastigote a amastigote e inicia un proceso de división por fisión binaria. En otros casos permanecen quiescentes hasta cuando alguna de las células parasitadas migra al torrente circulatorio y a través de él llega hasta los órganos linfoides secundarios, comprometiendo entonces a otros macrófagos y otras células dendítricas. Al alcanzar un cierto número de parásitos en el interior de las vacuolas fagocíticas generan citolisis y salen al exterior para invadir una nueva célula6,8.
Con miras a combatir la infección, es claro que el sistema inmune intenta destruir las células infectadas, comportándose así el parásito como un antígeno de tipo endógeno. Por esta razón la respuesta predominante será celular citotóxica dirigida por los linfocitos T CD4+ con actividad T1, productores de interferón gamma (IFNg) y factor de necrosis tumoral (TNF). Sin embargo, el parásito modula las condiciones ambientales suficientes para que el linfocito T CD4+ predomine una respuesta T2 humoral de poca efectividad, para controlar el parásito. Por esta razón es indispensable que se sinteticen, dentro de las células infectadas, radicales derivados del oxígeno con alta actividad microbicida. Sin embargo, la demora es instaurar estos mecanismos de control va haciendo crónica la enfermedad.
En cuanto a los signos observados con mayor frecuencia en nuestros pacientes se destacan fiebre y hepatoesplenomegalia, observados en el 100% de los casos. Como ya se ha mencionado el parásito vive con mayor facilidad en el sistema de células dendríticas y macrófagos, en las que induce la síntesis de lagunas citoquinas que promueven el crecimiento celular y por ende el crecimiento de estos órganos. Este hecho facilita el diagnóstico, ya sea por aspirado medular o del bazo, donde se acumulan los amastigotes, sobre todo en este último por la riqueza de células dendríticas foliculares. En la literatura se han descrito nuevos métodos diagnósticos que parecen dar mayor sensibilidad, pero por su complejidad no han sido implementados aún en nuestro medio.
Del mismo modo es importante descartar la presencia de anemia y leucopenia. La anemia como consecuencia de la destrucción promovida por el hiperesplenismo y la leucopenia porque el parásito tiende a bloquear la producción de los factores estimuladores de colonias, puesto que estos tienen la posibilidad de aumentar la actividad antiparasitaria de las células presentadoras de antígeno, especialmente por la producción del óxido nítrico7. Es tan marcada la leucopenia que algunos de nuestros pacientes se complicaron con infecciones secundarias como bronconeumonías y diarreas, entidades que requirieron un tratamiento prolongado (Figura No. 1).
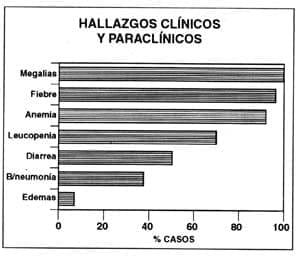
Figura No. 1. Hallazgos de los 56 casos analizados entre 1977 y 1996.
La proteína NRAMP1 aumenta la resistencia del huésped a la infección, pues se relaciona con la explosión oxidativa de los fagocitos como el macrófago, síntesis del óxido nítrico, procesamiento de antígenos y expresión del HLA II y regulación de la producción de citoquinas como el TNFµ , la IL-1b y las quimoquinas. Aunado a que se ha encontrado que algunos individuos tienen mutaciones que el gen de esta proteína, hecho que explciaría su susceptibilidad12-14.
En nuestros pacientes, como era de esperarse no hubo predominio por sexo. Sin embargo, la enfermedad característicamente afectó a menores de 2 años (84.5%). En los menores de dos años existe una expresión reducida del CD21, molécula importante en la activación de los linfocitos B, por su interacción con proteínas del complemento como el C3d y cuya aparición en membrana de las células foliculares dendríticas en el bazo aumenta paulatinamente, factor que se ha correlacionado con una adecuada respuesta inmune contra antígenos tipo polisacárido. Es posible que la interacción del factor del complemento C3d con el CD21 induzca una mejor respuesta inmune frente al parásito, hecho que valdría la pena aclarar.
En síntesis, la leishmaniasis visceral es un problema de salud pública importante en nuestro país que afecta principalmente a los niños menores de dos años, lo cual es un hallazgo nuevo y relevante a tener en cuenta en nuestra población pediátrica. Es necesario realizar más estudios para esclarecer porqué esta patología afecta con más frecuencia a los niños de esta edad.
Bibliografía
1. Coredor A, Ronderos M, et al. Leishmaniasis visceral en Colombia. Boletín epidemiológico nacional 1982; 1-30.
2. Grimaldi G, Tesh R, et al. Distribución geográfica y epidemiológica de la leishmaniasis en el nuevo mundo. Am J Trop Med and Hyg 1989; 687-719.
3. Badaro, James. Estudio prospectivo de leishmaniasis visceral en área endémica en Brasil. J Infect Dis 1986, 154: 639-49.
4. Mayrink W, Araujo P. Diagnóstico do calazar. II-EStudo o teste de montenegro e pesquisa de leishmania em material de pele provenieente de paceintes portadores de calazar, antes e apos terapeutica antimonial. Rev Inst Med Trop Sao Paulo 1971; 13: 268-71.
5. Corredor A, Boshell J, et al. Distribución y etiología de leishmaniasis en Colombia. Amer J Trop Med Hyg 1990, 43(5): 203-43.
6. Descoteaux A, Boshell J, et al. Leishmania donovani lipophosphoglycan selectively inhibits signal transduction in macrophages J Inmunol 1991; 146: 2747-53.
7. Frankernburg S, Leibovici V etal. Effect of glycolipids of leishmania parasites on human monocyte activity. J Inmunol 1990; 145: 4284-9.
8. Walton B. Leishmaniasis. Parasitología y medicina tropical R. Goldsmith and D. Heyneman. México DF, Manual moderno 1995; 361-93.
9. Rodríguez G. Leishmaniasis. Biomédica 1983; 3: 77-99.
10. Evans T, Fatima Fdm et al. American visceral leishmaniasis (Kala-azar). West J Med 1985; 142: 777-81.
11. Chanon J, Blackwell J. Molecular biology of leishmania. Parasitol today 1986; 2: 45-53.
12. Liu J, Fujiyama T et al. Idnetification of polymorphisms and sequence variants in the human homologue of the mouse natural resistance-associated macrophage protein gene. Am J Hum Genet 1995; 56: 845-53.
13. Newport M, Levin M, et al. Evidence for exclusion of a mutation in NRAMP as the cause of familial disseminated atypical mycobacterial infection in a Maltese kindred. J Med Genet 1995; 32: 904-6.
14. Shaw MA, Davies C, et all. Human genetic susceptibility and infection with leishmaniasis peruviana. Am J Hum Gen 1995; 57: 1159-68.
15. Sypek J, Wyler D. Antileishmanial defense in macrophages triggered by tumor necrosis factor expressed on CD4+ T lymphocyte plasma membrane. J Exp Med 1991; 44: 390-3.
