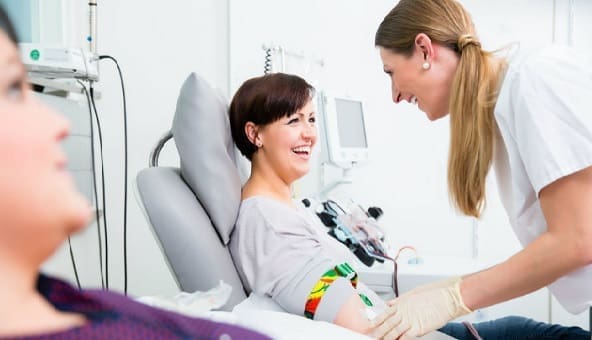
Intervención de enfermería
Free Topics: The patient with continuous venovenous hemofiltration. Nursing intervention
Resumen
En la Unidad de Cuidados Intensivos es frecuente encontrar pacientes que por diversas causas renales y no renales precisan la hemofiltración Veno-venosa continua, una técnica que requiere la intervención de enfermería con el fin de prevenir complicaciones derivadas del paciente o del procedimiento.
Este artículo expone un proceso completo de enfermería, propone diagnósticos, objetivos, actividades y evaluación del mismo con el fin de hacerlo exitoso.
Se realizó una revisión bibliográfica en donde se seleccionaron 11 artículos buscando que respondieran a los objetivos planteados: describir acciones específicas de cuidado de enfermería frente al paciente en estado crítico con hemofiltración veno-venosa continua antes, durante y después del tratamiento.
Se concluye que dentro de las complicaciones descritas por los diferentes autores se encuentran las relacionadas con el acceso vascular, disfunción mecánica, trombosis, hemorragia e infección, las cuales son prevenibles mediante la planeación y ejecución de un proceso de enfermería.
>> Ver: Beneficios para Médicos en la Compra de su Carro <<
Palabras clave:
Hemofiltración veno-venosa continua, proceso de enfermería, cuidado crítico.
Abstract
In the UCI one frequently encounters patients that require veno-venous hemofiltration for diverse causes, renal and no renal, a technique that demands nursing intervention oriented to the prevention of complications arising in the patient himself or herself or in the procedure. This article presents a complete nursing process, proposes diagnoses, objectives, activities, and evaluation, all oriented toward making the procedure successful.
Eleven articles were selected from a literature search, seeking that they responded to the proposed objectives: to describe specific nursing care actions for the patient in critical condition under continuous veno-venous hemofiltration, before, during, and following treatment.
It is concluded that among the described complications reported by the different authors appear those related to vascular access, mechanical dysfunction, thrombosis, hemorrhage, and infection, which are all preventable by careful planning and execution of he nursing process.
Key words:
Continuous veno-venous hemofiltration, nursing process, critical care.
Introducción
Hemofiltración Veno-venosa Continua
La hemofiltración veno-venosa continua es una medida terapéutica que se utiliza en pacientes en estado crítico por diversas causas, renales o no renales. Es una terapia que requiere maquinaria y equipos específicos y que como todo procedimiento puede acarrear complicaciones, las cuales pueden ser prevenibles mediante la planificación de cuidados de enfermería.
Estudio de revisión documental donde se seleccionaron 10 artículos escritos por enfermeros y médicos intensivistas desde el año 2000 y se basa el análisis y recopilación de información acerca de las actividades específicas que se llevan a cabo antes, durante y después de este procedimiento.
Pretende planear un proceso de enfermería frente a la hemofiltración veno-venosa continua en el paciente en estado crítico, con el fin de evitar posibles complicaciones descritas según la bibliografía encontrada.
Definiciones
Hemofiltración Veno-venosa Continua
Intervención de Enfermería
Acciones específicas que el profesional en enfermería realiza al paciente con hemofiltración veno-venosa continua antes, durante y después del procedimiento, mediante la planeación y ejecución de un proceso de enfermería; conformado por diagnóstico, objetivos actividades y evaluación, con el fin de evitar complicaciones y hacer de éste un procedimiento exitoso.
Paciente en Estado Crítico
Es aquella persona que presenta cambios agudos en los parámetros fisiológicos y bioquímicos que lo ponen en riesgo de morir, pero tiene posibilidades evidentes de recuperación.
Hemofiltración Veno-Venosa Continua
Terapia sustitutiva de la función renal que se realiza en forma ininterrumpida y consiste en hacer circular la sangre del paciente por una membrana para obtener un ultrafiltrado del plasma.
Marco Teórico
Hemofiltración Veno-venosa Continua
La idea de utilizar la hemofiltración veno-venosa continua (HVVC), surge a partir de una publicación por Lauery colaboradores (1) en 1983, donde describían el método y su utilidad en el tratamiento del paciente en estado crítico con insuficiencia renal aguda.
En la actualidad, la hemofiltración continua es una técnica que gracias a una eliminación lenta y continuada de ultra filtrado, permite un buen control del balance hidroelectrolítico en pacientes con fracaso renal y oliguria, con una buena tolerancia hemodinámica en pacientes en estado crítico, convirtiéndose en una técnica ampliamente utilizada en las unidades de cuidado intensivo.
La hemofiltración veno-venosa continua es una terapia sustitutiva de la función renal que se realiza en forma ininterrumpida en la cual se realiza una remoción del plasma, agua y solutos, la cual ocurre por convección y ultra filtración.
Objetivos de la HVVC
- Proveer una adecuada purificación sanguínea de las toxinas urémicas.
- Permitir la corrección del desequilibrio hidroelectrolítico y ácido básico.
- Acelerar la recuperación de la funciona renal después de la insuficiencia renal aguda.
- Eliminación de mediadores inflamatorios en pacientes con sepsis.
Ventajas de la hemofiltración veno-venosa continua en la unidad de cuidados intensivos
A medida que la hemofiltración veno-venosa continua se ha utilizado en el paciente crítico, se han encontrado diversas ventajas:
- Evita cambios bruscos de volemia porque es un tratamiento lento y continuo, lo cual permite una mayor estabilidad hemodinámica en el paciente en estado crítico.
- La eliminación gradual y continua de agua y metabolitos tóxicos permite gran flexibilidad electrolítica, mejor control metabólico al tiempo que la concentración de electrolitos se puede aumentar o disminuir de forma gradual e independiente de los cambios en el volumen corporal.
- Permite la aclaración de sustancias circulantes de peso molecular medio alto como los mediadores de inflamación citoquinas, anafilotoxinas, involucrados en la patogénesis del síndrome de distrés respiratorio agudo y el síndrome de disfunción multiorgánica.
Complicaciones
Hemofiltración Veno-venosa Continua
La hemofiltración veno- venosa continua, por ser una técnica invasiva y de depuración extracorpórea, está sujeta a complicaciones que se pueden clasificar en dos grupos: las que dependen del sistema o la técnica y las que están relacionadas con la clínica del paciente.
Complicaciones técnicas
Hemofiltración Veno-venosa Continua
Acceso vascular
Las venas deben ser de grueso calibre que permitan el uso de catéteres de diámetro elevado y disminuir las resistencias del mismo. El inadecuado funcionamiento temprano del catéter puede deberse a una incorrecta posición del mismo, ligadura a tensión o acodamiento repetido. El tardío está causado por trombosis endoluminal, venosa o distal del catéter.
Otras complicaciones como el sangrado, hematoma en el punto de inserción, se pueden deber a técnica de punción inadecuada o a falta de compresión al retiro del catéter. La obstrucción del catéter depende del material, tamaño, longitud, resistencia y técnica de inserción. La utilización cuidadosa de la anticoagulación, una técnica de inserción adecuada y los cuidados posteriores del catéter, reducen sus complicaciones, a las cuales el especialista de enfermería debe estar atento.
Recirculación
Este fenómeno ocurre cuando se hemofiltra la sangre ya hemofiltrada con el inconveniente de la pérdida de eficacia del tratamiento. El catéter femoral corto presenta el grado más alto de recirculación. Cuando se conecta se debe tener especial atención en no invertir las luces ya que esto aumenta la recirculación.
Desconexión de las líneas
La desconexión accidental pone en peligro la vida del paciente. Puede deberse a pacientes inquietos poco controlados, a una sutura inapropiada a la piel o malas conexiones. En caso de que esto ocurra se debe parar la bomba y pinzar los extremos de las líneas y el catéter y volver a conectar.
Embolismo aéreo
Esta complicación puede ser consecuencia de la ruptura o desconexión del catéter. Los síntomas y signos que presenta el paciente son: cianosis, de-saturación de oxígeno, insuficiencia respiratoria, alteración del estado de conciencia, enfermedad cerebrovascular aguda. Se debe cambiar de inmediato la línea e interrumpir la hemofiltración hasta tanto se solucione el problema.
Otras causas que puede producir aire en el sistema, pueden ser: un purgado incompleto, que la línea de retorno no esté bien instalada en el detector de aire, en cuyo caso, se debe pinzar el catéter, desconectar las líneas y recircular el sistema, frente a la sospecha de embolismo aéreo colocar al paciente en posición Trendelemburg lateral izquierdo.
Coagulación del hemofiltro
La coagulación del hemofiltro es la causa principal de recambio del sistema. Para evitar la obstrucción prematura por coágulos es fundamental establecer una pauta de anticoagulación dependiente de los valores previos de PTT Y PT.
Para alargar la vida media del hemofiltro es importante realizar un adecuado purgado de todo el circuito y en especial del dializador, con el fin de eliminar el aire del sistema (ya que favorece la coagulación) e impregnar las membranas del filtro con solución heparinizada.(2)
Complicaciones Clínicas
Hemofiltración Veno-venosa Continua
Sangrado
Las características del paciente, el tipo de membrana y la permeabilidad, la utilización de la bomba y el tipo de anticoagulante, determinarán el riesgo de sangrado. Una cuidadosa anticoagulación es el factor fundamental para prolongar la supervivencia del filtro y reducir el sangrado.
La elección del anticoagulante dependerá del paciente, la técnica de diálisis y la disponibilidad de los tratamientos.
Puede aparecer sangrado al final de la terapia al retiro del catéter temporal, por lo que se debe hacer compresión de forma continuada.
Reacciones alérgicas
Algunas membranas con menor biocompatilibidad, la silicona de los tubos de conexión o el óxido de etileno utilizado como esterilizante del circuito extracorpóreo, pueden producir reacciones alérgicas e incluso shock anafiláctico.
Trombosis
La posibilidad de trombosis vascular parece ser más frecuente de lo que clínicamente se sospecha.
Existen algunos factores de riesgo como: edad avanzada, ateroesclerosis y lesión vascular por mala técnica.
La vena subclavia es la de mayor riesgo para estenosis y trombosis tardía. Si se presenta puede disminuir críticamente la perfusión del miembro donde se encuentra el catéter. Se recomienda controlar la perfusión distal.
Infección
El origen más frecuente es el catéter. El riesgo de infección aumenta a partir del cuarto día. En general existe correlación entre la flora cutánea y el catéter vía femoral y subclavia.
Se recomienda manipular de forma estéril el circuito extracorpóreo, cambiar las líneas y los filtros cada 24 horas, incluso si estos siguen funcionando bien, pues es una medida importante para prevenir la infección y la sepsis secundarias al circuito extracorpóreo.
Hipotensión
Es la complicación más frecuente en los primeros momentos del tratamiento. La estabilidad cardiovascular está relacionada con la membrana. Otros factores son: la depleción hidrosalina previa, efecto del tratamiento hipotensor previo, hipoxia tisular, e incluso, la temperatura elevada del líquido de reposición puede provocar vasodilatación.
La hipotensión suele responder en forma rápida a las maniobras habituales (reposición, volumen, posición de Trendelemburg) y al disminuir la tasa de ultra filtrado, sin tener que disminuir el flujo de sangre a no ser que no haya respuestas a las medidas previas.
Hipertensión
Se puede producir por: estimulación renina-angiotensina por hipovolemia, eliminación por el ultra filtrado del tratamiento antihipertensivo, hipercalcemia que favorecerá la contractibilidad miocárdica y el tono vascular.
Agua y sodio
Tanto la hipervolemia como la deshidratación son fáciles de prevenir ajustando de manera adecuada las pérdidas deseadas y el volumen de reposición.
Arritmias
Están en relación con trastornos bruscos del equilibrio ácido-base, electrolitos o hipoxia. Son más frecuentes en pacientes mayores de 55 años y antecedentes de cardiopatía isquémica.
Anemia y hemólisis
El paso continuo de sangre a través del sistema extracorpóreo puede producir hemólisis, hemorragia aguda y causar anemia progresiva.
Alteraciones metabolismo-catabolismo
En las terapias de reemplazo renal continuo, se producen pérdidas de aminoácidos por el filtro (hasta 30%), glucosa (6,8 g/día), proteínas musculares cuando se interacciona sangre-membrana, además de la vitamina C y ácido fólico.
Alteraciones del balance de líquidos, electrolitos y equilibrio ácido-base
El balance líquido y electrolítico del paciente depende de la composición del líquido de reposición y de la tasa de ultra filtrado. Es obligatorio monitorizar y registrar en forma meticulosa la entrada y salida de líquidos. Debe tenerse cuidado con los posibles errores de registro.
Electrolitos
Durante la terapia de reemplazo renal continuo hay pérdida de K+ (potasio) intra y extracelular. Si el paciente no está hipercalémico, debe añadirse potasio al líquido de reposición para evitar la hipocalemia y el consiguiente riesgo de arritmia. También disminuyen el calcio, magnesio y el fósforo.(3)
Autor
Hemofiltración Veno-venosa Continua
* Liz Beth Mendivelso. Enfermera especialista en Cuidado Crítico de la Pontificia Universidad Javeriana. Unidad de Cuidado Intensivo, Hospital Universitario Fundación Santa Fe de Bogotá.
** Norma Cecilia Hurtado. Enfermera especialista en Cuidado Crítico de la Pontificia Universidad Javeriana. Salas de Cirugía Fundación Cardio infantil, Bogotá, D.C., Colombia.
Correspondencia: lizmv@hotmail.com