11 Módulo 7. Transfusión de Plaquetas: Una Guía de Práctica Clínica de la AABB14
Aproximadamente 2,2 millones de dosis de plaquetas se transfunden anualmente en los Estados Unidos (1).
Una alta proporción de estas unidades de plaquetas se transfunden profilácticamente para reducir el riesgo de sangrado espontáneo en pacientes que son trombocitopénicos después de la quimioterapia o trasplante de células progenitoras hematopoyéticas (CPH) (1-3).
A diferencia de otros componentes de la sangre, las plaquetas deben almacenarse a temperatura ambiente. Limitando su vida útil a sólo 5 días debido al riesgo de crecimiento bacteriano durante el almacenamiento. (Ver también: Neonatal y Pediatría en el Uso de Componentes Sanguíneos)
Por lo tanto, mantener inventarios de plaquetas en los hospitales es logísticamente difícil y demanda recursos elevados (4-6). La transfusión de plaquetas está asociada con varios riesgos para el receptor (Tabla 8), incluyendo reacciones alérgicas y febriles no hemolíticas.
La sepsis resultante de una unidad de plaquetas contaminada con bacterias representa la complicación infecciosa más frecuente de cualquier producto de sangre hoy en día (7-8). En cualquier situación en la que se esté considerando la transfusión de plaquetas. Estos riesgos deben ser equilibrados con el potencial de beneficios clínicos.

Definiciones
En esta guía, una unidad de plaquetas se refiere a 1 unidad de plaquetas por aféresis o un grupo de 4 a 6 concentrados de plaquetas provenientes de sangre total, que típicamente contienen de 3 a 4 x1011 plaquetas.
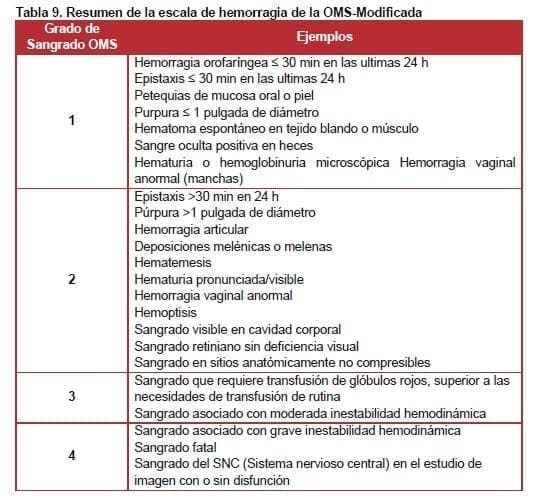
La trombocitopenia se refiere a un recuento plaquetario debajo del límite inferior del rango normal utilizado por el laboratorio que realiza el conteo. Siete ensayos con plaquetas incluidos en la revisión sistemática (15-21) utilizaron una escala de la Organización Mundial de la Salud (22) para determinar los desenlaces de sangrado del paciente (23).
Un resumen de la escala modificada de la Organización Mundial de la Salud se presenta en la Tabla 9.
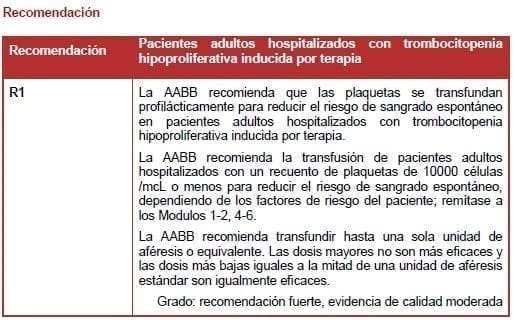
11.1 Pacientes adultos hospitalizados con trombocitopenia hipoproliferativa inducida por terapia
Resumen de la evidencia
Tres ECA (n=1047) compararon los desenlaces de sangrado en pacientes hospitalizados con radiación y/o trombocitopenia hipoproliferativa inducida por quimioterapia asignados para recibir o no recibir tratamiento profiláctico de transfusión de plaquetas (19, 21, 24, 25). Todos los pacientes tenían malignidad hematológica tratados con quimioterapia o CPH.
Las transfusiones de plaquetas profilácticas redujeron significativamente el riesgo de sangrado espontáneo grado 2 o mayor (odds ratio [OR], 0,53 [IC del 95%, 0,32 a 0,87]). La mayoría de los eventos hemorrágicos se clasificaron como grado 2.
En los 2 ensayos más grandes (19,21), la hemorragia de grado 2 o mayor presentada en los pacientes asignados al grupo que no recibió la profilaxis ocurría con mayor frecuencia entre pacientes que recibieron quimioterapia para la leucemia aguda en comparación con los receptores autólogos de CPH (58% vs.47% (19, 25); 51% vs. 28% [21]).
La cifra umbral de recuento de plaquetas en la cual las plaquetas deben ser transfundidas profilácticamente para reducir el riesgo de hemorragia en pacientes hospitalizados con trombocitopenia hipoproliferativa inducida por terapia se determinó en 4 ECA (n =658).
Los pacientes fueron asignados para recibir transfusión profiláctica de plaquetas en un conteo matutino menor a 10.000 células /μL vs 20.000 células /μL (10×109 vs 20×109 células/L) (26-28) o 30.000 células /μL (30 x109 células/L) (15).
Un umbral de recuento mayor de plaquetas (20 x109 células/L o 30 x109 células/L) no se asoció con una incidencia significativamente menor de sangrado grado 2 o mayor (OR, 0,74 [IC, 0,41 a 1,35]) o mortalidad relacionada con sangrado (OR, 0,37 [IC, 0,02 a 9,22]).
El número total de días con sangrado fue mayor en el grupo umbral de 10.000 células /μL (10 x109 células/L).
El umbral de 10.000 células/μL (10×109 células/L) se asoció con menor uso de plaquetas y menos reacciones transfusionales.
Cuatro ECA (n=1132) examinaron si las medidas transfusionales profilácticas de plaquetas de dosis bajas (definidas como la mitad de la dosis estándar de 3 a 4 × 1011 plaquetas) proporcionaría una hemostasia igual a la de plaquetas de dosis estándar en pacientes trombocitopenia hipoproliferativa inducida por terapia (16, 18, 20, 29).
No hubo diferencias en la hemorragia grado 2 o mayor en receptores de dosis estándar vs dosis bajas de plaquetas (OR, 0,91 [IC, 0,70 a 1,19]).
Altas dosis de plaquetas (aproximadamente el doble de la dosis estándar) se compararon con la dosis estándar de plaquetas en 2 ECA (n=951) (17, 18). La transfusión profiláctica de dosis altas de plaquetas no redujo el riesgo de sangrado en comparación con plaquetas de dosis estándar de plaquetas (OR, 1,05 [IC, 0,79 a 1.40]).
(Lea También: Pacientes Adulto Mayor con Cirugía Programada no Neuroaxial)
11.1.1 Justificación de las recomendaciones
Antes de introducir la profilaxis plaquetaria rutinaria, la hemorragia grave fue una causa común de muerte entre los pacientes que reciben quimioterapia de alta dosis (30,31). Hoy en día, la hemorragia grave se encuentra raramente en esta configuración.
Los estudios originales de profilaxis plaquetaria se realizaron hace décadas, y tanto la quimioterapia como la atención para pacientes con cáncer han cambiado dramáticamente con el tiempo.
Por lo tanto, los ensayos aleatorizados realizado por Wandt (21) y Stanworth (19) y sus colegas fueron diseñados para responder a la pregunta de si una estrategia profiláctica comparada con una estrategia terapéutica de transfusión de plaquetas brinda beneficios en el cuidado contemporáneo del cáncer.
En el estudio de Wandt y colegas (21), la hemorragia de grado 2 o mayor se observó en el 42% de los pacientes asignados a recibir transfusiones terapéuticas de plaquetas solamente. En comparación con el 19% de los pacientes asignados para recibir transfusión profiláctica de plaquetas para un recuento de plaquetas de 10×109 células/L o menos (p < 0,001).
También, en el subgrupo de pacientes con leucemia mieloide aguda, la hemorragia intracerebral (grado 4) se presentó significativamente más a menudo en el grupo que recibió plaquetas terapéuticas comparado con el que recibió plaquetas profilácticas (7% vs 2%, p = 0,010).
En 11 de 13 casos, el sangrado fue detectable en la tomografía computarizada, pero no había aparentes secuelas clínicas.
La tomografía computarizada solo se solicitó para investigar un nuevo dolor de cabeza u otros síntomas cerebrales en los pacientes del grupo plaquetario terapéutico:
Por lo que la hemorragia subclínica intracerebral en el grupo que recibió tratamiento profiláctico de plaquetas pudo haber sido sub diagnosticada. En el Estudio de Plaquetas Profilácticas (19). Se observaron diferencias más sutiles en los resultados de sangrado entre los grupos de estudio.
Se presentaron hemorragias Grado 2 o mayores en el 50% de los pacientes asignados al grupo que no recibió profilaxis. En comparación con el 43% de los pacientes que recibieron transfusión profiláctica de plaquetas (P = 0,06 para no inferioridad).
En pacientes recibiendo quimioterapia (no CPH), hubo un aumento significativo de la hemorragia de grado 2 o mayor en el grupo que no recibió profilaxis (diferencia de riesgo, 20% [IC del 90%, 7,9% a 32,2%]).
También hubo una tendencia no significativa hacia el aumento de hemorragia grados 3 y 4 para todos los pacientes del grupo que no recibió profilaxis. Así, tanto las conclusiones de Wandt como el estudio de plaquetas profilácticas apoyan las transfusiones profilácticas de plaquetas en pacientes con trombocitopenia hipoproliferativa inducida por terapia.
Transfusión profiláctica de plaquetas
En esta población, se recomienda la transfusión profiláctica de plaquetas para un recuento de plaquetas matutino de 10.000 células /μL (10×109 células/L) o menos.
Algunos datos sugieren que el riesgo de sangrado no aumenta hasta que el recuento de plaquetas disminuye a menos de aproximadamente 6.000 células/μL (6×109 células/L) (18, 32). Pero el umbral del recuento plaquetario de 10.000 células/μL (10×109 células/L) parece proporcionar un buen equilibrio de seguridad y practicidad. Además, la precisión del recuento de plaquetas extremadamente bajo es cuestionable (33, 34).
La recomendación para la transfusión profiláctica de plaquetas basada en un umbral de recuento de plaquetas de 10.000 células/μL (10×109 células/L) sólo se aplica a pacientes hospitalizados.
La transfusión profiláctica de plaquetas basada en un umbral de conteo plaquetario mas liberal (mayor) puede ser apropiado cuando se tratan pacientes ambulatorios, por razones prácticas (menos visitas clínicas).
El estudio Dosis de Plaquetas (18) estableció que los pacientes que reciben transfusiones profilácticas de plaquetas en bajas dosis, con un recuento de plaquetas matutino de 10.000 células/μL (10×109 células/L) o menos tenían el mismo riesgo de hemorragia que los pacientes que recibían dosis de plaquetas estándar o elevadas.
Sin embargo, la transfusión de dosis bajas de plaquetas requería mayor número de transfusiones -más frecuentemente- debido a que proporcionaban un incremento más bajo.
Es seguro ofrecer bajas dosis de plaquetas como profilaxis a pacientes con trombocitopenia hipoproliferativa inducida por terapia, bien sea de forma rutinaria o como una maniobra temporal para los momentos de escasez de plaquetas. No se ha demostrado que las transfusiones profilácticas de plaquetas en dosis altas proporcionen beneficios adicionales. Por lo que no se recomiendan como terapia de rutina para pacientes hospitalizados.
11.2 Pacientes adultos con procedimientos invasivos menores
Resumen de la evidencia
Se identificaron ocho estudios observacionales de colocación de catéter venoso central (CVC) en el escenario de trombocitopenia (n=1.311 canulaciones) (12, 35-41). Muchos de los pacientes tenían leucemia aguda o estaban en proceso de trasplante de células progenitoras hematopoyéticas (CPH); sin embargo, pacientes con insuficiencia renal, pacientes críticamente enfermos, y otros fueron incluidos. Las tasas de complicación general por hemorragia fueron bajas, oscilando entre el 0% y el 9% de los catéteres colocados.
La serie más grande de catéteres venosos no tunelizados incluyó 604 canulaciones en 193 pacientes consecutivos (41).
En el análisis multivariado, sólo los pacientes con recuentos de plaquetas pre-procedimiento inferior a 20.000 células/μL (20×109 células/L) (n=93) tenían un mayor riesgo de sangrado en comparación con pacientes con recuentos de plaquetas mayores a 100.000 cel/μL (100×109 células/L). El 96% de los episodios hemorrágicos fueron grado 1, y el 4% restante de grado 2, requiriendo sólo compresión local.
En otro estudio unicéntrico, los resultados de sangrado fueron notificados en 3.170 catéteres venosos tunelizados guiados por ecografía sometidos a ultrasonografía en 2.512 pacientes (38).
No se produjeron complicaciones hemorrágicas en las 344 implantaciones de CVC realizadas con un recuento de plaquetas previo al procedimiento de menos de 50.000 células/μL (50×109 células/L), incluyendo 42 casos con un recuento de plaquetas menor a 25.000 células/μL (25×109 células /L).
Se evaluaron los datos de 7 estudios observacionales de niños o adultos trombocitopénicos:
A quienes se les realizó punción lumbar diagnóstica y/o terapéutica (PL) (42-49). El más grande fue un estudio observacional unicéntrico con 5.223 PL en 956 pacientes pediátricos con leucemia linfoblástica aguda (45).
Se realizaron un total de 199 PL con recuentos plaquetarios de 20.000 células/μL (20×109 células /L) o menos, y 742 PL con recuento de plaquetas entre 21.000 células/μL (21×109 células/L) y 50.000 células/μL (50×109 células/L).
No se observaron complicaciones por sangrado, independientemente del recuento de plaquetas. Con un IC del 95%, las complicaciones serias se presentaron en el 1,75% de pacientes con recuento de plaquetas de 20.000 células/μL (20×109 células /L) o menos y; 0,37% en pacientes con recuentos de plaquetas de 50.000 células/μL (50×109 células/L) o menos.
Las punciones lumbares traumáticas (> 500 glóbulos rojos por campo de alto poder) ocurrieron en el 10.5% de los procedimientos, pero no se asoció con los resultados clínicos. Las series reportadas más grandes en adultos incluyeron 195 PL diagnósticas o terapéuticas en 66 pacientes adultos con leucemia aguda y trombocitopenia (49).
Los pacientes fueron transfundidos profilácticamente con plaquetas para un recuento de plaquetas pre-procedimiento inferior a 20.000 células/μL (20×109 células /L). Se realizaron 35 PL en pacientes con recuentos plaquetarios de 20.000 a 30.000 células/μL (20×109 a 30×109 células/L), y 40 se realizaron con recuentos plaquetarios de 31.000 a 50.000 células/μL (31×109 a 50×109 células /L). No se observaron complicaciones hemorrágicas.
11.2.1 Justificación de las recomendaciones
Las complicaciones hemorrágicas graves después de la colocación del CVC son raras, y cuando ocurren, a menudo no están relacionados con el recuento de plaquetas (como en el caso de la punción arterial accidental). En conjunto, los datos existentes respaldan el uso de un umbral de recuento de plaquetas de 20.000 células/μL (20×109 células/L) para la implantación de CVC.
Los estudios informados incluyeron pacientes con una amplia gama de diagnósticos primarios; esta recomendación pretende ser ampliamente aplicable a pacientes adultos con trombocitopenia hipoproliferativa.
Las complicaciones hemorrágicas son raras en la PL, pero la hemorragia en cualquier parte del sistema nervioso central (SNC) tiene potencial para causar secuelas neurológicas devastadoras.
En la ausencia de mejores datos publicados que respalden la seguridad de un umbral más bajo en pacientes adultos, parece prudente utilizar un umbral moderadamente liberal de recuento de plaquetas para la PL, esto es, 50.000 células/μL (50×109 células/L).
El umbral de 50.000 células /μL (50×109 células /L) está destinado solamente a PL simples diagnósticas o terapéuticas. A pesar de la falta de datos de soporte, un mayor recuento de plaquetas se recomienda a menudo para otros procedimientos, como la anestesia epidural (50, 51).

14 Las tablas de evidencia pueden consultarse en la guía original