Dr. Juan Fernando Uribe Arcila
Urólogo – Hospital Pablo Tobón – Medellín
Miembro de Número Sociedad Colombiana de Urología
¿Por qué las metástasis del adenocarcinoma prostático son al hueso?
¿Por qué son blásticas?
¿Por qué el hueso es frágil y quebradizo?
El Adenocarcinoma prostático (CAP), es una buena parte del trabajo del urólogo y aunque cada vez tenemos más información sobre cómo mejorar el diagnóstico y cómo enfocar el tratamiento, desconocemos en forma crasa fragmentos de la fase final de la enfermedad, especialmente en lo que se refiere a metástasis y hormono resistencia, que son el terreno fangoso donde ignoramos más información.
Gregory Mundy el endocrinólogo inglés experto en el metabolismo del hueso escribió alguna vez con muy buen sentido, que “las metástasis óseas son una complicación catastrófica para la mayoría de pacientes con cáncer. No solamente porque son causa de un dolor intratable, de fracturas luego de traumas triviales y compresión de la médula espinal, sino porque significan que el proceso maligno es incurable.”1
Confirmando lo anterior, estas son las cifras asociadas con las metástasis óseas:2,3,4,5
- Antes de la existencia del PSA el 50% de los pacientes tenían al diagnóstico metastasis óseas.
- Luego de la popularización del PSA el16% de los pacientes tienen al diagnóstico metástasis óseas.
- La incidencia de metástasis óseas para tumores en general (No prostáticos) es 15-30%.
- Incidencia de metástasis óseas para CAP en particular es 50 – 70%.
- La incidencia de metástasis óseas para CAP avanzado es 80% – 100%.
- De los pacientes con metástasis óseas solo el 25% alcanzan los 5 años de supervivencia y la mediana de supervivencia es de apenas 40 meses.
- 28.900 hombres murieron en USA en el año 2004 por CAP.
- Lo cierto es que nadie muere de CAP sin tener metástasis distantes, de las cuales las más frecuentes son las óseas.
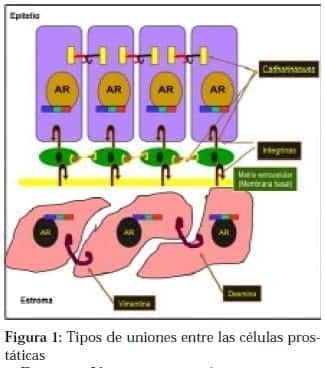
Para comprender adecuadamente el proceso de la metástasis del CAP, es necesario darles un vistazo a los tipos de uniones normales presentes en las células prostáticas, ya que su disolución es fundamental para que las células cancerosas puedan viajar por el torrente sanguíneo.
Los tipos de unión son los siguientes: (Ver figura 1)2,3,4,5,6,7
 Desmina: Uniones estromales
Desmina: Uniones estromales- Vimentina: Uniones estromales
- Integrinas: Células basales a matriz extracelular
- Cadherinas: Integración célula a célula
- La Desmina y Vimentina: Son responsables de la unión estromal (Entre células del músculo y fibroblastos).
- Las Caderinas hacen la Integración celular (de célula a célula) en la capa epitelial y en las basales entre sí y entre células basales y células epiteliales.
- Integrinas: Unión de células basales a la matriz extracelular (MB).
- Lamininas: Unión a la membrana basal del epitelio.
- Fibronectina: Unión de fibroblastos a membrana basal (Matriz).
- Selectinas: Permiten reptar a las células (y lograr su unión a carbohidratos).
- Chaperoninas: Conducen a las proteínas que se forman por acción en el AR.
El ambiente óseo
El hueso es una mezcla de minerales como hidroxiapatita, más cristales de calcio amorfo que corresponden a dos tercios de su peso y una matriz ósea mezcla de colágeno y agua con proteínas como osteonectina, fibronectina, vitronectina, osteocalcina, osteopontina, sialoproteina ósea y factores de crecimiento idénticos a los del tejido prostático como TGF B e IGF-I que corresponden a un tercio del peso. (Figura 2)2,4,8,9
 El hueso posee dos tipos de células fundamentales:
El hueso posee dos tipos de células fundamentales:
a. Los Osteoblastos
Que son las células formadoras de hueso nuevo, que se originan en las células mesenquimatosas. Los osteoblastos dependen para su desarrollo de factores de crecimiento, ya reconocidos en la próstata como el TGF beta, que en realidad son 15 subtipos y constituyen una superfamilia, el FGF (Factor estimulante de fibroblastos), el PDGF (Factor estimulante de plaquetas) y otros como los BMP (Factores morfogénicos de hueso).
Todos son capaces de inducir formación de hueso ectópico in vivo. (Figura 3)2,4,8,9
Más información de Cáncer de Próstata Parte II
- El Fenotipo Metastásico en el Cáncer de Próstata
- El Fenotipo Hormonoresistente en el Cáncer de Próstata
- Carcinoma Neuroendocrino en el Cáncer de Próstata
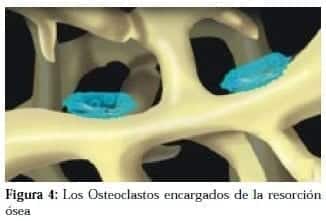
b. Los Osteoclastos
Son células multinucleadas de borde aserrado, encargadas de la resorción del hueso, originadas en células sanguíneas (los monocitos). Están afectadas por múltiples substancias sistémicas y locales que pueden activarlos o inhibirlos: (Figura 4)
 • Factores sistémicos inhibitorios:
• Factores sistémicos inhibitorios:
Calcitonina, testosterona y estrógenos
• Factores locales inhibidores:
TGF-B, Interleukinas 4 y 10, Interferón gama, y Osteoprotegerina
• Factores sistémicos estimuladores:
Hormona paratiroidea (PTH), factor de crecimiento relacionado con la PTH, calcitriol y Tiroxina
• Factores locales estimulantes:
Interleukinas 3-11, factores de necrosis tumoral alfa y beta, RANKL.
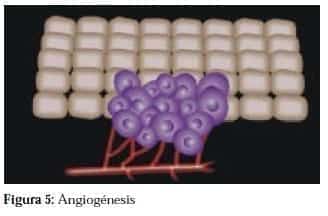
La segunda misión del tumor, luego de desarrollarse en sí mismo, es crear sitios independientes de crecimiento (metástasis). Para cumplir con esta misión requieren de autopistas para viajar, por tanto, hacen sus rutas mediante la angiogénesis. Para el reclutamiento de vasos el tumor produce endotelina 1 (ET1), factor de crecimiento epidérmico vascular (VEGF) y factor de crecimiento relacionado con las plaquetas (PDGF). (Figura 5)2,4,8,9
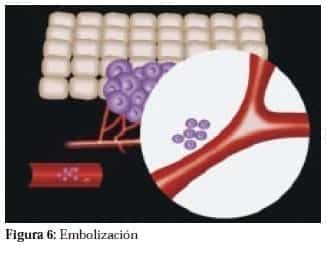
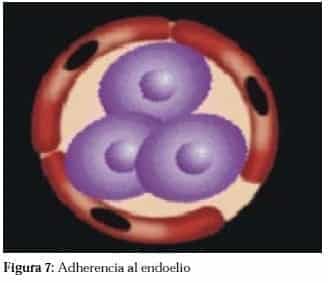
 Posteriormente al angiogénesis viene un fenómeno de embolización de las células tumorales a los vasos sanguíneos (Figura 6) y de adherencia de las células tumorales al endotelio vascular (Figura 7).
Posteriormente al angiogénesis viene un fenómeno de embolización de las células tumorales a los vasos sanguíneos (Figura 6) y de adherencia de las células tumorales al endotelio vascular (Figura 7).
 |
 |
El tumor produce MMP2 (Matrix metaloproteinasa 2) como se mencionó en la primera parte (Ver “progresión del tumor” en la parte I), que es capaz de digerir la membrana basal, facilitando la invasión de tejidos y la embolización por el torrente sanguíneo. Hasta aquí podrían viajar a cualquier sitio del organismo, no necesariamente al hueso.
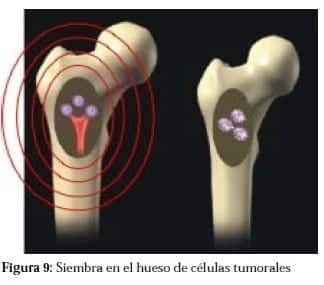
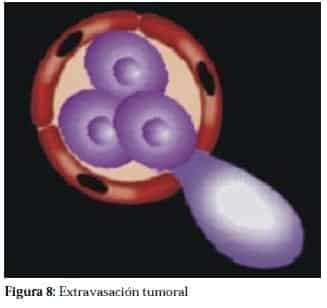
Luego las células hacen extravasación de las células tumorales (Figura 8) y la siembra en un terreno apropiado (Figura 9), en este caso el hueso, siguiendo la teoría de “seed and soil” (semilla-terreno) que tiene una asombrosa semejanza con la parábola bíblica del sembrador.
 |
|
¿Por qué el hueso?
La matriz ósea, los factores de crecimiento y las proteínas de la matriz ósea, son la clave de por qué la avidez del tumor de próstata por el hueso. En otras palabras, las células se extravasan desde los vasos sanguíneos donde les gusta, en un ambiente fértil para el tumor.
Una vez sembradas las otras células del tumor que siguen produciendo metástasis desde la fuente primaria, buscarán las células embolizadas al hueso.2,3,4,8,10
El microambiente dentro de la matriz ósea representa normalmente el balance entre el proceso de formación por osteoblastos y la remodelación por osteoclastos. Una vez dentro de ese microambiente, las células tumorales son capaces de producir factores bioquímicos que causan resorción del hueso, por estimulo de los osteoclastos y/o formación de hueso por estímulo de los osteoblastos.
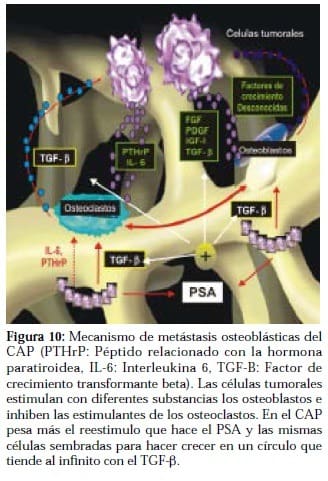
El péptido relacionado con la hormona paratiroidea (PTHrP) junto con la interleukina 6 (IL-6) que es la principal de las citoquinas, son capaces de hacer fértil el terreno del hueso para la siembra de células tumorales. Ella estimula los osteoclastos y por tanto la osteolisis del hueso, por lo tanto, debe estar activada en las metástasis líticas, pero inactivada en las metástasis blásticas para permitir la producción de hueso. (Figura 10)
 Una vez sembradas, las células tumorales prostáticas en el hueso producirán las mismas substancias para perpetuar el ciclo.
Una vez sembradas, las células tumorales prostáticas en el hueso producirán las mismas substancias para perpetuar el ciclo.
En el caso de las metástasis blásticas, el TGF-B (que es muy abundante en el hueso) será estimulado por las proteasas, como el Antígeno específico de próstata PSA, producido en el mismo hueso invadido, cumpliendo la función de activar los osteoblastos e inhibir el PTHrP activadora de los osteoclastos, pero adicionalmente estimular el tumor primario al ser el TGF-B un factor de crecimiento para el tumor.
Este círculo vicioso es uno de los varios creados por el tumor para garantizar su supervivencia, lo que contribuye a amplificar y perpetuar hasta el infinito el proceso de metabolismo óseo.(Figura 10).
El TGF B que es beneficioso para el tumor es activado por múltiples vías (PSA, Células tumorales, osteoclastos). (Figura 10)
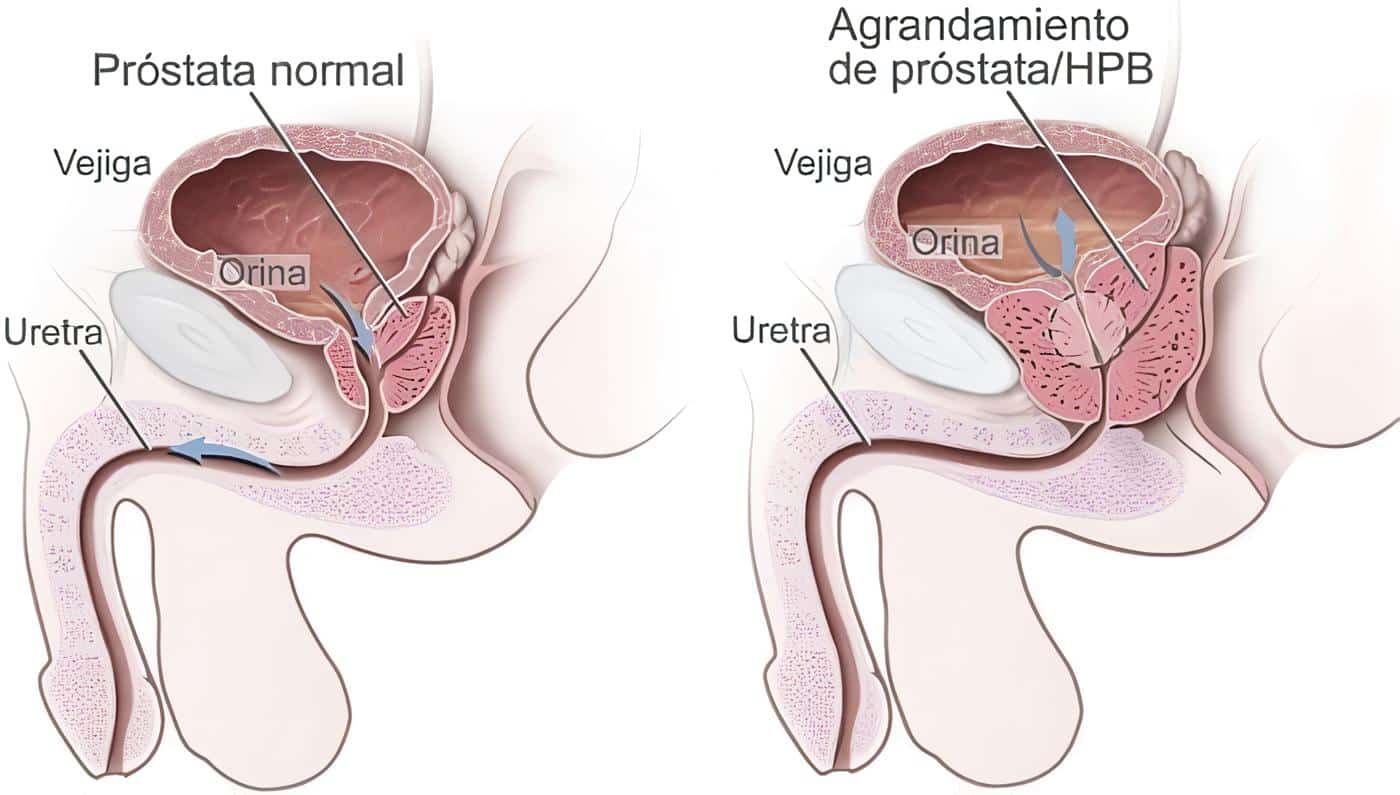
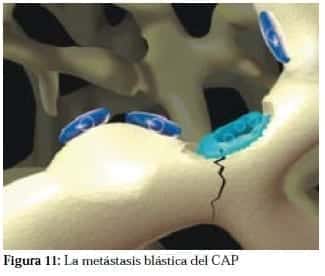
El resultado es una metástasis blástica con osteolisis vecina, existe la misma cantidad formada de hueso que la destruida, lo que convierte realmente en una metástasis mixta con hueso débil y fracturable. La metastasis blástica implica remodelación igual que resorción, pero en sitios diferentes o remodelación mayor que resorción. (Figura 11)
 En la parte I de este artículo se había explicitado como es el desarrollo del fenotipo del cáncer de próstata. En esta segunda parte se hace referencia a la conformación de un fenotipo metastásico en el que ocurren los fenómenos bioquímicos mencionados anteriormente. (Ver Figura 15 de la Parte I)2,4,8,9
En la parte I de este artículo se había explicitado como es el desarrollo del fenotipo del cáncer de próstata. En esta segunda parte se hace referencia a la conformación de un fenotipo metastásico en el que ocurren los fenómenos bioquímicos mencionados anteriormente. (Ver Figura 15 de la Parte I)2,4,8,9

 Desmina: Uniones estromales
Desmina: Uniones estromales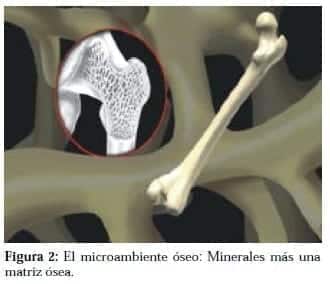 El hueso posee dos tipos de células fundamentales:
El hueso posee dos tipos de células fundamentales: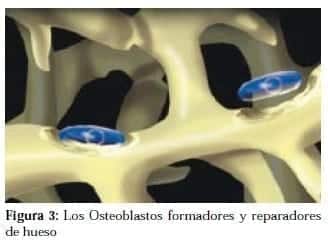
 • Factores sistémicos inhibitorios:
• Factores sistémicos inhibitorios: