Trabajos de investigación
Tratadas con valerianato de Estradiol y 17 alfa Hidroxiprogesterona
Antonio González; Residente del Departamento de Obstetricia y Ginecología.
Fabio Sánchez; Profesor Departamento de Obstetricia y Ginecología y Centro de Investigación Médicas.
Dirección: Cra. 26 No. 10-112 – Apto 702 – Medellín (Ant.)
Investigación financiada por la universidad de Antioquia, COLCIENCIAS, Laboratorios Sheiney AG Berlin de Colombia.
Resumen
Introducción:
El cambio hormonal más precoz que se detecta durante la menopausia fisiológica es la elevación de la FSH, fenómeno que ocurre antes de que desciendan los estrógenos. Se afirma que la integridad hipotálamo hipófisis se conserva a lo largo del tiempo incluso en la menopausia.
Objetivo:
Evaluar la integridad del eje hipotálamo hipófisis en mujeres en menopausia mediante el comportamiento de la medición de la FSH a la aplicación intermitente de diferentes dosis de 17 a hidroxi – progesterona en mujeres tratadas previamente con valerianato de estradiol.
Material y Métodos:
Se estudiaron 20 pacientes en menopausia con niveles mayores de 18 ng/ml de FSH y menos de 30 pg/ml de estradiol, sin tener ninguna terapia hormonal previa.
A todas las pacientes se les administró valerianato de estradiol siguiendo el esquema de FIV, el día 15 del ciclo se les aplicó a 15 pacientes, 500 mg de caproato de 17 a hidroxi-progesterona cada 7 días pro 3 dosis, y a 5 pacientes 1000 mg. A 10 de las pacientes se les aplicó además 5000 y 10000 UI de HCG cada 2 1/2 días respectivamente a partir del día 19 del ciclo. (se denomina día cero para las gráficas)
Los datos obtenidos se evaluaron por un análisis de varianza en dos vías (ANOVA).
Resultados:
El promedio de edad de las pacientes estudiadas es de 56 años, el promedio de FSH al inicio del estudio fue 19,44+ 2.76 se observa en el grupo total de pacientes un incremento de FSH en un 100% (39.28 + 4.55) concomitante con el incremento en los niveles de estradiol y especialmente de 17 a hidroxi – progesterona, para descender nuevamente a niveles por debajo de la basal (9.98 + 2.17) a pesar de continuar la elevación de ambas hormonas.
Diferencias estadísticamente significativas en la variación de estas hormonas.
Cuando se organizan las pacientes en 2 grupos con respecto a la mayor o menos cantidad de 17 a hidroxi-progesterona aplicada, se observa que el incremento es semejante al grupo total pero la depresión de FSH es mayor (4.48 + 1.15) cuando la concentración de 17 a hidroxi-progesterona es mayor (0.73 +0.06).
Discusión:
La FSH sufre un incremento con la elevación de los niveles plasmáticos de estradiol y especialmente de 17 a hidroxi-progesterona y posteriormente se presenta una privación por debajo de los niveles basales, efecto que se hace más evidente cuando se clasifica el grupo de pacientes de acuerdo a la mayor o menos concentración de 17 a hidroxi-progesterona que alcanza la menor concentración de FSH.
Por lo anterior se puede concluir que en la menopausia el eje hipotálamo hipófisis está funcionalmente activo y que la 17 a hidroxi-progesterona asociada al efecto permisito del estradiol ejerce un doble efecto en la hipófisis: aumentar la exocitosis masiva de FSH y posteriormente ejerce una acción de privada hormonal.
Palabras Claves: Menopausia, Reserva Hipotálamo hipófisis, 17 a hidroxi-progesterona. FSH, Estradiol.
Summary
Introduction:
The change the hormonal very precocius that we see during the physical menopause is the elevation of the FSH the happen before of that descend the estrogenos. Suy abont the entire hipotalmo hipofisi we keep a song time include in the menopause.
Objetive:
Question about eje hipothalamus, hypophysis for women in menopause intervening the medition of FHS to the aplication of diferents doses of seventeen (17) hidroxiprogesterona in first women wite valerianato of estradiol.
Material and Methods:
Studied twenty (20) patients witen menopause with larger nivels of eighteen (18) ng/ml of FSH and dess of thirty (30) pg/ml of estradiol, withont to have nothing hormonal therapy first.
For all patients give then valerinanato of estradiol witen the diagram of Fiv, on fifteen (15) patients.
Five hundred (500) mg of caproato of seventeen (17) hidroprogesterona each seven (7) day for three doses, and five (5) patients 1000 mg to ten (10) the patients not more five thousand (5000) and the thousand (10000) UO of HCG chaque two (2) 1/2 days being on day nineteen (19) of century (this name days zero for graphic).
The daytes got has of varianza in two (2) ways (ANOVA).
Result:
The age of patients studied is of fifty six (56) year, the average of FSH begin of study was 19.44 + 1.04 and of estradiol 8.50 + 2.76 we look in the group total of patients and increment of FHS a 100% (39.28 + 4.55) concomitant with the increment the nivels of estradiol and especialy of 17 a hidroprogesterona for descend newly to level for down of the basal (9.98 + 2.17) but to continued the elevation together hormonal, different statistical significats in the variation of these hormonal. When organized the patients in 2 group with reference to the larger or zero quantyty of 17 hidroxiprogesterona applicable, we look that the increment is similar to group total but the depresion of FSH is larger (4.48 + 1.15) cohen the concentration of 17 x hidroxiprogesterona is larger (0.73 + 0.06).
Discussion:
The FSH suffer an increment with the elevation of the levels plasmatic of estradiol and especialy of 17 a hidroxiprogesterona and the preset a privation for down of the levels basales, effect that done more evident when classify the group of patients according to the larger or less concentration of 17 a hidroxiprogesterona reach the less concentration of FSH.
For the last can conclude that in the menopausia there axis hipotahalamus hypophisis this funcytionaly active and the 17 progesterona associate with the effect permisive to the estradiol make a double effect in the hipofisis to incrase the oxocitosis masive of FHS and the practice an action the prevention hormonal.
Key Words: Menopause, Reserve, Hypothalamus, Hupophysis Seventen (17), x Hidroprogesterona, FSH, Estradiol.
Introducción
El cambio hormonal más precoz que se detecta durante la menopausia fisiológica o quirúrgica es la elevación de la FSH, fenómeno que aparece un tiempo antes de la caída de los niveles circulantes de estradiol y como consecuencia de la disminución de la producción de inhibina en el ovario y la secreción continua de GnRH en el hipotálamo 1-2-3-4.
Sin embargo se afirma que después de la menopausia, se conserva a través del tiempo la integridad del eje hipotálamo – hipófisis, es así como se ha demostrado que la FSH se puede bloquear significativamente con la administración parenteral y oral de estradiol a pesar de la ausencia de inhibina pero sin llegar a niveles basales 5-6-7.
En la mujer con disgenesia gonadal, tratada previamente con valerianato de estradiol, se puede inducir una elevación significativa de FSH y LH con la aplicación aguda de progestágenos8, además en mujeres fértiles se induce un pico de gonadotropinas en la mitad del ciclo, posterior al pico de progesterona9-10.
También el Estradiol tiene el papel de bloquear la respuesta de las gonadotropinas a la administración parenteral de GnRH, siendo más sensible la FSH, la cual se frena co dosis de 0.02 a 0.04 mg de etinilestradiol. En tanto son necesarias dosis hasta de 6 mgs de etinil estradio para frenar la LH2. Por lo anterior se puede concluir que la regulación de gonadotropinas en la hipófisis es multifactorial.
La presente investigación se programó con el fin de conocer la integridad del eje hipotálamo-hipófisis como también evaluar el comportamiento de la FSH ante la aplicación intermitente de 17a OH progesterona durante la menopausia, previa sensibilización con valerinato de estradiol.
Materiales y métodos
Pacientes:
Se seleccionaron 20 pacientes que consultaron al servicio de Obstetricia y Ginecología, Hospital Universitario San Vicente de Paúl, Medellín, durante el año 1992, y quienes fueron programadas para histerectomía por enfermedad orgánica tal como prolapso genital o neoplasia intraepitelial, que tuvieran más de más de 1 año en menopausia, y niveles plasmáticos de FSH mayores de 18 ng/ml y estradiol menores de 30 pg/ml. Ninguna paciente ingirió terapia hormonal de sustitución durante los últimos 3 meses.
Se seleccionaron pacientes menopáusicas con el fin de eliminar la acción de hormonas endógenas (estrógenos, andrógenos o progesterona), producidas en el ovario, que pudieran actuar como factor perturbador y poder lograr así obtener modificaciones en la secreción de FSH, secundaria a la terapia hormonal exógena, no se evaluó la secreción de LH por presentar reacción cruzada con la HCG9-10-11-12-13.
A cada una de las pacientes se les informó individualmente acerca de los objetivos, programación, efectos secundarios y pliegos de la investigación; además se les dejó en libertad de aceptar o retirarse del programa. Cada una de las pacientes firmó un documento que autorizaba la investigación.
Metodología
Siguiendo el método experimental, las pacientes fueron divididas en 4 grupos de acuerdo al esquema de aplicación de los medicamentos y se incluyeron en cada grupo de acuerdo al orden de llegada. Inicialmente se programó el grupo I, luego el II, III, y al final el IV, con el fin de facilitar el control de los esquemas.
Esquemas terapéutico:
Antes de iniciar la investigación, se les informó a las pacientes los medicamentos que debían ingerir, y las fechas de las tomas de muestras en el servicio.
A todas las pacientes se les inició el tratamiento con valerianato de estradiol (Progynava®), siguiendo el mismo esquema que se utiliza para pacientes con disgenesia gonadal en los programas de fertilización in vitro, con el fin de remedar la primera mitad del ciclo ovárico y sensibilizar el gonadotropo con dosis fisiológicas de E214
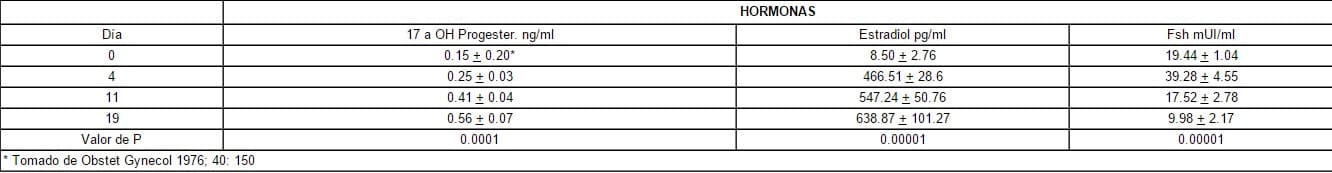
Tabla 1. Concentración de FSH y Estradiol con relación a la concentración plasmática dela 17 a hidroxi-progesterona, en los diferentes tiempos, en 20 pacientes en Menopausia
El esquema terapéutico utilizado en el siguiente:
1 comprimido (2 mg), 1 al 10 día.
3 comprimidos (6 mg), 11 al 14 día.
1 comprimido (2 mg), 15 al 18 día.
2 comprimidos (4 mg), 19 a 35 día.
Posteriormente desde el día 15 del ciclo artificial y cada 7 días se les aplicaron esquemas terapéuticos diferentes de acuerdo al grupo al que pertenecían así:
Grupo I 500 mg de caproato de 17 a OH progesterona (17ª OHP) IM cada día, 3 dosis.
Grupo II 1.000 mg de caproato de 17 a OHP cada 7 días, 3 dosis.
Grupo III 500 mg de caproato de 17 a OHP cada 7 días por 3 dosis, y 5.000 UI de Gonadatropina Cariónica Humana (Primogonil®) IM cada 2 1/2 días por 7 dosis.
Grupo IV 500 mg de caproato de 17 a hidroxi-progesterona cada 7 días por 3 dosis y 10.000 UI de HCG, IM cada 2 y 1/2 días por 7 días.
La dosis de valerianato de estradiol se le entrego a la paciente con sus respectivas instrucciones. En la segunda fase del ciclo se le aplicó en la institución la ampolla de 17OH progesterona, los días 15, 22 y 29, y la HCG los días 19, 21, 24, 26, 29, 31 y 34 del ciclo artificial.
Todas las aplicaciones fueron intramusculares a las 9 am., excepto la HCG los días 21, 26 y 31 la cual se aplicó a las 21 horas en la residencia de la paciente y quien con posterioridad debía traer la respectiva ampolla vacía como control de su aplicación

Figura 1. Esquema de aplicación de Tratamiento Hormonal a 29 mujeres en Menopausia
Todo esquema terapéutico fue supervisado permanentemente por uno de los autores.
Control hormonal:
La respuesta hormonal fue monitorizada por medición de niveles séricos, para ello se tomaron muestras de 10 cc de sangre de la vena cubital anterior, al inicio del estudio y los días 19, 24 y 33 (+4, +11, Y +19 de la aplicación de la 17 a hidroxi-progesterona); la sangre se almacenó en tubo seco, se dejó 1 hora en reposo hasta obtener la retracción del coágulo; el plasma se fraccionó en 2 alicuotas y se conservo en refrigeración a -20°C hasta su procesamiento. Todos los sueros se procesaron al término de la investigación.
Determinaciones hormonales:
Las hormonas FSH, HCG, Estradiol (E2) y 17 a OH progesterona fueron determinadas por RIA, suministrado por Diagnostic Products Corp (Los Ángeles, CA); todas las determinaciones se hicieron con el mismo estuche y en el mismo laboratorio.
La mínima dosis detectable para FSH es 0.1 mUI/ml, de HCG 1.1 mUL/ml, estradiol 8 pgr/ml y 17 hidroxiprogesterona 0.07 ng/ml; el coeficiente de variación (CV) fue de 1.63 para FSH, 5.13 para HCG, 4.3 5 E2) y 1.93 para la 17OH progesterona.
Análisis estadístico:
Las pacientes se dividieron en 2 grupos, según el esquema hormonal asignado y de acuerdo con los diferentes dosis de 17 17 a OH progesterona así:
Grupo A:
15 pacientes a quienes se le aplicó 500 mg de caproato de 17 a OH progesterona intramuscular cada 7 días por 2 dosis, y el Grupo B: 5 pacientes a quienes se les administraron 1.000 mg de caproato de a OH progesterona intramuscular cada 7 días por 2 dosis.
Toda información fue recopilada en un formulario previamente precodificado y con datos almacenados en computador. Todos los análisis se hicieron utilizando un paquete estadístico. Todos los análisis se hicieron utilizados un paquete estadístico; se emplearon métodos descriptivos y para el estudio analítico el método ANOVA en 2 vías.
Resultados
El promedio de edad de las 20 mujeres participantes en el estudio fue de 56 años; mínimo 50 y máximo 64 años.
La indicación para la histerectomía fue en 17 mujeres prolapso genital, y en 3 neoplasia intraepiteliar cervical.
El promedio inicial de FSH en las 20 pacientes fue 19,44 + 2.76 pg/ml, niveles séricos que confirman la menopausia en las pacientes de acuerdo a los criterios establecidos.
Los efectos secundarios con la administración hormonal fueron mínimos: náuseas, epigastralgias, tensión mamarias que en ningún caso obligó a la suspensión del mismo. Sólo se presentó una complicación postoperatoria: obstrucción intestinal por bridas, sin relación con las drogas administradas.
Cuando se evaluó el comportamiento de la FSH:
Con respecto a la concentración de 17 a hidroxi – progesterona, en el grupo total de pacientes estudiadas, se apreció un incremento de los niveles circulares hasta de un 100%: de 19.44 + 1.04 ng/ml inicial a 39.28 + 4.55 ng/ml el día + 4, cambio que ocurre concomitantemente con la elevación de los niveles circulantes de 17 a hidroxi-progesterona y de E2, las cuales alcanzan niveles preovulatorios: 466.51 + 28.60 pg/ml, hallazgo que es contrario a lo que se esperaba.
Luego de la segunda determinación, día + 11, empieza a declinar bruscamente la concentración de FSH (por debajo del 50%), en la medida en que se va incrementando la concentración de E2, y principalmente de la 17 a OH progesterona, hasta alcanzar la mínima concentración de FSH: 9.98 + 2.17 correspondiente al día + 11, momento en el cual la 17 a hidroxi-progesterona alcanza su mayor concentración: 0.56 + 0.07, cambios que son estadísticamente significativos, (p < 0.00001). Tabla 1).
Cuando se analizan separadamente los dos grupos en estudio (Tabla 2):
Se puede apreciar que el comportamiento de la FSH y el E2, es muy semejante al comportamiento del grupo total, una elevación de la FSH a los 4 días de aplicada la 17 a OH progesterona y luego un descenso progresivo, acompañada de un incremento de los niveles de E2, y especialmente de 17 a OH progesterona.
Además no existe una diferencia estadísticamente significativa entre los 2 grupos; cuando se analizan las variaciones de FSH y Estradiol en donde para FSH (p<0.5256) y para E2, (p<0.5232), en tanto para la 17 a OH progesterona si hay una diferencia estadísticamente significativa (p<0.015) a favor del grupo B, debido a que se le aplicó la mayor concentración de la hormona. Además en este grupo se aprecia una mayor correlación entre el descenso de la FSH y la mayor concentración de la 17 a OH progesterona.
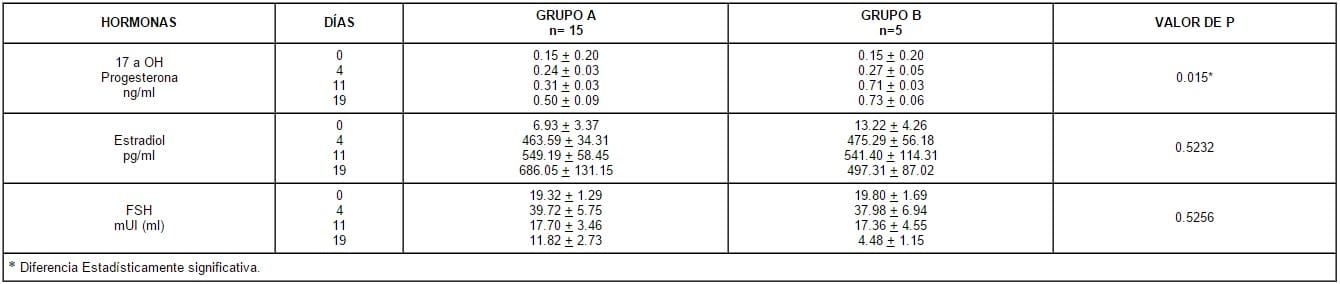
Si se analiza el comportamiento de la FSH en la población total y en los diferentes grupos, tabla 1 y 2, se puede apreciar un incremento inicial y luego un descenso progresivo que está en relación con el incremento de E2, y principalmente de la 17 a OH progesterona; descenso que es más significativo en el Grupo B, en donde la FSH alcanza la mínima concentración 4.48 + 1.15 ng/ml contra 11.82 + 2.73 ng/ml en el Grupo A, fenómeno que coincide con el mayor incremento de 17 a OH progesterona, 0.73 + 0.06 para el Grupo B contra 0.50 + 0.09 en el Grupo B, el cual tiene una diferencia que es estadísticamente significativa.
Paralelo con estas modificaciones, el E2, mostró un incremento progresivo, que aunque fue mayor en el Grupo a: 686 + 131.15 que en el B: 497.31 + 87.02, no fue estadísticamente significativo.

Figura 2. Concentración de 17 a Hidroxiprogesterona en 20 mujeres en menopausia en diferentes grupos y tiempos
Discusión
Al iniciarse la menopausia se incrementa de 2 a 3 veces los niveles de FSH con respecto al nivel que se presenta durante el ciclo ovárico normal, elevación que precede a la LH, como consecuencia y secundariamente de estradiol1-2. Esta elevación es mayor para la FSH como consecuencia de su vida media, que es de 39 horas, en tanto para la LH es sólo de 21 minutos, y es más precoz la elevación de la FSH debido a que la inhibida que regula la FSH, se frena más rápidamente que los esteroides androgénicos que regula la LH.
Con el fin de conocer el comportamiento del eje hipotálamo-hipófisis y específicamente de la FSHa la administración de 17 a OH progesterona de depósito, se sometieron 20 pacientes a un tratamiento prolongado con estrógenos durante 35 días, administrados por vía oral y siguiendo el esquema previamente descrito, con el fin de sensibilizar las células del sistema hipotálamo – hipófisis.
Al administrador a las 20 pacientes la dosis inicial de 250 mg de 17 a OH progesterona, se apreció 4 días después y contrario a lo esperado, un incremento de FSH a niveles del 191,8%, tal como ocurre durante la fase preovulatoria del ciclo como consecuencia del pico de progesterona y 17 a OH progesterona.
Posteriormente en la medida en que se aumentó la concentración de 17 a OH progesterona,
Se disminuyó la concentración de FSH, apreciándose un comportamiento paradójico. Comportamiento que se hizo más evidente en el grupo que tuvo la mayor concentración plasmática de 17 a OH progesterona. Este comportamiento paradójico de la secreción de FSH, se pudiera explicar como consecuencia del papel que tuviera a 17 a OH progesterona a nivel del gonadotropo, en donde inicialmente se desencadenaría la exocitosis masiva de la hormona, y como resultado el pico de la FSH, hasta llegar a agotarlo, momento en el cual se frenaría no sólo la síntesis a nivel gonadotropo, sino también se retardarían los pulsos de la GnRH, pulsatilidad que se conserva durante la menopausia11. Esta respuesta de FSH es muy semejante a la que se observa cuando se aplica progesterona por vía parenteral en pacientes con disgenesia gonadal tratada con E28.
También durante la menopausia se puede desencadenar una mayor liberación de FSH y LH secundaria a la aplicación de GnRH parenteral, posiblemente como consecuencia de un mayor almacenamiento de la hormona en el gonadotropo13.
Fronchimont ha estudiado la respuesta gonadotropa a la GnRH bajo el estímulo de dosis bajas de 0.02 y 0.04 mg/día disminuyen la FSH, pero no modifican la LH; dosis intermedias de 0.6 mg/día aumentan la respuesta de la LH. En tanto son necesarias dosis considerablemente más altas, alrededor de 6 mg/día, para lograr reducir significativamente la respuesta de la LG2.
La mujer en menopausia:
Los estrógenos la progesterona ejercen sobre el gonadotropo un efecto inhibidor y estimulador dependiendo de concentraciones óptimas2. La asociación de estrógenos y progestágenos en dosis suficientes son capaces de inducir un pico de FSH y LH en mujeres en menopausia, comparables al pico observado en la mitad del ciclo normal de una mujer durante el período de actividad ovárica, fenómeno que se reprodujo en el presente trabajo.
Este mismo autor2 estudió la acción de los distintos progestágenos sobre la respuesta de las gonadotropinas a las GnRH, es así como observó con la administración de estos medicamentos una disminución de los niveles basales de FSH y LH pero sin modificar la respuesta del gonadotropo a la estimación con GnRH, lo que indica que hay una acción inhibidora de los progestágenos sobre la secreción de gonadotropinas y sobre la secreción GnRH endógena2, fenómeno también demostrado en la presente investigación.
Este comportamiento de la FSH en pacientes con menopausia y previamente sensibilizados con valerianato de estradiol:
Con la aplicación de 17 a OH progesterona de depósito IM, evidencia la integridad del eje hipotálamo hipófisis ovario, en estas pacientes.
Estos hallazgos servirán para dilucidar el papel que tienen los progestágenos y especialmente la 17 a hidroxi-progesterona durante el pico preoulatorio y posiblemente de la progesterona, quienes potenciarían la liberación masiva de gonadotropinas, concepto que estaría contra las teorías de otros autores quienes afirman que el pico preovularoio de la 17 a OH progesterona es un índice de luteinización temprana del folículo secundario a la acción de la LH12, y más bien se afirma que estas hormonas progestacionales son un índice de óptima maduración folicular y que es su luteinización temprana la que regula secundariamente el eje hipótalamo hipófisis, y desencadenan la liberación masiva de FSH y principalmente de LH, es decir que es folículo maduro el cual es capaz de regular la secreción de gonadatropinas a nivel del sistema nervioso central.
Bibliografía
- 1. Knobil, E. The neuroendocrine control of the menstrual cicle. Rec. Prog. Hom. Res. 1980; 36: 52 – 88.
- 2. Franchimont, P. Gaspond, U. Axe hypotalamo-hiphopisaiere ét ménopause. In R, Scholler, pén et post menopausic pp 31-41, SEPE, París, 1979.
- 3. Monroe, SE. Jaffe,RB, Midgley, AR. Regulation of human gonadotropins XII. Changes in serum gonadotropins in mentruating women in response to oophorectomy. J. Clin Endocrinol. 1972; 34: 420 -422.
- 4. Aksel, S. Shoemberg, DW. Tyrev, L. Hammond, CB. Vasomotor Symptoms, serum estrogens, and gonadotropin level in surgical menopause. Am J. Obstet Gyencol 1976; 126: 165-169.
- 5. Tsai, CC. Yen, SSC. Acute effects of intravenous infusion of 17B-estradiol on gonadotropin release in pre and post menopausal women. J Clin Endocrinol. 1971; 32: 766-771.
- 6. Geola, F. Frumar, Am. Tataryn, IV., et al. Biological effects of various doses of conjugated equine estrogens in postmenopausal women. J. Clin Endocrinol Metab. 1980; 51: 620-625.
- 7. Rigg, LA. Hermann, H. Yen, SSC. Absorption of estrogens from vaginal cream. N Engl Medic. 1978; 298: 195-197.
- 8. Yen, SSC. Tsai, CC. Vandenberg, G. Rebar, R. Gonadotropin dynamics in patients with gonadal disgenesis: A model for ther study of gonadotropin regulation. J. Clin Endocrinol Metab. 1972; 35: 897 -904.
- 9. Laborde, N. Carril, M et al. The secretion of progesterone during preovulatory period in women with certified ovulation. J. Clin Endocrinol Metab. 1976; 43: 1157-1163.
- 10. Chag, RJ. Jaffe, RB. Progesterone effects on gonadotropin release in women pretreated with estradiol. J. Clin Endocrinol Metab. 1978; 47: 119-125.
Referencias
- 11. Thomeycroft, IH. Sribyatta, B., et al. Measurement of serum LH, FSH. Progesterone, 17 Hydroxy – Progesterone and estradiol 17B level at 4 hour intervals during the periovulatory phase of the menstrual cycle. J. Clin Endocrinol Metab. 1974; 39: 754-758.
- 12. Alexander, SE. Aksel, S. Et al. The effect of aging on hypothalamic funtion inoophorectomized women. Am J. Obstet Gynecol. 1990; 162: 446-449.
- 13. Maroulis, GB. Abraham, GE. Ovarium and adrenal contribitions to peripheral steroid levels in postmenopausal women. Obstet Gynecol. 1976; 48: 150-154.
- 14. Navot, D. Laufer, N. Kopolovic, j et al. Artificially induced endometrial cycles and stablishment of pregnancies in the absence of ovaries. N Eng J. Medic. 1986, 314: 806-811.
- 15. Lasley, BL. Wang, CF. Yen, SSC. The effects of estrogen and progesterone on the funtional capacity of the gonadotrophs. J Clin Endocrinol Metab. 1975; 41: 820-826.