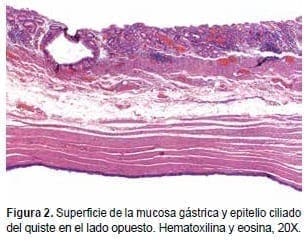
Clasificación Macroscópica
El CCT se presenta con varias morfologías y Kudo ha establecido una clasificación similar a la existente para cáncer gástrico temprano (Figura 1).
La mayoría de las lesiones se presentan en el recto y, en menor porcentaje, en el colon derecho. Los pólipos se dividen macroscópicamente en pediculados, planos, y deprimidos; un 42 a 85% de los CCT son pediculados y, 15 a 58%, planos o deprimidos (8).

Figura 1. Clasificación macroscópica del cáncer colorrectal temprano según Kudo. Dibujo, Mónica Martínez.
Las lesiones deprimidas pueden ser absolutamente deprimidas (tipo IIc) o pueden estar acompañadas por una mínima elevación marginal (tipo IIc+IIa).
La elevación marginal generalmente está cubierta por mucosa normal y se presenta así por compresión del tumor o por proliferación de células malignas en la submucosa (3).
Existe otro tipo de lesiones denominadas pólipos de extensión lateral (LST) que se caracterizan por ser de forma extensa y circunferencial en la pared intestinal.
Estas lesiones, a su vez, se clasifican en granulares y no granulares (3).
Kudo y colaboradores consideran que los adenomas planos pequeños crecen, ya sea hacia arriba (exofíticamente) para convertirse en pólipos pedículados, u, horizontalmente, para convertirse en LST.
Las lesiones deprimidas crecen en profundidad (endofíticamente), para convertirse en cánceres avanzados (5) (Figura 2).
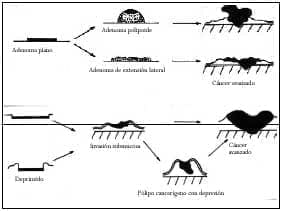
Figura 2. Evolución de los adenomas planos y lesiones deprimidas según Kudo.
Shimoda clasificó el patrón de crecimiento del CCT en dos tipos: polipoide (PG) y no polipoide (NPG).
Teniendo en cuenta esta clasificación y con la idea de establecer la diferencia en la tasa de crecimiento (tiempo de duplicación) al comparar las lesiones mucosas y las submucosas, Matsuri y colaboradores realizaron un estudio retrospectivo de seguimiento radiológico de 49 pacientes con CCT.
Se encontró que el tiempo de duplicación para el cáncer colorrectal temprano mucoso es largo, de 31,2 meses, mientras que, para las lesiones con compromiso submucoso, esta tasa se acelera hasta 25,8 meses.
No hay diferencia en la tasa de doblaje al comparar lesiones con los patrones de Shimoda de lesión polipoide y no polipoide. Entre más profundo sea el compromiso tumoral en la pared, más se acelera el crecimiento, especialmente después de comprometer la submucosa.
El cáncer colorrectal no tiene una tasa de crecimiento constante, más bien crece de forma exponencial (9).
Clasificación Macroscópica
La invasión submucosa fue descrita por Haggit y colaboradores, quienes clasificaron el CCT polipoide en lesiones de tipo pediculado y sésil.
Los pólipos pediculados tienen tallos con longitudes mayores que su diámetro, mientras que los sésiles no. El tallo está compuesto por mucosa normal y muscularis mucosae, o con un área central de tejido submucoso.
La unión entre el tallo y el adenoma (cabeza) usualmente es un punto de transición de epitelio normal a adenomatoso y se denomina cuello. Los linfáticos acompañan a la muscularis mucosae por el tallo hasta la cabeza.
Haggit estratificó los pacientes de acuerdo con grados definidos de invasión, así (Figuras 3 y 4):
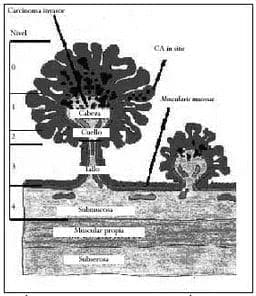
Figura 3. Grados de invasión en lesiones polipoides según Haggit. Dibujo, Mónica Martínez.
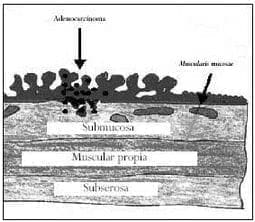
Figura 4. Grados de invasión en lesiones sésiles según Haggit. Dibujo, Mónica Martínez.
Grado 0, por arriba de la muscularis mucosae (in situ); Grado 1, a través de la muscularis mucosae hasta la submucosa, pero limitado a la cabeza del pólipo; Grado 2, cuando hay invasión del cuello; Grado 3, cuando hay invasión de cualquier parte del tallo; y, finalmente, Grado 4, cuando se invade la submucosa por debajo del tallo del pólipo pero por encima de la muscular propia.
La invasión dentro de un pólipo sésil es por definición de grado 4.
En sus trabajos, Haggit encontró que el grado 4 de invasión fue el único factor pronóstico resultante del análisis multivariado. Igualmente, definió el grado de invasión como el factor pronóstico primario para el cáncer invasor en un pólipo (6).
A pesar de que esta clasificación ha sido ampliamente empleada para evaluar la calidad de la excisión en polipectomías endoscópicas, pierde utilidad en el manejo de las lesiones planas, sin tallo o deprimidas
.Como parte de la estrategia de estadificación del CCT, Kikuchi cuantifica el grado de invasión vertical y horizontal de la submucosa de la siguiente forma: se divide la submucosa en tercio superior como Sm1, tercio medio, como Sm2 y tercio inferior, como Sm3.
A su vez, el tercio superior o Sm1 se divide en tres subtipos según el compromiso horizontal en relación con el tamaño del tumor.
De acuerdo con esto, se clasifica una lesión como Sm1a cuando hay invasión menor a una cuarta parte del espesor del tumor; Sm1b, cuando hay invasión submucosa entre un cuarto y la mitad del espesor tumoral.
Finalmente, cuando hay un compromiso horizontal del tercio superior de la submucosa mayor a la mitad del espesor del tumor, la lesión se clasifica como Sm1c (Figura 5).
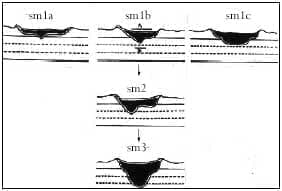
Figura 5. Clasifícación de la invasión submucosa en el cáncer colorrectal temprano,
según Kikuchi. Dibujo, Mónica Martínez.
El Sm1 tiene una profundidad máxima medida entre 200 y 300 micras (8). En pacientes con pólipos pediculados, Sm1 es similar a un grado 1 de Haggit, Sm2 equivale a los grados 2 y 3 de Haggit, y Sm3 representa un grado La estadificación del grado de invasión de la submucosa refleja el pronóstico de la lesión.
Una lesión Sm1b sin invasión vascular o un tumor Sm1a nunca dan metástasis. Las lesiones con compromiso más profundo, o más extenso, tienen la capacidad de dar metástasis.
Esta información es útil para determinar si hay indicación o necesidad de agregar tratamiento quirúrgico después de haber completado el tratamiento endoscópico de una lesión (Tabla 1).
Tabla 1. Grado de invasión submucosa y tasas de invasión vascular o metástasis (enero de 1985 a diciembre de 1996). Ly: invasión linfática, v:invasión venosa.World J Surg 1997; 21; No 7: 694-701.
![]()
Diagnóstico Endoscópico
Al evaluar endoscópicamente las diferentes formas morfológicas de presentación del CCT, existen algunas características a la visualización endoscópica que pueden sugerir infiltración submucosa y, por ende, riesgo de compromiso ganglionar por la lesión en cuestión.
En las lesiones levantadas, su dureza su llenura, la configuración de pólipo sobre pólipo, la ulceración en la cima, la presencia de pequeños puntos blancos a su alrededor y el sangrado local son todas características que sugieren invasión.
En las lesiones deprimidas, la presencia de puntos sangrantes, la interrupción del patrón capilar de la mucosa y la deformación local de la pared sugieren igualmente invasión de la lesión.
Es importante observar el movimiento de la lesión y los cambios en su apariencia con la insuflación y posterior descompresión aérea.
En caso de compromiso de la submucosa, se pierde el movimiento conjunto en bloque de la lesión y su mucosa vecina, haciéndose notoria una pequeña deformación local. Con la instilación de índigo carmín al 0,4% se observa con mayor claridad no solamente la lesión, sino también la interrupción de los surcos innominados de la mucosa, otro signo de malignidad de las lesiones deprimidas.
Estos surcos se preservan en presencia de cambios inflamatorios o hiperplásicos. El diagnóstico endoscópico de las lesiones planas y de los LST es más difícil, y es en estos casos en los que la cromoendoscopia, especialmente la tinción con índigo carmín, tiene su mayor utilidad al delimitar sus márgenes y exaltar su forma (3).
(Lea También: Riesgos y Tratamiento en Cáncer Colorrectal Temprano)
El desarrollo de la endoscopia de amplificación:
Ha permitido describir seis patrones diferentes de organización de las glándulas colónicas en la mucosa, los denominados pits (orificios en las criptas).
El pit tipo I o circular es el que se encuentra en la mucosa normal y en algunos casos de leiomiomas, en pacientes con enfermedad inflamatoria intestinal o pólipos inflamatorios.
Los pits tipo II o estrellados son característicos de áreas con cambios hiperplásicos.
Los adenomas mínimamente elevados y las lesiones levantadas presentan un pit tipo IIIL (grande tubular) y pit tipo IV (ramificado). El patrón tipo IIIs es casi exclusivo de las lesiones deprimidas.
Los adenomas de mayor tamaño, adenomas vellosos y los pólipos de extensión lateral exhiben un patrón ramificado o tipo IV (Figura 6).
Figura 6. Arreglo de las glándulas colónicas “Pit pattern”. Dibujo, Mónica Martínez.
A medida que la submucosa es invadida, su estructura se destruye y se torna más compleja con ausencia completa de un patrón glandular regular.
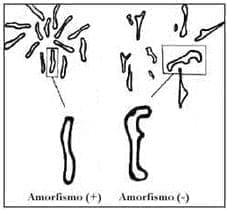
Este tipo de lesiones se clasifican como un pit tipo V o irregular. La presencia de asimetría y la falta de homogeneidad en el tamaño de las criptas, determinan el grado amorfo de la lesión.
Si el signo amorfo está presente, se clasifica la lesión como un patrón tipo Va, característico de un carcinoma invasor.
Si el compromiso de la submucosa es aún mayor (Sm2, Sm3), hay pérdida completa de la estructura y se clasifica como un patrón pit tipo Vn (5,3) (Figura 7).
 Figura 7. Variedades de patrón pit tipo V. Dibujo, Mónica Martínez.
Figura 7. Variedades de patrón pit tipo V. Dibujo, Mónica Martínez.
En resumen, el patrón pit observado con la colonoscopia de amplificación nos permite diferenciar el adenoma no invasor del carcinoma invasor y, de cierta forma, predecir la profundidad del compromiso tumoral antes de instaurar un tratamiento.
Esto mejora la exactitud del diagnóstico endoscópico del CCT, especialmente en las lesiones deprimidas (5,3).
Existe hoy en día evidencia sólida, de estudios clínicos randomizados, de que es posible disminuir la mortalidad asociada a cáncer colorrectal en un 15% a 25% con programas de tamizaje para sangre oculta en heces.
El mayor beneficio se obtiene con la detección mediante colonoscopia de CCT, en personas de riesgo estándar mayores de 50 años, después de un resultado de sangre oculta positivo.
Sin embargo, los programas de tamizaje en la población general no han podido demostrar una reducción en las tasas de incidencia de cáncer colorrectal, a pesar de resecar dos o tres veces más lesiones precursoras que en los grupos controles.
No existe un consenso de cómo vigilar los diferentes grupos de alto riesgo (pacientes con historia de cáncer colorrectal o adenomas, uno o más familiares en primer grado con cáncer colorrectal, historia de colitis ulcerativa); no es así con los pacientes con poliposis familiar adenomatosa múltiple o cáncer colorrectal hereditario no polipoide, grupos para los cuales existen guías claras de control periódico. La vigilancia genética sólo tiene utilidad en estos dos últimos grupos de pacientes (10).