1. Posición
Se coloca el paciente en posición de litotomía; lo más cómodo es efectuar el procedimiento en una mesa ortopédica o en una con estribos ginecológicos que permitan flexibilidad (Figura 5). Se aconseja que los muslos del paciente se coloquen separados, las rodillas deben quedar lo menos flexionadas posible, porque al momento de intervenir, pueden limitar la acción libre de las manos del cirujano, quien interviene situado entre las extremidades inferiores del enfermo.
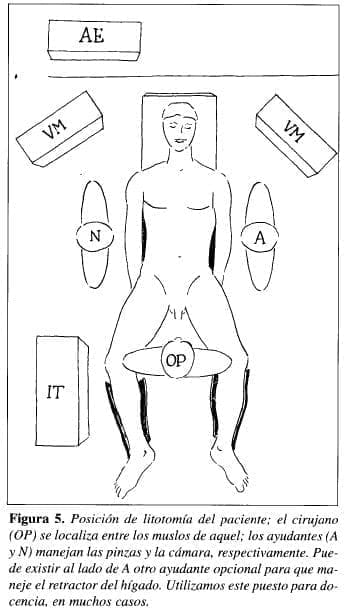
El anestesiólogo debe colocar al paciente en una ligera posición de Fowler. El ayudante principal está a la derecha del cirujano, al igual que un ayudante opcional para la retracción del hígado (esta función la desempeñan las personas que apenas comienzan su adiestramiento). El ayudante que maneja la cámara se localiza a la izquierda del cirujano.
2. Colocación de los trocares
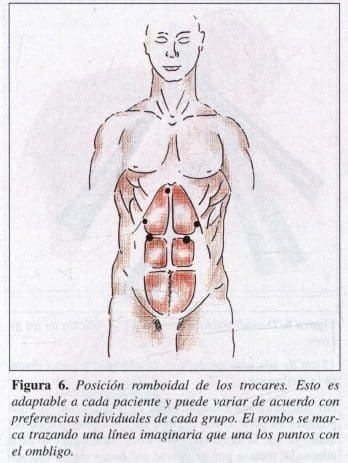
Muchas posiciones se han ideado por los diferentes grupos existentes. Para nuestro grupo, la posición ideal es la propuesta por el grupo de Peters y DeMeester, en Los Angeles, y promovida en nuestro país por Natan Zundel. Esta posición es la de rombo (Figura 6). Preferiblemente todos los trocares deben ser de 10-12 mm y tener sus reductores adecuados.
3. Ayudas técnicas
El cirujano interviene por el trocar supraumbilical izquierdo del enfermo. Por este trocar se introducen los instrumentos principales de disección. La intervención se realiza a dos manos, y el otro trocar de operación es el subcostal derecho, por el cual generalmente se introducen pinzas que ayudan a separar el hígado o a tomar tejidos para ser disecados por el otro sitio de entrada.
4. Disección del epiplón menor
Este es el paso inicial y se logra elevando el hígado. Para este fin, al principio utilizamos un grasper o agarrador que puesto en la parte superior del orificio crural, agarrando músculo, sostenía el hígado elevado. Luego empezamos a ver que muy frecuentemente el agarrador se soltaba, o que el lóbulo izquierdo del hígado era muy grande y optamos por usar de rutina un retractor de hígado. Con este instrumento se han obtenido excelentes resultados.
El ayudante principal toma el estómago alto con una pinza de Babcock que nosotros hemos llamado modificada, porque las partes de ella que se usan para asir el tejido son planas y atraumáticas.
En este paso el ayudante dirige la tracción hacia él, el epiplón menor se tensiona y muestra un área brillante, transparente, la cual puede ser abierta fácilmente con la tijera, por medio de corte o de cauterio. En la parte media muchas veces se localiza una vena, la gástrica izquierda que, por lo general, debe ligarse para obtener un campo más amplio; el problema está en que con ella va, por lo general, la rama hepática del vago cuya sección puede crear la predisposición a desarrollar cálculos biliares. La disección se dirige desde abajo hacia arriba y de derecha a izquierda, hasta encontrar más arriba la membrana frenoesofágica.
5. Apertura de la membrana frenoesofágica
Es el paso fundamental del procedimiento y requiere de un conocimiento en profundidad y de práctica en la técnica. Se realiza combinando el corte con el cauterio, aunque este último debe evitarse al máximo, para no crear zonas de debilitamiento del esófago. La membrana se abre de derecha a izquierda, y el grado de dificultad de esta maniobra depende de la esofagitis, ya que a mayor grado de compromiso mayor inflamación, y la disección se hace más dispendiosa; también depende del tamaño de la hernia hiatal, si ésta existe. Hernias mayores de 5 cm son difíciles de reducir completamente al abdomen, las reparaciones quedarán tensas y el nivel de reproducción será alto. En este paso, el ayudante toma el tejido graso de la unión esofagogástrica y lo arrastra hacia él para dejar ver el lado derecho, y hacia el cirujano o el camarógrafo para dejar ver el lado izquierdo. Abierta la membrana frenoesofágica se descubre el esófago y con maniobras de disección se tracciona alternativamente hacia arriba y abajo para descubrir una adecuada ventana (Figuras 7 a, b y c).

6. Disección de los pilares
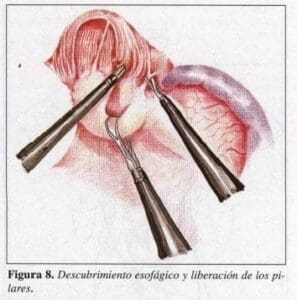
Se descubre primero el pilar derecho y entre éste y el esófago se hacen maniobras de levantamiento para abordar este órgano por detrás. Luego desde la derecha se va hacia la izquierda en busca del pilar izquierdo. En esta maniobra se debe evitar seccionar el nervio vago anterior. Localizado el pilar izquierdo, se diseca bien entre éste y el esófago, y con suave tracción se separan ambas estructuras (Figura 8).
7. Apertura de la ventana posterior
En este paso es fundamental haber despegado el esófago de ambos pilares. Entrando de derecha a izquierda se accede el esófago por su pared posterior y se libera de las adherencias.
La disección es roma y se hace estando en continuo contacto con la pared del órgano. Así se encuentra el pilar izquierdo y al desprender el tejido que hay frente a él, se abre una ventana que comunica la pared posterior del esófago con el fondo del estómago y el bazo.
El riesgo en este paso es el de no tomar como reparo el pilar izquierdo y dirigirse falsamente hacia la pleura, rompiendo inadvertidamente esta membrana.
8. Reparo del esófago y cierre crural
El esófago se puede reparar con un dren de Pemose o por medio de un retractar de esófago; al principio usamos el dren, pero se hacía. engorroso el procedimiento; por ello lo reemplazamos por la pinza angulada para retraer el esófago y así se manejó sin dificultad (Figuras 9a y b). Luego, se visualiza el hiato esofágico y se calibra, por lo general con 1 ó 2 puntos de un material inabsorbible. Con esta maniobra se logra que el segmento ya disecado del esófago permanezca en el abdomen y que la reparación que se realice no se retorne al tórax. Los puntos que usamos son de dos tipos:

a. De anudado externo, punto deslizante que baja sólo desde afuera.
b. De anudado interno, que se ejecuta también con un material inabsorbible.
El primer tipo de punto, se realizó como experiencia inicial y fue fácil de ejecutar con prolene 2-0 y aguja ct2. Como son deslizantes o corredizos, debe ponerse luego de efectuados, un clip sobre el nudo para protejerlo.
Se piensa que el segundo tipo de nudo es el ideal y prueba la destreza técnica del cirujano, pues al principio son difíciles de realizar. El material utilizado es generalmente seda 2 ó 3-0 con aguja. Para tal efecto cortamos la sutura, dejando 15 cm de ella para anudar con tranquilidad y poder manejarla fácilmente.
No utilizamos otros instrumentos de anudado interno, disponibles en nivel comercial que facilitan la ejecución del nudo, ya que la aguja recta de estos instrumentos no es la adecuada, incluso por su grosor; pensamos que el esófago al ser tomado por ella puede sufrir mucho más que con la aguja tradicional. Este tipo de instrumentos, por lo dicho, favorecen al cirujano y no al enfermo.
Es de anotar que en la técnica de Nissen tradicional el cierre crural no se realiza. En la actualidad, y según modificaciones hechas por algunos autores a la técnica, este punto es de vital importancia para evitar que la reparación se desplace al tórax y que se produzca una reproducción herniaria.
9. Realización del Colgajo. Técnicas de Nissen-Rossetti y Toupet
Elaborada la ventana, se toma el estómago por la pared anterior del fondo, empleando una porción de éste, suficiente para que el colgajo no quede tensionado (Figura 10). La medida exacta es difícil de precisar, pero al pasar el fondo de izquierda a derecha y llevarlo a la pared anterior debe cubrir el esófago en su pared anterior y llegar al fondo del otro lado (maniobra de abrazar el esófago completamente). No debe comprometerse la circulación del colgajo el cual debe conservar su color; si éste se torna violáceo, indica que la ventana no es lo suficientemente amplia o que el colgajo es corto y queda tensionado.
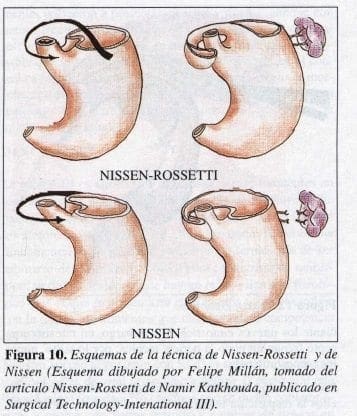
En la técnica propuesta por algunos grupos, como la de Nissen, se toma la pared posterior y se ligan dos o tres vasos gástricos cortos. Con esto se supone que hay menos disfagia. Como grupo, no hemos replicado los resultados anteriores y con el Nissen-Rossetti, vemos que la disfagia es incluso menor, ya que la pared anterior del fondo gástrico es lo suficientemente laxa como para que proporcione el colgajo deseado (Figura 11).
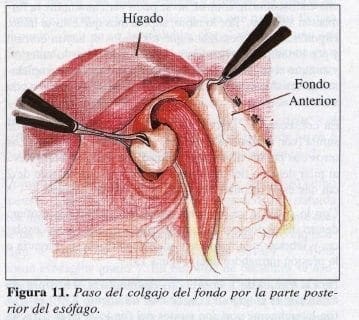
En este momento de la cirugía, es importante pasar por el esófago un dilatador para calibrar la reparación y no producir estrechez posterior. Utilizamos el Hurst 60 F. En esta maniobra no hemos tenido hasta la fecha ninguna perforación.
En seguida, se efectúa la reparación. Para la técnica de Nissen pasamos el primer punto en la parte más distal uniendo el estómago -unión esofagogástrica- al mismo estómago. No se dejan parches de teflón, y se hace con prolene 2-0 (por el poco coeficiente de fricción de éste) aguja ct2, o con seda gastrointestinal 3-0 (Figura 12).
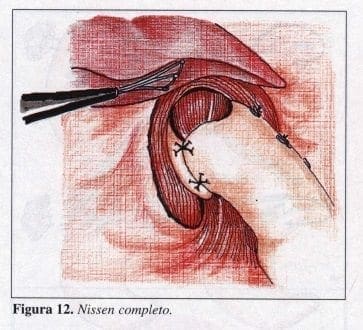
En este proceso se viven dos momentos; el primero de ellos lo constituye la duda para realizar la técnica por la dificultad para el anudado; pero la tecnología da facilidades mediante los nuevos endostich; sin embargó, en nuestro concepto frenan un poco la pericia técnica; por lo tanto, nunca los hemos utilizado.
En la revisión de nuestros pacientes, se observó en 2 de ellos la reaparición temprana de los síntomas y, al hacerles una endoscopia de control, no se pudo ver claramente la formación valvular. Por lo tanto, suponemos que ésta se dañó. Hipotéticamente pensamos que los nudos se hayan corrido y por lo tanto la reparación se haya dañado. Por lo anterior, y aunque el seguimiento de muchos otros ha sido completamente satisfactorio, decidimos hacer el anudado interno con seda.
En consecuencia, colocamos por lo general tres puntos de sutura (con cualquiera de los dos materiales y métodos). Los otros dos puntos no se pegan al esófago y el último se lleva al pilar derecho del diafragma. Así se logra un colgajo de 2 cm que es lo recomendado para no producir disfagia.
Con lo anterior, se logra aumentar la longitud del esófago dentro del abdomen, fijar el colgajo para que no se desplace, y fabricar una nueva válvula sometida en su mayoría a la presión intraabdominal (Figura 13).
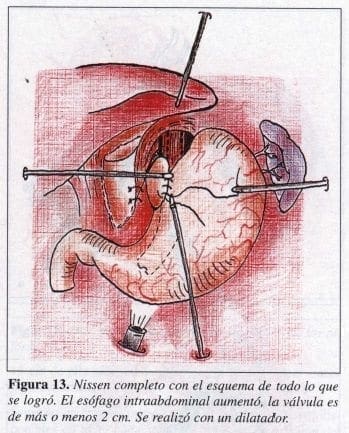
Para la técnica de Toupet el procedimiento es el mismo, excepto por el colgajo, el cual cubre solamente 2700; éste se fija lateralmente con dos puntos del fondo al pilar derecho y con dos puntos del mismo fondo al pilar izquierdo. Así mismo se ponen puntos de fijación entre el esófago y el fondo a cada lado (Figura 14). Terminado el procedimiento, frecuentemente se prueba la reparación pasando azul de metileno. Se revisa la cavidad y se hace hemostasia.
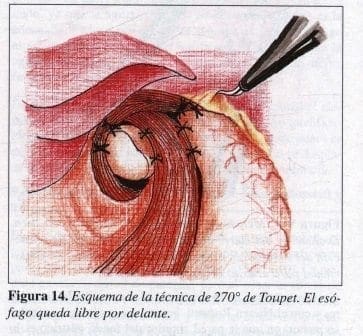
Es importante comentar que en ocasiones dentro del desarrollo de cualquier técnica, se presenta sangrado, el cual no debe lavarse con agua, ya que en estos espacios el agua nunca se logrará aspirar por completo y siempre llenará el campo impidiendo un procedimiento limpio. Por lo anterior, la sangre debe aspirarse y el sangrado por lo general cesará solo, o se puede controlar por medio de coagulación con electrocauterio.
Controles
En los controles endoscópicos al mes se encontró lo siguiente:
De los 28 enfermos que tenían esofagitis G III, 20 (71.4%) retomaron a esófago normal, 7 (25%) regresaron a esofagitis G 1, Y 1 (3.57%), a esofagitis G 11.Todos los pacientes con esofagitis G 11retomaron a esófago normal.
Los 3 pacientes con esofagitis G IV, mejoraron pero sólo 1 (33.3%) retomó a normal y los otros 2 regresaron a esofagitis 11.Todos los pacientes con esofagitis G I se normalizaron endoscópicamente.
De los pacientes diagnosticados como Barret, las biopsias posteriores demostraron el mismo proceso, pero con menor inflamación. En cuanto a la manometría, encontramos que de los 32 pacientes con presiones de base del EEI menores de 6 mmHg, se incrementó la presión en todos, siendo la menor presión lograda de 10 mmHg y la mayor de 38 mmHg. Presiones superiores a 35 mmHg se presentaron en 2 pacientes que tuvieron que ser sometidos a algún procedimiento.
Uno de ellos, dilatado con dilatadores de Savary-Miller con éxito después de una dilatación, y el otro se reintervino laparoscópicamente cambiándole el Nissen por el Toupet, ya que en la manometría postoperatoria se evidenciaron ondas alteradas y un EEI hipertónico. Los 8 pacientes con alteraciones de la motilidad, fueron intervenidos con técnica de Toupet y en los controles manométricos postoperatorios, se evidenció que la motilidad había mejorado y en ninguno se presentó disfagia, por un lapso mayor de 3 meses.
En ambas técnicas se presentó disfagia en el 84% de los pacientes, pero ésta fue menor de 1 mes, siendo mayor de 3 meses en 2 pacientes que fueron operados con la técnica de Nissen-Rossetti. Uno de ellos se intervino con dilatación y otro fue reintervenido y se le realizó un Toupet. Ambos pacientes mejoraron luego de la reintervención. Dentro del total de 100 pacientes tenemos otro reintervenido, pero no hace parte de esta serie por no cumplir con el protocolo.
Los niveles de pH para los 39 pacientes que mostraron alteraciones del mismo, mejoraron en todos, pero sólo en 20 cayeron por debajo de 14.7 según el score o marca de De- Meester, y el resto aunque mejoraron, no llegaron a la cifra normal.
Clínicamente se realizó evaluación del grupo y al completar 6 meses, se encontró que según el Visick, podemos decir que el estado de Visick I no se apreció en ningún enfermo; 45 pacientes llegaron a Visick 11, 3 a Visick III, y 2 a Visick IV. La molestia más importante postoperatoria es la flatulencia, que persiste por muchos meses; se presentó en el 30% de nuestros pacientes aun a los 6 meses. Los eructos también se presentan frecuentemente, siendo una reacción presente en el 10% a los 6 meses. El 5% presentataron diarrea ocasional a los 6 meses pero en ninguno fue incapacitante.
No se presentó síndrome del “globo de gas”. Tres de nuestros pacientes son Visick 111 porque en el período de 6 meses de seguimiento, luego de haber mejorado sintomáticamente, volvieron a presentar agriera s y pirosis, aunque con menor frecuencia y duración que en los episodios originales; en el momento siguen en estudio. En 1 de ellos es probable que se haya desprendido la válvula porque en el control endoscópico al hacer la retroflexión, no se vio la morfología típica de aquella. Este paciente está pendiente para realizarle una serie esofagogastroduodenal y evaluar la morfología de la unión.
Discusión
La esofagitis es uno de los diagnósticos más frecuentes en los resúmenes epidemiológicos anuales de la mayoría de países. Las manifestaciones de la enfermedad y su reflejo en los síntomas, son motivos de consulta diaria. El problema fundamental es poder decir cuándo un enfermo deja de ser tributario de tratamiento médico para convertirse en quirúrgico; se debe considerar que hay un reflujo llamado fisiológico y es el que se presenta en condiciones como el estrés o con la ingesta de alimentos que disminuyen la competencia del EEI.
Nuestro acceso al paciente con RGE es agresivo, ya que para nosotros es de vital importancia definir el curso real que llevará la enfermedad. No creemos que se pueda contemporizar y probar con varias terapias y cambiar de drogas en forma indiscriminada, hasta llegar a lo que muchos llaman el punto ideal; no se debe olvidar que el reflujo es una enfermedad crónica e incurable que responde al tratamiento médico juicioso que mejora los síntomas, pero que no se cura y recurre fácilmente al suspender la terapia. Además, las terapias médicas evaluadas en el tiempo son cada vez más inefectivas, por las resistencias a las diferentes drogas; y el reflujo debe tratarse agresivamente en el paciente joven o con complicaciones derivadas de la misma enfermedad.
Como se muestra en este trabajo, siempre se realizó como método diagnóstico una endoscopia digestiva alta seguida por una biopsia; con lo anterior se evalúa si el paciente presenta o no un Barret; creemos que éste ya es una complicación y, como tal, es clasificada por Savary y Miller como esofagitis grado V. En este tipo de pacientes se asume el tratamiento quirúrgico, si no hay contraindicación; esta posición se basa en la evidencia de que la enfermedad no es curable y por lo tanto, en el futuro el riesgo de carcinoma derivado de ella es más alto. Sabemos que en la literatura hay terapias no quirúrgicas para el Barret, pero con resultados pobres a largo plazo. En los pacientes de nuestra serie con Barret no se observó regresión total del problema, y la condición continuó pero con menor inflamación. Quedan pendientes los controles posteriores. Es verdad que la cirugía al menos detiene la causa provocadora (reflujo) de la esofagitis y disminuye el peligro de cáncer, aunque no desaparece.
Dentro de la evaluación en el laboratorio de esófago, hemos madurado la idea de que la phmetría es importante en casos dudosos de reflujo o en la evaluación de las manifestaciones atípicas del mismo. Este examen que sería el estándar para evaluar esta condición, puede ser reemplazado por la endoscopia en pacientes con esofagitis III y IV, como se ha demostrado ampliamente en la serie de 100 pacientes (12) recientemente presentada en el XXIII Congreso Nacional de la Sociedad Colombiana de Cirugía.
La manometría se convierte en la principal arma que tiene el cirujano para determinar qué hacer con su enfermo, y la aparición de ondas inefectivas en más de un 10% o de contracciones de baja amplitud y de disminuida presión, son condiciones que hacen que el paciente sea quirúrgico. Así mismo, se debe evaluar la presión de base del EEI, su longitud y su posición. Una manometría alterada tendrá poca mejoría con cualquier droga que se utilice, y los trastornos de la motilidad por lo general son secundarios a un reflujo perpetuado. Por lo anterior, pensamos que un criterio prudente, nos lleva a que el tratamiento de estas alteraciones es quirúrgico.
La gamagrafía la hemos empleado muy poco, ya que disponemos de los otros exámenes, y es un examen que podría ayudamos en algunos enfermos que se niegan a hacerse la manometría. El problema está en que no mide presiones y no cuantifica datos sobre efectividad contráctil, sólo muestra el vaciamiento y el porcentaje de reflujo. Con estos datos y en una forma no muy completa, podemos asumir ciertas condiciones del esófago examinado y determinar el tipo de procedimiento.
La radiología es un examen que lo hemos utilizado sólo para evaluar las estenosis y para determinar si la hernia hiatal reduce o no a la cavidad y, con esta información, deducir si se puede o no realizar la cirugía laparoscópica.
Por los resultados obtenidos, podemos decir que el 90% de nuestros enfermos, han respondido satisfactoriamente a la cirugía laparoscópica. La mejoría completa, incluyendo la motilidad en los pacientes sometidos a la técnica de Toupet, habla a favor de que esta técnica es apta para aquellos enfermos que por el reflujo, hayan alterado la motilidad. Los resultados que hasta el momento hemos evaluado en los 8 pacientes seguidos por 6 meses, son muy alentadores.
La técnica de Nissen-Rossetti la hemos utilizado en esta serie en 42 enfermos, y los resultados son excelentes. No tenemos Visick I porque para nosotros, esta condición por definición no existe en cirugía digestiva, ya que se define como tal aquel enfermo que luego del procedimiento no presenta alteración alguna y la satisfacción es total. Nuestros enfermos han presentado flatulencia, eructos, diarrea u otras condiciones que los clasifican como satisfechos pero en Visick II. (Con satisfacción pero con algunas alteraciones que son pasajeras y de tratamiento médico). Hay pocos Visick III Y IV, Yentran dentro del rango descrito por la literatura.
Conclusión
Nuestro seguimiento a 6 meses, para evaluar los enfermos sometidos a cirugía laparoscópica con un acceso como el que hemos propuesto, es satisfactorio. La técnica laparoscópica reproduce resultados similares a los de la técnica abierta, con menores efectos colaterales como dolor de la herida quirúrgica, estancia hospitalaria e incapacidad.
Por lo anterior, pensamos que la opción de cirugía debe ser considerada seriamente en enfermos con reflujo gastroesofágico patológico que se sale del tratamiento médico convencional y, si es factible, el acceso debe ser laparoscópico con técnica de Toupet para pacientes con alteración de la motilidad del esófago medida por manometría; o por la técnica de Nissen-Rossetti en los enfermos con manometría en la que la motilidad no se observa alterada en forma manifiesta.
Agradecimientos
Los autores agradecen la colaboración de Luis Felipe Millán, Profesor de Artes Plásticas de la Facultad de Artes y Humanidades de nuestra universidad, quien elaboró las ilustraciones de este trabajo.
Abstract
Gastroesophageal reflux as a phenomenon that surpasses the physiologic parameters becomes a chronic and recurrent disease that iscnot curable by medical therapy. Medical treatment ameliorates symptoms and improves the quality of lije, resulting in improved living conditions.
Patients with gastroesophageal reflux should undergo studies tending to categorize the severity of the problem, so as to decide the need for surgical treatment, always consideringthe inherent risk associated with the proposed procedure. Patients of advanced age and uncomplicated reflux are candidates for medical therapy.
On the contrary, younger patients with an extended lije span, in whom long-term drug management is not warranted, plus the fact that the disease tends to be recurrent and to develop complications,. should be consideredfor surgical treatment.
We present our experience with more than 100 patients undergoing laparoscopic surgical treatment over the past two years. Full follow-up has been possible in 50 of them. We discuss our management protocol and experience in the framework of the revolution introduced by laparoscopic surgery in the treatment of hiatal hernia and gastroesophageal reflux; this method of minimally invasive surgery exhibits very promising results with recorded improvement in 90% of cases.
Referencias
1. Dahlia M, Sataloff M, Kishore P: An objective assessment of laparoscopic antireflux surgery. Am J Surg 1997 Jul; 174 (1): 63-7
2. Crookes P, Peters J, DeMeester T: Physiology of the antireflux barrier and diagnostic tests of foregut function. Sem Laparose Surg 1995 Mar; 2 (1): 10-26
3. Smout A, Akkermans L: Enfermedad por reflujo gastroesofágico. En: Smout A, Akkermans L. eds., Fisiología y Patología de la Motilidad Gastrointestinal, 1′. Ed, Petersfield- Reino Unido, Wrightson Biomedical Publishing Ltda, 1992, pp. 67-86
4. Csendes A, Braguetto 1: Fisiología y Motilidad del Esófago. En: Braguetto 1, Csendes A, eds., Patología Benigna del Esófago, l’ Ed, Santiago de Chile, Mediterráneo Ltda, 1989, pp. 13-21
5. Monnier P, Baptiste J et al: Epidemiology and natural history of reflux esophagitis. Sem Laparose Surg 1995 Mar; 2 (1): 2-9
6. Knoll K: Manejo médico del reflujo gastroesofágico. Dig Dis Week, 1997 May. Conferencia magistral. Simp Soc Am Cirug, Tracto Alimentario
7. Mittal R, MacCallum R: Características y frecuencia de las relajaciones transitorias del EEI en pacientes con esofagitis por reflujo. Gastroenterology 1988 Mar; 95 (2,: 593-9
8. Hill L: Cirugía del Esófago. 3′. Ed. Londres, 1990
9. Geoffrey W: Barret’s Esophagus: Patophysiology and management. In: Bremner C, DeMeester T, Peracchia A, eds,. Modern approach to benign esophageal disease: Diagnosis and surgical therapy. 1′. Ed., Saint Louis, Missouri, Quality Medical Publishing Inc., 1995, pp. 69-82
10. Peters J, DeMeester T: Indications principals of procedure selection, and technique of laparoscopic Nissen funduplication. Sem Laparose Surg 1995 Mar; 2 (1): 27-44
11. Hinder R, MacBride P et al: Laparoscopic antireflux surgery in complicated gastroesophageal reflux disease. Sem Laparose Surg 1995 Mar; 2 (1): 45-53
12. Arango L, Angel A, Molina R: Comparación entre Endoscopia digestiva y pHmetría de 24 horas en el estudio del RGE. Presentación de 100 pacientes. Trabajo presentado en el XXIII Congreso Nacional de Avances en Cirugía, Santafé de Bogotá, agosto 1997
13. Arango L, Angel A, Romero O: Comparación entre Endoscopia Digestiva y Anatomía Patológica en pacientes con Esofagitis. Trabajo presentado en el XXIII Congreso Nacional de Avances en Cirugía, Santafé de Bogotá, agosto 1997
14. Materola C, Garrido L et al: Efectos del café sobre la motilidad esofágica: Estudio mediante manometría esofágica. Rev Chil Cir 1997 Jun; 49 (3): 249-55
15. Knoll K: Conceptos sobre manejo actual del RGE. Conferencia magistral. Dig Dis Week. Simposio de la AGA. Washington, mayo 1997
16. Hunter T: Manejo qUlrurglco del RGE. Conferencia magistral. Dig Dis Week. Simposio de la AGA. Washington, mayo 1997.
Correspondencia:
Dr. Lázaro Arango. Carrera 23 No. 62-05. Manizales, Colombia

