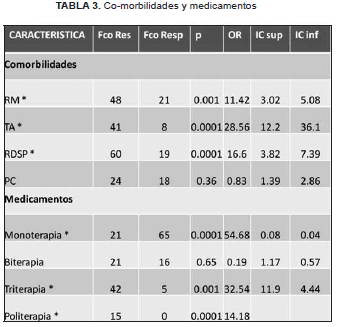
En nuestro estudio encontramos que el retardo mental es una patología 11 veces más frecuente entre los pacientes farmacorresistentes con respecto de los farmacorrespondedores, con un valor de p significativo. De igual manera el riesgo de tener un trastorno del aprendizaje en farmacorresistentes es 28 veces mayor. El retraso del desarrollo psicomotor también se encontró elevado entre aquellos pacientes con epilepsias de difícil control vs farmacorrespondedores (p < 0,05). En el caso de parálisis cerebral y autismo, no se observaron valores significativos. Ver Tabla 3.
Antecedentes farmacológicos
En nuestro estudio se observaron diferencias significativas en la cantidad de individuos en monoterapia que corresponde a los farmacorrespondedores y un número mayor de pacientes en politerapia pertenecientes al grupo farmacorresistente, tal como se esperaba. El valor de OR en este último caso corrobora el hecho de que padecer de epilepsia farmacorresistente condiciona un manejo más agresivo y dinámico en la escogencia de la farmacopea empleada, en procura de un mejor control de crisis. Ver Tabla 4.
Los niveles de los medicamentos en los casos en los cuales se pudo registrar esta variable, permaneció terapéutico en una parte importante de la muestra estudiada, pero cabe recordar que en nuestro país solo se puede medir el nivel de 4 fármacos antiepilépticos (VPA, PHT, PB, CBZ) y que los pacientes farmacorresistentes pasaron por las alternativas de primera línea mucho antes de tener en ellos un claro seguimiento con este tipo de paraclínicos o bien, los reportes eran extraviados por los acudientes del caso.De todas formas, no hubo diferencia significativa respecto al nivel terapéutico de los medicamentos evaluados, en ambos grupos. Ver Tabla 4.

Variables Genotípicas
Al calcular estas frecuencias alélicas en la población, se determinó que los grupos cumplían con Hardy Weinberg. Además, observamos que el coeficiente de Fst fue bajo, lo que nos demuestra ausencia de estratificación poblacional.
Las frecuencias genotípicas para casos fueron de: C/C 23.5%, C/T 55.8% y T/T 20.7%. Para los controles 1: C/C 13.1 %, C/T 54.9% y T/T 31.8%. Para los controles 2: C/C 18 %, C/T 51% y T/T 31%.
Al evaluar este polimorfismo (CC vs TT, codominante; CT vs TT, dominante; CC vs TC, recesivo) encontramos diferencias significativas en estado de dominancia (CT vs TT con un OR de 1,912088 (IC 1,63751-2,2327)), ver Tabla 5.
Discusión
En este estudio analítico tipo casos y controles que involucró a 302 individuos (111 que presentaron epilepsia farmacorresistente y 91 epilepsia controlada), encontramos datos significativos que asocian el genotipo ABCB1 3435 C>T con resistencia farmacológica a los anticonvulsivantes, hallazgos similares a los resultados encontrados por otros autores en diferentes investigaciones del mundo [17], sin embargo estos datos hay que mirarlos con precaución debido a varios factores como la definición de la entidad a evaluar, el tamaño de muestra de la población, el tipo de población (mezclada),entre otros factores.
Cuando se revisaron los estudios sobre esta variante alélica y farmacorresitencia, descubrimos en varios de ellos diferencias en cuanto a la definición de “epilepsia farmacorresistente”, lo que evidentemente puede llevar a una selección sesgada de Los niveles de los medicamentos en los casos la muestra, recordando que la definición en sí, fue desarrollada para pacientes adultos con la patología y no en niños, demostrando una falta de consenso en el tema para este grupo de población.
Al iniciar con el análisis fenotípico en nuestros casos y controles, no observamos diferencias significativas en cuanto al género, consanguinidad ni antecedentes familiares de epilepsia. Por otro lado, respecto al tipo de epilepsia, tampoco existieron diferencias significativas al comparar los diferentes tipos de epilepsia de la clasificación en los grupos analizados.

La clasificación estructural/metabólico de la nueva propuesta, (sintomático de la antigua), es la más frecuentemente encontrada en ambos grupos, lo que posiblemente está en relación con las dificultades propias del sistema de salud de los países subdesarrollados, los cuales permiten que patologías como la hipoxia y asfixia del periodo neonatal, sin mencionar la hipoglucemia y las enfermedades infecciosas prevenibles de la gestación, sigan siendo prevalentes en este grupo etario con sus importantes consecuencias neurológicas posteriores.
Respecto a las comorbilidades asociadas al tipo de epilepsia, descubrimos que, el padecer de epilepsia farmacorresistente incrementa 11 veces la probabilidad de encontrar en estos retardo mental, 28 veces la de padecer de alguno de los trastornos del aprendizaje y 16 veces de tener retraso del desarrollo psicomotor, sin olvidar es la causa de la epilepsia y no la epilepsia en sí, es la posible causante de dichas comorbilidades.
Para finalizar el análisis fenotípico, podemos decir que la monoterapia, como era de esperarse, es la forma de tratamiento más frecuente empleada por los pacientes farmacorrespondedores de una manera significativa, sin que esto implique que se constituya en un factor protector. La triterapia y politerapia resulta ser la forma de manejo más usada por los pacientes con epilepsia farmacorresistente, lo cual manifiesta la dificultad en el control de estas personas y el tratamiento agresivo y dinámico requerido para tratar de reducir al máximo la frecuencia e intensidad de sus crisis.
Desde el punto de vista genotípico, estos resultados son los primeros reportados en la literatura Latinoamérica y proponen a la mutación C>T en la posición 3435 del gen ABCB1 como factor de riesgo asociado a la epilepsia refractaria, tal como lo plantearon Siddiqui et al en 2003 y más recientemente por Kimchi et al, quienes postularon que el polimorfismo C3435T es la posible clave molecular que comanda la especificidad del sustrato al transportador, es decir, el FAE con ABCB1 [20].
Según nuestros datos, tener el polimorfismo C3435T del gen ABCB1 generaría un riesgo de 1,91 de tener una respuesta inadecuada al tratamiento farmacológico en epilepsia. Por lo tanto, presentar un estado heterocigoto (C Wild Type y T Mutante), haría que se expresara de forma inadecuada este transportador a nivel de barrera hematoencefálica,
afectando la transferencia de medicamentos liposolubles del líquido cefalorraquídeo a la sangre [15] y de la célula al espacio intercelular16, de modo que este cambio podría hacer que el medicamento saliera más rápido del blanco farmacológico y redujera su acción química [21].
Pero a pesar de la evidencia in vitro y epidemiológica a favor, otros estudios no han mostrado dicha asociación [19]. Estos resultados contradictorios, incrementan aun el debate del papel de este polimorfismo en la Epilepsia Refractaria y por lo tanto habría que discutir finalmente algunos elementos que pueden ayudar a entender esta discrepancia en los resultados.
Lo primero en tener en cuenta es el reducido tamaño de muestra de la mayoría estudios en mención y en especial en nuestro estudio, el cual, a pesar de ser realizado en 3 centros de referencia nacional, puede tener un “n” insuficiente para dar un real poder al resultado encontrado por nosotros. Esperamos incrementar dicha población para tener más evidencia para zanjar este problema. Segundo, hay que tener en cuenta las diferencias entre las poblacionales evaluadas a nivel mundial. La mayoría de estudios han sido realizados en caucásicos y asiáticos, no en poblaciones latinoamericanas. La distribución alélica es muy diferente entre poblaciones, producto de la diversa selección natural, patrones de migración y efectos fundadores y estocásticos [22]. Por ejemplo, la variante C es más frecuente que la T y es el alelo “ancestro dominante” (africanos 74%) [23]. Y tercero, la diferente dinámica poblacional puede llevar también a discrepancias en los patrones de fenotipos como por ejemplo el de farmacorresistencia.
La población asiática al parecer podría tener un patrón de respuesta diferente a los caucásicos en lo referente a los antiepilépticos [24]. No sabemos aún qué ocurre con la población latinoamericana.
Conclusiones
• Desde el punto de vista fenotípico encontramos que las poblaciones analizadas se comportaron de maneja semejante en las variables esperadas de edad, sexo,consanguinidad, antecedentes familiares y diagnóstico clínico.
• Encontramos diferencias significativas en algunas de las comorbilidades consideradas en el estudio (retardo mental, trastornos del aprendizaje y retraso global del desarrollo psicomotor) en casos vs controles, así como en el número de fármacos empleados por estos grupos.
• Este estudio es el primero a nivel latinoamericano en encontrar asociación la mutación
C>T en 3435 del gen ABCB1 y la presencia de epilepsia refractaria. Se debe aumentar el
tamaño de muestra de nuestra población para determinar la verdadera ausencia o presencia
de asociación la mutación C>T en 3435 del gen ABCB1 en población latinoamericana.
Agradecimientos
• A los pacientes y sus familias
• A los médicos tratantes, docentes universitarios,fellows, residentes e internos que trabajaron en este proyecto
• A los hospitales en donde se llevó a cabo esta investigación.
• A la Facultad de Medicina y a la Vicerrectoría de Investigación de la sede Bogotá DIB, de la Universidad Nacional, por financiar este proyecto.
Referencias
1. Sander J. The epidemiology of epilepsy revisited. Current opinion Neurology. 2003. 16: 165 -170.
2. Kotsopoulos IA, Evers SM, Ament AJ, de Krom MC.Estimating the costs of epilepsy: an international comparison of epilepsy cost studies. Epilepsia. 2001 May;42(5):634-40. Review.
3. Devinski O. Patients with refractory seizures. N Eng J Med 1999; 340: 1565 – 1570
4. Velez A and Eslava-Cobos J. Epilepsy in Colombia:Epidemiologic Profile and Classification of Epileptic Seizures and Syndromes. Epilepsia, 47(1):193–201,2006
5. https://neurologia.rediris.es/congreso-1/conferencias/epilepsia-1.html.
6. Arroyo S, Evaluación de la epilepsia farmacorresistente,rev neurol 2000; 30 (9): 881-886
7. Rogawski MA, Johnson MR. Intrinsic severity as a determinant of antiepileptic drug refractoriness. Epilepsy Currents, Vol. 8, No. 5 (September/October)2008 pp. 127–130
8. Swaiman, K et al. Pediatryc Neurology. Principles and Practice. Fourth Edition.2006 Chapter 40 and 51.
9. Annegers JF, Hauser WA, Elveback LR. Remission of seizures and relapse in patients with epilepsy. Epilepsia 1979; 20: 729-37.
10. Remy S, Beck H.Molecular and cellular mechanisms of pharmacoresistance in epilepsy. Brain
2006;129:18–35.
11. Proper EA, Hoogland G, Kappen SM, et al. Distribution of glutamate transporters in the hippocampus of patients with pharmacoresistant temporal lobe epilepsy. Brain 2002;125:32–4.
12. Dombrowski SM, Desai SY, Marroni M, et al. Overexpression of multidrug resistance genes in endothelial cells from patients with refractory epilepsy. Epilepsia 2001;42:1501–6
13. Juliano RL, Ling V. A surface glycoprotein modulating drug permeability in Chinese hamster ovary cell mutants. Biochim Biophys Acta 1976; 455: 152 – 162
14. Lazarowski A, Lubieniecki F, Camarero S. Multidrug Resistance Proteins in Tuberous Sclerosis and Refractory Epilepsy
15. Tishler DM,Weinberg KI, Hinton DR, et al. MDR1 gene expression in brain of patients with medically intractable epilepsy. Epilepsia 1995;36:1–6.
16. Wijnholds J. Drug resistance caused by multidrug resistance-associated proteins. In: Mechanisms of drug resistance in epilepsy: lessons from oncology. Novartis Foundation, Symposium 243. Chichester: John Wiley; 2002: 69-79.
17. Siddiqui, A., Kerb, R., Weale, M.E., Brinkmann, U.,Smith, A., Goldstein, D.B., Wood, N.W., Sisodiya,S.M., 2003. Association of multidrug resistance in epilepsy with a polymorphism in the drug-transporter gene ABCB1. N. Engl. J. Med. 348, 1442—1448.
18. Garcia Bournissen F, Moretti M, Juurlink D. Polymorphism of the MDR1/ABCB1 C3435T drug-transporter and resistance to anticonvulsant drugs: A metaanalysis. Epilepsia, 50(4):898–903, 2009.
19. Haerian, H Roslan, A. Raymond. ABCB1 C3435T polymorphism and the risk of resistance to antiepileptic drugs in epilepsy: A systematic review and meta-analysis, Seizure 19 (2010) 339–346
20. Kimchi-Sarfaty, C., Oh, J.M., Kim, I., Sauna, Z.E., Calcagno, A.M., Ambudkar, S.V., Gottesman, M.M., 2007. A silent polymorphism in the MDR1 gene changes substrate specificity. Science 315, 525—528
21. Haerian B, et al. , Role of ABCB1 C3435T Variant in Response to Antiepileptic Drugs in Epilepsy: A ReviewMed & Health 2009; 4(2): 64-75
22. Cardon, L.R. & Palmer, L.J. 2003. Population stratification and spurious allelic association. Lancet. 361:598–604.
23. Ameyaw, M.M., Regateiro, F., Li, T., Liu, X., Tariq, M., Mobarek, A., Thornton, N., Folayana, G.O., Githang’a, J., Indalo, A., Ofori-Adjei, D., Price-Evans, D.A. & McLeod, H.L. 2001. MDR1 pharmacogenetics: frequency of the C3435T mutation in exon 26 is significantly influenced by ethnicity. Pharmacogenetics J. 11:217-221.
24. Kwan P et al. Association between ABCB1 C3435T polymorphism and drug-resistant epilepsy in Han
Chinese. Epilepsy & Behavior 11 (2007) 112–117
Recibido: 15 de octubre de 2011
Aceptado: 30 de noviembre de 2011
Correspondencia a: Harvy Mauricio
Velasco Parra, MD, MSc, Esp.
hmvelascop@unal.edu.co