Resumen
Antecedentes: Los estudios clínicos son un tipo de investigación que ayudan a la ciencia médica a encontrar nuevas formas de prevenir, detectar, diagnosticar o tratar enfermedades y hoy en día son los estudios que aportan la mayor evidencia científica frente al uso de nuevas terapias farmacológicas.
Objetivo: Describir la situación actual de los estudios clínicos en Colombia.
Métodos: Se consultaron las bases de datos de registro de estudios clínicos, se realizó una revisión de los aspectos regulatorios y la normatividad relacionada.
Resultados: no es posible determinar la cantidad exacta de estudios clínicos registrados en Colombia debido a que no se cuenta con un sistema de registro. Los estudios clínicos registrados difieren en las bases de datos consultadas.
Desde 1995 a 2013 se identificaron 738 ensayos únicos, el 90% de ellos fueron patrocinados por industrias farmacéuticas, 62% fueron fase III y se han desarrollado principalmente en enfermedades crónicas como el cáncer, las enfermedades cardiovasculares y las degenerativas.
Conclusiones: Colombia carece de un sistema de registro de estudios clínicos que permita realizar un seguimiento adecuado por parte de la comunidad y los profesionales de la salud.
Debido a que el mayor porcentaje de estos estudios han sido patrocinados por la Industria Farmacéutica, se hace necesario fomentar y desarrollar estrategias que permitan el desarrollo de investigación propia.
Palabras clave:
Ensayos clínicos, legislación, Comités de Ética, Colombia.
Overview of Clinical Trials in Colombia
Abstract
Background: New ways to prevent, detect, diagnose or treat different conditions are subjects addressed by clinical trials. Most scientific support for new pharmacologic therapies comes through their results. Objectives: To describe current situation of clinical trials in Colombia.
Methods: Clinical trial registry databases were consulted and regulatory aspects were reviewed.
Results: We could not possibly determine the exact number of clinical trials registered in Colombia, since there is neither a reliable nor complete implemented registry system. Those registered differ in number in consulted databases. 738 clinical trials were identified from 1995 to 2013, 90% sponsored by the pharma industry. Most of them were Phase III (62%), done in chronic illnesses like cancer, cardiovascular and degenerative conditions.
Conclusions: For the community and health proffessionals to follow adequately clinical trials in Colombia, a good registration program must be implemented. Since most studies are now sponsored by pharmaceutical companies, it is also important to design strategies to impulse self-developed drug research.
Key words: Clinical trials, legislation, Ethics Committees, Colombia.
Introducción
Los estudios clínicos son un tipo de investigación que busca examinar nuevas formas de prevenir, detectar, diagnosticar o tratar enfermedades (1,2).
El desarrollo comienza con formular la pregunta clínica de investigación que usualmente es referida como hipótesis y se refina para determinar parámetros importantes del estudio como por ejemplo, el tipo de terapia que va a ser comparada, la naturaleza de los desenlaces medidos, el número de sujetos en cada grupo de tratamiento y los criterios de inclusión para el enrolamiento al estudio (3).
Usualmente los desenlaces que se evalúan con estos estudios están orientados esencialmente a valorar la eficacia de la terapia, la toxicidad relacionada con el medicamento, la calidad de vida, el tiempo de supervivencia global y libre de la enfermedad (4).
El aporte a la ciencia médica que hacen los estudios clínicos son esenciales para generar nuevo conocimiento y mejorar el enfoque y tratamiento de las enfermedades, pero el desarrollo de este tipo de estudios debe cumplir con los estándares éticos establecidos internacionalmente sobre investigación con seres humanos, que deben ser evaluados localmente por los comités de ética, quienes se encargan garantizar la integridad ética y la seguridad de los sujetos que participan en la investigación (5).
Investigación fue la infección VIH/ SIDA
Para garantizar la transparencia de la investigación fue la infección VIH/ SIDA con un 58.3% (7/12). Se encontró además en el 25% (3/12) de los casos el antecedente de neumonía. Dos pacientes se consideraron inmuno competentes, y tres pacientes presentaron como factor predisponente tabaquismo y en otro, psoriasis (Tabla 4). Y para consolidar la validez y el valor de los resultados de los datos científicos, la declaración deHelsinki estableció que “se debe registrar cada ensayo clínico en una base de datos de acceso público antes de reclutar el primer sujeto”, esta información debe contener datos sobre el diseño y la conducción del estudio; deberá ser de acceso público y ser administrada por una entidad de vigilancia y control en investigación.
Esa información deberá permitir que quienes participan en la toma de decisiones en el área de la atención de la salud tengan acceso a una visión completa de la investigación. El registro de todos los estudios clínicos es una responsabilidad científica, ética y moral con la sociedad(6).
Uno de los aspectos principales para el desarrollo de estos estudios que soporta la garantía de la calidad de la investigación:
Es la adherencia al marco regulatorio establecido tanto a nivel nacional e internacional y es fundamental su cumplimiento por parte de las Instituciones y los investigadores.
Debido a que la investigación clínica experimental tiene antecedentes lamentables que tuvieron lugar principalmente durante la segunda guerra mundial, desde 1947 se empezaron a establecer una serie de reglamentaciones relacionadas con el consentimiento y la voluntad de las personas para participar libre y autónomamente en investigaciones experimentales, estableciendo que el riesgo debe ser sopesado contra los beneficios y las acciones que causen daño deben ser evitadas (Código de Nüremberg) .
Posteriormente en 1964 con la declaración de Helsinki se establecieron los criterios éticos para la participación de seres humanos en investigaciones experimentales (7):
Luego en 1979 el reporte de Belmont estableció convicciones éticas necesarias en la investigación, en 1982 The Council for International Organizations of Medical Sciences (CIOMS) emitió directrices internacionales para la investigación (8) , posteriormente se creó The International Conference on Harmonisation (ICH) en 1990 para emitir recomendaciones y lograr una mayor armonización en la interpretación y aplicación de las directrices técnicas en Investigación experimental (9) y finalmente la Organización Mundial de la Salud (OMS) en 1995 emitió las guías de práctica clínica (GCP) que son las actuales normas aplicables a escala mundial para el desarrollo de la investigación con seres humanos (10).
En Colombia con la resolución 8430 de 1993 se establecieron las normas científicas, técnicas y administrativas para la investigación en salud y se establecieron los requisitos para el desarrollo de la actividad investigativa en salud; mediante la creación de los comités de ética en investigación y con la resolución 3823 de 1997 se estableció que todo patrocinador deberá contar con una aprobación previa emitida por el Instituto Nacional de Vigilancia de Medicamentos y Alimentos, (INVIMA) antes de iniciar cualquier investigación con medicamentos en seres humanos (11).
En el año 2008 con la resolución 2378 se adoptaron las Buenas Prácticas Clínicas (BPC):
Para certificar a las instituciones que conduzcan investigación con medicamentos en seres humanos; esta adopción se hizo de la “Guía de Buenas Prácticas Clínicas para investigaciones de productos farmacéuticos en seres humanos” que la Organización Mundial de la Salud (OMS) elaboró en 1995 con el fin de establecer estándares aplicables en todos los países.
A partir de esta norma ninguna institución podrá adelantar estudios de investigación con medicamentos en seres humanos, si no cuenta con esta certificación, ya que se considera que la certificación en BPC es una garantía de cumplimiento con los estándares internacionales de calidad científica y ética, que están dirigidos al diseño, realización, registro y redacción de informes de estudios que implican la participación de seres humanos (12).
El cumplimiento de las BPC, asegura públicamente que las Instituciones realizan, protección de los derechos, seguridad y bienestar de las personas que participan en los estudios clínicos de acuerdo con los principios de la declaración de Helsinki y este cumplimiento asegura también la credibilidad de los datos obtenidos de la investigación.
Para el 2013, en Colombia se encuentran 116 Instituciones certificadas por el INVIMA en BPC:
Son los únicos sitios autorizados para realizar estudios clínicos con medicamentos en seres humanos, de las cuales 107 (92,2%) son de naturaleza privada, 93 (80,2%) corresponden a instituciones prestadoras de servicios de salud y 21 (19,8%) a centros de investigación.
En cuanto a la distribución geográfica, en Bogotá se encuentran 44 (37,9%), Medellín 17 (14,7%), Barranquilla 14 (12,1%) Cali 11 (9,5%), Bucaramanga 7 (6%) otras ciudades 23 (19,8%). Así mismo se encuentran 63 comités de ética certificados por el INVIMA en buenas prácticas clínicas.
De esta manera Colombia ha implementado y establecido las condiciones que garantizan que la investigación experimental con seres humanos está cumpliendo con los estándares internacionales de calidad y seguridad.
Métodos – Situación de los Estudios Clínicos en Colombia
Se consultaron los estudios clínicos en los que Colombia participa o ha participado de la base de datos de Estados Unidos www.clinicaltrials.gov.co de Service of the U.S. National Institutes of Health; la base de datos de la plataforma de registros internacionales de ensayos clínicos de la Organización Mundial de la Salud International Clinical Trials Registry Platform (ICTRP) y la base de datos Biomed Central Limited de Europa www.controlled-trials.com.
Se consultaron también las actas de registro de protocolos de investigación clínica en Colombia que se encuentran publicadas en el INVIMA.
Resultados – Situación de los Estudios Clínicos en Colombia
Los ensayos clínicos vienen experimentado un importante crecimiento a nivel mundial reflejado especialmente en la última década.
De acuerdo con la información publicada en www.clinicaltrials.gov para el año 2005 estaban registrados aproximadamente 25.000 estudios y para el año 2013 aparecen 142.880.
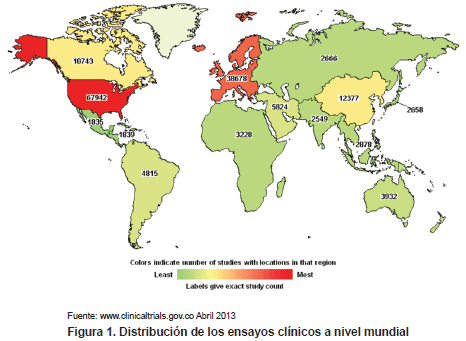
Aproximadamente el 52% se han realizado en Norte América, el 27% en Europa, el 18% en Asia y el 3% en América Latina (Figura 1), en donde Brasil registra el mayor número con 3.527, seguido por Argentina con 1.512, Chile 815, Perú 650 y Colombia con 628; sin embargo en la Plataforma de registros internacionales de ensayos clínicos (ICTRP) de la Organización Mundial de la Salud (OMS) aparecen 870 estudios para Colombia, mientras que en la base de datos de Biomed Central Limited se registran 439 y en el registro de protocolos de investigación clínica del INVIMA aparecen 418 estudios clínicos.
La gran mayoría de estudios aparecen registrados en más de una base de datos y al depurar la información entre estas bases de datos se identificaron 738 estudios únicos:
De los cuales 666 (90,2%) correspondieron a estudios multicéntricos patrocinados por la industria farmacéutica, 185 (25%) se encuentran activos, la distribución por fases de desarrollo correspondió a 15 (2%) estudios para la fase I, 185 (25%) estudios para la fase II, 458 (62%) estudios para la fase III y 74 (10%) estudios para la fase IV.
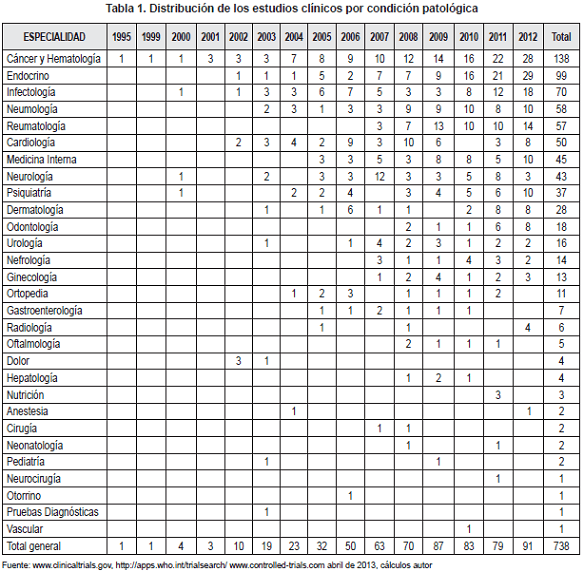
En cuanto a la distribución por especialidades y enfermedades, el cáncer y las patologías hematológicas ocuparon el primer lugar con 138 (17,6% principalmente cáncer de mama, pulmón, digestivo, renal, cervical y páncreas), seguido por endocrinología con 99 ensayos (12,7% principalmente diabetes mellitus), infectología con el 9 % (principalmente manejo del VIH), infectología con 70 (9,5%),neumología con 58 (7,4% principalmente asma y enfermedad pulmonar obstructiva crónica), reumatología con 57 (7,7% (principalmente artritis reumátide) cardiología con 50 (6,8%, (principalmente infarto de miocardio, síndrome coronario agudo), medicina interna 45 (6,1%), neurología 43 (5,8%), psiquiatría 37 (5%), dermatología 28 (3,8%) otros 113 (15,3%) (Tabla 1).
Discusión – Situación de los Estudios Clínicos en Colombia
Los resultados obtenidos de los estudios clínicos poseen la capacidad de aportar evidencia valiosa que puede llegar a satisfacer la necesidad de generar nuevo conocimiento para el manejo y tratamiento de las enfermedades más prevalentes y se constituyen en una herramienta primordial para el mejoramiento de la atención en salud en los países.
Con los datos obtenidos no es posible establecer la cantidad exacta de estudios clínicos que se han realizado a la fecha en Colombia.
Sin embargo, la cantidad que aparece registrada en las bases de datos consultadas es baja si se compara con países similares en la región y esta situación nos lleva a establecer qué aspectos son los que favorecen o limitan el desarrollo de nuevos estudios clínicos en el país.
A pesar de que en Colombia se cuenta con el INVIMA como agencia reguladora para la importación de suministros, medicamentos y estudios clínicos, con normatividad establecida, con Instituciones certificadas en buenas prácticas clínicas y con comités de ética en investigación que garantizan la integridad ética de la investigación en humanos y que son esenciales para el desarrollo de nuevas investigaciones con medicamentos, se hace necesario desarrollar un sistema de registro de estudios clínicos que cuente con información detallada de cada protocolo como fecha de inicio, fecha de cierre, tamaño de muestra, fase de desarrollo, estado de reclutamiento, tipo y diseño del estudio, países participantes, criterios de inclusión y exclusión, indicación, tipo de intervención, objetivos del estudio, datos de contacto, entre otros, para que se fomente la transparencia y la ética, y facilite de esta manera el acceso de esta información a la comunidad en general (13-15).
Existe otro aspecto que podría influenciar el desarrollo de nuevos estudios clínicos en Colombia y que tiene que ver con los comités de ética.
Actualmente la relación entre el número de Instituciones certificadas y el de comités de ética no es proporcional, debido a que sólo 63 Instituciones (54,3%) poseen comité propio; además, es bien sabido que los tiempos de evaluación de protocolos de investigación por parte de los comités tiende a ser muy prolongado y tal vez las causas de estas demoras se deban a la falta de conocimiento y/o entrenamiento de los integrantes de los comités en la evaluación de este tipo de investigaciones.
Analizando la información de los estudios clínicos realizados a la fecha en Colombia se ha evidenciado una situación similar a lo encontrado a nivel regional y mundial (16), en donde el mayor porcentaje de realización de estudios se ha concentrado típicamente en enfermedades crónicas como el cáncer, las enfermedades cardiovasculares y las degenerativas como artritis entre las más frecuentes, situación definida por los patrocinadores internacionales que no necesariamente se corresponde con la realidad sanitaria y con las necesidades del país según las tasas de mortalidad y morbi-mortalidad publicadas.
En cuanto a la fase de desarrollo más frecuente de estos estudios correspondió a la III; esta condición podría explicarse debido a que la gran mayoría corresponden a estudios internacionales y en múltiples centros, patrocinados principalmente por la industria farmacéutica.
La baja cantidad de estudios fase I corresponden a los estudios propios y esta situación nos lleva a plantear la necesidad de gestionar recursos económicos y fortalecer la formación en investigación en nuestras universidades para que de esta manera el desarrollo de investigación propia responda a las necesidades locales y así Colombia no sea únicamente un atractivo escenario para el desarrollo de estudios clínicos de las industrias farmacéuticas internacionales.
Conflictos de interés: Ninguno informado.
Referencias – Situación de los Estudios Clínicos en Colombia
- 1. National Cancer Institute. Cancer Clinical Trials [Internet]. 2013 [cited 2013 Jan 15]. Available from: https://www.cancer.gov/cancertopics/factsheet/Information/clinical-trials
- 2. Chow S-C. Design and analysis of clinical trials, Concepts and Methodologies. Second Edi. Library of Congress Cataloging-in-Publication Data is available., editor. New Jersey: John Wiley & Sons, Inc., Hoboken, New Jersey; 2004. p. 750.
- 3. Svolba G, Bauer P. Statistical quality control in clinical trials. Controlled clinical trials [Internet]. 1999 Dec;20(6):519–30. Available from: https://www.ncbi. nlm.nih.gov/pubmed/10588293
- 4. Pocock SJ. Clinical Trials: A Practical Approach. New York: Wiley medical publication.; 1984. p. 266.
- 5. Miranda M,C. Comités de ética de investigación en humanos: una experiencia colombiana. Revista Colombiana de Bioética. 2006;1(1):141–9.
- 6. World Health Organization. International Clinical Trials Registry Platform (ICTRP) [Internet]. 2013. Available from: International Clinical Trials Registry Platform (ICTRP).
- 7. Kong H, West S. Ethical principles for medical research involving human subjects. European journal of emergency medicine : official journal of the European Society for Emergency Medicine [Internet]. 2001 Sep;8(3):221–3. Available from: https://www.ncbi.nlm.nih.gov/pubmed/19886379.
- 8. The Council for International Organizations of Medical Sciences [Internet]. Available from: https://www.cioms.ch/
- 9. The International Conference on Harmonisation [Internet]. Available from: https://www.ich.org/
- 10. World Health Organization. Guidelines for good clinical practice (GCP) for trials on pharmaceutical products* [Internet]. 1995. p. 35. Available from: https://apps.who.int/prequal/info_general/documents/GCP/gcp1.pdf
Bibliografías – Situación de los Estudios Clínicos en Colombia
- 11. República de Colombia. Ministerio de Salud. Resolución 3823 por la cual se crea La Comisión Asesora de Ciencia y Tecnología del Ministerio de Salud y se dictan normas para regular las actividades de desarrollo científico en el sector salud. 1997.
- 12. República de Colombia. Ministerio de Salud. Resolución 2378, por la cual se adoptan las Buenas Prácticas Clínicas para las instituciones que conducen investigación con medicamentos en seres humanos. 2008.
- 13. Cuervo LG, Clark ML. El registro internacional de ensayos clínicos. Revista Panamericana de Salud Pública. 2006;19(6):365–70.
- 14. Antonio Ugalde, Homedes N. Cuatro palabras sobre ensayos clínicos : ciencia / negocio , riesgo / beneficio. Salud Colectiva. 2011;7(2):135–48.
- 15. Reveiz L, Saenz C, Murasaki RT, Cuervo LG, Ramalho L. Progress and challenges of clinical trials registration in latin america and the caribbean. Rev Peru Med Exp Salud Publica. 2011;28(4):676–81.
- 16. Parra-Salgado AM. Estado de la investigación clínica en Colombia relacionado con medicamentos en el desarrollo de nuevas moléculas. Universidad Nacional de Colombia, Facultad de Ciencias Departamento de Farmacia. Tesis de Grado. 2011. p. 123.
Dirección para correspondencia:
jcarreno@cancer.gov.co
Autores
1 Alexander Carreño Dueñas. MD, MSc. Grupo de Investigación clínica, Instituto Nacional de Cancerología, Bogotá D.C., Colombia