Actualmente este es un fenómeno bien conocido cuya intensidad depende de factores como la severidad y la cronicidad de la infección, el fondo genético del huésped, el tipo de parásito y el poli parasitismo (18).
Este conocimiento ha abierto nuevas perspectivas de tratamiento de las alergias y otras enfermedades inflamatorias crónicas no infecciosas, hasta el punto de usarse, ya en ensayos clínicos, la denominada terapia helmíntica en humanos, consistente en infectar los pacientes con helmintos no patógenos y aprovechar sus propiedades inmunomoduladoras (19,20).
Aunque estos enfoques han tenido resultados contradictorios y han suscitado polémicas, demuestran el valor potencial de aprovechar las propiedades inmunomoduladoras de los helmintos (21,22).
Dichas propiedades han sido demostradas, además de manera experimental, en un proceso ejemplar de investigación básica (23-27), que ha llevado al descubrimiento de un gran número de moléculas anti inflamatorias procedentes de diversos parásitos que infectan tanto al humano como a otros animales y destinadas a reemplazar la terapia con helmintos vivos (14,20,28).
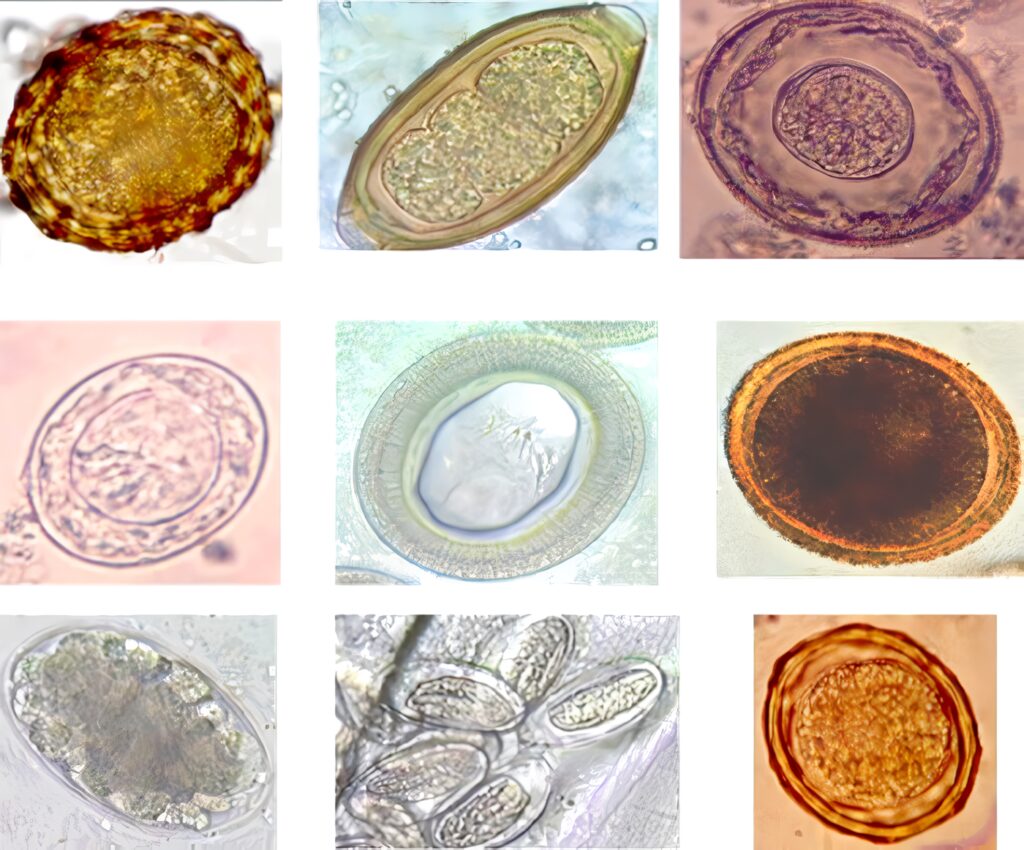
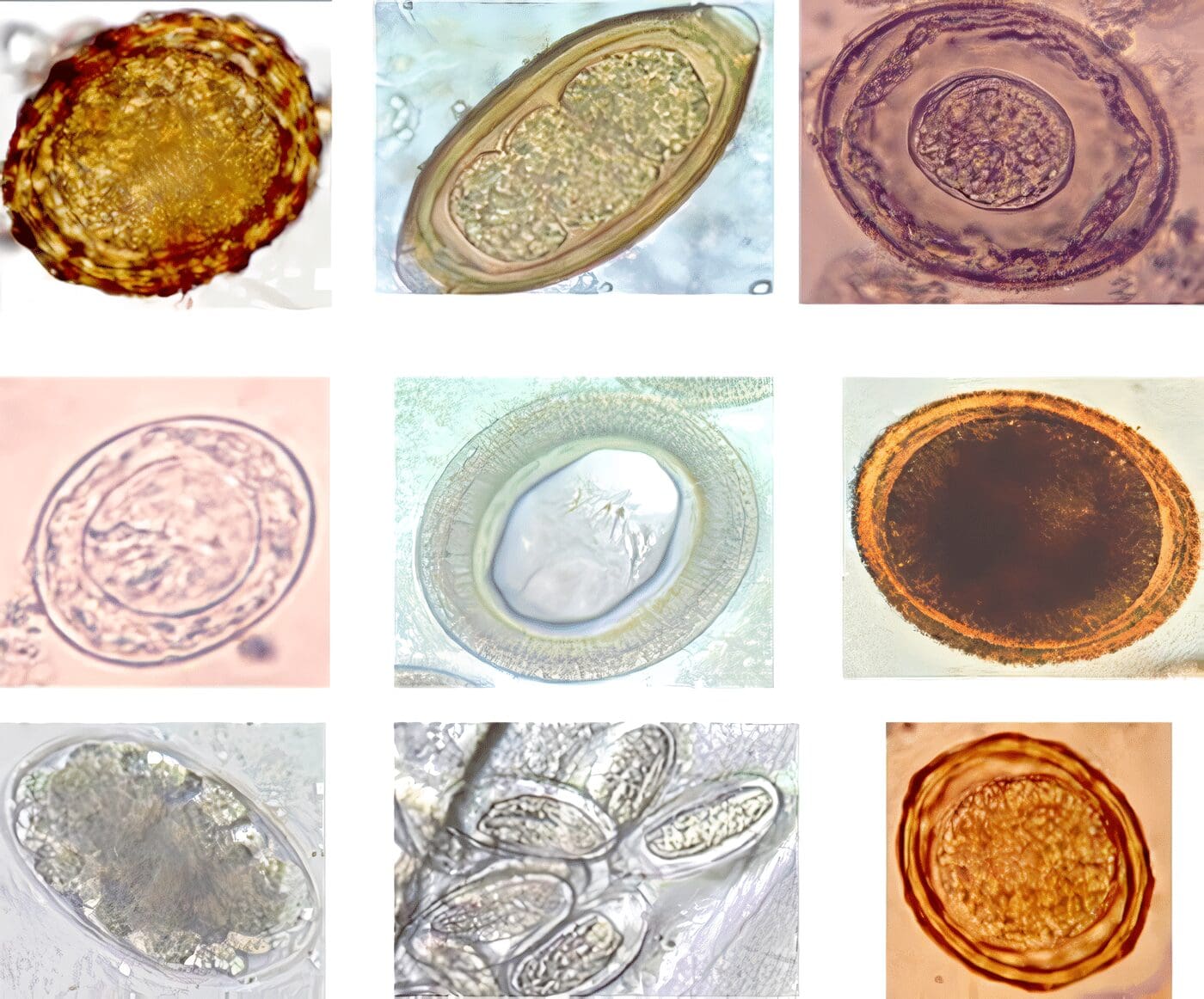
Entre las fuentes de esas moléculas está Ascaris lumbricoides, el cual merece especial mención porque es uno de los parásitos más frecuentes y además de sus graves efectos sobre la salud de los niños, es capaz de inducir inmunosupresión impidiendo la acción de los programas de vacunación contra virus y bacterias (16,29,30) y en otros escenarios puede aumentar la frecuencia y severidad de las alergias (31-33). (Ver también: Virus Zika)
Se calcula, de acuerdo con el genoma de Ascaris suum (34), que estas especies podrían tener alrededor de 15 moléculas inmunomoduladoras. Sin embargo, aunque este efecto ha sido estudiado a nivel experimental (35) son pocas las moléculas que se han aislado, siendo PAS- 1 una de las mejores analizadas (36-39).
Recientemente nuestro grupo ha explorado las propiedades anti inflamatorias de la cistatina de A. lumbricoides (rAl-CPI) (40), iniciando una nueva fase en la investigación del lado inmunosupresor de este nematodo. Las cistatinas pertenecen a una numerosa familia de inhibidores de proteasas de cisteína y se habían obtenido de Onchocerca volvulus, Acantocheilonema viteae, Brugia malayi y otros parásitos, siendo la de filaria (AvCystatin) la más estudiada (41,42).
La cistatina de Ascaris (rAl-CPI) disminuye considerablemente la inflamación del intestino cuando se emplea en un modelo de colitis inducida en ratones. Esto se acompañó de una sobreexpresión de los genes de IL- 10 y TGFB y una reducción de la expresión de IL-6 y TNFA.
Además indujo la producción de IL-10 y TGFB por los macrófagos (40), todos estos indicadores de una actividad anti inflamatoria importante, la cual ha sido confirmada a nivel pulmonar en un modelo murino de alergia respiratoria inducida por ácaros, en el que se observó además la inducción de células T reguladoras (43).
Dado que esta molécula tiene pocas posibilidades de inducir reacciones alérgicas adversas (44) es bastante promisoria en cuanto a su uso como anti inflamatorio en problemas intestinales y pulmonares.
El control de las helmintiasis es necesario y urgente
Como se deduce de esta breve revisión, la investigación sobre las enfermedades parasitarias es importante no solo desde el punto de vista científico sino también en medicina y salud pública. Hoy se ha extendido a otros temas distintos a su impacto negativo general en salud humana y animal, destacando los posibles efectos positivos sobre el desarrollo y control del sistema inmunológico.
Los descubrimientos sobre el efecto inmunomodulador de las helmintiasis nos han hecho caer en cuenta que, exceptuando el SIDA, son los procesos infecciosos que más suprimen mecanismos inmunitarios, despertando esperanzas para controlar la epidemia actual de enfermedades por exceso de dichos mecanismos.
Desde un punto de vista evolutivo podría pensarse que han sido parte esencial en la filogenia del sistema inmunitario, por lo que han sido incluidos en el grupo de «viejos amigos» junto con la microbiota y otros componentes de nuestro organismo (45). Sin embargo, es conveniente hacer algunas precisiones que eviten confusiones en el público general, pues ya se han generado preocupaciones en algunos grupos de la comunidad científica (22).
Los helmintos son parásitos y las helmintiasis son perjudiciales para la salud, en consecuencia su erradicación debe ser el principal objetivo, invirtiendo la atención y el dinero necesario para cambiar los componentes físicos y culturales que determinan su existencia.
Es absurdo y lamentable que en Colombia todavía encontremos municipios como Loma Arena (Bolívar) donde más del 60% de la población esté parasitada (46) y peor aún, que esta situación se haya mantenido por muchos años a pesar de haber sido registrado y comunicado por las vías apropiadas (47). Los parásitos que allí se encuentran son variados, incluyendo los denominados geohelmintos, cuya erradicación es técnicamente posible y dejó desde hace mucho tiempo de ser un problema científico para convertirse en objeto de las políticas de salud pública gubernamentales.
Conclusión
Es importante insistir en que sería muy equivocado creer que la sola ausencia de infecciones, cualquiera que sea su etiología pueda explicar el incremento de las enfermedades inflamatorias crónicas; se sobreentiende que muchos otros factores han intervenido.
En caso de ser verdaderas las hipótesis que hemos mencionado respecto al componente de la higiene, es posible que el control y la eventual erradicación de las helmintiasis del planeta, lo cual en términos científicos significa modificar la biodiversidad y nuestras relaciones naturales con el ambiente (11), afectará en alguna medida nuestra fisiología. Afortunadamente la investigación básica y biotecnológica nos permitirá conservar las moléculas inmunomoduladoras de origen parasitario que pudieran hacernos falta o que tal vez ya nos estén haciendo falta.
Agradecimientos
Varias de las investigaciones citadas han sido financiadas por Colciencias (Contrato 590-2013) y la Universidad de Cartagena (Convocatorias Internas).
Referencias
1. Gupta S. Trials and tribulations. Nature. 2017; 548: S28-S31.
2. Lundback B, Backman H, Lotvall J, Ronmark E. Is asth¬ma prevalence still increasing? Expert Rev Respir Med. 2016; 10: 39-51.
3. Platts-Mills TA. The allergy epidemics: 1870-2010. Jour¬nal Allergy Clin Immunol. 2015; 136: 3-13.
4. Caraballo L, Zakzuk J, Lee BW, Acevedo N, Soh JY, et al. Particularities of allergy in the Tropics. World Allergy Organ J. 2016; 9: 20.
5. Dennis R, Caraballo L, Garcia E, Caballero A, Aristiza¬bal G, et al. Asthma and other allergic conditions in Co¬lombia: a study in 6 cities. Ann Allergy Asthma Immunol. 2004; 93: 568-574.
6. Dennis RJ, Caraballo L, Garcia E, Rojas MX, Rondon MA, et al. (2012) Prevalence of asthma and other aller¬gic conditions in Colombia 2009-2010: a cross-sectional study. BMC Pulm Med 12: 17.
7. Strachan DP (1989) Hay fever, hygiene, and household size. BMJ 299: 1259-1260.
8. Bach JF (2002) The effect of infections on susceptibility to autoimmune and allergic diseases. N Engl J Med 347: 911-920.
9. Rook GA, Martinelli R, Brunet LR (2003) Innate immune re¬sponses to mycobacteria and the downregulation of atopic responses. Curr Opin Allergy Clin Immunol 3: 337-342.
10. Rook G, Backhed F, Levin BR, McFall-Ngai MJ, McLean AR (2017) Evolution, human-microbe interactions, and life history plasticity. Lancet 390: 521-530.
11. Haahtela T, Holgate S, Pawankar R, Akdis CA, Benja¬ponpitak S, et al. The biodiversity hypothesis and aller¬gic disease: world allergy organization position state¬ment. World Allergy Organ J. 2013; 6: 3.
12. Gerrard JW, Geddes CA, Reggin PL, Gerrard CD, Horne S. Serum IgE levels in white and metis communities in Saskatchewan. Ann Allergy. 1976; 37: 91-100.
13. Hotez PJ, Wilkins PP. Toxocariasis: America’s most com¬mon neglected infection of poverty and a helminthiasis of global importance? PLoS Negl Trop Dis. 2009; 3: e400.
14. Caraballo L. Ascaris and Allergy. In: Holland CV, editor. Ascaris: the neglected parasite: Elsevier. 2013; 21-50.
15. Caraballo L. Los diversos efectos de las helmintiasis so¬bre la inflamación alérgica. Rev Acad Colomb Cienc Ex Fis Nat. 2016; 40: 200-2008.
16. Cooper PaFC. Immunology of Ascaris and immunomod¬ulation. In: Holland CV, editor. Ascaris the neglected par¬asite. London: Elsevier. 2013; 3-19.
17. Caraballo L AN, Buendía E. Human Ascariasis Increas¬es the Allergic Response and Allergic Symptoms. Curr Trop Med Rep. 2015; 2: 224–232.
18. Alcantara-Neves NM, Veiga RV, Dattoli VC, Fiaccone RL, Esquivel R, et al. The effect of single and multiple infections on atopy and wheezing in children. J Allergy Clin Immunol. 2012; 129: 359-367, 367 e351-353.
19. Elliott DE, Weinstock JV. Nematodes and human thera¬peutic trials for inflammatory disease. Parasite Immunol 39. 2017.
20. Smallwood TB, Giacomin PR, Loukas A, Mulvenna JP, Clark RJ, et al. Helminth Immunomodulation in Autoim¬mune Disease. Front Immunol. 2017; 8: 453.
21. Evans H, Mitre E. Worms as therapeutic agents for al¬lergy and asthma: understanding why benefits in animal studies have not translated into clinical success. J Aller¬gy Clin Immunol. 2015; 135: 343-353.
22. Briggs N, Weatherhead J, Sastry KJ, Hotez PJ. The Hygiene Hypothesis and Its Inconvenient Truths about Helminth Infections. PLoS Negl Trop Dis 10: e0004944.
23. Maizels RM, Pearce EJ, Artis D, Yazdanbakhsh M, Wynn TA (2009) Regulation of pathogenesis and immunity in helminth infections. J Exp Med. 2016; 206: 2059-2066.
24. McSorley HJ, Hewitson JP, Maizels RM. Immunomodu¬lation by helminth parasites: defining mechanisms and mediators. Int J Parasitol. 2013; 43: 301-310.
25. Weinstock JV, Elliott DE. Helminth infections decrease host susceptibility to immune-mediated diseases. J Im¬munol. 2014; 193: 3239-3247.
26. Steinfelder S, O’Regan NL, Hartmann S. Diplomatic Assistance: Can Helminth-Modulated Macrophages Act as Treatment for Inflammatory Disease? PLoS Pathog. 2016, 12: e1005480.
27. Lambrecht BN, Hammad H. The immunology of the al¬lergy epidemic and the hygiene hypothesis. Nat Immu¬nol; 2017; 18: 1076-1083.
28. Wammes LJ, Mpairwe H, Elliott AM, Yazdanbakhsh M. Helminth therapy or elimination: epidemiological, immu¬nological, and clinical considerations. Lancet Infect Dis. 2014; 14: 1150-1162.
29. Salgame P, Yap GS, Gause WC. Effect of helminth-in¬duced immunity on infections with microbial pathogens. Nat Immunol. 2013; 14: 1118-1126.
30. Urban JF, Jr., Steenhard NR, Solano-Aguilar GI, Daw¬son HD, Iweala OI, et al. Infection with parasitic nem-atodes confounds vaccination efficacy. Vet Parasitol. 2007; 148: 14-20.
31. Hunninghake GM, Soto-Quiros ME, Avila L, Ly NP, Liang C, et al. Sensitization to Ascaris lumbricoides and se¬verity of childhood asthma in Costa Rica. J Allergy Clin Immunol. 2007; 119: 654-661.
32. Buendía E. The IgE respons e to Ascaris molecular com¬ponents is associated with clinical indicat rs of asthma severity. WAO Journal. 2015; 8: 8.
33. Ahumada V, Garcia E, Dennis R, Rojas MX, Rondon MA, et al. IgE responses to Ascaris and mite tropomyosins are risk factors for asthma. Clin Exp Allergy. 2015; 45: 1189-1200.
34. Jex AR, Liu S, Li B, Young ND, Hall RS, et al. Ascaris suum draft genome. Nature. 2011; 479: 529-533.
35. Titz TO, de Araujo CAA, Enobe CS, Rigato PO, Oshiro TM, et al. Ascaris suum infection modulates inflamma¬tion: Implication of CD4(+) CD25(high) Foxp3(+) T cells and IL-10. Parasite Immunol 39. 2017.
36. Oshiro TM, Macedo MS, Macedo-Soares MF. Anti-in¬flammatory activity of PAS-1, a protein component of Ascaris suum. Inflamm Res. 2005; 54: 17-21.
37. Araujo CA, Perini A, Martins MA, Macedo MS, Mace¬do-Soares MF. PAS-1, a protein from Ascaris suum, modulates allergic inflammation via IL-10 and IFN-gam¬ma, but not IL-12. Cytokine. 2008; 44: 335-341.
38. de Araujo CA, Perini A, Martins MA, Macedo MS, Mace¬do-Soares MF. PAS-1, an Ascaris suum protein, mod¬ulates allergic airway inflammation via CD8+gammad¬eltaTCR+ and CD4+CD25+FoxP3+ T cells. Scand J Immunol. 2010; 72: 491-503.
39. Antunes MF, Titz TO, Batista IF, Marques-Porto R, Olivei¬ra CF, et al. Immunosuppressive PAS-1 is an excretory/ secretory protein released by larval and adult worms of the ascarid nematode Ascaris suum. J Helminthol. 2015; 89: 367-374.
40. Coronado S, Barrios L, Zakzuk J, Regino R, Ahumada V, et al. A recombinant cystatin from Ascaris lumbricoides attenuates inflammation of DSS-induced colitis. Parasite Immunol 39. 2017.
41. Schuijs MJ, Hartmann S, Selkirk ME, Roberts LB, Open¬shaw PJ, et al. The Helminth-Derived Immunomodulator AvCystatin Reduces Virus Enhanced Inflammation by Induction of Regulatory IL-10+ T Cells. PLoS One. 2016; 11: e0161885.
42. Venugopal G, Mueller M, Hartmann S, Steinfelder S. Dif¬ferential immunomodulation in human monocytes ver¬sus macrophages by filarial cystatin. PLoS One. 2017; 12: e0188138.
43. Coronado S, Zakzuk J, Regino R, Ahumada V, Benedetti I, et al. Cystatin from the nematode ascaris lumbricoides reduces inflammation in a mouse model of allergic asth¬ma. Allergy. 2017; 72: 386-387.
44. Coronado S MM, Zakzuk J, Caraballo L. Ascaris lum¬bricoides cystatin induces specific IgE but not allergic response. Front Immunol. 2015. DOI: 10.3389/conf.fim¬mu.2015.05.00295.
45. Rook GA. 99th Dahlem conference on infection, inflam¬mation and chronic inflammatory disorders: darwinian medicine and the ‘hygiene’ or ‘old friends’ hypothesis. Clin Exp Immunol. 2010; 160: 70-79.
46. Zakzuk J, Casadiedo S, Mercado A, Alvis-Guzman N, Caraballo L. Ascaris lumbricoides induces, both, reduc¬tion and increase of asthma symptoms in a rural commu¬nity. ALLERGY. 2017; 72: 494-495.
47. Agudelo-López S ea. Prevalencia de Parasitosis Intestinales y Factores Asociados en un Corregimiento de la Costa Atlántica Colombiana. Rev Salud Publica. 2008; 10: 633-642.
Recibido: 3 de diciembre de 2017
Aceptado: 17 de diciembre de 2017
Correspondencia:
Luis Caraballo lcaraballog@unicartagena.edu.co