La ND afecta a un tercio de la población de DM 1 o DM 2. Los factores que afectan la progresión de la enfermedad incluyen la excreción de albúmina de acuerdo con la edad, la duración de la DM, el tabaquismo, el control adecuado o no de la glicemia, el nivel de colesterol y el uso de Inhibidores de la Enzima Convertidora de la Angiotensina (IECA), moléculas que a partir del captopril en el año 1979 se han venido utilizando, con el desarrollo posterior de los antagonistas de receptores de la angiotensina II (ARA II) y ahora, los bloqueadores de renina.
Para el año 2050 la prevalencia de la DM se incrementará con implicaciones socio-económicas, especialmente en los países en vía de desarrollo. La prevalencia global de la ND en los adultos se estima que se elevará de un 6.4% (285 millones de pacientes) en el 2010 a 7.7% (439 millones de pacientes) en el 2030.
Este incremento será mayor en los países en vías de desarrollo (69%) comparado con los países desarrollados (20%). Esto se dará en más del 90% de países muy poblados como China o India y este incremento se verá en nefrópatas por DM 2. (Lea también: Nefropatía Diabética: Otros Nuevos Pasos)
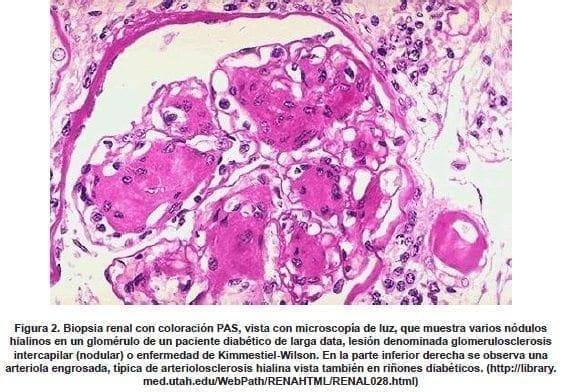
El estudio Joslin en 79 pacientes con DM 1, a inicialmente normoalbuminúricos, desarrollaron microalbuminuria y ERC, especialmente en grupos de avanzada edad, estados 4 y 5;; la desarrollaron en 12 años, en un 29%. De este 29%, la mitad nunca tuvo proteinuria o regresaron a normoalbuminuria (9 pacientes), probado por biopsia renal que tenía ND. Las causas se encuentran aún en investigación (13).
Para llegar a una ND terminal no es necesario que el paciente pase por la etapa de proteinuria. Es cierto que en el pasado prevalecía la visión de que la DM 2 se debía a lesiones en el glomérulo,con una caracterizada progresión de la microalbuminuria a la proteinuria y a la enfermedad renal crónica (ERC).
Ahora se han encontrado pacientes que llegan a diálisis sin proteinuria, y se ha establecido más allá de toda duda que existe un tipo de nefropatía diabética no-proteinúrica que puede ser el resultado de la enfermedad microvascular, como lo sugiere la observación de microinfartos cerebrales en la Resonancia Magnética Nuclear (RMN) con predicción subsiguiente de pérdida de la función renal.
Un hallazgo similar de disminución de la filtración glomerular (FG) con normo albuminuria fue confirmado en DM 1 Y DM 2, 30% con FG
Se ha observado albuminuria muy pronunciada en diabéticos sin IECA, comparados con pacientes que tomaban enalapril, según un trabajo del Grupo de Familias de Gargano, Italia (16). En estos últimos, hubo una reducción del 50 % en la excreción de albúmina.
La HbA1c debe estar en menos de 6 en las personas normales y en menos de 7, en diabéticos; la dosis de insulina se debe disminuir en el paciente con ERC. A los pacientes diabéticos se les pusieron 5 metas (Tabla 1). A los que cumplían menos de 3 metas, se les iban aumentando las lesiones y para los pacientes que cumplían 3 o más de estas metas, eran muy pocas las complicaciones después de 25 meses.
El mismo grupo estudió la relación entre la resistina sérica, la rata albúmina/creatinina urinaria (ACR) y la FG en 635 personas blancas, no diabéticas y no tratadas, encontrando que los niveles de resistina estaban independientemente asociadas con ACR y con FG en este grupo de pacientes, teniendo en cuenta que la resistina y la FG comparten algunos antecedentes genéticos. Su estudio sugiere fuertemente que la resistina juega un papel en la modulación de la función renal (17).
Como los pacientes con enfermedad renal terminal ( ERT) presentan anemia severa por deficencia
de eritropoyetina (EPO), edema, falla cardiaca y la diálisis generalmente mejora estos problemas, no se conoce aún cuál es el tiempo óptimo para iniciar la diálisis en estos enfermos, lo que hay que
investigar porque se ha sugerido que un comienzo temprano podría ser dañino, y aumentaría el riesgo de muerte. Investigadores japoneses se pusieron en la tarea de averiguar qué factores de riesgo de diálisis temprana podría haber en pacientes con ND.
De 52 pacientes, 19 estaban en diálisis temprana y 33, en diálisis tardía. Se observó una asociación significativa de diálisis temprana y edad superior a los 65 años, y la aparición de neumonía, por lo que ellos recomiendan reforzar la vacunación contra neumococo en pacientes mayores, para evitar la diálisis temprana (18).
Patogénesis de la Nefropatía Diabética
Esta es multifuncional. Tienen que ver en ella la HTA, el metabolismo anormal de los carbohidratos, metabolismo anormal de los lípidos, acumulación de lípidos, regulación de factores profibróticos (renina, angiotensina II, factor beta transformador del crecimiento y factor de crecimiento endotelial vascular), citocinas inflamatorias (FNT, interleukina 1B, quimioatraccion MM), incremento del estrés oxidativo, incremento en la producción de productos avanzados de la glicosilación (1, 19).
Manejo de la Diabetes
Esto se hará según el estado en que se encuentre el paciente. Si es normotenso y no tiene albuminuria alta, se requiere controlarle la hipergli cemia y la presión arterial. Cuando ya empieza a notarse una albuminuria persistente, se deben dar IECA o ARA II.
Si el paciente pasa ya a un estado 3 de la ND, hay que dar IECA más ARA II, o más un diurético, combinados con una dieta y se deben añadir otros antihipertensivos (no se deben dar IECA/ARA II si la creatinina es superior a 3 mg/dl, pero se puede usar un diurético de asa, como la furosemida). Si hay proteinuria (o hiperlipidemia), añadir una estatina. Si prevenimos la ND, controlar la glicemia;; los pacientes tratados con terapia convencional con agentes orales deben pasar a insulina, o a un esquema agresivo de insulinoterapia (Tabla 1).

Una revisión sistemática con metaanálisis realizada para evaluar los beneficios y daños de la la insulinoterapia intensiva versus convencional en pacientes con DM 1, incluyó 18 ensayos clínicos aleatorios con 2254 participantes. Todos los ensayos tuvieron alto riesgo de sesgo. No hubo un efecto significativo sobre la mortalidad en la terapia intensiva, pero puede haber efectos benéficos en el aspecto macrovascular y en la nefropatía, aunque este enfoque tiene efectos perjudiciales por hipoglicemia grave (20).
La aplicación convencional de la insulina es cada doce horas, iniciando con 10 unidades antes del desayuno y comida, bien NPH o 70/30.
Se pue de iniciar administrando 0,3 U/kg/peso –pasando paulatinamente a una dosis de 0,5/0,6 mg/kg/peso diarios y distribuyendo 2/3 de la dosis antes del desayuno, y 1/3 antes de la cena, y una proporción rápida/NPH de 1/3 antes del desayuno y 1/2 antes de la cena. Teniendo en cuenta que para un adulto de 65-70 kg, la dosis total es usualmente de unas 40 unidades diarias (25 en a.m., 15 en p.m.), de las veinticinco unidades de la mañana podrían ser aproximadamente 20 de NPH y 5 de cristalina, y de las quince de la noche, 10 de NPH y 5 de cristalina.
Cuando las glicemias postprandiales están >180 mg/dL, es conveniente utilizar la mezcla 70/30. Estas dosificaciones son algo empíricas, pues dependen del grado de absorción y de la sensibilidad de los receptores (que tienen que ver con el peso, con medicamentos, etc.). Lo importante es cumplir con la meta de obtener hemoglobinas glicosiladas de <7%, o glicemia en ayunas normales y postprandiales un poco más altas (21).
En quienes se va incrementando la microalbuminuria, se debe usar terapia intensiva en lugar de terapia estándar de insulina. En este caso, para cuatro inyecciones diarias (y el correspondiente monitoreo), dar el 50% de la dosis como insulinas glargina o detemir, una vez al día;; además, insulina de acción rápida, 20% antes del desayuno, 15% antes del almuerzo y otro 15% antes de la comida (Tabla 2).

La terapia intensiva tiene más riesgo de hipoglicemia. Cada vez es más frecuente el uso de modernas bombas de infusión continua de insulina para enfermos con DM 1, en los que el medicamento se administra de acuerdo con la ingesta, el ejercicio y los niveles de glicemia, con buenos resultados por el entrenamiento adecuado que los pacientes reciben. Es conveniente recordar que los requerimientos diarios de insulina se reducen en pacientes con falla renal.
La hipertensión arterial también debe manejarse agresivamente, para proteger la función renal.
Inhibidores del Sistema Reninaangiotensina- Aldosterona
Los fármacos que inhiben el SRAA han demostrado su eficacia en el tratamiento de la hipertensión, la nefropatía diabética y son de elección en las estrategias terapéuticas para reducir el riesgo cardiovascular y se usan para retardar el comienzo o disminuir la progresión de la ND (22-25). Hasta ahora solo había dos posibilidades para inhibir el SRAA, usar los IECA o los ARA-II.
Recientemente se ha introducido en terapéutica el grupo de los inhibidores directos de la renina por vía oral, cuyo primer representante es el aliskiren, aprobado para el tratamiento de la hipertensión arterial (26).
Esto es importante porque la inhibición de la renina se plantea como la forma más eficaz de bloquear el SRAA al actuar en su punto inicial, la transformación de angiotensinógeno en angiotensina I, paso limitante del sistema, sin afectar al metabolismo de las kininas ni producir fenómeno de escape, además de reducir la actividad de renina plasmática.
Desde el punto de vista farmacológico, aliskiren se comporta como antagonista competitivo del angiotensinógeno en la renina, ya que ocupa el sitio activo de la enzima e impide que lo haga el angiotensinógeno y, por tanto su conversión en Angiotensina I (27, 28).
El uso de inhibidores del SRAA debe suspenderse en pacientes con niveles de creatinina sérica superior a 3 mg/dL. Hay partidarios del manejo agresivo con una combinación de IECA y ARA II, aunque es necesario la observación cautelosa por el riesgo de hiperkalemia o de disminución de la filltración glomerular.
Una revisión muy reciente sobre el tema del uso combinado de IECA y ARA II mostró que tanto en estudios experimentales como en humanos con ERC hay reducción de la proteinuria con prevención de la aparición de lesiones estructurales y de ESRD, de manera más efectiva que con una sola droga.
El “Protocolo de Remisión Clínica” fue utilizado en humanos, y la efectividad de dosis máximas tolerables de la combinación medicamentosa fue particularmente notoria en ERC no diabética. Sin embargo los estudios ONTARGET para pacientes con riesgo cardiovascular aumentado y ALTITUDE, para enfermos con DM 2 y nefropatía declarada, la adición de un IECA o un inhibidor de renina al ARA II losartán no arrojó resultados superiores al uso aislado del losartán.
El estudio VA NEPHRON D encontró que la terapia combinada de losartán y lisinopril disminuyó en un 34% el riesgo de reducciones predefinidas en la tasa estimada de filtración glomerular, ERT o muerte, en comparación con el uso de losartán solo en 1.448 pacientes con DM 2 y nepfropatía manifiesta. Infortunademente el efecto del tratamiento no logró alcanzar una significación nominal (p = 0,07) debido a la interrupción prematura del estudio.
Por lo tanto, el Protocolo de Remisión Clínica se considera la herramienta más poderosa para prevenir la progresión a ERT en la ERC proteinúrica no diabética. Los resultados del estudio VALID –actualmente en desarrollo– mostrarán si este enfoque se puede extender de forma segura a los pacientes con DM 2 (29).
Terapias Nuevas
No solo se debe controlar la glicemia sino también estrictamente la presión arterial y los factores de crecimiento profibrótico, que median el paso fibrótico en DM 1 y DM 2. El SRRA estimula factores factores de crecimiento implicados como efectores directores en fibrosis del glomérulo, como el factor de crecimiento tumoral B (30, 31).
En un estudio aleatorio con 77 pacientes y con Pirfenidona, pequeña molécula sintética con potente actividad antifibrótica, hubo mejoría de la tasa de filtración glomerular después de un año de estar usando Pirfenidona (32).
Las moléculas Betaglicano y Decorin son anticuerpos neutralizantes del TGF-B (33). La Fluorofenodina, otro agente piridínico, ha sido estudiado en un modelo de células renales estimuladas por la AT II;; reduce la producción de ROS e inhibe la expresión del TGF-B y es más potente que la pirfenidona (26). Una antraquinona (Rheína o ácido cásico) aislada del ruibarbo, mejora el daño renal, reduce la expansión de la matriz mesangial extracelular y en las células epiteliales (34, 35).
Entre otras moléculas que inhiben la fibrosis tenemos el ácido antranílico (Tranilast) y la Bardoxolena;; vale decir que la Bardoxolena creó una conmoción porque los resultados han sido de reversión, es decir, la recuperación de la FG en un trabajo con un seguimiento a un año, mostrando recuperación de entre 20 y 45 ml/min/1.73 m2, en un estudio doble ciego, aleatorizado (36). El Tranilast (ácido antranílico) suprime la síntesis de colágeno interfiriendo al TGF-B (37, 38).

