El oncogén HER 2 se encuentra amplificado entre una quinta y una tercera parte de los canceres de mama (9), lo cual justifica su estudio en todos los canceres invasivos de mama, y constituye tanto un factor pronóstico como una diana terapéutica (10), ya que dada la alta frecuencia del cáncer de mama en la consulta Oncológica, hace imprescindible su adecuada y segura confirmación.
Como se ha demostrado en diferentes publicaciones, la valoración del HER2 puede llegar a ser incorrecta hasta en un 20% de las muestras estudiadas (11), representando ello que hasta una quinta parte de las pacientes o bien reciba un tratamiento que no necesita y que tiene una toxicidad cardiaca no despreciable, o lo que es igual o peor, que no reciba la terapia antiHER2 teniendo el receptor sobreexpresado con el subsiguiente mayor riesgo de recidiva o diseminación.
Si a este porcentaje “esperable” de error en la identificación de la sobreexpresion del gen, le sumamos que en un nuestro medio (Colombia), una buena parte de las biopsias iniciales de las neoplasias de mama se procesan en laboratorios externos de Patología de mediano o bajo volumen, donde las técnicas de fijación pueden deteriorar parcialmente la calidad de las muestras que posteriormente se remiten a los centros de Patología de alto volumen como el nuestro, la posibilidad de una lectura inapropiada es aún mayor, pues una adecuada técnica de fijación es necesaria para el correcto procesamiento del tejido y la posterior validez del test (12).
Es por tanto una necesidad sentida para el Oncólogo Clínico cuando tiene enfrente una paciente con cáncer de mama, saber con exactitud si dicha paciente es portadora o no de la amplificación del HER2, para poder tratar a todas las que la tienen la amplificación y a ninguna de las que no se encuentre amplificado HER2.
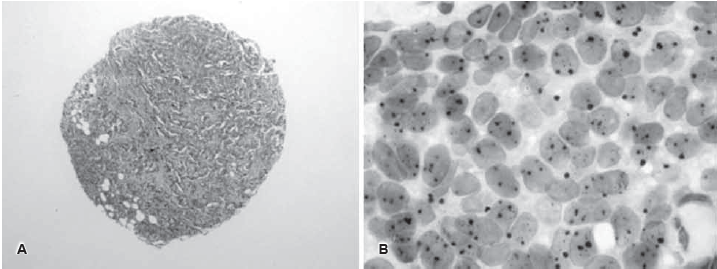
Figura 1. Caso discordante con la hibridación in situ fluorescente (FISH) A. Microarreglo de tejido, carcinoma
ductal infiltrante (Coloración de Hematoxilina y Eosina). B. Estudio de amplificación del oncogén HER2
(negro) y el centrómero del cromosoma 17 (rojo), se cuantificaron en total 40 núcleos, resultado final no
amplificado (Her2/Chr17 ratio: 1.72)
El desarrollo y la implementación de métodos de detección de la amplificación del HER2 que sean accesibles y reproducibles como el Dual ISH, y que por el tipo de procesamiento de la muestra o tejido sean mucho menos susceptibles al error, constituye un apoyo diagnóstico muy bienvenido en la consulta oncológica.
Como bien se explica en este artículo, el Servicio de Patología de la Fundación Valle del Lili logró validar un test de detección de la amplificación del gen altamente confiable y reproducible, que dadas las condiciones del entorno en que se mueve el paciente Oncológico en la región, debería convertirse en estándar de detección al ser comparable con el FISH.
Conclusiones
– La técnica de hibridación in situ cromogénica y con plata (Dual ISH) es una metodología validada por la FDA y que tiene tan buena sensibilidad y especificidad como la hibridación in situ fluorescente (FISH).
– Este método permite tener un estudio morfológico mejor del área a estudiar, es más costo efectivo
y tiene tantas ventajas como la técnica FISH.
– El Servicio de Patología de la Fundación Valle del Lili logró validar un test de detección de la amplificación del gen HER2 altamente confiable y reproducible.
Conflictos de Interés
Ninguno declarado
Fuentes de financiación
Fondos provenientes de la Fundación Valle del Lili, Departamento de Patología y Medicina de Laboratorio.
Referencias
1. Francis GD, Jones MA, Beadle GF, Stein SR. Brightfield in situ hybridization for HER2 gene amplification in breast cancer using tissue microarrays. Correlation between chromogenic (CISH) and automated silverenhanced (SISH) methods with patient outcome. Diagn Mol Pathol 2009; 18: 88-95.
2. Sua Luz F, Maestro de las Casas ML, Vidaurreta M, et al. Review: Fluorescent In Situ Hybridization (FISH), chromogenic in situ hybridization (CISH) and Chromogenic In Situ Hybridization with Silver (DISH): its use for detection of HER2 gene amplification in breast cancer. J Pathol Senol Breast. 2010; 23 (4): 168-172.
3. Ramieri MT, Murari R, Botti C, Pica E, Zotti G, Alo PL. Detection of HER2 amplification using the SISH technique in breast, colon, prostate, lung and ovarían carcinoma. Anticancer Res 2010; 30:1287-1292.
4. Papouchado BG, Myles J, Lloyd RV, Stoler M, oliveira AM, Downs-Kelly E, Morey A, Bilous M, Nagle R, Prescott N, Wang L, Dragovich L, McElhinny A, Garcia CF, Ranger-Moore J, Free H, Powell W, Loftus M, Pettay J, Gaire F, Roberts C, Dietel M, Roche P, Grogan T, Tubbs R. Silver in situ hybridization (SISH) for determination of HER2 gene status in breast carcinoma. Comparison with FISH and assessment of interobserver reproducibility. Am J Surg Pathol 2010; 34: 767-776.
5. Shousha S, Peston D, Amo Takyi B, Morgan M, Jasani B. Evaluation of automated silver-enhanced in situ hybridization (SISH) for detection of HER2 gene amplification in breast carcinoma excision and core biopsy specimens. Histopathol 2009; 54: 248-253.
6. Dietel M, Ellis IO, Hofler H, Kreipe H, Moch H, Dan kof A, Kolble K, Kristiansen G. Comparison of automated silver enhanced in situ hybridization (SISH) and fluorescence ISH (FISH) for the validation of HER2 gene status in breast carcinoma according to the guidelines of the American Society of Clinical Oncology and the College of American Pathologists. Virchow’s Arch 2007; 451: 19-25.
7. García-Caballero T, Grabau D, Green A et al. Determination of HER2 amplification in primary breast cáncer using dual-colour chromogenic in situ hybridization is comparable to fluorescence in situ hybridization: a European multicentre study involving 168 specimens. Histopathol 2010, 56, 472–480.
8. Aaron M Gruver, Ziad Peerwani, Raymond R Tubbs. Out of the darkness and into the light: bright field in situ hybridisation for delineation of ERBB2 (HER2) status in breast carcinoma. J Clin Pathol 2010; 63:210-219.
9. Slamon DJ, Clark GM, Wong SG, et al: Human breast cancer: Correlation of relapse and survival with amplification of the HER-2/neu oncogene. Science 235:177-182, 1987
10. Yamauchi H, Stearns V, Hayes DF: When is a tumor marker ready for prime time? A case study of c-erbB-2 as a predictive factor in breast cancer. Clin Oncol 19:2334-2356, 2001
11. Paik S, Bryant J, Tan-Chiu E, et al: Real-world performance of HER2 testing-National Surgical Adjuvant Breast and Bowel Project experience. J Natl Cancer Inst 94:852-854, 2002
12. Zarbo RJ, Hammond ME: Her-2/neu testing of cáncer patients in clinical practice. Arch Pathol Lab Med 127:549-553, 2003
Recibido: 15 de junio, 2014.
Aprobado: Agosto 15, 2014
Correspondencia: Dra. Luz Fernanda Sua.
Fundación Valle del Lili, Departamento de patología y medicina
de laboratorio. Av. Simón Bolívar. Cra 98 # 18-49, Cali,
Colombia. Email: lufer24@hotmail.com
