MEDICINA FAMILIAR
EDUCACIÓN CONTINUADA PARA EL MEDICO GENERAL
Desafortundamente, en la persona con DM2 es difícil determinar cuándo comenzó la diabetes, y por lo tanto no es raro encontrar signos de complicaciones microvasculares en el paciente recién diagnosticado. Es muy probable que ese paciente lleve al menos 5 a 10 años con la enfermedad silenciosa. De hecho, las primeras manifestaciones de las complicaciones microvasculares son asintomáticas:
– La retinopatía diabética
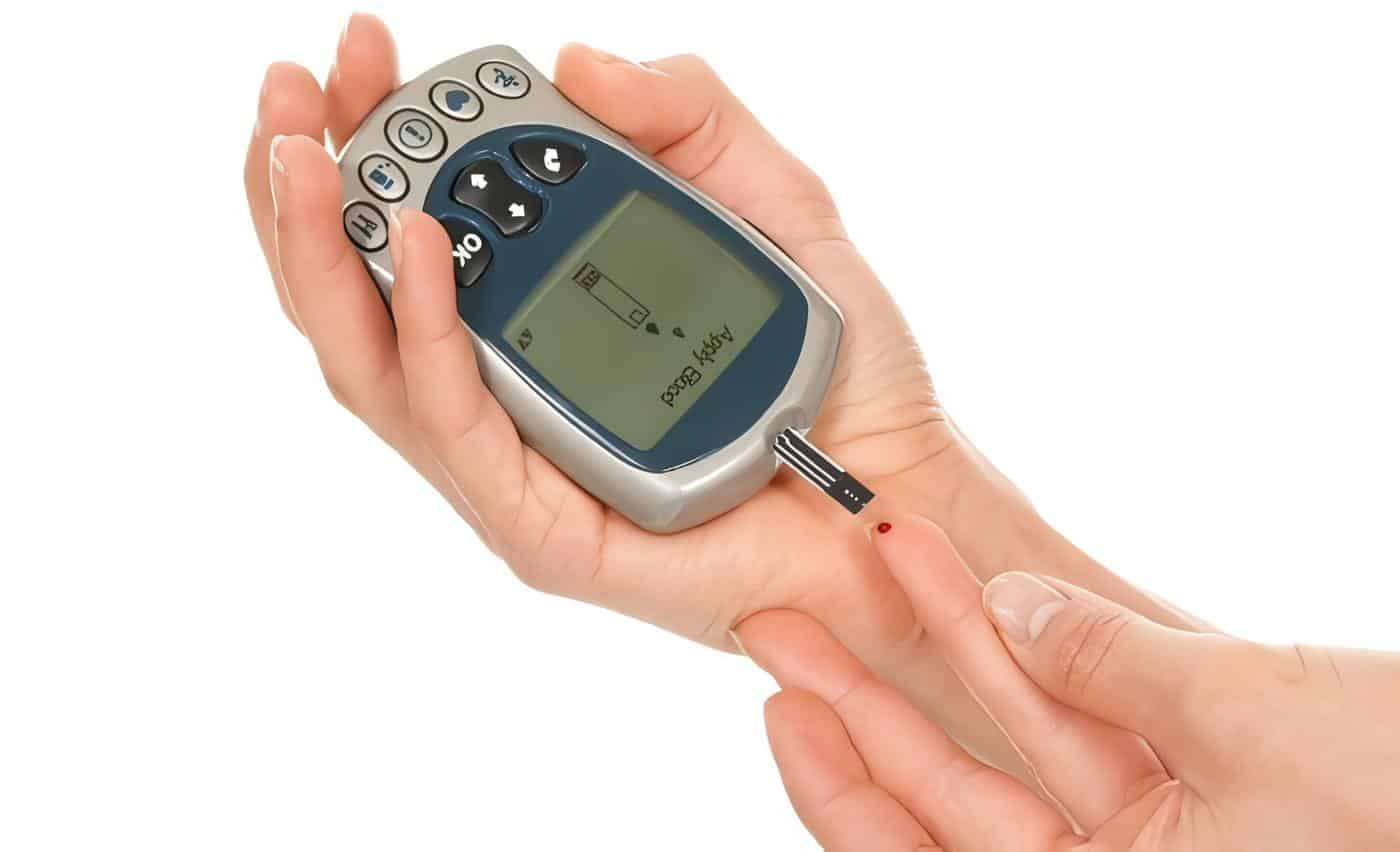
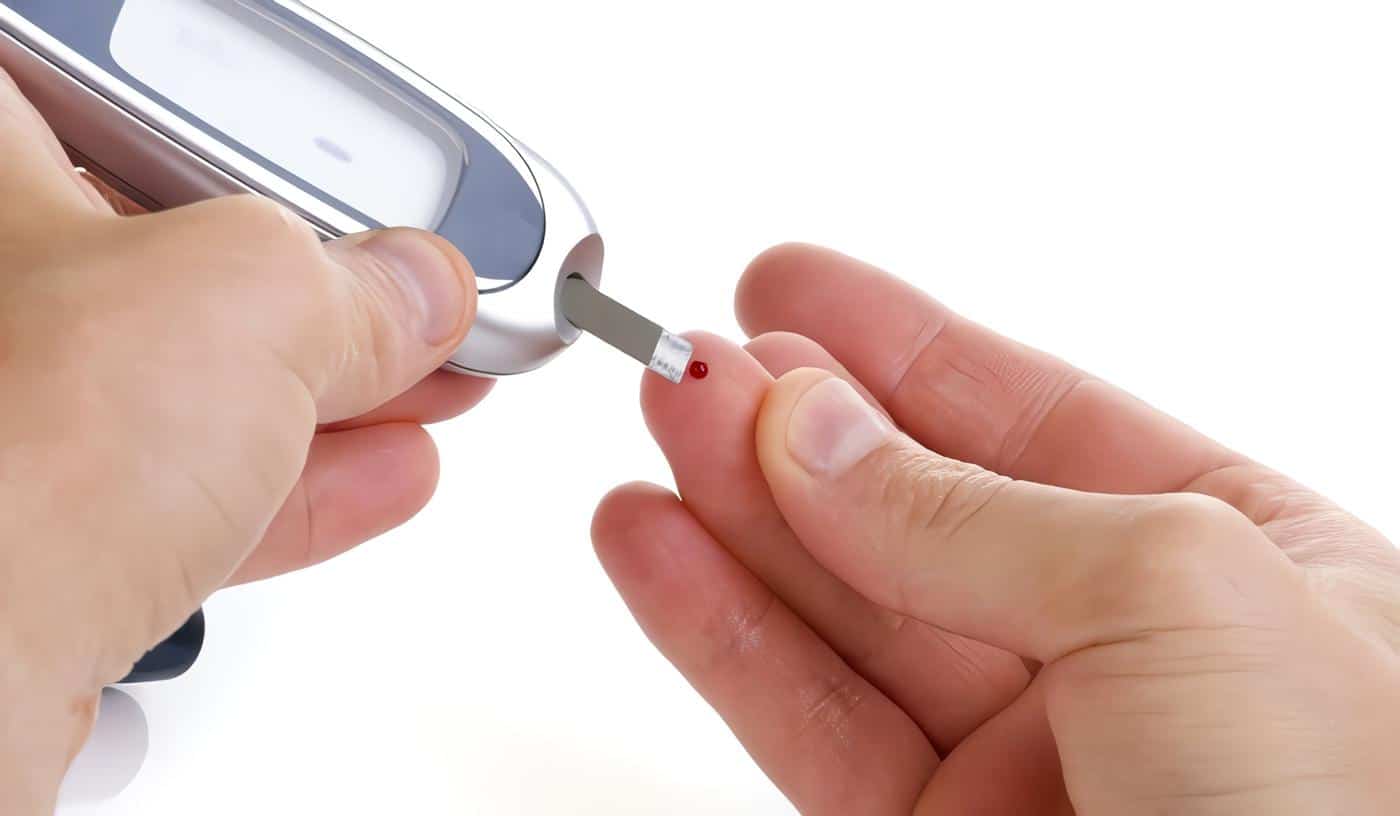
Se manifiesta inicialmente por la presencia de puntos rojos en la retina que pueden corresponder a microaneurismas o microhemorragias y que no afectan la visión. Sin embargo su presencia obliga a un examen oftalmológico especializado. Los cambios de la refracción pueden ocurrir por elevaciones marcadas de la glucemia que afectan el cristalino, y en ese caso son reversibles al cabo de uno a dos meses de control glucémico. Sin embargo una pérdida rápida y progresiva de la agudeza visual puede indicar la presencia de edema macular y debe ser evaluada por un oftalmólogo con experiencia en retinopatía diabética.
– La nefropatía diabética
Se manifiesta inicialmente por la detección de albúmina en orina en muy pequeñas cantidades (microalbuminuria).
Para ello es necesario medir la microalbuminuria en la primera orina de la mañana y calcular su relación con la creatinuria. Si esta relación es mayor de 30 mg por gramo de creatinuria y se confirma en un segundo examen, se considera diagnóstica de nefropatía temprana que obliga a la administración de inhibidores de la enzima convertidora de angiotensina (IECA) o a bloqueadores del receptor de angiotensina (ARA) cuyas dosis deben ser ajustadas para mantener una tensión arterial cercana a 120/80 si es posible.
Con un tratamiento adecuado, la microalbuminuria debe disminuír e inclusive normalizarse.
De lo contrario, el paciente debe ser remitido al especialista. Cuando la microalbuminuria es mayor de 300 mg por gramo de creatinuria o se detecta proteinuria mayor de 500 mg en 24 horas, el paciente tiene una nefropatía clínica que debe ser manejada por un especialista en diabetes quien buscará el concurso del nefrólogo cuando lo considere oportuno. Es importante anotar que la presencia de microalbuminuria indica disfunción endotelial y conlleva un riesgo tres veces mayor de tener un evento coronario, por lo cual obliga a un control muy estricto de todos los factores de riesgo cardiovasculares (ver adelante).
– La neuropatía periférica
Puede manifestarse clínicamente por disestesias y parestesias simétricas en los pies de predominio nocturno que mejoran al caminar. Estos síntomas pueden mejorar con la administración de 10 mg de amitriptilina en las noches o con 900 a 1200 mg diarios de gabapentino. Sin embargo puede cursar asintomática. La pérdida del reflejo aquiliano es un signo tardío de neuropatía periférica. El signo más precoz que se puede detectar clínicamente es la disminución de la sensibilidad vibratoria que se observa al aplicar un diapasón al dorso del grueso artejo o alguno de los maléolos del cuello del pie.
Cuando la disminución es severa, ya hay también una reducción crítica de la sensibilidad que pone al pie en riesgo de desarrollar una úlcera (pie diabético). Este punto crítico de la sensibilidad se puede detectar aplicando un monofilamento de 10 g en la planta del pie (especialmente bajo los artejos y bajo las cabezas de los metatarsianos). Si el paciente no lo siente en varias aplicaciones, debe ser remitido a una clínica del pie (o a un servicio de podología) para una evaluación completa con el objeto de impartir educación preventiva y corregir defectos del pie y del calzado. Si el paciente ya tiene un pie diabético (presencia de úlcera), debe se remitido al especialista en diabetes quien buscará el concurso de otros especialistas cuando lo considere oportuno (podólogo, ortopedista, cirujano vascular).
Una úlcera mal manejada puede conducir a gangrena y amputación.
Detección y manejo de factores de riesgo cardiovasculares
Las personas con DM2 tienen con mayor frecuencia factores de riesgo cardiovasculares (FRCV) y además estos tienen mayor impacto en el paciente, por lo cual deben ser manejados en forma más estricta:
– La dislipidemia
Más frecuente es la mixta, con un colesterol LDL (cLDL) moderadamente elevado, unos triglicéridos altos que lo pueden estar aún mas cuando la diabetes está descompensada, y un colesterol HDL bajo.
El adecuado control de la glucemia tiende a reducir especialmente los triglicéridos, por lo cual no se justifica iniciar un fibrato en un paciente descompensado, excepto si tiene concentraciones superiores a 1.000 mg/dl por el riesgo de pancreatitis. Las estatinas están indicadas si la persona con DM2 tiene un cLDL superior a 130 mg/dl a pesar de llevar una dieta baja en AG saturados y colesterol, y de haber alcanzado metas admisibles de glucemia y HbAlc. Si el paciente tiene otro FRCV además de la diabetes (incluyendo microalbuminuria) o si ha tenido un evento coronario (angina o infarto) debe tener un cLDL menor de 100 mg/dl por lo cual casi siempre es necesario prescribir una estatina desde el comienzo. Si los triglicéridos siguen elevados cuando se haya alcanzado la meta de cLDL con la estatina (mayores de 200 o de 150 mg/dl según el caso), puede ser necesaria la adición de un fibrato, pero este tipo de combinación puede tener efectos secundarios severos y debe ser indicada y manejada por un especialista en diabetes.
– La hipertensión arterial
Es mas frecuente en la persona con DM2 y es además un factor de riesgo para el deterioro de la función renal en el paciente con nefropatía. Por lo tanto toda persona con DM2 debe tener una TA cercana a 130/80 mmHg o menor. Si tiene microalbuminuria, el fármaco de elección es un IECA o un ARA. La combinación de los dos ha demostrado también ser útil, aunque puede ser más costo-efectivo adicionar un diurético tiazídico en bajas dosis cuando no es suficiente la monoterapia. También se puede agregar un calcioantagonista, especialmente en población geriátrica o cuando hay hipertensión sistólica aislada.
– El hábito de fumar cigarrillos es inadmisible en la persona con diabetes y debe proscribirse.
Detección y manejo de la enfermedad macrovascular
– La enfermedad coronaria es dos veces más frecuente en el hombre con diabetes y hasta cinco veces más frecuente si es mujer.
Además, puede cursar sin los síntomas clásicos de dolor anginoso. Algunos pacientes tienen síntomas atípicos de angina como aparición de disnea con el ejercicio. Por lo tanto, es necesario investigar la presencia de enfermedad coronaria mediante una prueba de esfuerzo. El electrocardiograma en reposo tiene poca sensibilidad para detectar enfermedad coronaria en las personas con DM2.
Además toda persona con DM2 debe tomar aspirina diariamente en dosis de 100 a 350 mg.
– La enfermedad vascular cerebral es mas frecuente en la persona con diabetes pero su prevención y manejo son similares a los de las personas sin diabetes.
– La enfermedad vascular periférica (EVP) es también mas frecuente en la persona con diabetes. El síntoma más precoz es la claudicación intermitente. Sin embargo, aún antes la persona puede perder los pulsos pedios y tibiales, lo cual es un indiciador de severidad que coloca al pie en riesgo y obliga a la remisión al especialista. El cigarrillo y el uso de betabloqueadores no cardioselectivos agravan la EVP y deben proscribirse.
No hay evidencia suficiente para recomendar agentes hemorreológicos como la pentoxifilina en todos los pacientes con EVP.
Hipotiroidismo
Introducción
Con frecuencia se sospecha hipotiroidismo como causa de múltiples problemas cuya relación con la hipofunción tiroidea es inespecífica, como es el caso de la baja talla, la obesidad, el cansancio fácil, la somnolencia, la depresión, los trastornos dermatológicos como piel seca o caída del cabello y los trastornos digestivos como el estreñimiento. El hipotiroidismo podría estar presente cuando estos problemas confluyen en un mismo sujeto y adquieren características particulares como el caso del paciente cuyo aumento de peso se acompaña de infiltración del tejido subcutáneo formando mixedema y de edema palpebral matutino, con una piel seca y de aspecto poco vital, mialgias, pérdida de lacola de las cejas, enronquecimiento de la voz, lentitud en movimientos y expresión, quien ha tenido que aumentar las cobijas por intolerancia al frío etc. Para llegar a este estado se requiere que el hipotiroidismo sea severo y prolongado.
En la tabla 8 se enumeran los síntomas y signos con la frecuencia con la que se encuentran en personas con hipotiroidismo.
Tabla 8. Signos y síntomas que se presentan con mayor frecuencia en personas con hipotiroidismo clínico. |
|||
Síntomas |
Frecuencia |
Signos |
Frecuencia |
| Astenia | 90% | Lentitud en los movimientos | 70 – 90% |
| Piel seca | 60 – 100% | 70 – 100% | |
| Intolerancia al frío | 60 – 95% | Piel y cabello ásperos | 70 – 90% |
| Voz ronca | 50 – 75% | Piel fría | 40 – 90% |
| Aumento de peso (2-3 kg) | 50 – 75% | Facies abotagada con edema palpebral | |
| Estreñimiento | 30 -65% | ||
| Menor sudoración | 10 – 65% | Bradicardia | 10 – 15 % |
| Parestesias | 50% | Disminución del reflejo aquiliano | 50% |
| Hipoacusia | 5 – 35% | ||
Setenta a ochenta por ciento de todos los casos de hipotiroidismo en el adulto se debe a tiroiditis crónica autoinmune (de Hashimoto). En los niños, la enfermedad tiroidea autoinmune es también la causa más común de hipotiroidismo adquirido. Conviene resaltar aquí que, a pesar de ser un problema autoinmune, la tiroiditis de Hashimoto no se modifica con el uso de corticoides ni de inmunosupresores y por lo tanto estos tratamientos no están indicados.
Los siguientes son algunos de los casos en que podría estar justificado el tamizaje para buscar hipotiroidismo, aunque pocos tienen evidencia de costo-beneficio:
– Recién nacidos.
– Mujeres mayores de 50 años
– Hipercolesterolemia severa
– Hiperprolactinemia
– Talla baja, especialmente si se está tratando con hormona del crecimiento
– Terapia con litio o amiodarona.
– Depresión de difícil manejo
– Bocio
– Cirugía de tiroides
– Irradiación del tiroides externa o interna (con Il3l)
– Enfermedad autoinmune (diabetes tipo 1, enfermedad de Addison, artritis reumatoidea, lupus eritematoso, síndrome de Sjögren, vitíligo, anemia perniciosa)
– Parientes en primer grado con enfermedad tiroidea autoinmune
La disfunción ovulatoria y la infertilidad en algunos casos se pueden asociar con hipotiroidismo.
(Lea También: Enfermedades Endocrinas, Hipertiroidismo)
Diagnóstico
La TSH elevada es la base para el diagnóstico de hipotiroidismo primario. Solamente cuando exista una falla de la hipófisis o del hipotálamo se encontraría disminuida, lo cual es mucho menos frecuente y se denomina hipotiroidismo secundario.
Cuando la TSH se encuentra elevada y el T4 total es normal, se hace el diagnóstico de hipotiroidismo sub-clínico. Si la TSH está elevada y el T4 total está por debajo del límite normal, se hace el diagnóstico de hipotiroidismo clínico.
Se puede reemplazar la medición del T4 total por la del T4 libre aunque esto aumenta el costo y no se realiza en todos los laboratorios. Solamente es indispensable medir T4 libre en recién nacidos, en mujeres embarazadas y en enfermos críticos donde se sospeche interferencia en la unión de la hormona a las proteínas transportadoras circulantes. Algunos fármacos pueden elevar las proteínas trasportadoras como los estrógenos en altas dosis y los anticonceptivos.
Esto da lugar a que el T4 total aumente, aunque el T4 libre y por consiguiente la función tiroidea permanecen normales. Por el contrario la fenilbutazona, los esteroides, los anabólicos y la dopamina disminuyen el T4 total, manteniendo el T4 libre y la función tiroidea normales.
Algunos laboratorios todavía miden “T3 Uptake” como una forma indirecta de evaluar las proteínas transportadoras, pero lo reportan como un porcentaje de T3 (lo que con frecuencia se confunde con T3 total). Este examen
tiene valor si se establece una relación entre el resultado del paciente y el de una muestra patrón y ésta se utiliza para “corregir” el T4 total, informándolo como “índice de tiroxina libre”.
La captación baja de Tecnecio99 en una gamagrafía no es diagnóstica de hipotiroidismo y de hecho puede encontrarse inclusive alta en casos de hipotiroidismo por tiroiditis de Hashimoto.
Tratamiento
Todo paciente con hipotiroidismo debe ser valorado, al menos inicialmente, por un endocrinólogo.
Es el profesional capacitado para evaluar la etiología del problema, su carácter transitorio o permanente, sus comorbilidades, sus posibles asociaciones con otros problemas endocrinos y para definir el plan de manejo.
El tratamiento del hipotiroidismo clínico consiste en suplir la deficiencia parcial o total de las hormonas tiroideas mediante la administración de levotiroxina, dejando que el propio organismo se encargue de la conversión de T4 a T3 con base en los requerimientos del momento.
La personas con hipotiroidismo clínico requieren suplencia completa con levotiroxina cuyas dosis pueden oscilar entre 75 y 125 microgramos usualmente. El ajuste se hace exclusivamente mediante la medición de TSH que debe ubicarse en el rango normal. Para ello se debe esperar un mínimo de seis a ocho semanas después de cada cambio. Nunca se debe hacer el ajuste con base en síntomas y a pesar de tener una TSH adecuada. El hipertiroidismo iatrogénico (TSH por debajo del rango normal) puede ser tan o más perjudicial que el hipotiroidismo.
En personas de edad o con patologías cardiovasculares asociadas la suplencia debe ser gradual, comenzando con dosis bajas.
Existe controversia sobre cuándo tratar el hipotiroidismo subclínico. En términos generales convendría tratarlo cuando se sospecha que va a evolucionar a un hipotiroidismo clínico o cuando está causando o empeorando algún trastorno clínico, lo cual no siempre se puede probar. El tratamiento, al igual que en el hipotiroidismo clínico, va dirigido a normalizar la TSH, para lo cual se suele requerir una dosis de levotiroxina baja (50 microgramos). Si el proceso es evolutivo, los requerimientos de suplencia irán aumentando.
Algunas de las condiciones en que se justifica tratar esta condición se enumeran a continuación:
– TSH mayor de 10 mU/l (en ancianos mayor de 20 mU/l)
– Presencia de bocio
– Anticuerpos antiperoxidasa (o antimicrosomales) positivos
– Antecedente de haber sido tratado con Il3l
– Antecedente de cirugía tiroidea
– Tratamiento con litio o amiodarona (indicación que puede ser transitoria)
– Depresión de difícil manejo
– Hiperprolactinemia, aunque cuando es muy elevada y especialmente cuando no corrige con la normalización de la TSH, se debe investigar la causa y tratarla.
– Hipercolesterolemia, aunque por lo general el tratamiento del hipotiroidismo subclínico puede facilitar su manejo pero no es la causa, por lo que se requiere tratamiento específico con una estatina para alcanzar la meta adecuada.
El paciente que está recibiendo suplencia tiroidea debe tener claro el objetivo del tratamiento.
Con frecuencia espera que éste le solucione todos sus problemas y exige ajustes de la dosis para corregir síntomas que no tienen relación con el hipotiroidismo (como el aumento de peso).