5.11
La neuroimagen se utiliza principalmente para identificar otras causas de trastorno neurocognoscitivo. Particularmente aquellas susceptibles de intervención quirúrgica (por ejemplo, lesiones focales o hidrocefalia de presión normal). Se estima que del 9% de casos de demencia que se identifican como potencialmente reversibles, sólo 0,6% se revierten total o parcialmente (50). Sin embargo, si se identifica una causa reversible, el impacto en los resultados para la persona con trastorno neurocognoscitivo mayor podría ser crítico.
También se pueden realizar neuroimágenes para ayudar a diferenciar el subtipo de demencia. El diagnóstico de subtipos puede ser complejo ya que muchos casos del trastorno neurocognoscitivo mayor implican múltiples etiologías (por ejemplo, enfermedad de Alzheimer y demencia vascular o enfermedad de Alzheimer y cuerpos de Lewy a pesar de ser extremadamente infrecuente). El propósito del diagnóstico es identificar la causa predominante para el manejo. Las neuroimágenes pueden ser de gran valor al comunicar el diagnóstico a una persona con trastorno neurocognoscitivo mayor y a su cuidador(es), familia y explicar la causa patológica de la enfermedad.

Imagen estructural
Antecedentes
La imagen estructural del cerebro se puede realizar usando tomografía computarizada (TC) o resonancia magnética estructural (RM). Estas imágenes pueden delinear las estructuras cerebrales y proporcionar información sobre anomalías estructurales.
Las anormalidades estructurales, como la enfermedad cerebrovascular o patrones de atrofia cerebral. Pueden ayudar en el diagnóstico de subtipos de demencia (por ejemplo, la atrofia medial del lóbulo temporal puede ayudar en el diagnóstico de la enfermedad de Alzheimer)(51). La RM tiene una resolución mayor que la TC y puede detectar cambios anatómicos y vasculares más sutiles (52). Sin embargo, una revisión de 38 estudios, entre ellos cuatro que compararon directamente la precisión de la RM y la TC. Encontraron evidencia insuficiente que sugiera que la RM fuera superior a la TC para identificar cambios cerebrovasculares en casos de EA, DV y demencia mixta confirmados con autopsia (53).
La RM está contraindicada en algunos pacientes, como aquellos portadores de marcapasos, estimuladores del nervio vago. Cardio – desfribriladores implantables, implantes cocleares y bombas de insulina (51-53). La resonancia magnética también es inadecuada para los pacientes que son claustrofóbicos o incapaces de permanecer quietos por largos períodos.
El comité directivo NICE:
Recomendó el uso de imágenes estructurales en la evaluación de las personas con sospecha de trastorno neurocognoscitivo mayor para excluir otras causas de trastorno neurocognoscitivo y ayudar a establecer el diagnóstico de subtipo. (Los resultados de la búsqueda sistemática no se presentaron en su informe).
El GD (GPC Australiana) acordó que la imagen estructural era necesaria para excluir las etiologías cerebrales en la mayoría de las personas con sospecha de trastorno neurocognoscitivo mayor. Y , por lo tanto, esto se declaró como un punto de buena práctica. Recomendaciones basadas en la evidencia con respecto al uso de imágenes estructurales en subgrupos de personas con trastorno neurocognoscitivo mayor. Se consideraron innecesarias en ausencia de pruebas de los daños asociados con la imagen estructural.
Imagen funcional
Antecedentes
La neuroimagen funcional representa los cambios en el funcionamiento del tejido cerebral. La tomografía computarizada de emisión monofotónica (SPECT) o la tomografía por emisión de positrones (PET) se pueden utilizar para identificar áreas del metabolismo de glucosa o perfusión cerebral disminuidas. Lo que indica lesiones o pérdidas neuronales. El SPECT se realiza con una variedad de trazadores incluyendo hexametil propilen-amino-oxima o exametazima (99mTc-HMPAO), N-isopropil- (Iodo – 123) p – yodoamfetamina (123I – IMP) y dímero de etilen-cisteínato (99mTc – ECD).
La imagen funcional para el diagnóstico del trastorno neurocognoscitivo mayor también puede efectuarse usando PET. Esta revisión comparó el desempeño de 18F-FDG-PET con el de la SPECT en el diagnóstico de la enfermedad de Alzheimer (EA) donde otros métodos de diagnóstico no son concluyentes. El GD (GPC Australia) realizó una evaluación de la PET en el diagnóstico del trastorno neurocognoscitivo mayor. Encontrando datos clínicos comparativos limitados. Y concluyendo que 18F-FDG-PET y el SPECT tenían precisión de diagnóstico similar para detectar la enfermedad de Alzheimer (54). Además, revisiones recientes han concluido que la evidencia del uso de 18F-FDG-PET no fundamenta su utilización rutinaria en el diagnóstico de la enfermedad de Alzheimer o en personas con trastorno neurocognoscitivo leve para predecir la conversión a la enfermedad de Alzheimer (46,48,55).

(Lea También: Información y Apoyo para la Persona con Trastorno Neurocognoscitivo Mayore)
Evidencia y conclusiones
El comité directivo NICE utilizó evidencia de una revisión sistemática existente para realizar una recomendación sobre el uso de HMPAO SPECT en la diferenciación de subtipos de trastorno neurocognoscitivo (56). Sin embargo, no se considera la precisión de SPECT por encima de la evaluación global estándar incluyendo a la imagen estructural. No se excluyeron estudios de casos y controles. Basándose en la escasez de estudios y en las opiniones de expertos clínicos. El GD (GPC Australiana) consideró que el valor adicional de SPECT a la evaluación general estándar en la diferenciación de subtipos de trastorno neurocognoscitivo no apoyaba una recomendación para su uso.
Diferenciación entre el deterioro cognitivo leve y trastorno neurocognoscitivo mayor
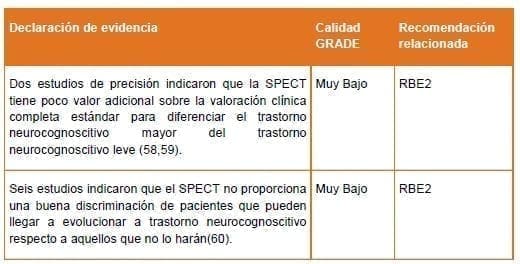
En una evaluación de tecnología de la salud publicada en 2006, no se identificaron estudios que informen de la precisión del SPECT sobre la valoración clínica en la diferenciación entre el trastorno neurocognoscitivo mayor y el trastorno neurocognoscitivo leve (57). En la actualización de la evidencia se identificaron tres estudios que proporcionaron datos sobre el valor de SPECT por encima de la evaluación clínica.
Dos estudios proporcionaron alguna información sobre la exactitud de SPECT cuando se usó de forma adicional a la evaluación clínica. Un estudio alemán informo de 12 pacientes de clínicas de memoria inicialmente diagnosticados con trastorno neurocognoscitivo leve (58). El SPECT cambió el diagnóstico de MCI a trastorno neurocognoscitivo mayor en ocho pacientes, correctamente en cuatro de estos casos (un 50%). En este estudio, el SPECT no tenía ningún valor adicional en general. Pero se consideró que había un alto riesgo de sesgo en estos resultados. En otro estudio, la SPECT 99mTc-HMPAO fue de poco valor diagnóstico en un grupo de pacientes jóvenes con trastorno neurocognoscitivo leve que asistían a una clínica de memoria con diagnóstico incierto siguiendo una valoración completa estándar que incluía imagen estructural (59).
Una auditoria médica de las remisiones para la realización de SPECT en el área rural de Nueva Gales del Sur reportó tasas de concordancia entre SPECT, TC y las valoraciones neuropsicológicas (60). En este estudio, 31% de las remisiones fueron de médicos generales y 98% fueron por sospecha de trastorno neurocognoscitivo mayor. En 76% de las personas con una comparación entre la TC y la valoración neuropsicológica disponible, el SPECT concordó con los resultados. Por lo tanto, es poco probable que haya tenido un impacto importante en el diagnóstico o manejo. Aunque pudiera incrementar la confianza en el diagnóstico y la elección del tratamiento cuando los resultados son concordantes.
Predicción de la progresión de la MCI a trastorno neurocognoscitivo mayor
Una revisión sistemática reporto la precisión del SPECT para diferenciar entre MCI progresivo y el no progresivo encontrando que el SPECT solo tuvo una sensibilidad y especificidad moderada al predecir la conversión de trastorno neurocognoscitivo leve a trastorno cognoscitivo mayor debido a enfermedad de Alzheimer (61). Un resultado de SPECT positivo, no proporcionó discriminación de pacientes que pueden llegar a evolucionar a trastorno neurocognoscitivo mayor respecto a aquellos que no lo harán. Además, no es claro el manejo y los desenlaces para personas con MCI que reciben un resultado del SPECT positivo y que pueden llegar a evolucionar a trastorno neurocognoscitivo mayor.
5.12 Comunicación del diagnóstico
Antecedentes
Recibir el diagnóstico del trastorno neurocognoscitivo mayor tiene un enorme impacto en el paciente, su cuidador(es) y su familia. Tras el diagnóstico, las personas suelen reportar sentimientos de pérdida, ira, incertidumbre y frustración (32). El término ” trastorno neurocognoscitivo mayor” puede estar asociado con estigma para el paciente, su cuidador(es), familias, cónyuge y/o pareja. Esto puede ser aún mayor en ciertos grupos culturales (62–64). Sin embargo, algunas personas reportan sentimientos de alivio por tener una explicación de sus síntomas(65).
La información del diagnóstico a una persona con trastorno neurocognoscitivo mayor es fundamental para el principio de autonomía personal. Aunque un número muy pequeño de personas puede optar por no conocer el diagnóstico, es claro que la mayoría de pacientes quiere ser informado. Y, por lo tanto, es importante que los profesionales de la salud sean honestos y veraces cuando comuniquen el diagnóstico al paciente, su cuidador(es), familias, cónyuge y/o pareja. El diagnóstico debe comunicarse de una manera que sea comprensible para el paciente con respecto a sus necesidades individuales de lenguaje y comunicación (65).