Sistema Nervioso
Epidemiología
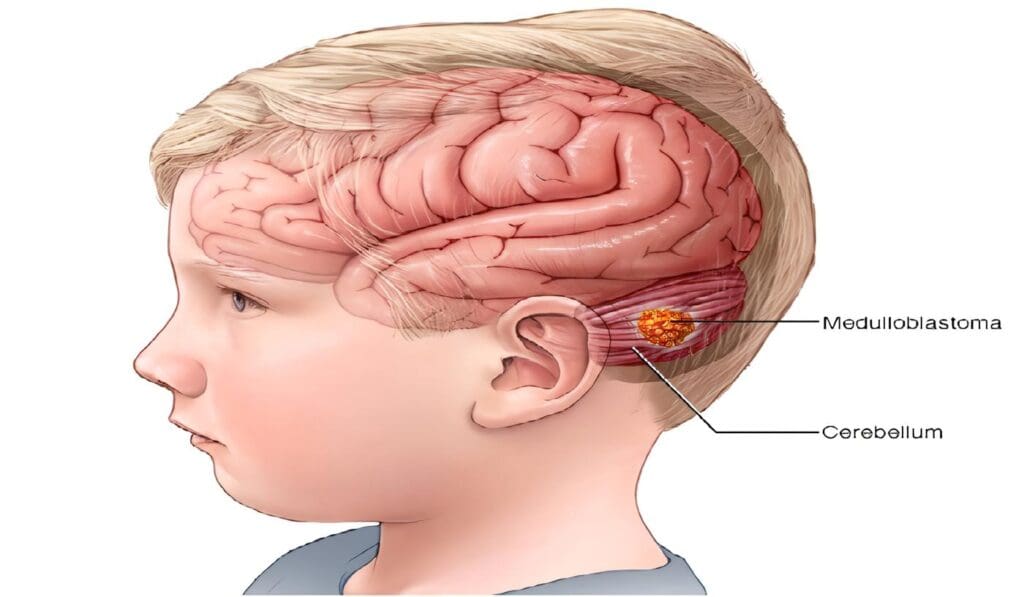
El meduloblastoma es un tumor maligno, de localización predominante en el cerebelo, más frecuente en niños y en adultos jóvenes. El 70% de los casos se presenta en personas menores de 20 años y son raros en los mayores de 40 años.
Corresponde al 25 a 30% de los tumores malignos del sistema nervioso central en personas menores de 20 años y su mayor incidencia está entre los 5 y 9 años de edad. (Ver también: Retinoblastoma)
Etiopatogenia
Tienen origen embrionario, en las células de la capa granulosa del cerebelo. Poseen marcadores inmunohistoquímicos de células primitivas neuroepiteliales común con los demás tumores neurectodérmicos primitivos del sistema nervioso central, como son el ependimoblastoma, el neuroblastoma y el pinealo-blastoma.
Entre 90 y 95% de los casos tienen presentación esporádica, y un 5% se asocia con desórdenes hereditarios y mutaciones de genes específicos, como pueden ser los casos asociados al síndrome de Gorling (tumores de células basales en piel y meduloblastoma), en el cual se evidencia una mutación del gen PTCH (gen supresor).
El otro desorden hereditario es el síndrome de Turcot (gliomas, meduloblastoma y dos formas de poliposis colónica) donde las alteraciones se expresan en el cromosoma 5.
Cuadro Clínico
El meduloblastoma es un tumor básicamente de fosa posterior, predominante en el vermis cerebeloso en los niños y en los hemisferios cerebeloso en los adultos.
La presentación clínica más frecuente es un síndrome de hipertensión endocraneana, caracterizado por cefalea global matinal que se aumenta con el esfuerzo, visión borrosa, náusea y vómito que no mejoran con medicamentos corrientes, y compromiso del estado mental con confusión y desorientación.
También se acompaña de síndrome cerebeloso, con ataxia, dismetría, reflejos pendulares y compromiso de pares craneanos por infiltración directa del tumor a nivel del tallo y/o a la base del cráneo o por la misma hipertensión endocraneana, en especial paresia del sexto par y/o del segundo par, con diplopia y alteración de la agudeza visual por atrofia óptica.
Diagnóstico
La escanografía cerebral (TAC) con contraste es de utilidad, pero el estudio más sensible y específico es la resonancia magnética con gadolinio, que debe incluir la médula espinal para estadificación.
Las imágenes revelan una masa medial o paramedial que realza el contraste y que frecuentemente comprime el cuarto ventrículo, con regiones de necrosis, hemorrágicas o con cambios quísticos, nódulos o patrón linear de realce del contraste en los ventrículos, en la superficie del cerebro o en el canal espinal.
La citología del liquido cefalorraquídeo es un examen mandatorio que debe hacerse preferiblemente durante el acto quirúrgico. Se deben tomar muestras de la región ventricular, por razón de los riesgos con la toma preoperatoria antes de liberar el flujo del líquido cefalorraquídeo. Debe repetirse 10 días luego de la cirugía.
Más o menos un 30% de los meduloblastoma exhiben compromiso metastásico o diseminacion subarcnoidea.
Otros estudios adicionales, si bien no se realizan para el diagnóstico, se requieren para la estadificación del tumor y para la evaluación previa al inicio del tratamiento.
Gamagrafia ósea.
Mielograma y biopsia de la medula ósea.
Radiografia de tórax
TAC cerebral.
Estadificación
Se utiliza la clasificación de Chang (Pomeroy 1999)
T1 Tumor menor de 3 cm.
T2 Tumor mayor de 3 cm.
T3A Tumor mayor de 3 cm, con extensión al acueducto de Silvio y/o a los agujeros de Luschka.
T3B Tumor mayor de 3 cm, con extensión al tallo cerebral.
T4 Tumor mayor de 3 cm, con extensión al acueducto de Silvio sobrepasándolo y/o sobrepasando el agujero magno.
Nota: No se considera el número de estructuras invadidas ni la presencia de hidrocefalia.
El T3B que no se haya demostrado por imágenes puede ser definido intraoperatoriamente.
M0 No existe evidencia de metástasis a nivel subaracnoídeo o metástasis hematógenas.
M1 Citología de líquido cefalorraquídeo positiva.
M2 Siembras nodulares en el espacio subaracnoideo del cerebelo, cerebro, el tercer ventrículo ventrículos laterales.
M3 Siembras nodulares en el espacio subaracnoideo espinal.
M4 Metástasis fuera del eje cerebro-espinal.
Clasificación Histopatológica
1) Clásico (indiferenciado).
2) Meduloblastoma desmoplásico.
3) Meduloblastoma de célula grande.
4) Meduloblastoma con diferenciación divergente:
a) Medulomioblastoma.
b) Meduloblastoma melanótico.
c) Meduloblastoma lipomatoso.
5) Meduloblastoma con diferenciación glial y/o neuronal-neuroblástica.
Factores Pronósticos
Alto riesgo
1. Resección de menos del 75% o tumor residual mayor de 1,5 cm.
2. Invasión del tallo o de la medula.
3. Metástasis subaracnoidea.
4. Citología positiva después de 10 días de cirugía.
5. Enfermedad mayor o igual a M1.
6. Enfermedad mayor o igual a T3B.
7. Edad menor de 3 años, por la restricción en el uso de la radioterapia.
Bajo riesgo
1. Sin residuo tumoral o residuo menor de 1,5 cm post cirugía.
2. Tumores clasificados T1, T2 , T3a y M0.
3. LCR negativo a los 10 días postcirugía.
La tasa de supervivencia a 5 años es de 25 a 30 % en los grupos de alto riesgo y del 70 a 80% en los de buen pronóstico o bajo riesgo.
(Lea También: Metástasis Cerebrales)
Tratamiento
Cirugía
El objetivo de la cirugía es diagnóstico. En primer lugar, lograr la resección completa, la citorreducción o la repermeabilización de las vías de drenaje del líquido cefalorraquídeo, sin incrementar el déficit neurológico.
La mayoría de los meduloblastomas presenta hidrocefalia en el momento del diagnóstico. Se prefiere no hacer derivación ventriculo-peritoneal o ventrículo-atrial por el riesgo de diseminación extracraneal del tumor. También, se realiza ventrículostomía transoperatoria para disminuir la presión intracraneana y para facilitar la resección quirúrgica, además del estudio citológico del líquido cefalorraquídeo.
Se practica un craneotomía suboccipital central o paramediana, según la localización del tumor, mediante técnica microquirúrgica; lo ideal es la resección macroscopicamente completa de la lesión, ya que es un factor pronóstico importante para la supervivencia. Especial importancia debe tener la resección de la infiltración del tumor a través de los recesos laterales del cuarto ventriculo o del tallo cerebral, para no lesionar los pares craneales.
Se informa mortalidad quirúrgica entre 0 y 8%.
Quimioterapia adyuvante
La quimioterapia es similar en niños y adultos, y se estratifica de acuerdo a los factores pronósticos, en grupos de alto y bajo riesgo.
Todos los pacientes deben ser evaluados previamente a iniciar quimioterapia y antes de cada ciclo de tratamiento mediante hemograma, pruebas de función renal incluyendo depuración de creatinina en orina de 24 horas, pruebas de función hepática, uroanálisis y audiometría, exámenes que se deben repetir al completar 400 mg/m2 del cisplatino.
Quimioterapia adyuvante en meduloblastoma de bajo riesgo
Esquema de Tratamiento
Durante la radioterapia cráneoespinal:
Vincristina semanal 1,5 mg/m2
A las tres después de la radioterapia se inicia la segunda fase de quimioterapia con cinco ciclos, de siete semanas cada uno, así:
Cisplatino 75 mg/m2, IV, día 1
Vincristina 1,5 mg/m2, IV, días 1, 8, 22 y 29
Ciclofosfamida 1g/m2, IV, días 22 y 23
Quimioterapia adyuvante en meduloblastoma de alto riesgo Esquema de Tratamiento
Durante la radioterapia, etopósido 35 mg/m2/día, vía oral, días 1 a 21, y días 29 a 49.
La respuesta debe ser evaluada en la décima semana, mediante examen clínico y de imágenes (resonancia magnética con gadolinio del cerebro y medula espinal), 3 semanas post radioterapia.
La quimioterapia se debe continuar con tres ciclos, con intervalo de tres semanas cada uno así:
Cisplatino: 90 mg/m2, IV, día 1.
Etopósido: (VP-16) 150 mg/m2, IV, días 1-2-3 en infusión por dos horas, controlando la tensión arterial.
Opcional: etopósido (VP-16) 35 mg/m2, VO, días 1 a 21.
Opcional: factor estimulante de granulocitos G-CSF, 5 mcg/kg/día, por cinco días, iniciando 24 horas después de finalizada la quimioterapia y si los neutrofilos absulutos descienden a menos de 500 en el primer ciclo.
Se continúa con siete ciclos, con intervalo de 4 semanas cada uno así: Vincristina 1,5 mg/m2, IV, día 1.
Ciclofosfamida 1 g/m2/día, IV, días 1 y 2 por infusión de 30 minutos, previa hidratación y continuándose liquidos endovenosos.
Mesna: 360 mg/m2, IV, (en infusión de 30 minutos, horas cero, tres y seis de cada día de ciclofosfamida).
Radioterapia
Teniendo en cuenta la diseminación subaracnoidea de este tipo de tumor, la radiacion debe incluir el cráneo y el canal raquídeo. Las fallas pueden presentarse por dosis inadecuada en el sitio del tumor primario (fosa posterior).
En los pacientes de alto y bajo riesgo se recomienda fraccionamiento diario de 150 a 180 cGy para una dosis total craneoespinal de 3600 cGy y una dosis de refuerzo al lecho tumoral de 1800 cGy, para un total acumulado de 5400 cGy en el lecho tumoral.
En los niños menores de tres años se utiliza el mismo esquema, pero la dosis se reduce en 20 a 25%, tanto la craneoespinal como la del lecho tumoral, aplicando previamente la quimioterapia durante un año o año y medio para diferir al máximo el uso de la radioterapia.
Técnica de radioterapia
Se utilizan campos laterales opuestos, holoencefálicos (cráneo) cuyo límite inferior es C2-C3; se utilizan campos espinales directos posteriores para incluir todo el canal raquídeo; si el paciente es un niño mayor o un adulto, los campos espinales se deben separar por la ley de separación de campos. Todos los pacientes deben tener un inmovilizador personalizado para garantizar la exactitud del tratamiento.
La separación de campos holoencefálicos y espinal superior debe realizarse con la angulación del colimador. El ancho de los campos espinales debe garantizar la dosimetría adecuada al canal espinal, la separación de campos holoencefálicos y al espinal superior
Todos los pacientes deben ser simulados, tener placa verificadora semanal para garantizar la calidad del tratamiento y cuadro hemático semanal para vigilar la reserva de médula ósea.
Lecturas Recomendadas
- 1. CHANG CH, HOUSEPAIN EM, HERBERT C. An operative staging system and megavoltage. Radiotherapeutic technic for cerebellar medulloblastomas. Radiology 1969;93:1351
- 2. GAIJAR A. Recent Advances in Therapy for Medulloblastoma. En: American Society of Clinical Oncology 1999 Educational Book, MC Perry (Editor). American Society of Clinical Oncology. Alexandria, VA, 1999; p 579-586.
- 3. LEIBEL S. Neoplasms of the central nervous system En: Principles and Practice of Oncology. DeVita VT Jr, Hellman S, Rosenberg SA (eds). Lippincott-Raven 5th edition. Philadelphia, 1997; p 2022-2082.
- 4. PECH IV, PETERSON K, CAIMEROSS JG. Chemotherapy for brain tumors. Oncology 1998; 12:537-43.
- 5. POMEROY SL. Pathogenesis and clinical features of meduloblastoma. Up to Date, 1999; 8(1):1-3.
- 6. FRIEDMAN H, OAKES WJ. New therapeutic options in the management of childhood brain tumors. Oncology 1992; 6:27-36.