8.4
Paula Fonnegra Uribe. Médico Cirujano Universidad del Bosque Especialista Toxicología Clínica Universidad del Rosario Toxicóloga Clínica Clínicos IPS Miembro de la Asociación de Toxicología Clínica Colombiana – ATCC–
Camilo Rojas. Médico Cirujano Universidad Nacional Especialista Toxicología Clínica Universidad del Rosario Toxicólogo Clínico Clínicos IPS Miembro de la Asociación de Toxicología Clínica Colombiana – ATCC –
Luis Carlos Rojas. Médico Cirujano Universidad del Rosario Residente Toxicología Clínica Universidad del Rosario Miembro de la Asociación de Toxicología Clínica Colombiana – ATCC–
Jair A. Ruiz G. Médico Cirujano Universidad del Rosario Residente Toxicología Clínica Universidad del Rosario Miembro de la Asociación de Toxicología Clínica Colombiana – ATCC–
Generalidades
El fósforo es un elemento ubicado en la tabla periódica con el número atómico 15 y peso molecular de 30.97 daltons; comparte propiedades químicas con el nitrógeno y el arsénico. Puede encontrarse en dos formas, polimorfismos o alótropos conocidos como el fósforo rojo, con toxicidad limitada en seres humanos, y el blanco. Éste último se ha usado en la producción de fuegos artificiales (“diablitos, diablillos, martinicas, totes”), rodenticidas y municiones usadas en la primera guerra mundial para las minas antipersona1,2,3.
Actualmente no hay rodenticidas en Colombia con éste elemento. El fósforo blanco tiene la capacidad de reaccionar espontáneamente con el aire formando pentóxido fosfórico (P4O10) y este a su vez entra en contacto con el agua formando el ácido fosfórico conocido por las quemaduras que produce debido a sus características corrosivas4.
Toxicocinética
El fósforo blanco es liposoluble y tiene buena absorción en el tracto gastrointestinal. La cual se incrementa con la coingesta de etanol y de alimentos ricos en grasa. La absorción también puede ocurrir por vía inhalatoria y dérmica, asociado a la generación de quemaduras extensas1,5.
Una vez se absorbe, aproximadamente hacia las 3 horas, se distribuye en el hígado y en el riñón. Se estima en reportes de casos que dosis de 1 mg ya puede generar efectos nocivos severos en el adulto4.
Fisiopatología
Existen tres mecanismos asociados a la fisiopatología de la intoxicación por fósforo blanco4:
- Reacción exotérmica: dada por la reacción del pentóxido fosfórico con el agua al formar ácido fosfórico. Es considerado el mecanismo más lesivo para los tejidos que finalmente permite la entrada del ácido hacia el torrente sanguíneo.
- Producción de ácido: el ácido fosfórico tiene propiedades corrosivas que promueven lesión del retículo endoplásmico rugoso y la mitocondria.
- Deshidratación: el ácido fosfórico tiene la capacidad de generar en las moléculas orgánicas reacciones de deshidratación que favorecen la unión de estas al pentóxido fosfórico perpetuando la lesión tisular.
Finalmente, estas sustancias generan una alta tasa producción de radicales libres y bloqueo en la producción de ATP. Además de su daño celular directo que lleva a apoptosis y necrosis4,6,7.
Manifestaciones clínicas
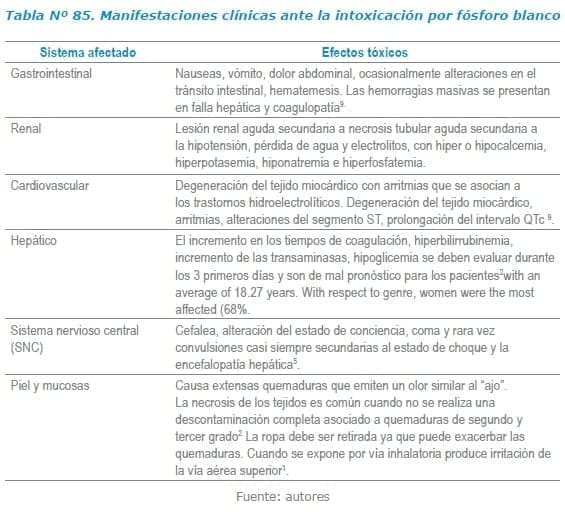
En la intoxicación por fósforo blanco se comprometen múltiples sistemas como el tegumentario, cardiovascular, hepático, renal, gastrointestinal y sistema nervioso central (Tabla Nº 85). Se presenta en tres fases según la evolución posterior a la exposición (Tabla Nº 86). Sin embargo, si en las primeras seis horas se encuentra en el paciente alteración del estado de conciencia, cianosis, acidosis metabólica, hipotensión, hipoglicemia y tiempos de protrombina prolongados se consideran como indicadores de mal pronóstico2,8.

Diagnóstico
El diagnóstico es básicamente clínico teniendo en cuenta el antecedente exposicional ya que los niveles séricos no reflejan la concentración de fósforo elemental. Sin embargo, es importante realizar seguimiento de electrolitos, glicemia, gases arteriales, función renal, tiempos de coagulación y hemograma. Descartándose otras patologías previamente si no se cuenta con más información detallada5,6,10.
Tratamiento
Medidas generales
Antes de manipular el paciente es importante tener en cuenta la seguridad de los trabajadores de la salud ya que cualquier material que haya tenido contacto incluyendo los fluidos corporales productos de la emesis y las deposiciones diarreicas deben ser consideradas peligrosos. El personal debe manipular al paciente bajo todas las normas de bioseguridad incluyendo mascarilla facial por el riesgo de inhalar el material volátil9,4,11,12.
Una vez se cumple con estas reglas, se debe proceder a estabilizar la persona afectada, teniendo en cuenta los signos vitales con una estricta vigilancia clínica de cualquier trastorno metabólico que sugiera lesión hepática; a su vez debe solicitar paraclínicos como hemograma, creatinina, nitrógeno ureico, ionograma (incluyendo sodio, potasio, cloro, fósforo, calcio y magnesio). El paciente debe ser manejado en un centro de atención de tercer nivel de complejidad donde se cuente con un equipo interdisciplinario liderado por un toxicólogo clínico, que pueda realizar el adecuado seguimiento del enfermo.
Se recomienda mantener adecuadas concentraciones séricas de glucosa, corrección de cualquier alteración hidroelectrolítica documentada. Es de tener en cuenta que el uso de corticoides en estos pacientes no ha demostrado ningún beneficio en las intoxicaciones con fósforo blanco1,2,11 .
Exposición dermatológica:
Teniendo en cuenta que la formación de ácido no está directamente relacionada con las lesiones cutáneas. Es importante que se haga un adecuado lavado de las heridas con agua, gasas húmedas, sulfato de cobre o solución salina al 0.9% evitando que el fósforo haga contacto con el aire.
Es importante realizar una adecuada descontaminación y en caso de ser necesario se debe llevar a debridamiento. No se recomienda usar ningún tipo de ungüentos hasta que no se haya logrado determinar por completo que la lesión no tiene rastro de fósforo en su interior1,11,13,14,15.
Exposición gastrointestinal:
Aunque no existe suficiente evidencia que sustente el manejo más adecuado para estos pacientes. Se ha observado que el uso de carbón activado podría ser útil. El lavado gástrico en la primera hora posterior a la ingesta se puede usar como una medida de descontaminación. Sin embargo, es necesario recordar que existe el riesgo de ocasionar un incendio o explosión por la volatilidad del producto y perforar el esófago2,9.
No existe un antídoto para estos eventos; en reportes de caso y análisis experimentales se ha usado N-acetilcisteína para manejar la hepatotoxicidad con respuesta variable (ver dosis en el capítulo de Antídotos).
La vitamina E, utilizada como antioxidante, puede usarse para evitar los daños en el tejido hepático. Sin embargo, no existe evidencia sobre el beneficio de su uso. De seleccionar esta opción, deben administrarse 400 UI c/8h VO.
La hemoperfusión es una alternativa útil cuando se realiza tempranamente, y en casos extremos, en los que el paciente desarrolle falla hepática fulminante, se podría considerar la opción de trasplante hepático.
Es importante resaltar que el manejo que se le debe dar a estos pacientes es de monitoreo y soporte hemodinámico, ventilatorio, hidroelectrolítico y metabólico1,16,17 (ver el capítulo de Generalidades de manejo del paciente intoxicado en el Servicio de Urgencias).
Criterios de remisión
Deben ser remitidos a hospital de alto nivel de complejidad, todos los pacientes en quienes se sospeche intoxicación por fósforo blanco, buscando que puedan ser evaluados por Toxicología Clínica en conjunto con otras especialidades y procurando la atención. Para algunos casos, en Unidad de Cuidado Intensivo para manejo integral.
Referencias
- 1. Hoffman R, Goldfrank L, Howland M, Nelson L. Glodfrank’s Toxicologic Emergencies. 10th ed. Flomenbaum N, editor. Mc Graw Hill. New York; 2015. 556-581 p.
- 2. González-Andrade F, Sánchez-Q D, Martínez-Jarreta B, Borja J. Acute exposure to white phosphorus: A topical problem in Ecuador (South America). Leg Med. 2002;4(3):187–92.
- 3. González-Andrade F, López-Pulles R. White phosphorus poisoning by oral ingestion of firecrackers or little devils: current experience in Ecuador. Clin Toxicol (Phila) [Internet]. 2011;49(1):29–33. Disponible en: http://www.ncbi.nlm.nih.gov/pubmed/21288149
- 4. (ATSDR) A for TS and DR. Toxicological profile for white phosphosrus. US Dep Heal Hum Serv [Internet]. 1997; Disponible en: http://dx.doi.org/10.1155/2013/286524
- 5. Santos O, Restrepo J, Velasquez L, Castano J, Correa G, Sepulveda E, et al. Acute liver failure due to white phosphorus ingestion. Ann Hepatol [Internet]. 2009;8(2):162–5. Disponible en: http://www.medigraphic.com/pdfs/hepato/ah-2009/ah092r.pdf\n http://ovidsp.ovid.com/ovidweb.cgi?T=JS&PAGE=reference&D=emed9&NEWS=N&AN=2009356748
- 6. Figueredo L, Acosta FEG, Fernando M, Castañeda O, J LF. Intoxicación por fósforo blanco. Rev Colomb Neumol. 16(3):198–203.
- 7. Sparling DW, Gustafson M, Klein P, Karouna-Renier N. Toxicity of white phosphorus to waterfowl: acute exposure in mallards. J Wildl Dis.1997;33(2):187–97.
- 8. Irizarry AL, Chief F, Zygmunt E. White Phosphorus Exposure: Background, pathophysiology, epidemiology. Medscape Ref [Internet]. 2015;1–5. Disponible en: http://emedicine.medscape.com/article/833585-overview#a5
- 9. Shannon M, Borron S, Burns M. Haddad and Winchester’s Clinical Management of Poisoning and Drug Overdose. 4th ed. Saunders Elsevier. Philadelphia; 2007.
Bibliografías
- 10. Frank M, Schmucker U, Nowotny T, Ekkernkamp A, Hinz P. Not all that glistens is gold: civilian white phosphorus burn injuries. Am J Emerg Med. 2008;26:974.e3–974.e5.
- 11. Chou TD, Lee TW, Chen SL, Tung YM, Dai NT, Chen SG, et al. The management of white phosphorus burns. Burns. 2001;27(5):492–7.
- 12. Pande TK, Pandey S. White Phosphorus Poisoning – Explosive Encounter. Japi. 2004;52(March):249–50.
- 13. Al Barqouni LN, Skaik SI, Nafiz R Abu Shaban, Barqouni N. White phosphorus burn. Lancet. 2010;376(9734):68.
- 14. Berndtson AE, Fagin A, Sen S, Greenhalgh DG, Palmieri TL. White Phosphorus Burns and Arsenic Inhalation. J Burn Care Res [Internet]. 2014;35(2):e128–31. Disponible en: http://content.wkhealth.com/linkback/openurl?sid=WKPTLP:landingpage&an=01253092-201403000-00018
- 15. Witkowski W, Surowiecka-Pastewka A, Biesaga M, Gierczak T. Experimental Comparison of Efficiency of First Aid Dressings in Burning White Phosphorus on Bacon Model. Med Sci Monit [Internet]. 2015;21:2361–6. Available from: http://www.medscimonit.com/abstract/index/idArt/894991
- 16. Ramírez-Sánches MS, Pascuzzo-Lima C, Bastidas O. Tratamiento de intoxiaciones por compuestos hepatotóxicos: N-acetilcisteína y carboximetilcisteína. Arch Venez Pueric Pediatr. 2009;72(2):68–72.
- 17. Laguado NF, Ricardo D, Soto F. Intoxicación por fósforo blanco en pediatría. Médicas UIS. 2007;20:61–6.