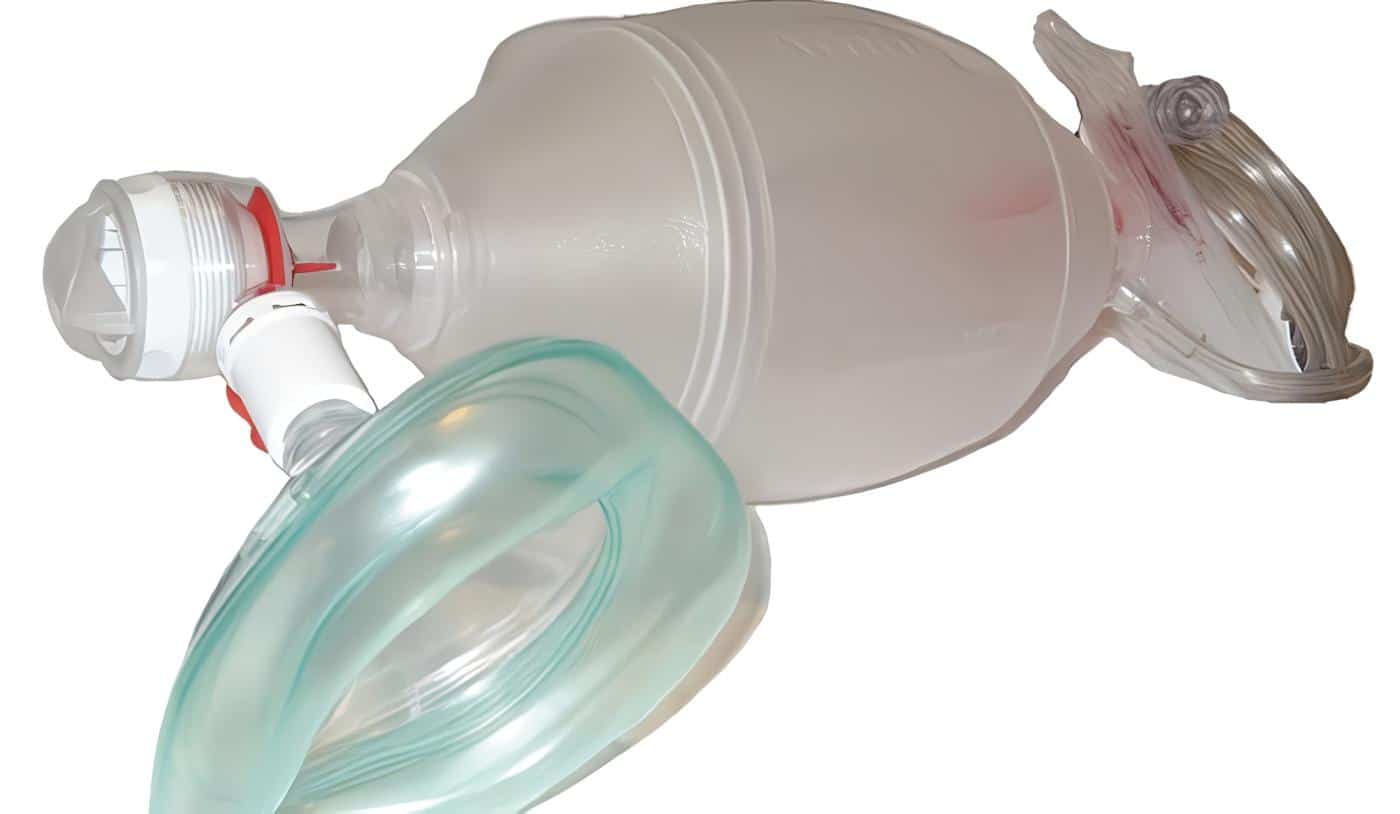
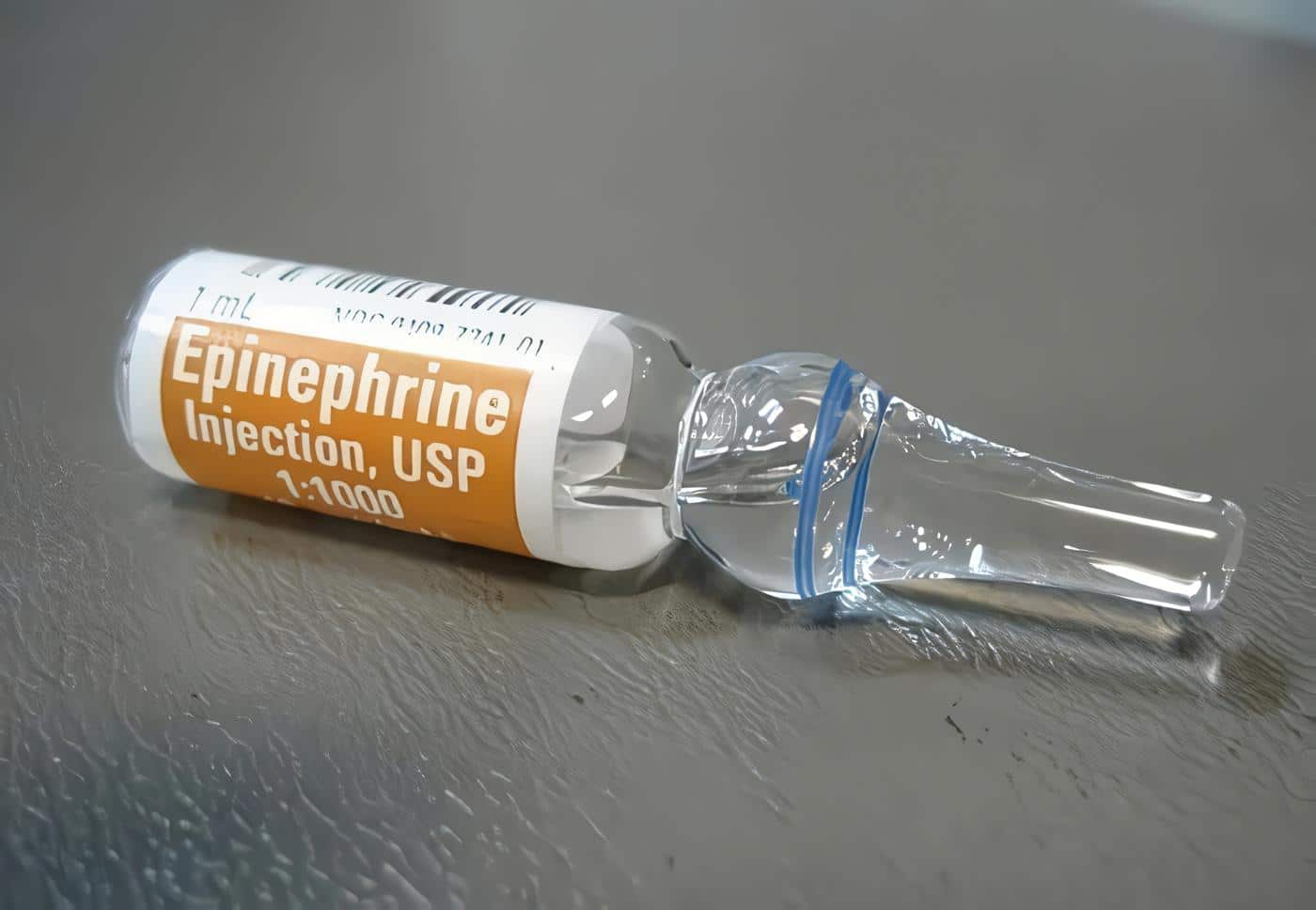
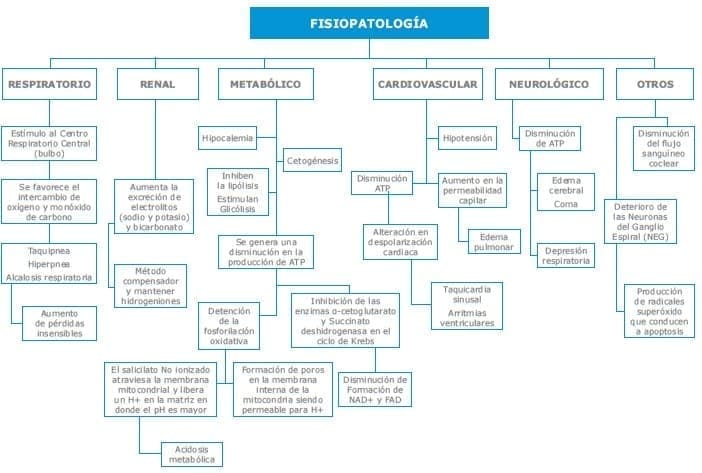
Anexo Nº 1. Salicilatos. Fisiopatología
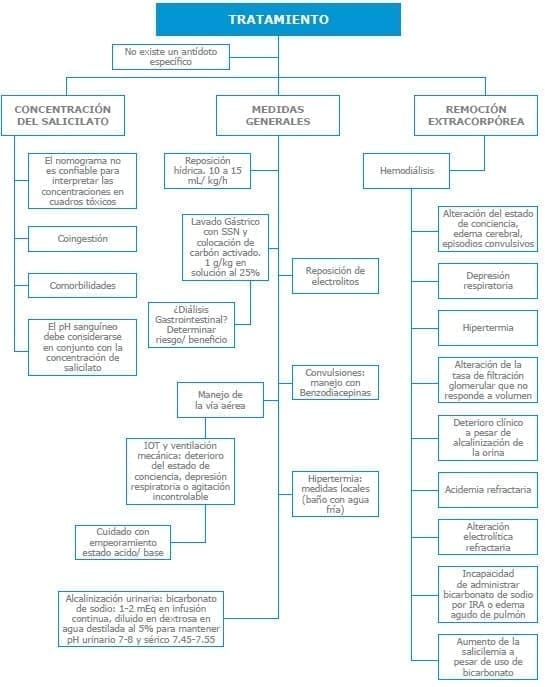
Anexo Nº 2. Salicilatos – Tratamiento
Anexo Nº 3 – 4. Treatment Guidelines for Neonatal Narcotic Abstinence Syndrome with Diluted Oral Morphine and Clonidine
Background
Morphine sulfate has been recommended by the AAP as the first-line agent for the pharmacologic treatment for neonatal narcotic abstinence syndrome (NNAS).
Clonidine has been widely used as a non-opioid alternative for managing opioid withdrawal in adults. A recent study (Agthe et al, Pediatrics 2009) comparing Morphine with a combination of Morphine and Clonidine for the treatment of NNAS demonstrated shorter duration of therapy, lower Morphine doses, and shorter hospital stays for infants receiving combination therapy. Clonidine use has been shown to be associated with a clinically-insignificant lowering of the heart rate (5bpm) and blood pressure (5mmHg). No other adverse effects were noted.
Management
The pharmaceutical treatment should be used in combination with supportive measures including: swaddling, holding, decreasing environmental stimuli, pacifiers, and rocking.
Initiation
- Begin NNAS scoring every 4-6 hrs (every other feeding).
- Initiate combination therapy with oral Morphine and Clonidine for three consecutive withdrawal scores are ≥8 or any one-time score is ≥12 using the Neonatal Withdrawal Inventory (NWI) scale.
- Initial doses:
a. Morphine at 0.05 mg/kg/dose PO every 3 hours with feedings.
b. Clonidine at 0.75 mcg/kg/dose every 3 hours (rounded to nearest 0.1mcg) - Increase Morphine dose by 0.01mg/kg/dose every 12 hours until withdrawal symptoms are controlled (two consecutive NWI scores <8). Morphine dosing should be titrated to the desired effect, with a usual maximum dose of 0.2 mg/kg every 3 hours.
- Adjust Clonidine dose to weight weekly to maintain daily dose of 6mcg/kg/day.
- If maximum dose for Morphine is reached (0.2 mg/kg/dose): Consider adding Phenobarbital (loading dose 20mg/kg in two divided dose of 10mg/kg every 12 hours), followed by a maintenance dose of 5mg/kg/ day once daily. Clonidine should be discontinued 24 hours after completion of the Phenobarbital loading dose.
Weaning
- Weaning should begin after NNAS symptoms are controlled for 48 hrs (total NWI score ≤24 over three consecutive measurements).
- Begin weaning Morphine by 0.04mg (flat dose) or by 10% of the highest dose, whichever is greater. Weaning can be done every day provided that the NWI scores are stable during weaning. If two scores in a 24-hour period are ≥ 8, consider increasing the dose back to the previous effective dose.
- Morphine may be discontinued from a dose of 0.06mg (flat dose).
- After 24 hours off Morphine, the Clonidine may be decreased by 50%. If NWI scores remain stable for 12 hours, the Clonidine may be discontinued. If total NWI scores exceed 24 over the next three measurements after stopping Clonidine, restart Morphine at 0.04mg every 3-4 hours with feeding.
- Patient may be discharged if NWI scores remain stable (total NWI Score ≤24 over three consecutive measurements for 1-2 days) off medication and the following criteria are met –
- Infant is taking oral feeds and gaining weight
- All newborn assessments/procedures have been completed (Hepatitis B Vaccination, hearing screening test, State Screening Tests)
- Social work has cleared the infant and a suitable home is arranged
- VNA is set up if deemed necessary
- Follow-up with the PMD is arranged
BP Monitoring
- Monitor BP per unit protocol (at least q shift) for the first 48 hours after starting Clonidine. If blood pressure remains stable, continue BP measurements every 12 hours during treatment.
- Monitor BP per unit protocol (at least q shift) when discontinuing Clonidine and for the first 24 hours off Clonidine.
References
- AAP Committee on Drugs. Neonatal Drug Withdrawal. Pediatrics 1998; 101: 1079-1088.
- Agthe AG, et al. Clonidine as an Adjunct Therapy to Opioids for Neonatal
- Abstinence Syndrome: A Randomized, Controlled Trial. Pediatrics. 2009 May;123(5):e849-56. Epub 2009 Apr 27.
- Opiate Treatment for Opiate Withdrawal in Newborn Infants. 2005 Cochrane Review.
- Zahorodny W, Rom C, Whitney W, Giddens S, Samuel M, Maichuk G, Marshall R. The neonatal withdrawal inventory: a simplified score of newborn withdrawal. J Dev Behav Pediatr. 1998 Apr;19(2):89-93.
Reviewed by
Yogangi Malhotra, MD, Dael Nelson, PAC, David Cheromcha, MD, Richard Ehrenkranz, MD, Matthew Grossman, MD, Barbara Sabo, APRN.
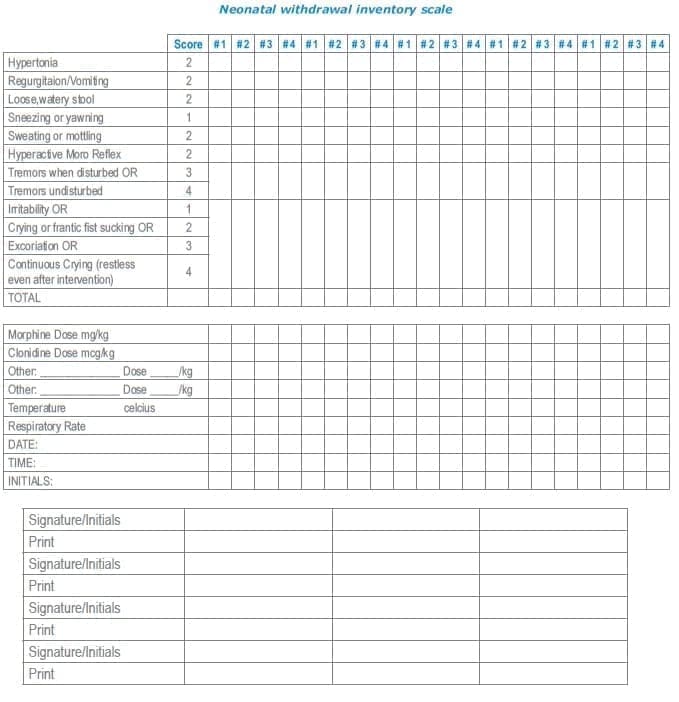
Neonatal withdrawal inventory scale helpful hints:
STEPS IN SCORING
- Conduct scoring within one hour prior to every other feeding (a 6 hour caregiving interval). If NPO conduct scoring every 6 hours.
- Observe infant without disturbing the infant for 1 minute.
- Encourage the baby to a quiet awake state. Take note of the infant’s ability to transition states smoothly.
- While in quiet awake state, assess moro reflex, measure axillary temperature, inspect skin for signs of excoriation and change diaper.
- Following your observations, score the infant using the neonatal withdrawal inventory criteria.
SCORING FYIs
HYPERTONIA
Score for increased tone that may interfere with suck swallow coordination as compared with a non-withdrawing newborn of comparable gestation and condition.
For the intubated or NPO infant, this section should assess the infant’s muscle tone as compared to the non-withdrawing newborn of comparable gestation and condition.
REGURGITATION
Score for true emesis of formula/BM seen in the mouth not associated with burping following a feeding.
For the intubated who is feeding score for true emesis seen following a gavage feeding or for an aspirate prior to the feeding greater than 1/3 of the previous feeding for NPO infants, only score if infant has large aspirate or is vomiting.
LOOSE, WATERY STOOLS
Stools are minimally formed or no solid stool noted. Often you will see a water ring in the diaper.
SNEEZING OR YAWNING
Score if the baby sneezes or yawns at least 6-8 times in the 6-hour time frame.
SWEATING OR MOTTLING
Score if you see sweating on the upper lip or forehead. Ensure the infant is not over bundled and the isolette is not overheated. Score for mottling not associated with hypothermia/cold stress (axillary temp < 36.0).
HYPERACTIVE MORO RELEEX
A moro reflex is expected… Score infant if an exaggerated moro response is exhibited compared to the non-withdrawing newborn of comparable gestation and condition. For the intubated infant do a modified moro.
TREMORS
Tremors are high frequency, low amplitude “shaking” of the arms and/or legs. If tremors are only present when disturbed such as after a physical exam, unbundling, taking vital , etc. then score as 3. If the tremors are present without any stimulation, then score a 4.
BEHAVIOR
Choose the one description which describes the baby ANY TIME during the 6 hour scoring interval.
Irritable: remains restless even after feeding or other intervention to calm infant such as swaddling, rocking,offering pacifier, kangaroo care.
Crying or frantic first sucking
Fresh excorioation of chin, face, knees or elbows. This means the baby is so irritable he/she is rubbing the face or extremities on the bedding, causin excoriation of the points of contact. Do not score for a diaper rash.
Continuous crying and an inability to sleep or feed dispite all interventions for calming the baby.
Anexo No. 5. Importación de Medicamentos Vitales no Disponibles
Medicamento vital no disponible
“Es un medicamento indispensable, e irremplazable, para salvaguardar la vida o aliviar el sufrimiento de un paciente, o un grupo de pacientes, y que, por condiciones de baja rentabilidad en su comercialización, no se encuentra disponible en el país o las cantidades no son suficientes (…)”1.
Existen tres modalidades para la solicitud.
Solicitud de importación para más de un paciente (cantidades comerciales), se requiere que el producto se encuentre en normas farmacológicas (es decir tener evaluación farmacológica: demostrar eficacia y seguridad), en los casos de paciente específico y urgencia clínica se debe allegar evidencia científica robusta de la eficacia y seguridad del producto.
| Ítem |
| Autorización importación como medicamento vital no disponible para un paciente. |
| Autorización de importación como medicamento vital no disponible para varios pacientes y de producción nacional. |
| Autorización importación vital no disponible en caso de urgencia clínica. |
El solicitante podrá ser cualquier entidad pública o privada legalmente constituida, debidamente autorizada para la distribución de medicamentos de acuerdo con las normas vigentes o aquellas que las modifiquen o sustituyan. (Usualmente son importadores que tienen las empresas administradoras de planes de beneficios, EAPB).
Las tarifas las encontrará en https://www.invima.gov.co/tramites-y-servicios/tarifas.html
| Código | Ítem |
| 4002-24 | Autorización importación como medicamento vital no disponible para un paciente. |
| 4002-25 | Autorización de importación como medicamento vital no disponible para varios pacientes y de producción nacional. |
| 4002-26 | Autorización importación vital no disponible en caso de urgencia clínica. |
Fuente. www.invima.gov.co
Listado de los códigos de las tarifas para tramitar solicitudes de medicamentos como vitales no disponibles.
Autorización de importación para un paciente específico
La importación de un medicamento vital no disponible, para un paciente específico, podrá ser realizada por el mismo paciente o por una persona natural o jurídica pública o privada legalmente constituida previo cumplimiento de los siguientes requisitos:
- Solicitud expresa de la autorización de importación presentada ante el INVIMA.
- Nombre completo del paciente y su documento de identidad.
- Principio activo en su denominación genérica y composición del medicamento.
- Fórmula médica y resumen de la historia clínica en donde se indique la dosis, tiempo de duración del tratamiento, nombre del medicamento y cantidad, la cual debe estar firmada por el médico tratante, con indicación y número de su tarjeta profesional.
- Copia del recibo de consignación correspondiente.
Autorización de importación de medicamentos vitales no disponibles para uso exclusivo en casos de urgencia clínica.
En el caso de medicamentos vitales no disponibles de uso exclusivo en urgencia clínica, se podrá autorizar la importación de cantidades no comerciales sin la documentación referida al paciente, en cuyo evento bastará la sustentación médica correspondiente.
La EP S solicita en forma directa, o a través de una importadora, a la Dirección de Operaciones Sanitarias la autorización para la importación de este medicamento allegando los soportes listados previamente y cancelando la tarifa correspondiente El Listado de Medicamentos Vitales No Disponibles actualizado se puede consultar en: https://www.invima.gov.co/images/pdf/salas-especializadas/Sala_Especializada_de_Medicamentos/LISTADO-DE-MEDICAMENTOS-VITALESNO-DISPONIBLES_Noviembre-2016.pdf
Referencias
- Ministerio de la Protección Social. Decreto Nº 0481 de 2004. Disponible en: https://www.minsalud.gov.co/sites/rid/Lists/BibliotecaDigital/RIDE/DE/DIJ/Decreto-0481-de-2004.pdf
Anexo No. 6. Eventos toxicológicos que actualmente son de notificación obligatoria al Sistema de Vigilancia en Salud Pública ( SIVIGILA)
 Anexo No. 7 Ficha de notificación al SIVIGILA
Anexo No. 7 Ficha de notificación al SIVIGILA
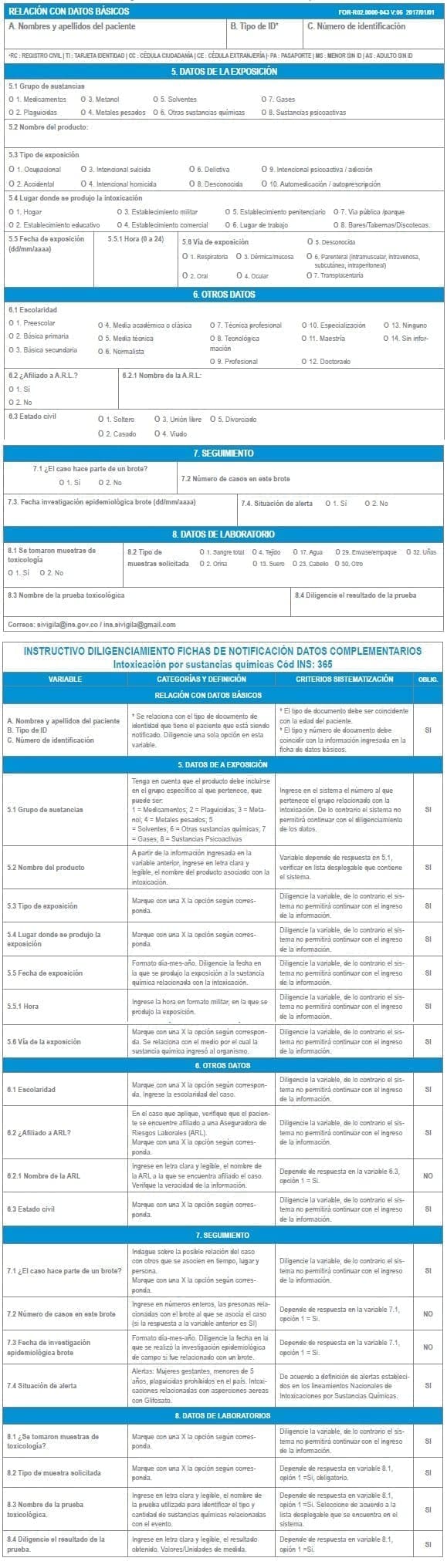
SISTEMA NACIONAL DE VIGILANCIA EN SALUD PÚBLICA
Subsistema de información SIVIGILA
Ficha de notificación
Intoxicaciones por sustancias químicas Código INS: 365
La ficha de notificación es para fines de vigilancia en salud pública y todas las entidades que participen en el proceso deben garantizar la confidencialidad de la información LEY 1273/09 y 1266/09
Anexo No. 8. Raticidas artesanales e ilegales
Diana Marcela Pava Garzón
Médico Línea Nacional de Toxicología Ministerio de Salud y Protección Social
Candidata a Magister en Toxicología Universidad Nacional de Colombia
Miembro Grupo de Investigación sustancias psicoactivas
Universidad Nacional de Colombia
En la práctica clínica es frecuente el ingreso de pacientes con intoxicaciones, que involucran raticidas desconocidos o no rotulados ya sean en presentaciones liquidas o sólidas, con diferentes intencionalidades como suicida, accidental (especialmente en población pediátrica), entre otras. Esto causa dificultad en el manejo clínico ante la ausencia de signos y síntomas que los contextualicen en toxidromes clínicos.
En el año 2015, se asesoraron en la Línea Nacional de Toxicología un total de 196 casos, y para el año 2016 fueron 177 casos que registraron eventos causados por raticidas de composición desconocida.
A continuación, se presenta la galería de imágenes de algunos raticidas, no registrados ante autoridad competente, implicados en casos de intoxicación, los cuales fueron asesorados por la Línea Nacional de Toxicología año 2015-2016. La composición de estos productos es muy variable, pudiéndose encontrar Aldicarb (Carbamato), o Fluoracetato de sodio, o anticoagulantes, u otras sustancias o mezclas de las anteriores.

Instituciones de control y alertas
Instituto Colombiano Agropecuario (ICA)
Al reportar e indagar por productos plaguicidas a las Autoridades Nacionales Competentes, se contribuye al Sistema de Vigilancia de Plaguicidas.
Para ello, el Instituto Colombiano Agropecuario (ICA), que es la Autoridad Nacional Competente para el registro y control de los plaguicidas de uso agropecuario, dispone del siguiente contacto:
Coordinador del Grupo de Planificación Gestión de Calidad y Farmacovigilancia.
Dirección Técnica de Inocuidad e Insumos Veterinarios.
Teléfono (57) (1) 3323700 extensión 1227. Bogotá, Colombia.
Instituto Nacional de Vigilancia y Control de Medicamentos y Alimentos (INVIMA)
El INVIMA, es la autoridad nacional competente para el registro y control de los plaguicidas de uso doméstico. Para mayor información acerca de los productos controlados por esta entidad, se puede ingresar al siguiente link:
http://farmacovigilancia.invima.gov.co:8082/Consultas/consultas/consreg_encabcum.jsp
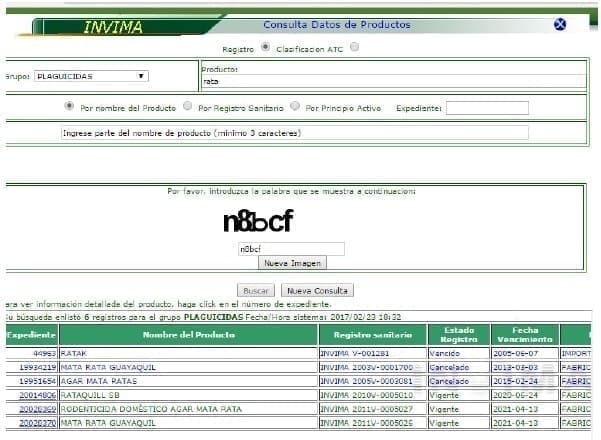
Ejemplo: se realizó consulta de registro en el portal de INVIMA, donde encontró actualizado a fecha 24 de febrero de 2017 los siguientes registros de raticida:

 Anexo No. 7 Ficha de notificación al SIVIGILA
Anexo No. 7 Ficha de notificación al SIVIGILA