3.3
Marie Claire Berrouet Mejía. Médico Especialista en Toxicología Clínica UDEA Toxicóloga Clínica Hospital General de Medellín -Clínica Soma Docente de Farmacología y Toxicología Universidad CES, Medellín Miembro de la Asociación de Toxicología Clínica Colombiana – ATCC–
Andrés Felipe Estrada Atehortua Médico Especialista en Medicina de Urgencias CES Urgentólogo Hospital Pablo Tobón Docente Facultad de Medicina Universidad Pontificia Bolivariana
Ubier Eduardo Gómez. Calzada Médico Especialista en Toxicología Clínica Profesor de Farmacología y Toxicología Universidad de Antioquia, Medellín Toxicólogo Hospital San Vicente Fundación de Medellín Miembro de la Asociación de Toxicología Clínica Colombiana – ATCC–
Generalidades
Una de las claves importantes para sospechar que estamos ante un paciente intoxicado, es el compromiso de uno o más sistemas del cuerpo.
Las alteraciones hidroelectrolíticas y ácido base son hallazgos frecuentes tanto en los cuadros agudos como crónicos, su identificación temprana no solo brinda una clave diagnóstica importante para el abordaje de pacientes con intoxicación desconocida, sino que la corrección de estas mismas alteraciones es fundamental para la recuperación del paciente y la disminución de las secuelas1-3.
El registro sistemático de los signos vitales no solo será de utilidad en el abordaje del paciente intoxicado, sino que puede ayudar a sospechar la presencia de algunos desórdenes acido base y de electrolitos.
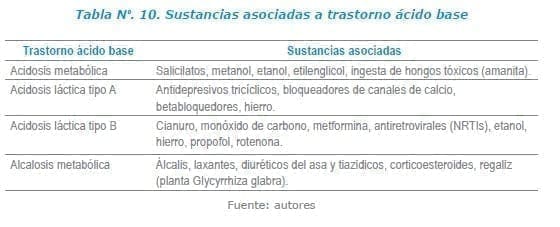
Por ejemplo, un paciente hipotenso en el contexto de una sobredosis de bloqueadores de canales de calcio, betabloqueadores o bloqueadores α1, por la hipoperfusión asociada se puede sospechar una acidosis metabólica1-3.
El patrón respiratorio aporta claves diagnósticas y se debe tener en consideración, alteraciones como la taquipnea, que puede ser secundaria a un estímulo directo del centro respiratorio como el producido por los salicilatos puede ser una respuesta compensadora a un xenobiótico que esté produciendo acidosis metabólica.
La bradipnea por su parte puede asociarse a opioides o sustancias sedantes como alcohol, clozapina, antihistamínicos, benzodiacepinas y antidepresivos1-3.
Con respecto al estado de hidratación evaluado a través de la humedad de las mucosas:
Es importante tener en consideración que muchas sustancias como fenotiazinas, antihistamínicos, antidepresivos entre otros pueden producir mucosas secas por un efecto anticolinérgico sin que esto signifique que el paciente se encuentra deshidratado.
Lo anterior es fundamental para hacer uso racional de los cristaloides, pues no todo paciente requiere grandes cantidades de cristaloides, dado que estos en ocasiones pueden empeorar un estado de acidosis basal (por ejemplo, la solución salina al 0.9%, que por cada litro de solución aporta 154 mEq de sodio y 154 mEq de cloro: acidosis hiperclorémica).
Los paraclínicos fundamentales para valorar el estado ácido base y las alteraciones hidroelectrolíticas son el ionograma y los gases arteriales o venosos. Este último aspecto es importante entendiendo que si se sospecha una alteración metabólica se puede evaluar a través de gases venosos, un procedimiento de recolección más sencillo, menos doloroso y complicado para el paciente.
En centros de baja complejidad que no cuentan con este recurso es válido recordar que a partir de otras ayudas diagnósticas se puede obtener una aproximación a alteraciones electrolíticas, este es el caso del electrocardiograma; en la Tabla Nº 9, se enumeran algunas alteraciones hidroelectrolíticas y su asociación con hallazgos electrocardiográficos4.

Algunos otros paraclínicos como el citoquímico de orina nos aporta información a partir de variables como la gravedad específica, un valor mayor a 1.015 evidencia una orina concentrada y se puede asociar a un estado de depleción de volumen, valores menores a 1.010 que indican hipostenuria muestran una incapacidad para concentrar orina, lo cual se puede asociar a intoxicaciones como: litio, antiinflamatorios no esteroideos o envenenamiento crotálico5.
Además de los valores anteriores, el citoquímico de orina nos permite evaluar la presencia de cuerpos cetónicos los cuales se pueden ver en la cetoacidosis alcohólica y en la intoxicación por salicilatos5.
Alteraciones ácido base en el paciente intoxicado
Acidosis metabólica
El término acidosis y alcalosis hace referencia a un cambio en el pH. La acidosis metabólica es definida como un pH <7.35 y acompañada de una disminución de bicarbonato y una base exceso negativa; es una alteración frecuente de encontrar en pacientes intoxicados.
La importancia de su rápido reconocimiento y corrección radica en que puede empeorar el pronóstico al asociarse a alteraciones del sensorio, arritmias, hipotensión y otras alteraciones electrolíticas como hipercalemia entre otras6-8.
Los tóxicos asociados a acidosis metabólica pueden explicar esta alteración fundamentalmente por los siguientes mecanismos:
- Compensación de una alcalosis respiratoria.
- Aumento en la producción de ácido bien sea porque se trata de sustancias ácidas, se generen metabolitos ácidos o cetoácidos.
- Alteración en la eliminación de ácido (ejemplo acidosis tubular renal tipo 1 y tipo 4).
- Interferencia con la producción de ATP.
- Pérdida de bicarbonato.
Brecha anionica (anión gap):
En el abordaje del paciente con acidosis metabólica se pueden considerar dos opciones: una con brecha aniónica (anión gap) aumentada y la otra con brecha aniónica normal. Para calcular la misma se utiliza la siguiente formula:
AG = [Na+]-[Cl-]+ [HCO3-]
El valor normal de la brecha aniónica se encuentra entre 8 y 12 mEq/L, si bien es cierto que situaciones como la hipoalbuminemia y la hipofosfatemia pueden dificultar su interpretación, en el paciente intoxicado, donde la mayoría de las veces no tienen comorbilidades y son cuadros agudos, éste método tiene una gran utilidad clínica9-11.
Existe una nemotecnia para recordar las sustancias asociadas a acidosis metabólica con brecha aniónica aumentada: CATMUDPILES
C = Cianuro
A = Cetoacidosis alcohólica
T = Tolueno
M = Metanol – metformina
U = Uremia
D = Cetoacidosis diabética
P = Paraldehído
I = Hierro
L = Lactato
E = Etilenglicol
S = Salicilatos
Acidosis láctica
Sabiendo que una causa de acidosis en el paciente intoxicado es la acidosis láctica, vale la pena recordar que el metabolismo del lactato es influenciado por el estado redox de la célula, el cual a su vez se refleja en la relación entre las formas oxidada y reducida de la Nicotinamida Adenina Dinucleótido: NAD (forma oxidada) y NADH (forma reducida).
La importancia de esta coenzima, es su papel en el intercambio de electrones e hidrogeniones en los procesos de producción de energía9-11. Una reacción fundamental en que interviene es la reacción de equilibrio en la producción entre ácido pirúvico y ácido láctico como se muestra en el siguiente esquema:
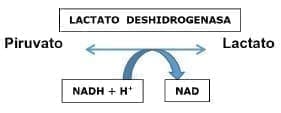
Podemos concluir que la relación piruvato lactato está influenciada por la relación NAD+ y NADH, así que los factores que alteren el equilibrio redox pueden aumentar la producción de lactato. En general hay tres mecanismos fundamentales que explican el exceso de lactato en sangre, dentro de ellos están:
- Incremento en la producción de piruvato (ejemplo: alcalosis respiratoria, intoxicación por salicilatos).
- Alteración en el estado redox con acúmulo de NADH alterando la conversión de piruvato a lactato (ejemplo: convulsiones, intoxicaciones por monóxido de carbono, cianuro, zidovudina).
- Alteraciones en la utilización de lactato: falla hepática, alcoholismo, etc.
La acidosis metabólica puede clasificarse a su vez en tipo A, la cual es explicada por alteraciones en la oxigenación de los tejidos y en tipo B donde no se identifica hipoperfusión y generalmente se asocia a toxinas que alteren el metabolismo celular, como en el caso de algunos tóxicos hematológicos: cianuro, monóxido de carbono, sulfuro de hidrógeno, sustancias que produzcan metahemoglobina, etc.10-13.
Acidosis asociada a cetonas
Dentro de las principales causas tóxicas de cetosis están: la cetoacidosis alcohólica, isopropanol, acetona (removedor de esmalte), ácido valproico y salicilatos. De ellas, las que se asocian con acidosis son la cetoacidosis alcohólica y los salicilatos12, 16,17.
La cetoacidosis alcohólica es un diagnóstico que se debe tener presente en los servicios de urgencias, como diagnóstico diferencial de alcoholes tóxicos como metanol, ésta ocurre en alcohólicos crónicos que beben por periodos prolongados sin una buena nutrición12,16,17.
Alcalosis metabólica
Aunque es un poco menos frecuente en el intoxicado, también se debe sospechar, esta se acompaña de un pH >7.45, elevación del bicarbonato y una base exceso positiva. Los mecanismos que la pueden explicar son12,14-15:
- Pérdida de cloro.
- Aumento de bicarbonato.
- Aumento de la acción mineralocorticoide.
- Compensación de acidosis respiratoria.
(Lea También: Secuencia Rápida de Intubación en el Paciente Intoxicado)
Acidosis y alcalosis respiratoria
La acidosis respiratoria puede ser considerada como un marcador de hiperventilación y tiene como características un PH < 7.40 y la presencia de hipercapnia. Dentro de las causas tóxicas asociadas se encuentran: barbitúricos, opioides, antidepresivos, gamahidroxibutirato (éxtasis líquido) sustancias con efecto sedante y se puede ver como complicación del síndrome intermedio asociado a organofosforados9,12.
La alcalosis respiratoria resulta de un aumento en la eliminación de CO2 teniendo como característica un pH > 7.40 y la presencia de hipocapnia, aunque frecuentemente se asocia a la compensación de otro trastorno como la acidosis metabólica. Los xenobiótico asociados a la misma son: salicilatos, siendo en esta intoxicación uno de los primeros hallazgos encontrados y explicado por un efecto directo central que lleva a un aumento en la frecuencia respiratoria9-12.
Cabe señalar que hay muchos medicamentos o toxicidades crónicas que pueden producir patrones de hiperventilación para tratar de compensar una alteración en el intercambio gaseoso, dentro de estas causas se debe tener en cuenta las sustancias asociadas a fibrosis como: paraquat, amiodarona, metotrexate, nitrofurantoina, bleomicina, silicosis y asbestosis entre otras9,10,12.
También es importante considerar como causas de alcalosis respiratoria aquellas condiciones o toxinas asociadas a edema pulmonar dentro de ellas están: bloqueadores de canales de calcio, desferoxamina, envenenamiento por escorpiones, glifosato y naloxona9, 10,12,14.
Manejo y criterios de remisión
El pronóstico del paciente intoxicado no depende en la gran mayoría sólo del manejo de antídotos sino además de hacer un correcto abordaje inicial, identificar y corregir complicaciones para disminuir secuelas.
El manejo de cada alteración debe ser dirigido a identificar la causa y corregirla (hipoperfusión, alteraciones en la ventilación, etc). Conociendo que muchos medicamentos producen alteraciones acido base y electrolíticas es fundamental tener un alto índice de sospecha de las diferentes alteraciones para hacer un manejo adecuado.
En intoxicaciones donde se sospeche la presencia de estas alteraciones y por la baja complejidad no se cuente con las ayudas diagnósticas necesarias es importante remitir a un centro de mayor complejidad para un manejo multidisciplinario, pues en ocasiones se requerirá de diferentes técnicas como cuantificación de iones y electrolitos, monitoreo invasivo o terapia de reemplazo renal según el caso.
Bibliografia
- 1. Erickson T. he Approach to the Patient with an Unknown Overdose. Emerg Med Clin N Am. 2007; 25: 249–281.
- 2. Hill. G , Babatunde O, Dawood N. Patients Presenting with Acute Toxin Ingestion. Anesthesiology Clin. 2010; 28: 117–137.
- 3. Vale A, Bradberry S. Acute Medicine: Part 2 Management of poisoning Medicine, 2013; 41(3): 179-181.
- 4. Germán, C. M., Mario, A. G. El Uroanálisis: un gran aliado del médico. Sociedad Colombiana de Urología. 2007.
- 5. Enger E. Acidosis, gaps and poisoning. Acta Med Scand. 1982; 212: 1-3.
- 6. Fencl V, Jabor A, Kazda A, Figge J. Diagnosis of metabolic acidbasedisturbances in critically ill patients. Am J Respir Crit Care Med. 2000; 162:2246.
- 7. Harrigan RA, Nathan MS, Beattie P. Oral agents for the treatment of type 2 diabetes mellitus: pharmacology, toxicity, and treatment. Ann Emerg Med. 2001; 38:68.
- 8. Salpeter SR, Greyber E, Pasternak GA, et al. Risk of fatal and nonfatal lactic acidosis with metformin use in type 2 diabetes mellitus: systematic review andmeta-analysis. Arch Intern Med. 2003; 163: 2594–602.
Referencias
- 9. Kreisberg RA. Lactate homeostasis and lactic acidosis. Ann Intern Med. 1980; 92:227.
- 10. Luchette FA, Jenkins WA, Friend LA, et al. Hypoxia is not the sole cause of lactate production during shock. J Trauma. 2002; 52:415.
- 11. Levy B. Lactate and shock state: the metabolic view. Curr Opin Crit Care. 2006; 12:315.
- 12. Wiener SW. Toxicologic Acid-base disorders. Emerg Med Clin North Am. 2014 Feb; 32(1):149-65
- 13. Sia P, Plumb TJ, Fillaus JA. Type B lactic acidosis associated with multiple myeloma. Am J Kidney Dis. 2013; 62: 633.
- 14. Jones A. Poisoning: Part 1 of 2 Metabolic effects of poisoning What’s new? Practice points Medicine, 2012;40(2): 55-58.
- 15. Nelson L, Lewin N, Howland MA, Hoffman R, Goldfrank L, Flomenbaum N. Goldfrank’s Toxicologic Emergencies, Ninth.