7.6 (Pregunta 6)
En pacientes específicos transfundidos regular y crónicamente, ¿a qué umbral de Hb deben transfundirse para evitar desenlaces adversos?
Evidencia
Los pacientes que requieren transfusiones crónicas de glóbulos rojos representan una proporción significativa del consumo de sangre. Esto incluye pacientes con β talasemia mayor, enfermedad de células falciformes y mielodisplasia.
Por lo tanto, el uso apropiado de glóbulos rojos en estos pacientes es de gran importancia. Tanto para el bienestar del paciente como para el uso apropiado de un recurso escaso y valioso.
La hipo-producción crónica de glóbulos rojos significa que generalmente se requieren transfusiones regulares para mantener la Hb en un nivel particular. Las Guías de Práctica Clínica de 2001 sobre el uso de componentes sanguíneos (1) indicaron que mantener la Hb >80 g/L (8g/dL) probablemente fuera apropiado sobre la base de principios fisiológicos.
Estos pacientes suelen ser tratados como pacientes ambulatorios.
Por lo tanto, por razones prácticas, a menudo se prescribe un número predeterminado de unidades de GR (destinadas a lograr una concentración de Hb definida). En lugar de evaluar su respuesta a cada unidad transfundida.
Además, estos pacientes pueden ser transfundidos deliberadamente a un nivel más alto de Hb que el fisiológicamente necesario. En un intento de maximizar el intervalo entre transfusiones.
Esta toma de decisiones parece estar basada en la práctica histórica. Los umbrales para iniciar la transfusión en estos pacientes son diferentes a los umbrales de los pacientes con anemia que no tienen disfunción de la médula ósea.
Debido a la naturaleza crónica del trastorno, los pacientes con anemia crónica pueden recibir múltiples transfusiones durante un largo período.
Por lo tanto, además de los riesgos habituales asociados con la transfusión, los pacientes corren el riesgo de complicaciones asociadas al antígeno leucocitario humano (HLA), la aloinmunización, y la sobrecarga de hierro. Para este último, se debe considerar el uso de la terapia quelante.
(Lea También: Niveles de Hemoglobina en Pacientes con Neoplasias Malignas)
7.6.1 Talasemia
El uso de transfusiones crónicas de glóbulos rojos se intensificó en 1978. Cuando se introdujo la terapia de quelación de hierro con infusiones de desferrioxamina subcutánea para mejorar el manejo de la sobrecarga de hierro en la ß talasemia mayor.
El objetivo de las transfusiones era prevenir la anemia severa, la mortalidad temprana, promover el crecimiento, el desarrollo, el bienestar y la calidad de vida.
Minimizar o prevenir la expansión de la masa de la médula
También tenían la intención de minimizar o prevenir la expansión de la masa de la médula que conduce a deformidades óseas tales como: hiperplasia maxilar y tejido hematopoyético extra medular, que típicamente ocurren en el hígado y el bazo y a lo largo de la columna vertebral.
La aparición de cualquiera de estas complicaciones en la infancia y la niñez se utiliza como un criterio para iniciar el tratamiento de transfusión sanguínea. Con el objetivo ampliamente aceptado de mantener una concentración de Hb pre-transfusión de al menos entre 90 -110 g/L (9 – 10 g/dL), y una media de aproximadamente 120 g/L (12 g/dL).
Esta concentración de Hb pre-transfusión se adoptó empíricamente, después de que los ensayos de niveles más bajos encontraran que algunas de las complicaciones de la sub-transfusión (ej. la expansión de la médula ósea) siguieron apareciendo.
Por lo tanto, a finales de 1970 y 1980, hubo una adopción generalizada de la Hb pretransfusional en un intervalo entre 90 – 110 g/L (9 – 10 g/dL), que era el máximo alcanzable con 3 – 4 transfusiones semanales. Hasta el día de hoy, este tratamiento se acepta como óptimo cuando se combina con una adecuada terapia quelante.
El hiperesplenismo que requiere esplenectomía ocurre en al menos el 50% de los pacientes y suele llevarse a cabo cuando el requisito de transfusión de sangre excede 200 – 250 ml/kg/año. La esplenectomía generalmente resulta en una reducción significativa en el requerimiento de transfusión.
Pacientes con β-talasemia intermedia parecen ser menos comunes
En contraste con la β-talasemia mayor, estudios recientes han reportado que las complicaciones en pacientes con β-talasemia intermedia parecen ser menos comunes.
Esto es particularmente demasiado tarde en la vida de los pacientes sometidos a transfusión regular, y es más común en los pacientes que se han sometido a esplenectomía.
Así, la transfusión regular puede convertirse en una opción más común para el manejo y la prevención de complicaciones que ocurren más tarde en la vida en este subgrupo de pacientes.
Sin embargo, el manejo de la β-talasemia intermedia continuará siendo personalizado hasta que se conozca más acerca de estas complicaciones tardías.
La adecuación de la transfusión de sangre y la terapia de quelación en los prestadores de servicios de salud depende de la adecuación de los recursos locales (incluyendo el servicio de transfusión sanguínea) y la financiación de un agente quelante de hierro apropiado.
Hay pocos estudios para apoyar esta estrategia de manejo. Sin embargo, los pacientes manejados de esta manera están sobreviviendo en su sexta década de vida.
La revisión de literatura encontró sólo unos pocos estudios que abordaron objetivamente aspectos de estos problemas.
Un estudio de cohorte retrospectivo de calidad moderada (nivel III) proporcionó evidencia para la asociación del nivel actual de pre transfusión con una supervivencia más larga (138).
El estudio informó que los sujetos con una concentración pretransfusional de Hb >90 g/L (9 g/dL) tuvieron supervivencia significativamente más larga que aquellos con un nivel ≤90 g/L (<9 g/dL).
Estudios de cohorte prospectivos
Dos estudios de cohorte prospectivos (nivel II) (139,140) y un estudio de cohorte retrospectivo (nivel III) (141) investigaron la relación entre las concentraciones pretransfusionales de Hb y el volumen de transfusión.
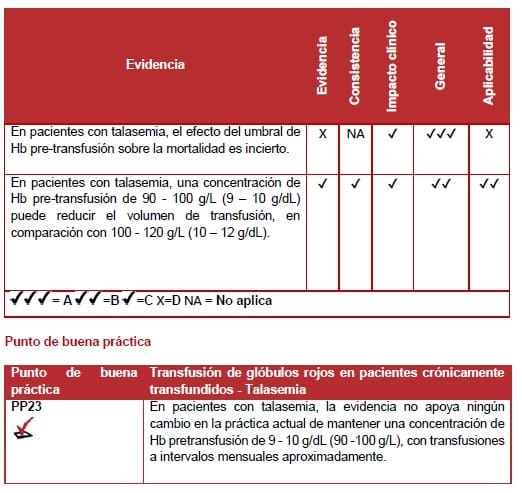
Cazzola (141) y Masera (139) encontraron que los pacientes mantenidos con una concentración media pretransfusional de Hb entre 90 – 100 g/L (9 – 10 g/dL) y 102 g/L 10.2 g/dL) respectivamente. Requirieron volúmenes de transfusión significativamente menores que los pacientes con niveles de pre transfusión más altos.
Masera (139) encontró que esta diferencia se mantuvo durante los primeros 5 meses, después de lo cual no hubo diferencias significativas.
Cazzola (141) no encontró diferencias entre los subgrupos con o sin esplenectomía, y Masera (139) incluyó sólo pacientes esplenectomizados.
Torcharus (140) informó que los pacientes pediátricos con una concentración pretransfusional de Hb >80 g/L (>8 g/dL) tenían un volumen transfusional medio más alto que los sujetos con una media de Hb pre transfusional de 60 – 70 g/L (6 -7 g/dL). Estos resultados apoyan la práctica actual.
Los problemas de calidad de vida han sido importantes en el manejo óptimo de pacientes con β-talasemia mayor dependiente de transfusiones.
Se requieren estudios de cohortes prospectivos o retrospectivos de alta calidad en esta área.
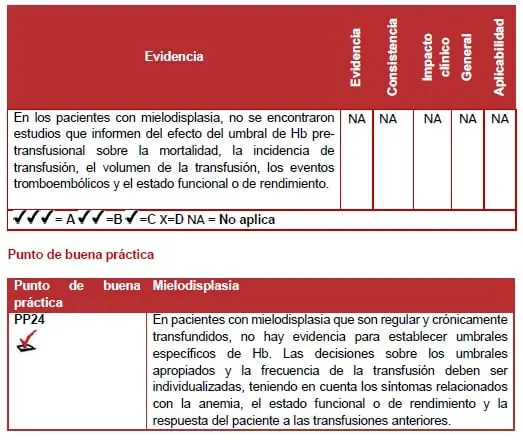
7.6.2 Mielodisplasia
El síndrome mielodisplásico (SMD) se refiere a un grupo de trastornos de las células progenitoras de la médula ósea que implican la producción ineficaz (displasia) de la serie mieloide. Los pacientes con SMD desarrollan una o más citopenias debido al fallo progresivo de la médula ósea.
Aunque el Síndrome mielodisplásico (SMD) puede progresar a leucemia aguda, una proporción significativa de morbilidad y mortalidad se relaciona con las citopenias. El SMD ocurre predominantemente en pacientes mayores.
La anemia es común en el SMD, y el tratamiento de soporte con transfusión de glóbulos rojos se ha prescrito tradicionalmente. El objetivo principal de la transfusión de glóbulos rojos es prevenir o tratar complicaciones como el compromiso cardiovascular y cerebrovascular.
También se utiliza para mejorar la calidad de vida en pacientes con SMD que presentan síntomas significativos de malestar y fatiga.
Sin embargo, estos síntomas pueden o no estar relacionados con la anemia, y la evaluación de la respuesta clínica a la transfusión es por lo tanto importante.
Estudios en pacientes con Síndrome Mielodisplásico (SMD)
La revisión sistemática tuvo como objetivo identificar estudios en pacientes con Síndrome Mielodisplásico (SMD). Para determinar a qué umbral de Hb debe darse la transfusión para evitar complicaciones adversas. Estas complicaciones incluyen la morbilidad. La mortalidad y la reducción del estado funcional o de rendimiento.
No se identificaron estudios que evaluaran la asociación entre las concentraciones de Hb pre-transfusión y la mortalidad. El estado funcional o de rendimiento. Los eventos tromboembólicos arteriales o la incidencia o volumen de transfusiones de GR. Se identificaron dieciocho estudios de cohorte, los cuales evaluaron la Hb y los resultados en pacientes con Síndrome Mielodisplásico (SMD).
Sin embargo, ninguno proporcionó análisis relacionados con la concentración de Hb pre-transfusión. Más bien, tenían como objetivo principal evaluar el impacto de la concentración de Hb en el momento del diagnóstico.
La mayoría de los estudios encontraron que la concentración de Hb en el momento del diagnóstico era un predictor significativo de supervivencia. Un hecho que es bien reconocido.
Sólo un estudio informó que la concentración de Hb también puede mostrar una correlación con los resultados de las pruebas de estado funcional o de desempeño en pacientes con Síndrome Mielodisplásico (SMD) (142).
Por lo tanto, no hay evidencia para guiar a los médicos sobre el umbral de Hb para la transfusión en pacientes con SMD y anemia crónica. Se necesitan más estudios para evaluar el beneficio de la transfusión en esta población.
Las decisiones sobre la necesidad y la frecuencia de la transfusión requieren una evaluación riesgo-beneficio en cada paciente. Teniendo en cuenta su estado funcional o de rendimiento y la concentración de Hb.