10.5.1.4
Para los pacientes fetales, neonatales o pediátricos, ¿la selección de componentes sanguíneos específicos (ejemplo: componentes sanguíneos negativos para CMV). En comparación con los productos sanguíneos de rutina, mejora los desenlaces?
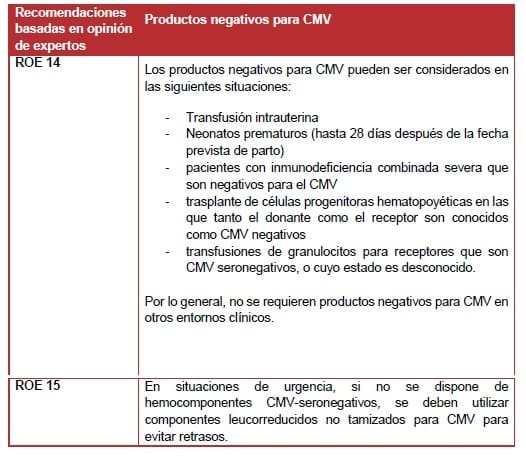
El citomegalovirus (CMV) es común; da lugar a una infección crónica, persistente y (en su mayor parte) asintomática. Sin embargo, la infección por CMV puede ser grave o potencialmente mortal en el feto o el recién nacido, y en pacientes con deficiencia severa de células T. El CMV puede ser transmitido por componentes sanguíneos celulares. Pero el riesgo de infección transfusional para CMV se ha reducido a medida que el uso de sangre entera fresca ha disminuido y el uso de componentes sanguíneos leucoreducidos se ha vuelto rutinario.
El riesgo de transmisión de CMV a través de los componentes sanguíneos se reduce significativamente ya sea por el tamizaje del donante para el CMV o la leucorreducción prealmacenamiento (219-221). Sin embargo, la transmisión del CMV todavía puede ocurrir a partir de los productos CMV seronegativos debido a la aceptación de donantes que están en el período de ventana entre la adquisición de virus y la seroconversión (que pueden tener alta carga viral). La transmisión a partir de componentes leucorreducidos seropositivos puede ocurrir debido a fallo del filtro de leucodepleción (222-223).
Selección de componentes sanguíneos negativos para CMV.
Neonatos y transfusiones intrauterinas
Las pautas para los recién nacidos varían ampliamente, e incluyen recomendaciones tanto a favor como en contra del uso rutinario de productos seronegativos para CMV (203-204, 224-226). Con la leucorreducción rutinaria. Es probable que el riesgo de transmisión a partir de componentes sanguíneos celulares sea bajo (222). Mientras que la leche materna representa una fuente común de infección.
Trasplante de médula ósea, trasplante de órganos sólidos y otros pacientes de hematología y oncología
El uso de componentes sanguíneos CMV-seronegativos y componentes sanguíneos leucorreducidos es probablemente equivalente en estas poblaciones, y ambos resultan en una baja tasa de transmisión (226-228). La declaración del Comité Asesor sobre Seguridad en Sangre, Tejidos y Órganos del Reino Unido (SaBTO) señala que los glóbulos y las plaquetas seronegativos para CMV pueden ser reemplazados con componentes leucodepletados pre-almacenamiento para todos estos grupos de pacientes, incluyendo aquellos que pueden requerir un trasplante en el futuro (226).
El uso rutinario del monitorización por PCR de CMV en pacientes con trasplante de médula ósea seronegativos (y sus donantes) permite la detección temprana y el tratamiento de la infección por CMV (ya sea adquiridas de forma primaria o relacionadas con la transfusión).
VIH y pacientes inmunodeficientes
La declaración SaBTO concluye que la leucodepleción pre-almacenamiento es suficiente para prevenir la transmisión de CMV en pacientes infectados por el VIH. En pacientes con inmunodeficiencia combinada grave (SCID) que son negativos para el CMV, debe considerarse el uso de productos negativos para CMV.
Transfusiones de granulocitos
Las transfusiones de granulocitos con CMV positivo tienen el potencial de transmitir grandes cantidades de CMV intracelular. La leucorreducción está contraindicada (porque atraparía los granulocitos). Por lo tanto, se deben proporcionar granulocitos CMV seronegativos para los receptores que son CMV seronegativos o cuyo estado frente a este virus es desconocido (226).
10.5.1.5 Uso de plaquetas compatibilizadas para antígenos plaquetarios humanos
Los antígenos plaquetarios humanos (HPA) están formados por polimorfismos de nucleótido sencillo (SNP) en los genes de la glicoproteína plaquetaria. Estas variantes de glicoproteínas pueden conducir a la formación de anticuerpos anti-HPA cuando las personas se exponen a una glicoproteína que no se produce en sus propias plaquetas. Estas exposiciones suelen ser secundarias al embarazo o a la transfusión de plaquetas.
Un gran número de HPA se ha reportado (229). En las poblaciones caucásicas, los aloanticuerpos más comunes se dirigen contra HPA-1a, seguido por anti-HPA-5b (230-231). Otros aloanticuerpos pueden ocurrir con mayor frecuencia en poblaciones no caucásicas (232).
Los HPA han sido implicados en la trombocitopenia aloinmune fetal y neonatal (TFNA), purpura post-transfusión (PTP) y, raramente, refractariedad plaquetaria mediada por inmunidad.
La TFNA es la principal causa de trombocitopenia grave en el feto y el recién nacido y de hemorragia intracraneal (HIC) en los recién nacidos a término (233-234). Suele ser el resultado de la aloinmunización materna contra el antígeno plaquetario paterno. Lo que conduce a la formación de inmunoglobulina clase G (IgG) que pueden cruzar la placenta.
La TFNA no tratada se asocia con una alta tasa de HIC (~25%):
Siendo la mayor parte antes del nacimiento; postnatalmente, el riesgo es mayor en los primeros 8 días (235). Sin embargo, la trombocitopenia puede durar varias semanas.
El rápido diagnóstico y tratamiento de la TFNA es vital debido al alto riesgo de HIC (234-235). Se debe investigar el tipo de HPA de los padres y se deben realizar pruebas de compatibilidad en los casos sospechosos.
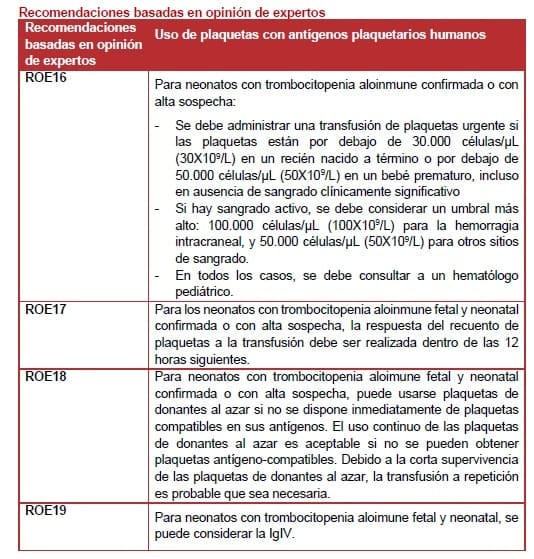
Los umbrales óptimos para la transfusión de plaquetas son inciertos (19). Las pautas del Comité Británico de Estándares en Hematología recomiendan un umbral de plaquetas de 30×109/L (30.000 cel/μL) en neonatos a término (203), y 50×109/L en neonatos prematuros (50.000 cel/μL) (235). Se considera que un umbral más alto es apropiado si hay sangrado activo (50×109/L, o 100×109/L para el sangrado intracraneal).
Las plaquetas antígeno-negativas probablemente sean eficaces en el 95% de los casos (132, 234, 236-237). Si las plaquetas negativas para el antígeno no están disponibles. Deben usarse plaquetas de donantes aleatorios. Las plaquetas maternas ya no son recomendadas porque hay problemas logísticos importantes que retrasan la transfusión (234-235, 238).
(Lea También: Transfusión Fetal)
10.5.1.6 Uso de plaquetas compatibilizadas para antígenos leucocitarios humanos
La compatibilización para el antígeno leucocitario humano (HLA) de las plaquetas debe ser considerada para el tratamiento de la refractariedad plaquetaria. Para fines prácticos, la refractariedad plaquetaria se define por un incremento plaquetario absoluto de menos de 10-20×109/L, una hora después de la transfusión de plaquetas, en dos ocasiones consecutivas.
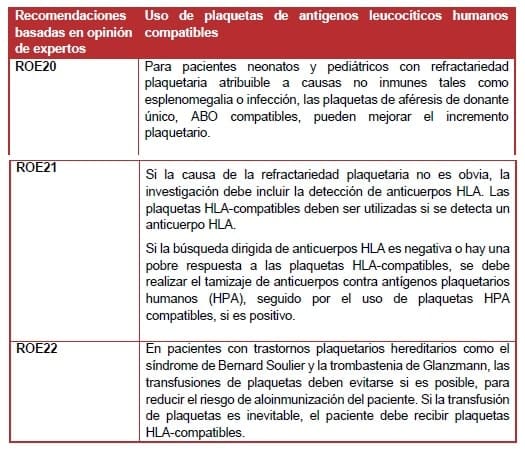
La mayoría de los casos de refractariedad plaquetaria se deben a causas no inmunes tales como esplenomegalia, fiebre, infección, coagulación intravascular diseminada, enfermedad veno-oclusiva y enfermedad de injerto contra huésped. El uso de plaquetas de aféresis frescas de un solo donante (en oposición a un producto combinado –pool o varias unidades de plaquetas provenientes de sangre total), ABO compatibles, puede mejorar el incremento de plaquetas. En estos casos, la práctica habitual es continuar las transfusiones de plaquetas diarias donde está indicada la profilaxis, aunque no se sabe si este enfoque proporciona beneficios en comparación con la retención de la transfusión.
En la minoría de los casos, la refractariedad plaquetaria es atribuible a causas inmunes (239). Desde la introducción de plaquetas leucodepletadas, la incidencia de aloinmunización debida a causas inmunes ha disminuido (240). La refractariedad plaquetaria inmune es más comúnmente atribuible a anticuerpos contra el HLA y menos a menudo a anticuerpos contra HPA.
La investigación inicial de la refractariedad plaquetaria debe incluir la detección de anticuerpos HLA.
Las plaquetas de aféresis ABO-compatibles, deben utilizarse mientras se espera el resultado de la detección de anticuerpos HLA. Donde hay anticuerpos HLA, deben usarse plaquetas HLA-compatibles. Si no se detectan anticuerpos HLA o hay una pobre respuesta a las plaquetas HLA-compatibles y no hay una causa obvia no inmune. Debe hacerse la prueba de los anticuerpos HPA. Si se detectan anticuerpos HPA, deben utilizarse plaquetas HPA compatibles (128).
La recomendación actual de evitar la transfusión si es posible, es para pacientes con trastornos plaquetarios hereditarios (ejemplo: síndrome de Bernard Soulier o la trombastenia de Glanzmann). Para reducir el riesgo de aloimmunización. Si hay una hemorragia significativa que no ha respondido a otros tratamientos. Estos pacientes deben recibir plaquetas HLA compatibles. Debido a la potencial necesidad de transfusiones plaquetarias a repetición y el consecuente aumento en el riesgo de aloinmunización (241-242). Estas recomendaciones pueden ser revisadas en el futuro debido a la reducción de la aloinmunización HLA causada por la leucodepleción universal (132).
10.5.1.7 GR lavados
El lavado de GR antes de la transfusión se lleva a cabo para eliminar sustancias (anticuerpos, proteínas plasmáticas, soluciones aditivas, niveles elevados de electrolitos, otros metabolitos celulares o citoquinas) que pueden ser perjudiciales para algunos pacientes (224).
Las unidades lavadas contienen un 10-20% menos de GR que las unidades originales, pero también están libres del 99% de las proteínas plasmáticas y tienen cantidades reducidas de solución aditiva y potasio extracelular. Otros beneficios potenciales incluyen la reducción de los efectos inmunomoduladores de la transfusión (243-245). En cuanto a los riesgos, los glóbulos rojos pueden ser dañados durante el proceso y, por tanto, más susceptibles a la hemólisis (19).
Los glóbulos rojos lavados pueden ser utilizados, sin embargo, el lavado es agotador en tiempo y recursos, añadiendo 1-2 horas al tiempo de preparación del producto (244). Para pacientes sometidos a cirugía, se puede usar una máquina de rescate celular para lavar los glóbulos rojos si hay personal capacitado y equipo disponible.
La transfusión intrauterina, los GR lavados y empaquetados en un hematocrito de 75-85% se pueden utilizar para reducir el volumen transfundido al feto (245-247).
Los pacientes pediátricos que reciben transfusión de gran volumen, los GR lavados pueden tener ventajas. Pero éstas deben ser sopesadas frente al aumento en el tiempo de preparación (206). Pacientes pediátricos sometidos a cirugía cardíaca. Una revisión sistemática que incluyó tres ensayos pequeños y heterogéneos (dos con células lavadas en el banco de sangre y una utilizando una técnica de rescate celular) que comparabanlos GR lavados con los no lavados, no fue concluyente (51). En pacientes crónicamente transfundidos. Los GR lavados pueden ser considerados para el manejo de reacciones transfusionales graves, incluyendo aquellas debidas a deficiencia de IgA (51, 248-250).
Para la mayoría de las transfusiones de pequeño volumen, el riesgo de hiperpotasemia es extremadamente bajo (231), y la seguridad de las soluciones aditivas utilizadas para los GR está establecida (205). Por lo tanto, no es necesario el lavado rutinario para eliminar el potasio o la solución aditiva (205).
En general, no hay pruebas suficientes para determinar si los GR lavados mejoran los resultados en pacientes fetales, neonatales o pediátricos.