5.2 Análisis de costo-efectividad de diferentes estrategias de tamización para cáncer de cuello uterino en Colombia.
5.2.1 Introducción
El cáncer de cuello uterino (CCU) también conocido como cérvix uterino, se origina en las células que revisten el cuello del útero. Los dos tipos principales de células que cubren dicha área son las células escamosas y las células glandulares, ubicadas en un punto llamado zona de transformación debido al cambio que se produce a razón del envejecimiento o del hecho de haber dado a luz. La mayoría de los cánceres de cuello uterino se origina en las células de la zona de transformación (3) manifestándose inicialmente a través de lesiones pre cancerosas de lenta y progresiva evolución, que pueden ser precedidos por etapas de displasia leve, moderada y severa (4).
El CCU ha sido reconocido ampliamente como una de las enfermedades de mayor carga en todo el mundo debido a las altas cifras de incidencia y mortalidad que presenta. Es el tercer tipo de cáncer más frecuente entre las mujeres a nivel global, ocupa uno de los lugares de mayor importancia dentro de las causas de muerte para dicha población, (5) y es la mayor causa de años de vida perdidos (por cáncer) entre las mujeres de América Latina y el Caribe.(6)
En Colombia, según lo reportado por el Instituto Nacional de cancerología (INC) para el periodo 2002-2006, el cáncer de cuello uterino se ubicó como la primera causa de muerte y como el segundo tipo de cáncer más incidente dentro de la población de mujeres adultas del país, con una tasa cruda anual de incidencia de 26.1 por cada 100000 habitantes, antecedido únicamente por el cáncer de mama.(7)
El principal factor de riesgo asociado a la ocurrencia de CCU
Se atribuye a la infección por el Virus del Papiloma Humano (VPH) que constituye la infección de transmisión sexual (ITS) más común entre las mujeres, mostrando una mayor prevalencia en las mujeres jóvenes, y en las mayores de 65 años de edad. (8) Aunque los VPH, etiológicamente se relacionan en mayor medida con la ocurrencia de casos de cáncer cervico-uterino, también se les atribuye el desarrollo de neoplasias extra-cervicales, sin embargo, su incidencia en este grupo es de solo el 12% del total de los cánceres asociados a este virus.(9) Razón por la cual, el CCU representa el mayor foco de atención y constituye uno de los escenarios de mayor cubrimiento por parte de los diferentes sistemas de salud.
El diseño y ejecución de programas o estrategias de prevención secundaria y tratamiento implementadas durante las últimas 3 décadas, han logrado disminuir las tasas de incidencia y mortalidad de esta enfermedad en países desarrollados. Sin embargo, la situación en países en vía de desarrollo difiere bastante, dado que las tasas que describen su comportamiento se mantienen o incluso muestran un aumento en el número de casos nuevos diagnosticados.(10)
En el año de 1991 se implementó en el país el programa de detección temprana de CCU
A pesar de haber contribuido a la reducción de la mortalidad por esta causa en los últimos 7 años, los resultados esperados no corresponden con las cifras reportadas en la actualidad (11). La supervivencia del CCU en países como Colombia, difiere considerablemente de lo logrado en países desarrollados, lo cual se justifica entre otros factores, a la ineficacia de los programas de tamización que consecuentemente se atribuye a los altos costos operativos que conlleva su implementación, al recurso humano necesario para el manejo de la enfermedad, y al tratamiento y seguimiento de las mujeres con anormalidades citológicas que de no ser efectivo conduce a un diagnóstico tardío de la enfermedad (12).
5.2.2 Justificación de la evaluación
El CCU es una enfermedad de progresión lenta y generalmente silenciosa, razón por la cual, en muchas ocasiones el establecimiento del diagnóstico se realiza en etapas ya avanzadas de la enfermedad. Sin embargo, en los casos en que su detección se lleva a cabo de forma temprana, la probabilidad de controlar, detener y/o curar la enfermedad, adquiere mayores y mejores oportunidades.
En países desarrollados, los programas de tamización con citología, han conducido a una reducción significativa en la incidencia de cáncer cervical, resultado que difiere respecto a países en desarrollo como Colombia, donde los programas de tamización basados en citología han sido menos exitosos.
El advenimiento de nuevas estrategias en la prevención secundaria del cáncer de cuello uterino, entre las que se encuentra la tamización con pruebas moleculares de ADN para VPH y la LBC, entre otras, parecen ofrecer resultados prometedores, sin embargo, los costos asociados a dichas tecnologías suelen ser bastante altos (13), y dada la limitada disponibilidad de recursos en países como el nuestro, la estimación de la efectividad y de los costos de las diferentes alternativas para la prevención secundaria de esta enfermedad, constituye para los tomadores de decisiones una herramienta fundamental en la tarea de establecer cuál de las diferentes estrategias ofrece la mejor relación entre ambos indicadores.
Las condiciones particulares de cada localización geográfica
Hacen que los resultados de estudios económicos desarrollados en otros países encaminados a establecer la razón de costo-efectividad, costo-beneficio o costo-utilidad para cada una de las tecnologías emergentes no puedan ser generalizadas o extrapolables al contexto local, razón por la cual, este tipo de investigaciones deben ser desarrollados para cada contexto usando datos locales y considerando las características particulares de cada caso, de manera que los resultados puedan ser lo más aproximados a la realidad del medio en que son evaluadas.
En Colombia, actualmente se cuenta con el desarrollo y los resultados de una evaluación económica llevada a cabo por el autor de la presente investigación, en la que se evaluó la costo-efectividad de la citología convencional Vs las pruebas moleculares de DNA para VPH en Colombia, sin embargo, este estudio no incluye estrategias como la LBS o las la combinación de pruebas moleculares con triage que pudiesen representar mayores beneficios en términos de costo-efectividad, razón por la cual, el presente estudio actualiza la investigación previa, incluyendo a estas nuevas estrategias de tamización.
5.2.3 Descripción de las tecnologías de interés
5.2.3.1 Citología convencional
La citología convencional (CC) también conocida como prueba de Papanicolaou en honor a de George N. Papanicolaou quien descubrió que las células de cáncer de cuello uterino pueden ser observados en los frotis vaginales, trata de un método de prevención secundaria, que tiene como principal objetivo, identificar las lesiones precancerosas que necesitan seguimiento y / o tratamiento (14).
Es una prueba microscópica de células del cuello uterino obtenidas mediante raspado. En la prueba se toma una muestra de células del exterior y del canal del cuello uterino raspando suavemente con una espátula de madera o plástico. Una vez se extrae la muestra, las células se extienden sobre una laminilla de vidrio y se rocían con un fijador o se introducen en una botella que contiene un conservante para enviarlas luego al laboratorio. Su análisis permite la detección de cambios celulares que sugieran trasformaciones malignas (15).
El uso de la CC ha demostrado efectividad en la reducción de las tasas de muerte asociadas con carcinoma de cuello uterino invasivo, sin embargo, la sensibilidad de la prueba se ve altamente afectada durante la recolección de la muestra, por la presencia de células de la sangre, mucosas y zonas de superposición de las células epiteliales que pueden interferir con el diagnóstico correcto, así como el retraso en la fijación de los frotis después de tomar la muestra que puede llevar a la deformación de la morfología celular. (16).
5.2.3.2 Pruebas moleculares de ADN-VPH
Gracias a la difusión de estudios realizados por el científico Harald Zur Hausen y la doctora Nubia Muñoz, que pusieron en evidencia el estrecho vínculo entre el cáncer de cuello uterino y la infección de transmisión sexual por VPH, la ciencia ha podido establecer y desarrollar pruebas moleculares de ADN- VPH útiles en la prevención del CCU.
El uso de este tipo de pruebas, facilita la identificación de la infección por el virus y la tipificación de las infecciones en los genotipos virales 16 y 18 responsables de casi el 70% de los cánceres de cuello uterino (17) y han sido ampliamente adoptadas dentro de las estrategias de triage para pacientes con células escamosas atípicas de significado indeterminado (ASCUS), siendo actualmente usadas también en el tamizaje primario junto con las pruebas de citología cervical en pacientes mayores de 30 años (18).
Las pruebas se basan en la separación de las dos cadenas de ácidos nucleicos, en un medio líquido determinado adicionando posteriormente un ADN viral ya conocido e igualmente separado, con el propósito de buscar la hibridización o unión de cadenas homólogas (15).
Las pruebas de mayor uso para la identificación de la infección por VPH, se llevan a cabo mediante ensayos de PCR (polymerase chain reaction) o pruebas de captura de híbridos (Hybrid Capture, HC)
La PCR se reconoce por ser una técnica muy específica y sensible, capaz de detectar entre 10 y 200 copias de genoma viral por muestra. Esta técnica identifica el ADN diana a través de la utilización de oligonucleótidos iniciadores que complementan de forma específica con las regiones flanqueantes del ADN que será amplificado mediante ciclos sucesivos de desnaturalización, anclaje y extensión, hasta obtener una señal visible en geles de agarosa teñidos con bromuro de etidio (19).
Por su parte la prueba para la detección del VPH, por captura de híbridos II, analiza las presencias de ADN viral a través del uso de partículas de ADN producidas en el laboratorio (sondas), complementarias con las bases nitrogenadas del ADN viral (híbridos). La prueba permite la detección de 13 tipos de VPH de alto riesgo por medio de la utilización de un cóctel de sondas para estos tipos virales (16,18,31,33,35,39,45,51,52,56,58,59 y 68) (20)
5.2.3.3 Citología en base líquida
La citología en base líquida (LCB por su sigla en inglés) es un método introducido en el año 1996 que tiene como propósito la preparación de muestras celulares de mayor y mejor calidad, de manera que sea posible reducir el porcentaje de muestras inadecuadas, mejorando así, la sensibilidad y especificidad en la detección de anormalidades celulares. Esta técnica se caracteriza por ofrecer muestras de alta calidad y mayor preservación del material celular libre de elementos como sangre y células inflamatorias que inciden en la lectura del frotis, lo cual aumenta la exactitud diagnóstica y reduce los resultados citológicos falsos negativos, además de ofrecer la posibilidad de utilizar el material residual para pruebas complementarias al estudio morfológico (21).
Las muestras se recogen de la misma forma que se hace en la citología convencional, la diferencia radica en el uso de un dispositivo similar a un cepillo en vez del uso de la espátula. La cabeza del dispositivo se lava en un frasco de líquido conservante de modo que la mayor parte o la totalidad de las células se conservan. Posteriormente, la muestra se lleva al laboratorio donde se mezcla para dispersar las células, retirando restos celulares que puedan alterar los resultados. Finalmente una capa fina de células del cuello uterino se deposita sobre un portaobjetos de microscopio para su posterior análisis (22) .
5.2.4 Revisión sistemática de efectividad y seguridad
5.2.4.1 Pregunta de evaluación
¿Cuál es la efectividad de los diferentes esquema de tamización (citología convencional, pruebas moleculares ADN-VPH, Citología en base líquida) para la detección de lesiones pre neoplásicas y CCU en mujeres que hayan iniciado actividad sexual?

Los datos clínicos correspondientes a la efectividad y seguridad de las pruebas evaluadas incluidas en la adaptación del modelo actual, fueron en su mayoría, derivadas del estudio original desarrollado por O, Gamboa et al. (23), en el que se evaluó la costo-efectividad de la citología convencional vs las pruebas moleculares de DNA para VPH en Colombia y para el cuál fue desarrollada en su momento una revisión sistemática completa.
Con el propósito de actualizar la información relacionada con los valores operativos de las pruebas incluidas, se realizó una búsqueda en la base de datos Pubmed acerca de evidencia científica de la que se extrajo la información pertinente.
5.2.4.2 Criterios de elegibilidad de la evidencia
5.2.4.2.1 Criterios de inclusión
La unidad de análisis de dicha revisión fueron artículos publicados en revistas científicas:
- Revisión sistemática con meta-análisis
- Publicados en idioma inglés, español.
5.2.4.2.2 Criterios de exclusión
No se incluyeron revisiones no sistemáticas de la literatura, resúmenes o cartas al editor.
5.2.4.3 Estrategia de búsqueda
La estrategia de búsqueda empleada se presenta a continuación.
Search ((cytology) OR (pap smear) OR (HPV DNA testing) OR (Liquid-based cytology) OR (Human Papillomavirus Testing)) AND (CIN2+ OR CIN3+) Filters: Meta-Analysis; Systematic Reviews
5.2.4.4 Tamización de referencias y selección de estudios
Con base en los resultados de las estrategias de búsqueda diseñada, se conformó una base de datos de posibles documentos que cumplieran con los criterios antes mencionados. Los documentos seleccionados fueron descargados en texto completo, a los cuales se les realizó una tamización final.
5.2.4.5 Evaluación de la calidad de la evidencia
Las revisiones sistemáticas con meta-análisis fueron evaluadas con herramienta AMSTAR de manera que se pudiese tener en cuenta dicha información en el análisis de los resultados obtenidos en la presente evaluación.
5.2.4.6 Extracción de datos y síntesis de la evidencia
Dos revisores (OAG , AMG) realizaron la extracción de los datos de manera independiente usando una herramienta diseñada para este propósito. Cualquier diferencia fue resuelta por consenso entre los revisores.
5.2.4.7 Resultados
5.2.5.7.1 Búsqueda de evidencia
El flujograma de búsqueda en el que se describen el número de estudios potencialmente relevantes arrojados por la búsqueda y los filtros aplicados para la obtención de los estudios definitivos que fueron analizados en texto completo.
5.2.5.7.2 Tamización de referencias y selección de estudios
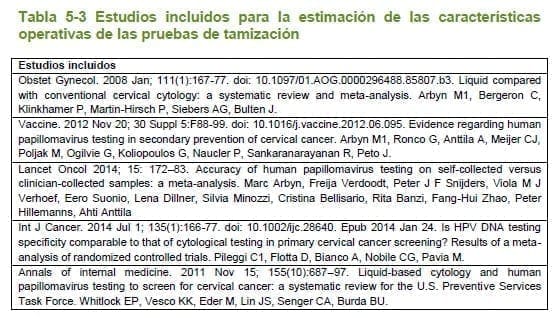
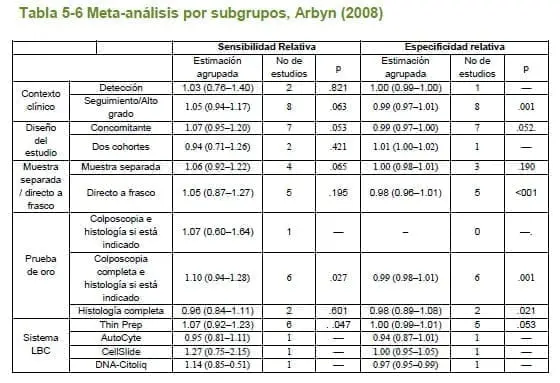
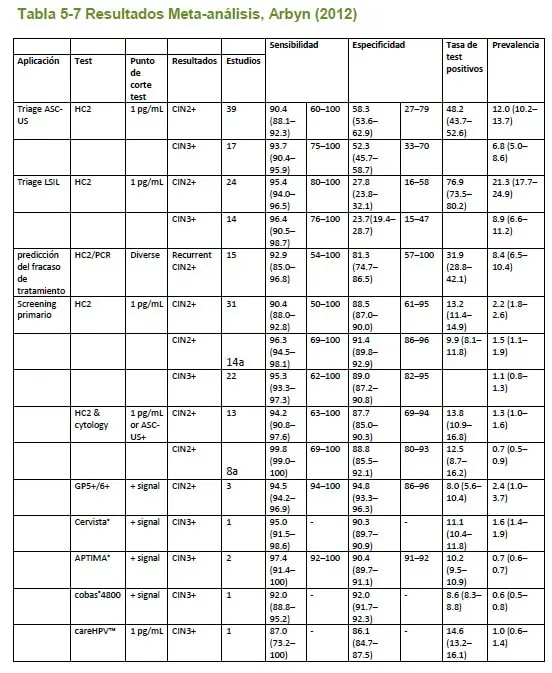
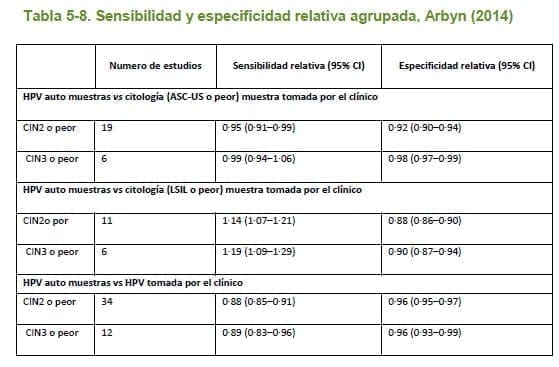
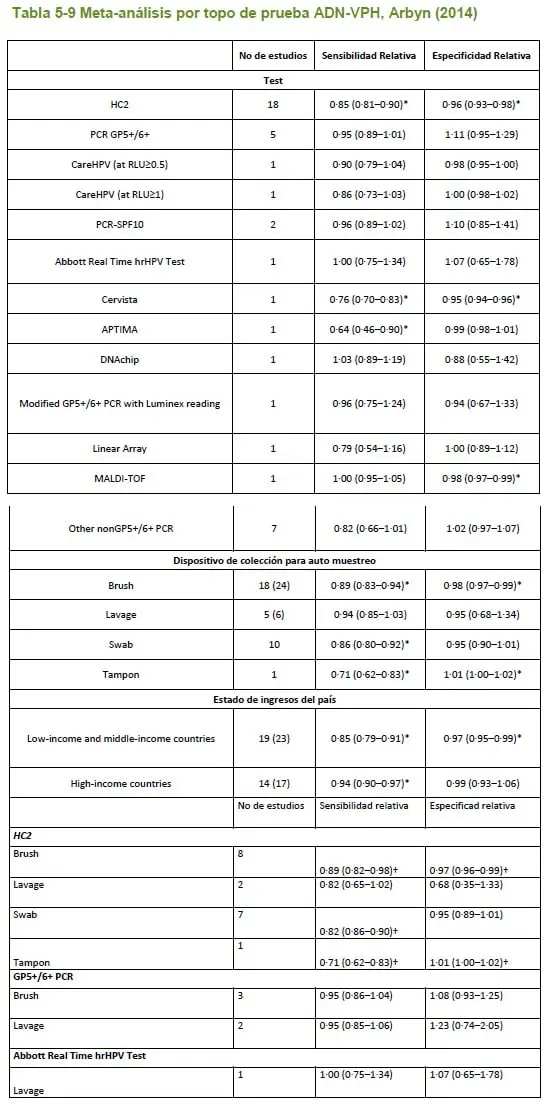
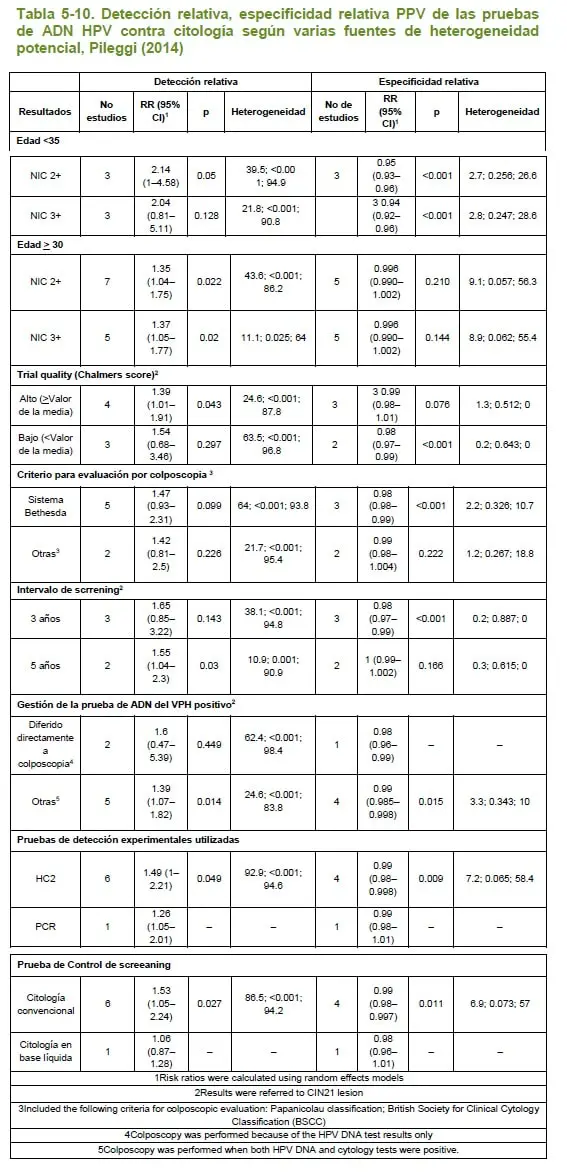
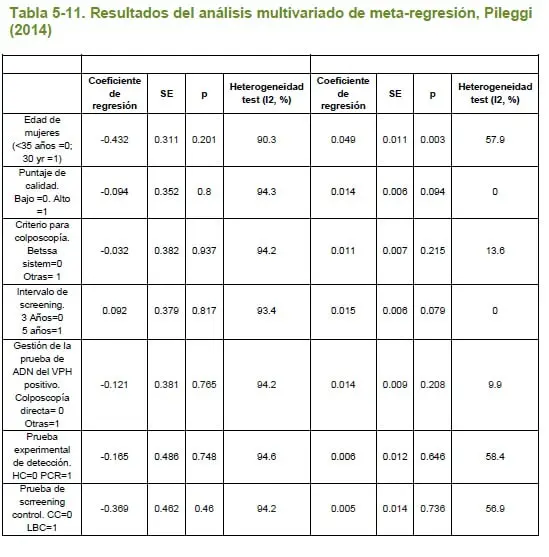
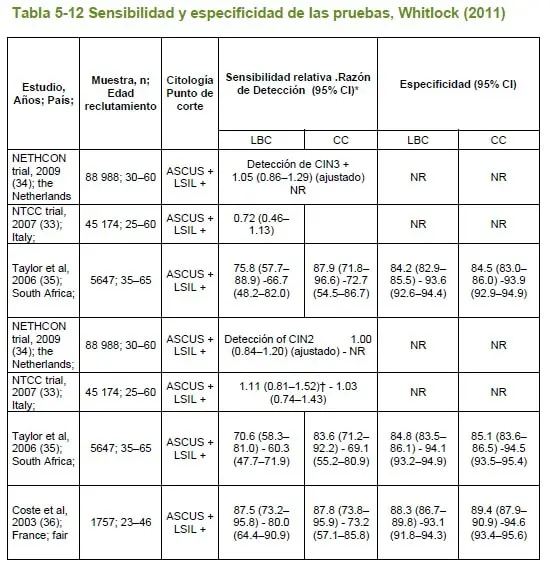
Luego de la lectura detallada de los documentos arrojados por la búsqueda, se tuvieron en cuenta los estudios reportados en la tabla 5.3, por ser considerados los de mayor actualidad.
5.2.5.7.3 Calidad de la evidencia
Con el propósito de valorar la calidad metodológica de las revisiones sistemáticas incluidas como definitivas en la búsqueda, se aplicó la herramienta AMSTAR mediante la que se estableció una calidad ALTA para el 80% (3 estudios) de las revisiones y de calidad media para el otro 20% (1 estudios).
5.2.5.7.4 Descripción de los estudios incluidos
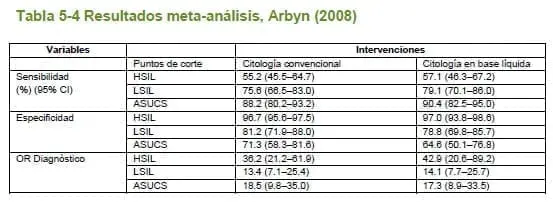
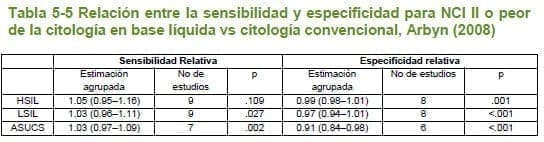
A continuación se describen los hallazgos más importantes presentados en cada uno de los estudios incluidos.
5.2.5 Revisión sistemática de estudios de costoefectividad
5.2.5.1 Pregunta de evaluación
¿Cuál es la costo-efectividad de los diferentes esquema de tamización (citología convencional, pruebas moleculares ADN-VPH, Citología en base líquida) para la detección de lesiones precancerosas y CCU en mujeres que hayan iniciado actividad sexual?

5.2.5.2 Metodología
Teniendo en cuenta que actualmente se cuenta con una evaluación económica desarrollada previamente en el contexto local por Gamboa, et al. (23) y que sirvió de base para el desarrollo del presente análisis, no se llevó a cabo una revisión sistemática de evaluaciones económicas dado que el método empleado y el modelo usado para responder nuestra pregunta de investigación obedece a una adaptación de la evaluación mencionada.
5.2.6 Evaluación económica
Como parte fundamental en el desarrollo de cualquier evaluación de tecnología sanitaria, es necesario definir de manera minuciosa y según las particularidades de la tecnología en evaluación, cuáles serán los aspectos y características de la metodología a desarrollar. A continuación se presenta la enmarcación realizada para la evaluación económica en mención.
5.2.6.1 problema de decisión
El desarrollo de la evaluación económica está dirigido a ofrecer un sustento científico respecto a cuál de las estrategias de tamización para mujeres que han iniciado actividad sexual, es la más indicada en términos de costo-efectividad.
5.2.6.2 Población objetivo
Dado que la principal causa asociada al CCU es la infección por VPH, se determinó como población objeto de la presente evaluación, a todas las mujeres que han iniciado actividad sexual y por tanto están en mayor riesgo de desarrollar la enfermedad.
5.2.6.3 Intervencion
-
Pruebas moleculares ADN-VPH (PCR o Captura de híbridos) en los siguiente esquemas:
o Primero, Prueba ADN-VPH (Tomada por un profesional de salud) cada 5 años, iniciando la tamización a los 30 años de edad.
o Segundo, Prueba ADN-VPH (Tomada por un profesional de salud) triage con citología en base líquida cada 5 años, iniciando la tamización a los 25 años de edad.
o Tercero, Prueba ADN-VPH (Tomada por un profesional de salud) y triage con citología convencional cada 5 años, iniciando la tamización a los 25 años de edad.o Citología en base líquida cada 3 años desde los 25 años continuando con prueba ADN-VPH (Tomada por un profesional de salud) y triage con citología en base líquida cada 5 años, a partir de los 30 años.
o Cuarto, Citología convencional cada 3 años desde los 25 años continuando con prueba ADN-VPH (Tomada por un profesional de salud) y triage con citología convencional cada 5 años, a partir de los 30 años.
o Quinto, Prueba ADN-VPH (Auto toma) cada 3 años, iniciando la tamización a los 30 años de edad.
o Sexto, Prueba ADN-VPH (Auto toma) y triage con citología en base líquida cada 3 años, iniciando la tamización a los 25 años de edad.
o Séptimo, Prueba ADN-VPH (Auto toma) y triage con citología convencional cada 3 años, iniciando la tamización a los 25 años de edad.
o Citología en base líquida cada 3 años desde los 25 años continuando con prueba ADN-VPH (Auto toma) y triage con citología en base líquida cada 3 años, a partir de los 30 años.
o Octavo, Citología convencional cada 3 años desde los 25 años continuando con prueba ADN-VPH (Auto toma) y triage con citología convencional cada 3 años, a partir de los 30 años. -
Citología en base líquida bajo los siguientes esquemas:
o 2 citologías negativas en años consecutivos, continuando cada 3 años a partir de los 25 años.
o 3 citologías negativas en años consecutivos continuando cada 3 años a partir de los 25 años. -
Citología convencional bajo el siguiente esquema:
o 3 citologías negativas en años consecutivos continuando cada 3 años a partir de los 25 años.
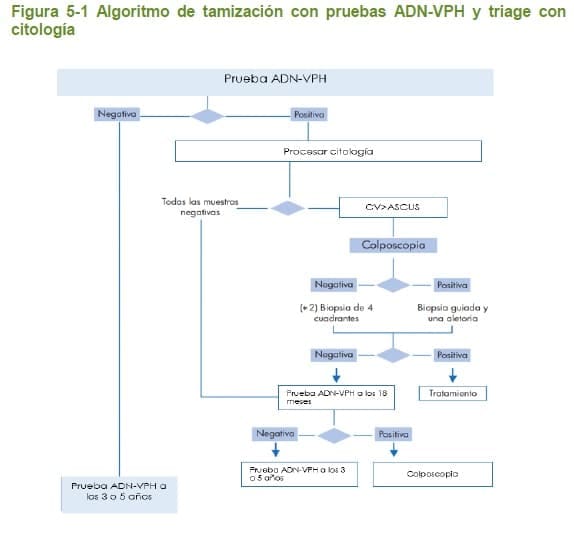
En la figura 5.1 se muestra el algoritmo de la tamización con las pruebas ADN-VPH en las cuales se realiza triage con citología.
5.2.6.4 Comparadores
- Citología convencional bajo el siguiente esquema:
o 2 citologías negativas en años consecutivos, continuando cada 3 años a partir de los 25 años. - No tamización.
5.2.6.5 DesenlaceS
Los años de vida ganados (AVG) asociados a cada estrategia de tamización fueron usados como medida de resultado en salud.
Los años de vida ajustados por calidad (AVAC) no fueron usados como desenlace, dado que en el contexto local, no se cuenta con la valoración de los pesos de estados de salud para CCU necesarios para el cálculo de dicha medida.
5.2.6.6 Horizonte temporal
Teniendo en cuenta que el objetivo de la evaluación incluye valorar los costos y resultados en salud de las tecnologías evaluadas, se requiere un horizonte amplio (expectativa de vida de las mujeres colombianas (76 años)) que permita estimar desenlaces finales (mortalidad) importantes para los pacientes con CCU.
5.2.6.7 Perspectiva
Siguiendo las recomendaciones de la guía metodológica y considerando que el CCU supone un costo significativo para el sistema de salud, la perspectiva utilizada fue la del tercer pagador.
5.2.6.8 Tasa de descuento
Los resultados en salud y los costos fueron descontados a una tasa anual del 3%, realizando análisis de sensibilidad para tasas del 0%, 3,5%, 7% y 12%.
5.2.6.9 Costos
La perspectiva usada fue la del tercero pagador, solo se incluyeron costos directos expresados en pesos colombianos.
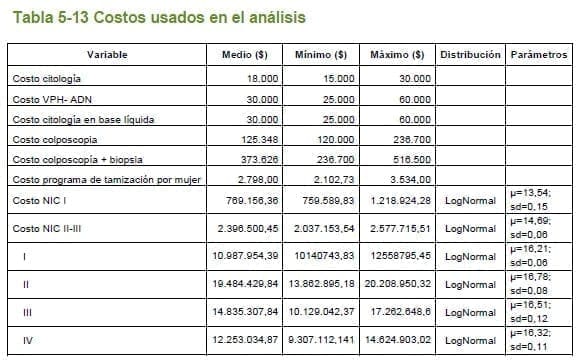
El Instituto Nacional de Cancerología, realizó una estimación de los costos del manejo de las lesiones pre neoplásicas y CCU en el 2012, información que fue usada para el presente análisis.
La metodología usada en la estimación se muestra a continuación:
Se estimaron los costos de las lesiones pre-neoplásicas y del cáncer de cuello uterino para cada uno de los estadios de la enfermedad. Los costos asociados al tratamiento incluyeron, el personal asistencial, los tratamientos médicos y el tratamiento de las complicaciones. Para el cálculo de éstos se utilizó la metodología de casos tipo en la cual se identificaron, cuantificaron y valoraron los eventos generadores de costos como se explica a continuación.
5.2.6.9.1 Identificación
En la identificación de los eventos generadores de costos se revisaron protocolos de manejo del Instituto Nacional de Cancerología (28) y las guías del National Comprehensive Cancer Network NCCN. (29) Los eventos generadores de costos identificados, se incluyeron en formatos de recolección de información validados y diligenciados por los expertos clínicos de la Guía (ginecología oncológica, oncología y radioterapia). En los formatos se incluyó información sobre: diagnóstico inicial, diagnóstico de extensión, tratamiento quirúrgico, tratamiento de quimioterapia, tratamiento de radioterapia y seguimiento.
5.2.6.9.2 Cuantificación
Para la estimación de la cantidad y la frecuencia de uso de cada recurso identificado, se utilizó la opinión de expertos. El panel de expertos estuvo conformado por cuatro ginecólogos oncólogos, dos oncólogos clínicos y tres radioterapeutas.
5.2.6.9.3 Valoración monetaria
La valoración monetaria se realizó usando los manuales ISS + 30% 2001 y SOAT(30) (31) . La información reportada por el SISMED (32) y por la resolución 4316 de 2011 fue usada para la valoración de los medicamentos. La información reportada por el SISMED fue actualizada a 2012 usando el índice de precios al consumidor (IPC), informado por el DANE. En caso de no encontrarse información para algún procedimiento o medicamento en las fuentes anteriormente mencionadas, se usó la información del Instituto Nacional de Cancerología.
Los procedimientos identificados fueron expresados en unidades de valor relativo (UVR) para el manual ISS y el número de salarios mínimos legales diarios para el manual SOAT. El valor de la UVR usado fue el determinado en el manual ISS, teniendo en cuenta las variaciones de éste de acuerdo a las características de los procedimientos. Para el caso del manual SOAT, fue usado el valor del salario mínimo legal vigente para Colombia en el 2012 ($18.890).
En la estimación de los costos de los medicamentos, se realizaron los siguientes procedimientos: 1) se extrajo la información de los medicamentos que no tenían topes de precio informados en la resolución 4316 de 2011; 2) los medicamentos fueron codificados usando la clasificación Anatómica, Terapéutica, Química (ATC); 3) dado que un mismo principio activo puede tener varias presentaciones y ser producido por diferentes compañías farmacéuticas, se estimó un costo ponderado por dosis del medicamento, usando como ponderador las unidades reportadas; 4) se estimó el costo por miligramo del medicamento.
El costo ponderado por dosis se calculó de acuerdo a la siguiente fórmula:
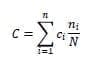
Donde
C= costo por dosis ponderado
n = número de presentaciones del medicamento (la presentación quedo definida por los miligramos por tableta, vial, etc. y la marca, por lo tanto, una misma marca podía tener más de una presentación)
ci= es el costo por dosis de la i-ésima presentación del medicamento, con i = 1, 2,…,n
ni= número de unidades reportadas para i-ésima presentación del medicamento, con i = 1, 2,…,n
N= total de unidades reportadas para el medicamento
Se estimaron los costos totales para las lesiones pre neoplásicas y para cada estadio del cáncer de cuello uterino como se muestra a continuación:
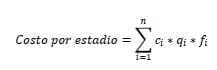
Donde
n = número de procedimientos (diagnóstico o terapéuticos) o medicamentos
ci= es el costo del i-ésimo procedimiento o medicamento, con i = 1, 2,…,n
qi= es la cantidad del i-ésimo procedimiento o medicamento, con i = 1, 2,…,n
fi= es la frecuencia del i-ésimo procedimiento o medicamento, con i = 1, 2,…,n
En los medicamentos el precio medio corresponde a la información de la columna precios del canal institucional, el precio mínimo y máximo corresponde a las columnas mínimo y máximo del mismo canal. Los medicamentos con precio tope este fue usado como máximo.
En el caso de los procedimientos el precio medio corresponde a la información del manual ISS 2001 + 30%. El mínimo y máximo corresponde a la información del manual ISS 2001 sin ajuste y al manual SOAT respectivamente.
5.2.6.10 Modelo matemático
Para el desarrollo de la presente evaluación, se adaptó el modelo de Markov publicado en el 2008 por Gamboa O, et al (23). Un modelo de Markov, que simula la historia natural de las neoplasias de cuello uterino fue adaptado y a partir de éste se construyeron quince modelos que incluyeron las estrategias de tamización en evaluación.
El modelo simula la historia natural de la infección por VPH, se inicia con una cohorte de mujeres (12 años) sin infección por VPH, las cuales se pueden infectar por VPH de alto o bajo riesgo de acuerdo a la incidencia por edad, una vez adquieren la infección está pueden resolver de manera espontánea o progresar a lesión (NIC) de bajo o alto grado. En el modelo solo las infecciones por VPH de alto riesgo pueden progresar a lesiones de alto grado (NIC II-III) y a partir de estas progresar a cáncer invasor. La estructura del modelo usado se muestra en la figura 5.2.
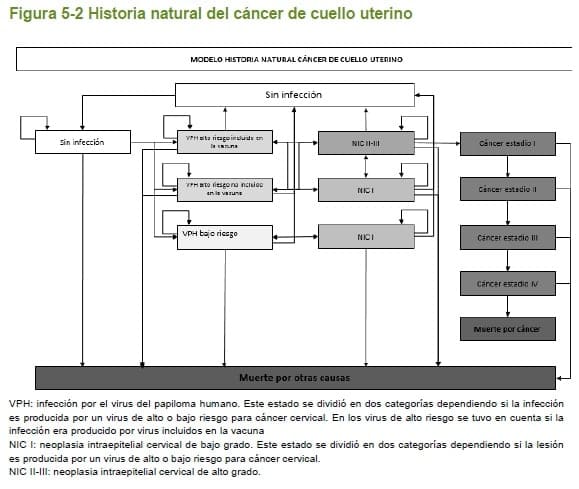
5.2.6.10.1 Supuestos del modelo
- Se inicia con un grupo de adolescentes de 12 años sin infección por el virus del papiloma humano (VPH).
- Todos los casos de cáncer de cuello uterino sin diferenciación del tipo histológico se desarrollan a partir de infecciones por VPH de alto riesgo. Se asumió que las infecciones por VPH de bajo riesgo no progresan a cáncer cervical (33,34).
- Probabilidades de infección por VPH dependen de la edad de la mujer, al igual que las probabilidades de regresión o progresión de las infecciones que también dependen del tipo de VPH (alto o bajo riesgo) (35,36).
- Las probabilidades de regresión de las lesiones cervicales intraepiteliales de bajo y alto grado (LSIL y HSIL respectivamente) dependen de la edad de la mujer y del tipo de VPH que las produjo (37).
- Las probabilidades de progresión de las lesiones de alto grado a cáncer invasor dependen de la edad de la mujer y del tipo de virus de alto riesgo asociado a la lesión(37)).
- Una vez se alcance el estado de cáncer invasor no hay regresión a estados previos de la enfermedad. Solo existe la posibilidad de permanecer en ese estado, progresar al siguiente estado o morir por cáncer u otras causas.
- Cinco años después del tratamiento para el CCU las probabilidades de morir son iguales a las de la población general (38).
- Se definió cobertura como la probabilidad de realizarse la prueba de tamización en el último año.
-
Se definió seguimiento como la probabilidad de que una mujer asista a las consultas de diagnóstico y tratamiento después de un resultado positivo en la prueba de tamización.
- Después de un resultado positivo en la prueba de tamización y de la intervención subsiguiente, la mujer vuelve a iniciar el esquema de tamización que se esté modelando.
- Se contemplaron los costos de implementación de los programas de tamización para las diferentes estrategias.
- La cobertura de la tamización usada en el análisis fue de 72,6 % (60% – 80%), de acuerdo a lo informado en la Encuesta Nacional de Demografía y Salud de 2010 para Colombia (39).
- Se asumió un porcentaje de seguimiento del 65,8% (58% – 70,6%) en las mujeres con resultados positivos a las pruebas de tamización.
5.2.6.10.2 Datos incluidos en el modelo
Los datos de la historia natural se extrajeron de varias fuentes incluyendo la cohorte bogotana de VPH, trabajos locales previos y revisiones sistemáticas de la historia natural del cáncer cervical los cuales fueron publicados por Gamboa O et al (23).
Las características operativas de las pruebas de tamización se extrajeron de revisiones sistemáticas de la literatura. Los años de vida ganados fueron usados como medida de efectividad de las diferentes estrategias de tamización. La mortalidad asociada a cada estrategia de tamización es un resultado del modelo y no un dato de entrada, por lo tanto no fue asumida a priori una reducción específica de mortalidad.
Las probabilidades de morir por otras causas se calcularon de acuerdo a la edad de la mujer, con datos oficiales de mortalidad para el año 2008 en Colombia (40).
Para el cálculo de las probabilidades de transición se siguieron las recomendaciones de Miller y et al (41) y se definieron rangos para los análisis de sensibilidad.
En la tabla 5.14, se muestran los datos de sensibilidad y especificidad usados en el modelo
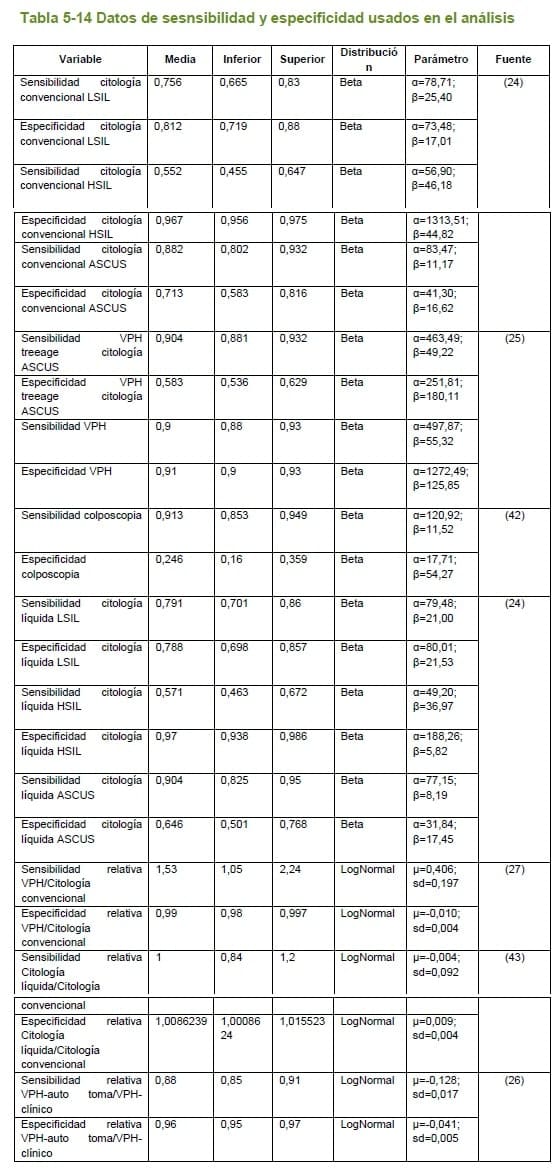
5.2.6.11 Resultados
Se calcularon razones de costo-efectividad incremental (RCEI) definidas estas como el cociente entre la diferencia en costos y la diferencia en resultados de las alternativas en evaluación. Realizaron análisis de sensibilidad sobre las características operativas de las pruebas de tamización, los costos de las pruebas tamización, de los procedimientos diagnósticos y del tratamiento. Se realizaron análisis de sensibilidad probabilísticos y se construyeron curvas de aceptabilidad.
Como umbral fue usado el producto interno bruto PIB per cápita, de acuerdo a lo recomendado por la OMS y el IETS para este tipo de estudios, que para Colombia en el 2013 fue de $15.008.793
Se consideró que una alternativa era muy costo-efectiva si el costo por año de vida adicional ganado era menor del PIB, costo-efectiva si estaba entre 2 a 3 veces el PIB y no costo-efectiva si era mayor a 3 veces el PIB (44).
5.2.6.11.1 Resultados del caso base
En la figura 5.3, se muestra la frontera eficiente para las diferentes estrategias de tamización evaluadas, en donde se observa que solo cuatro estrategias quedan sobre ésta. En la tabla 5.14 se muestran las RCEI para las estrategias en mención, encontrando que la tamización con prueba ADN-VPH y triage con citología convencional cada 5 años sería muy costo-efectiva para el país, las tres estrategias de tamización restantes serían costo-efectivas tomando como umbral tres veces el PIB per cápita.
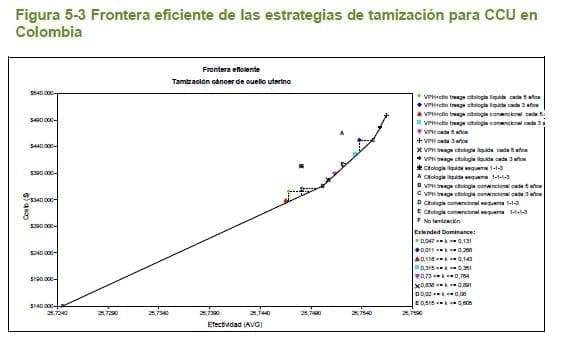
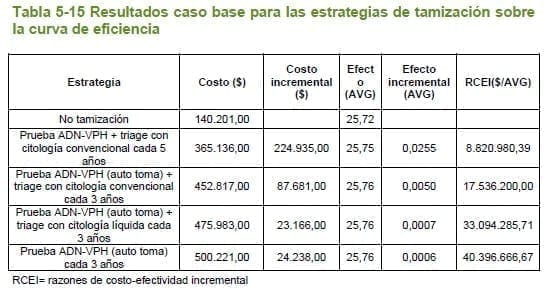
5.2.6.11.2 Análisis de sensibilidad determinÍstico
En la figura 5.4, se muestran los análisis de sensibilidad de una vía para diferentes variables evaluadas en donde se observa que la estrategia con prueba ADN-VPH y triage con citología cada 5 años deja de ser muy costo-efectiva, si el precio de la prueba es de $60.000 o cuando la sensibilidad de la citología de triage disminuye o cuando la sensibilidad de la citología convencional de tamización se aproxima a la sensibilidad de la prueba ADN-VPH, en estos escenarios la estrategia es dominada (más costosa y menos efectiva) por las otras alternativas evaluadas. Es importante mencionar que esta estrategia deja de ser costo-efectiva si el costo de la prueba de ADN-VPH es superior a $39.000.
Los resultados fueron muy sensibles a la tasa de descuento, dejando de ser costo-efectiva la estrategia de prueba ADN-VPH y triage con citología convencional cada 5 años cuando el descuento fue del 12%. En este escenario ninguna estrategia de tamización sería costo-efectiva para el país.
Llama la atención que en un escenario con baja cobertura y seguimiento de las mujeres con resultados positivos a las pruebas de tamización, la estrategia de prueba de ADN-VPH cada 5 años sin triage con citología sería muy costo-efectiva para el país. Esta estrategia también es muy costo-efectiva si la sensibilidad de la citología de triage disminuye (umbral LSIL o umbral HSIL).
Las estrategias de tamización con citología convencional serían muy costo-efectivas
Si el costo de la prueba de VPH es mayor a $60.000 (esquema 1-1-3 y 1-1-1-3), el costo de la citología es de $15.000 (esquema 1-1-1-3) y si la sensibilidad de la citología se aproxima a la de la prueba ADN-VPH (esquema 1-1-3 y 1-1-1-3) y costo-efectivas si la cobertura y el seguimiento es alto (esquema 1-1-1-3). Para el resto de escenarios serían estrategias dominadas.
Es importante mencionar, que las estrategias de inicio con citología a los 25 años, continuando con prueba de ADN-VPH y triage con citología desde los 30 años, son dominadas (más costosas y menos efectivas) que las estrategias de inicio con prueba ADN-VPH y triage desde los 25 años.
Finalmente las estrategias de prueba ADN-VPH (auto toma) cada tres años con y sin triage con citología (convencional o líquida) fueron costo-efectivas en la mayoría de escenarios evaluados si se toma como umbral tres veces en PIB per cápita de Colombia.
5.2.6.11.3 Análisis de senSibilidad probabilístico
En la figura 5.5 se muestra la curva y frontera de aceptabilidad de las estrategias de tamización para CCU evaluadas donde se observa que para ninguno de los umbrales de disponibilidad a pagar por AVG adicional ganado, las estrategias de tamización con citología convencional o en base líquida serian costo-efectivas para Colombia.
La elección dependerá de la disponibilidad a pagar, si se está entre diez y veinte millones la estrategia a seleccionar sería prueba de ADN-VPH y triage con citología convencional cada 5 años, entre veinte y cuarenta millones prueba ADN-VPH (auto toma) y triage con citología convencional cada 3 años y para umbrales mayores a cuarenta millones la elección sería prueba ADN-VPH (auto toma) cada 3 años.
Vale la pena recalcar, que solo las estrategias de prueba ADN-VPH y triage con citología cada 5 años y prueba ADN-VPH cada 3 años (para umbrales superiores a cien millones) , superan la probabilidad del 50 % de ser costo-efectivas indicando la presencia incertidumbre alta sobre cuál de las estrategias es la más costo-efectiva.
5.2.6.12 Discusión
El estudio encontró que la alternativa más costo-efectiva para la tamización del CCU en Colombia es la prueba ADN-VPH y triage con citología cada 5 años iniciando a los 25 años, resultado similar al encontrado en el estudio previo (23) en donde la estrategia más costo-efectiva fue la prueba ADN-VPH con triage con citología convencional cada 5 años iniciando a los 30 años.
En relación al estudio previo este difiere en el algoritmo de tamización, en el estudio previo a las mujeres con resultados positivos a la prueba y negativos a la citología se les realizaba una nueva prueba al año con triage con citología, en el presente estudio se les realiza una nueva prueba a los 18 meses sin triage con citología pasando directamente a colposcopia las mujeres con resultados positivos en la prueba de ADN-VPH.
Las estrategias con pruebas ADN -VPH son costo efectivas si el costo por prueba es inferior o igual a $39.000, para costos mayores estas estrategias no son costo-efectiva e incluso son dominadas si el costo es superior a $60.000. En los análisis de sensibilidad se observa que la prueba es muy costo-efectiva en la mayoría de los escenarios analizados, siendo solo dominada cuando el costo es superior al $60.000 o la sensibilidad de la citología convencional se aproxima a la sensibilidad de la prueba de ADN-VPH.
Resultados similares se observaron en los análisis de sensibilidad probabilísticos en donde las estrategias con prueba ADN-VPH con y sin triage con citología convencional o liquida fueron más costo-efectivas que las estrategias de tamización solo con citología.
Nuestro análisis tiene varias limitaciones.
Primero, los datos fueron combinados desde múltiples fuentes que varían en el diseño utilizado (cohortes, ensayos clínicos, registros poblacionales, entre otras) con diferentes criterios de elegibilidad de las participantes, cuyas consecuencias se evaluaron en cortos periodos de tiempo y fueron extrapoladas a largos periodos.
Sin embargo, se realizando análisis de sensibilidad extensos para ver la robustez de los resultados, encontrando que en la mayoría de escenarios simulados la decisión no cambia. Sin embargo, se observa en el análisis probabilístico que solo dos estrategias superaron alcanzaron una probabilidad mayor al 50% de ser costo-efectivas indicando que existe incertidumbre alta en la determinación de cual estrategia es la más costo-efectiva.
El estudio no incluyo pruebas moleculares como la prueba de mRNA para las proteínas E6/E7 o las pruebas de genotipificación de los virus de alto riesgo 16,18 y 45, que actualmente se encuentran en fase de investigación en el país, como estrategias de triage para las mujeres con resultados positivos a las pruebas de ADN-VPH. Una vez esté disponible esta información, sería necesario actualizar el presente estudio.
Finalmente una política óptima de tamización en cáncer cervical necesita considerar:
La realización de estrategias de tamización, diferentes alternativas de manejo de los resultados anormales, y la efectividad de distintas opciones de tratamiento de las lesiones precancerosas. Un modelo de la historia natural del cáncer cervical debe permitir una representación razonable de la heterogeneidad en el riesgo de la población y necesita ser capaz de incorporar información de accesibilidad, cumplimiento y factibilidad de una estrategia de tamización aplicada en una población.
Los ensayos clínicos o los estudios de cohorte, no son capaces de incorporar todos estos elementos, y evaluar todas las posibles estrategias para todas las posibles poblaciones, en un solo estudio. Los ensayos clínicos no son capaces de incluir todos los costos y resultados en salud necesarios para permitir que sus resultados se soporten de un conocimiento sólido en términos de política.
Estos factores junto con la necesidad de tomar una decisión en un escenario particular en el cual la información es incompleta, convierten a los modelos analíticos de decisión en una herramienta útil en salud pública como es el caso del presente estudio, en donde los resultados encontrados serán útiles en la formulación de políticas públicas para el control del cáncer de cuello uterino en Colombia.
5.2.6.13 Conclusión
La tamización con prueba ADN-VPH y triage con citología convencional cada 5 años iniciando a los 25 años sería la alternativa más costo-efectiva para Colombia. La decisión dependerá además de la disponibilidad a pagar, del impacto a los presupuestos de salud y de la comparación de esta tecnología con otras que compiten por los mismos recursos.
Referencias
- 1. Legood R, Gray AM, Mahé C, Wolstenholme J, Jayant K, Nene BM, et al. Screening for cervical cancer in India: How much will it cost? A trial based analysis of the cost per case detected. International journal of cancer. Journal international du cancer [Internet]. 2005 Dec 20 [cited 2014 Nov 30];117(6):981–7. Available from: http://www.ncbi.nlm.nih.gov/pubmed/16003735
- 2. Instituto Nacional de Cancerología (INC). Atlas de mortalidad por cáncer en Colombia. INC. Bogotá, Colombia; 2010.
- 3. Society AC. Prevención y detección temprana del cáncer de cuello uterino [Internet]. [cited 2014 Nov 17]. Available from: http://www.cancer.org/espanol/cancer/cancerdecuellouterino/recursosadicionales/fragmentado/cancer-de-cuello-uterino-prevencion-y-deteccion-temprana-what-is-cervical-cancer
- 4. Fuchs-Tarlovsky V, Bejarano-Rosales M, Gutiérrez-Salmeán G, Casillas M. A, López-Alvarenga JC, Ceballos-Reyes GM. Effect of antioxidant supplementation over oxidative stress and quality of life in cervical cancer. Nutrición Hospitalaria [Internet]. Aula Médica Ediciones; [cited 2014 Nov 28];26(4):819–26. Available from: http://scielo.isciii.es/scielo.php?script=sci_arttext&pid=S0212-16112011000400023&lng=en&nrm=iso&tlng=en
- 5. Jemal A, Bray F, Center MM, Ferlay J, Ward E, Forman D. Global cancer statistics. CA: a cancer journal for clinicians [Internet]. [cited 2014 Jul 12];61(2):69–90. Available from: http://www.ncbi.nlm.nih.gov/pubmed/21296855
- 6. Almonte M, Murillo R, Sánchez GI, Jerónimo J, Salmerón J, Ferreccio C, et al. Nuevos paradigmas y desafíos en la prevención y control del cáncer de cuello uterino en América Latina. Salud Pública de México [Internet]. Instituto Nacional de Salud Pública; 2010 Dec [cited 2014 Nov 19];52(6):544–59. Available from: http://www.scielosp.org/scielo.php?script=sci_arttext&pid=S0036-36342010000600010&lng=en&nrm=iso&tlng=en
- 7. Instituto Nacional de Cancerología. Incidencia estimada y mortalidad por cáncer en Colombia 2002-2006 [Internet]. Publicaciones. Bogotá, Colombia; 2007 [cited 2014 Nov 8]. p. 1–98. Available from: http://www.cancer.gov.co/~incancer/instituto//files/libros/archivos/a9412b1cdffddfb228e09f7d31e9e124_Incidencia Estimada Y Mortalidad 2002-2006.pdf
Bibliografías
- 8. De La Hoz-Restrepo F, Alvis-Guzmán N, Narváez J, Chocontá-Piraquive LA. Evaluación de la Carga de Enfermedad por el Virus del Papiloma Humano en Bogotá. Revista de Salud Pública [Internet]. Instituto de Salud Publica, Faculdad de Medicina – Universidad Nacional de Colombia; 2009 Jun [cited 2014 Nov 19];11(3):454–67. Available from: http://www.scielosp.org/scielo.php?script=sci_arttext&pid=S0124-00642009000300014&lng=en&nrm=iso&tlng=en
- 9. Picconi MA. Human papillomavirus detection in cervical cancer prevention. Medicina [Internet]. 2013 Jan [cited 2014 Nov 19];73(6):585–96. Available from: http://www.ncbi.nlm.nih.gov/pubmed/24356274
- 10. Vasconcelos CTM, Damasceno MMC, Lima FET, Pinheiro AKB. Integrative review of the nursing interventions used for the early detection of cervical uterine cancer. Revista Latino-Americana de Enfermagem [Internet]. Escola de Enfermagem de Ribeirão Preto / Universidade de São Paulo; 2011 Apr [cited 2014 Nov 19];19(2):437–44. Available from: http://www.scielo.br/scielo.php?script=sci_arttext&pid=S0104-11692011000200028&lng=en&nrm=iso&tlng=es
- 11. Aponte-González J, Fajardo-Bernal L, Diaz J, Eslava-Schmalbach J, Gamboa O, Hay JW. Cost-effectiveness analysis of the bivalent and quadrivalent human papillomavirus vaccines from a societal perspective in Colombia. PloS one [Internet]. 2013 Jan [cited 2014 Nov 24];8(11):e80639. Available from: http://www.pubmedcentral.nih.gov/articlerender.fcgi?artid=3832449&tool=pmcentrez&rendertype=abstract
- 12. Pardo C, Cendales R. Survival analysis of cervical cancer patients. Biomédica : revista del Instituto Nacional de Salud [Internet]. 2009 Sep [cited 2014 Nov 28];29(3):437–47. Available from: http://www.ncbi.nlm.nih.gov/pubmed/20436995
Fuentes
- 13. Goldie SJ, Gaffikin L, Goldhaber-Fiebert JD, Gordillo-Tobar A, Levin C, Mahé C, et al. Cost-effectiveness of cervical-cancer screening in five developing countries. The New England journal of medicine [Internet]. 2005 Nov 17 [cited 2014 Nov 28];353(20):2158–68. Available from: http://www.ncbi.nlm.nih.gov/pubmed/16291985
- 14. Dim CC. Towards improving cervical cancer screening in Nigeria: a review of the basics of cervical neoplasm and cytology. Nigerian journal of clinical practice [Internet]. [cited 2014 Nov 30];15(3):247–52. Available from: http://www.ncbi.nlm.nih.gov/pubmed/22960955
- 15. Instituto Nacional de Cancerología (INC). Recomendaciones para la tamización de neoplasias del cuello uterino en mujeres sin antecedentes de patología cervical (preinvasora o invasora) en Colombia [Internet]. INC. Bogotá, Colombia: INC; 2007. Available from: http://www.cancer.gov.co/~incancer/instituto//files/libros/archivos/1b244b0cbac755bffb2b14154a3effc0_Guia N3 tamización de cuello uterino.pdf
- 16. Moosa NY, Khattak N, Alam MI, Sher A, Shah W, Mobashar S, et al. Comparison of cervical cell morphology using two different cytology techniques for early detection of pre-cancerous lesions. Asian Pacific journal of cancer prevention : APJCP [Internet]. 2014 Jan [cited 2014 Nov 30];15(2):975–81. Available from: http://www.ncbi.nlm.nih.gov/pubmed/24568528
- 17. Cavazza M, Correnti M. Pruebas moleculares para la detección del virus papiloma humano. Desafíos y posibilidades. Dermatología Venezolana. 2004;42(3).
- 18. Dehn D, Torkko KC, Shroyer KR. Human papillomavirus testing and molecular markers of cervical dysplasia and carcinoma. Cancer [Internet]. 2007 Mar 25 [cited 2014 Nov 29];111(1):1–14. Available from: http://www.ncbi.nlm.nih.gov/pubmed/17219448
Lecturas Recomendadas
- 19. Quintero Vega M, Cruz Gómez JF, Bastidas M, Márquez L, Puig Pons J. Detección y tipificación de virus del papiloma humano (VPH) mediante PCR- RFLP. Revista de Obstetricia y Ginecología de Venezuela [Internet]. Sociedad de obstetricia y ginecología de Venezuela.; [cited 2014 Nov 29];68(1):25–31. Available from: http://www.scielo.org.ve/scielo.php?script=sci_arttext&pid=S0048-77322008000100006&lng=es&nrm=iso&tlng=es
- 20. Wiesner C, Gonzalez M, Acosta J, Ortiz N, Espinoza C, Gonzalez C, et al. Manual para la prevención y tamización de cáncer de cuello uterino Estrategia “Prueba ADN-VPH.” Instituto . Bogotá; 2011. p. 25.
- 21. Toro de Méndez M, Ferrández Izquierdo A. Detección de virus papiloma humano (HPV) a partir de muestras celulares de cuello uterino en base líquida: Correlación con la inmunorreactividad de la proteína p16INK4a. Investigación Clínica [Internet]. Universidad del Zulia; [cited 2014 Nov 29];52(1):3–14. Available from: http://www.scielo.org.ve/scielo.php?script=sci_arttext&pid=S0535-51332011000100002&lng=es&nrm=iso&tlng=es
- 22. NICE. Guidance on the use of liquid-based cytology for cervical screening [Internet]. NICE technology appraisal guidance 69. 2003 [cited 2014 Nov 24]. Available from: https://www.nice.org.uk/guidance/ta69/resources/guidance-guidance-on-the-use-of-liquidbased-cytology-for-cervical-screening-pdf
- 23. Gamboa O, Chicaíza L, García-Molina M, Díaz J, González M, Murillo R, et al. Cost-effectiveness of conventional cytology and HPV DNA testing for cervical cancer screening in Colombia. Salud pública de México [Internet]. [cited 2014 Nov 27];50(4):276–85. Available from: http://www.ncbi.nlm.nih.gov/pubmed/18670718
- 24. Arbyn M, Bergeron C, Klinkhamer P, Martin-Hirsch P, Siebers AG, Bulten J. Liquid compared with conventional cervical cytology: a systematic review and meta-analysis. Obstetrics and gynecology [Internet]. 2008 Jan [cited 2014 Dec 3];111(1):167–77. Available from: http://www.ncbi.nlm.nih.gov/pubmed/18165406
Referencias Bibliográficas
- 25. Arbyn M, Ronco G, Anttila A, Meijer CJLM, Poljak M, Ogilvie G, et al. Evidence regarding human papillomavirus testing in secondary prevention of cervical cancer. Vaccine [Internet]. 2012 Nov 20 [cited 2014 Dec 3];30 Suppl 5:F88–99. Available from: http://www.sciencedirect.com/science/article/pii/S0264410X12010055
- 26. Arbyn M, Verdoodt F, Snijders PJF, Verhoef VMJ, Suonio E, Dillner L, et al. Accuracy of human papillomavirus testing on self-collected versus clinician-collected samples: a meta-analysis. The Lancet. Oncology [Internet]. 2014 Feb [cited 2014 Dec 1];15(2):172–83. Available from: http://www.thelancet.com/journals/a/article/PIIS1470-2045(13)70570-9/fulltext
- 27. Pileggi C, Flotta D, Bianco A, Nobile CGA, Pavia M. Is HPV DNA testing specificity comparable to that of cytological testing in primary cervical cancer screening? Results of a meta-analysis of randomized controlled trials. International journal of cancer. Journal international du cancer [Internet]. 2014 Jul 1 [cited 2014 Dec 1];135(1):166–77. Available from: http://www.ncbi.nlm.nih.gov/pubmed/24302411
- 28. Instituto Nacional de Cancerología. Protocolos de manejo del paciente con cáncer. Legis S.A. Bogotá, Colombia; 2010.
- 29. National Comprehensive Cancer Network (NCCN). . Cervical Cancer. NCCN Guidelines 2011 [Internet]. 2011. Available from: www.nccn.com
- 30. ISS. Manual Tarifario ISS. Acuerdo 256. Colombia; 2001 [Internet]. Available from: http://lexsaludcolombia.files.wordpress.com/2010/10/tarifas-iss-2001.pdf.
- 31. Manual Tarifario SOAT. 2013 [Internet]. 2013. Available from: http://www.consultorsalud.com/decretos/955-manual-tarifario-soat-2013
- 32. Tarifario SISMED. [Internet]. Available from: http://web.sispro.gov.co/WebPublico/SISMED/LibroVirtual/index2.html
- 33. Clifford G, Franceschi S, Diaz M, Muñoz N, Villa LL. Chapter 3: HPV type-distribution in women with and without cervical neoplastic diseases. Vaccine [Internet]. 2006 Aug 31 [cited 2014 Nov 30];24 Suppl 3:S3/26–34. Available from: http://www.ncbi.nlm.nih.gov/pubmed/16950015
Fuentes Bibliográficas
- 34. Muñoz N, Bosch FX, de Sanjosé S, Herrero R, Castellsagué X, Shah K V, et al. Epidemiologic classification of human papillomavirus types associated with cervical cancer. The New England journal of medicine [Internet]. 2003 Mar 6 [cited 2014 Nov 30];348(6):518–27. Available from: http://www.ncbi.nlm.nih.gov/pubmed/12571259
- 35. Molano M, Van den Brule A, Plummer M, Weiderpass E, Posso H, Arslan A, et al. Determinants of clearance of human papillomavirus infections in Colombian women with normal cytology: a population-based, 5-year follow-up study. American journal of epidemiology [Internet]. 2003 Sep 1 [cited 2014 Nov 30];158(5):486–94. Available from: http://www.ncbi.nlm.nih.gov/pubmed/12936904
- 36. Muñoz N, Méndez F, Posso H, Molano M, van den Brule AJC, Ronderos M, et al. Incidence, duration, and determinants of cervical human papillomavirus infection in a cohort of Colombian women with normal cytological results. The Journal of infectious diseases [Internet]. 2004 Dec 15 [cited 2014 Nov 30];190(12):2077–87. Available from: http://www.ncbi.nlm.nih.gov/pubmed/15551205
- 37. Moscicki A-B, Schiffman M, Kjaer S, Villa LL. Chapter 5: Updating the natural history of HPV and anogenital cancer. Vaccine [Internet]. 2006 Aug 31 [cited 2014 Nov 30];24 Suppl 3:S3/42–51. Available from: http://www.ncbi.nlm.nih.gov/pubmed/16950017
- 38. Myers ER, McCrory DC, Nanda K, Bastian L, Matchar DB. Mathematical model for the natural history of human papillomavirus infection and cervical carcinogenesis. American journal of epidemiology [Internet]. 2000 Jun 15 [cited 2014 Nov 30];151(12):1158–71. Available from: http://www.ncbi.nlm.nih.gov/pubmed/10905528
Otras Referencias
- 39. PROFAMILIA. DETECCIÓN TEMPRANA DEL CÁNCER DE CUELLO UTERINO Y MAMA [Internet]. Encuesta Nacional de Demografía y Salud 2010. 2010 [cited 2011 Oct 28]. Available from: http://www.profamilia.org.co/encuestas/Profamilia/Profamilia/index.php?option=com_content&view=article&id=148&Itemid=118
- 40. Departamento administrativo distrital de estadistica DANE. Estadísticas vitales. [Internet]. DANE. [cited 2011 Jun 19]. Available from: http://www.dane.gov.co/
- 41. Miller DK, Homan SM. Determining transition probabilities: confusion and suggestions. Medical decision making : an international journal of the Society for Medical Decision Making [Internet]. [cited 2014 Nov 21];14(1):52–8. Available from: http://www.ncbi.nlm.nih.gov/pubmed/8152357
- 42. Underwood M, Arbyn M, Parry-Smith W, De Bellis-Ayres S, Todd R, Redman CWE, et al. Accuracy of colposcopy-directed punch biopsies: a systematic review and meta-analysis. BJOG : an international journal of obstetrics and gynaecology [Internet]. 2012 Oct [cited 2014 Dec 3];119(11):1293–301. Available from: http://www.ncbi.nlm.nih.gov/pubmed/22882742
- 43. Whitlock EP, Vesco KK, Eder M, Lin JS, Senger CA, Burda BU. Liquid-based cytology and human papillomavirus testing to screen for cervical cancer: a systematic review for the U.S. Preventive Services Task Force. Annals of internal medicine [Internet]. 2011 Nov 15 [cited 2014 Dec 3];155(10):687–97, W214–5. Available from: http://www.ncbi.nlm.nih.gov/pubmed/22006930
- 44. World Health Organization. Macroeconomics and health: investing in health for economic development: report of the Commission on Macroeconomics and Health. 2001.