Tamización
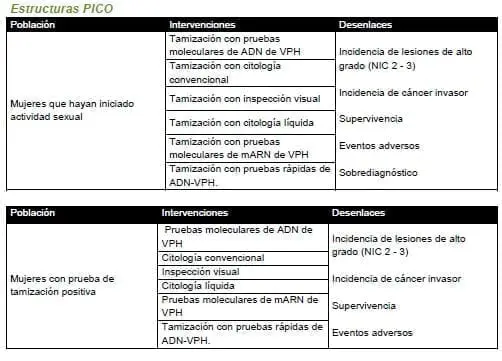
1.¿Con qué esquema se debe realizar la tamización en mujeres que hayan iniciado actividad sexual (citología, inspección visual, pruebas moleculares) para detectar lesiones precancerosas y cáncer de cuello uterino? ¿Qué intervalos debe tener dicho esquema?
¿A qué edades debe iniciarse y finalizarse la tamización? ¿Cuál estrategia de clasificación diagnóstica debe realizarse en mujeres con resultados positivos a la tamización (citología, inspección visual, pruebas moleculares)? (Lea también: Lesiones Precancerosas de Cuello Uterino, Metodología GRADE)
3.1.1 Introducción
En la primera mitad del siglo XX se introdujo la citología de cuello uterino como una prueba para la tamización de cáncer de cuello uterino que consiste en su práctica rutinaria, entre la población asintomática de mujeres, para detectar aquellas que presentan cambios celulares de cuello uterino, lesiones pre-cancerosas o cáncer en estadios tempranos, para generar un tratamiento preventivo o para permitir una mayor tasa de curación y por tanto una reducción en la mortalidad por cáncer (1).
La citología ha sido ampliamente utilizada en el mundo y se ha podido evaluar su rendimiento; a pesar de tener una sensibilidad de baja a moderada su uso ha permitido reducir la incidencia de cáncer cervical así como la mortalidad en un 80% en los países de mayores ingresos (2).
Sin embargo, en países de medianos y de bajos recursos, aunque se ha reducido la incidencia de cáncer de cuello uterino de manera importante, continua siendo un problema de salud pública, y no ha logrado un importante impacto en la reducción de la mortalidad por esta causa (3).
En la actualidad, se han evaluado otras pruebas alternativas de tamización, diferentes a la citología
Como son las técnicas de inspección visual y tratamiento inmediato, así como las pruebas de biología molecular (4).
Primeras permiten la identificación de lesiones de bajo y alto grado mediante el uso de ácido acético diluido del 3 al 5% con o sin lugol, que son insumos de bajo costo, no requieren de una compleja infraestructura de laboratorio, ni personal especializado para realizarlo, son fáciles de implementar en zonas rurales y con baja infraestructura tecnológica; su sensibilidad es similar o incluso un poco mejor que la de la citología. Las pruebas de biología molecular son técnicas de laboratorio altamente sensibles y reproducibles para detectar los tipos de VPH de alto riesgo (4, 5).
Estas últimas pruebas requieren de una infraestructura similar a la de la citología, pero tienen la ventaja de tener una mejor sensibilidad que ésta, aunque una menor especificidad (6). Los estudios han mostrado evidencia convincente en la reducción de la mortalidad por esta causa mediante el uso de éstas dos alternativas de tamización (6-8).
De acuerdo con las recomendaciones basadas en la evidencia generadas por el INC en el año 2007
Se sugirió que la edad de inicio de las técnicas de inspección visual y tratamiento inmediato debía ser desde los 30 hasta los 50 años de edad por las limitaciones de la técnica después de la menopausia.
Igualmente se sugirió que en los casos negativos el intervalo debía ser cada 3 años (9). Sin embargo, se sabe que hacerla una o dos veces en la vida en estos rangos de edad disminuye la incidencia de carcinoma infiltrante y su mortalidad.
Para las pruebas moleculares el INC recomendó en esta misma guía, que la edad de inicio para la tamización debía ser los 30 años, y la edad de finalización los 65 años de edad, y que el intervalo para su aplicación podía ser de cinco años (9).
Teniendo en cuenta que esta GPC pretende actualizar la evidencia, las preguntas sobre edad de inicio y finalización de la tamización resultan relevantes teniendo en cuenta además que el país inició la vacunación masiva contra el virus de VPH para las niñas entre 9 a 17 años.
Por otra parte, las pruebas moleculares para la detección de VPH son dispositivos tecnológicos diversos
Pueden realizarse de manera directa mediante la identificación del genoma de VPH de alto riesgo (VPH-AR), de amplificación de un fragmento de ADN viral con o sin genotipificación o mediante la detección de ARNm.
Las primeras, identifican de manera directa el ADN de alguno(s) de los 13 tipos de VPH que son considerados carcinogénicos sin realizar amplificación previa del ADN. Las segundas amplifican un fragmento del ADN viral mediante la reacción en cadena de la polimerasa (PCR) para obtener millones de copias tanto de manera convencional como en tiempo real.
Pruebas de genotipificación, permiten identificar los tipos virales de manera específica (usualmente el VPH 16 y 18) y las de ARNm identifican la expresión de las oncoproteínas E6 y E7 del VPH (6). Teniendo en cuenta estas consideraciones se considera necesario generar recomendaciones específicas sobre el tipo de prueba molecular (ADN-ARN) que se debe realizar como base de la tamización primaria.
Los resultados falsos a la tamización pueden producir efectos adversos en la población beneficiada. El ideal de una prueba de tamización es que sea lo suficientemente sensible para no generar una alta tasa de falsos negativos que hace inefectiva la intervención y debe tener además, una aceptable o alta especificidad con el fin de no generar falsos positivos; los cuales implican la remisión innecesaria de mujeres a colposcopia y biopsia (1).
Desafortunadamente, la mayoría de pruebas de VPH basadas en ADN viral tienen un bajo valor predictivo positivo y una baja especificidad. Como resultado, la remisión de todas las mujeres con resultados positivos a procedimientos diagnósticos representaría una gran carga para ellas y los sistemas de salud, debido al potencial de realizar sobretratamiento o procedimientos innecesarios a las mujeres (10) y un impacto negativo de tipo psicosocial (11).
Necesidad de clasificar o de hacer un triage de las mujeres positivas en la tamización primaria
Teniendo en consideración lo anterior, se ha considerado la necesidad de clasificar o de hacer un triage de las mujeres positivas en la tamización primaria, que consiste en aplicar una prueba adicional con el fin de identificar aquellas que verdaderamente requieren procedimientos diagnósticos adicionales.
Entre las alternativas del triage que se han propuesto se encuentran las pruebas orientadas a detectar la lesión celular como son la citología convencional o de base líquida, las técnicas de inspección visual y el p16/Ki67.
Igualmente se encuentran las pruebas orientadas a identificar el estado de integración viral o los tipos virales de mayor riesgo (tipificación viral, mRNA viral, etcétera).
Con base en lo anterior se justifica que en la presente guía para la atención de las mujeres asintomáticas, a riesgo de desarrollar cáncer de cuello uterino, se inicie una búsqueda de la evidencia que permita la generación de recomendaciones sobre el esquema de tamización y la prueba de clasificación diagnóstica en población general.
3.1.2 Resumen de la evidencia
Para responder esta pregunta, una búsqueda de Guías de Práctica Clínica (GPC) fue realizada. Los resultados de la búsqueda, así como las GPC incluidas y excluidas. Luego del proceso de selección, cuatro GPC, que evidenciaron concordancia con el alcance y objetivo de la guía en desarrollo y seguimiento de la metodología GRADE, fueron incluidas.
Las dos GPC que mostraron calidad adecuada fueron revisadas en detalle con el objetivo de encontrar información relacionada con la pregunta de la presente guía, sus intervenciones y desenlaces.
La GPC de la Canadian Task Force on Preventive Health Care (CTFPHC) (12) evaluó dos de las intervenciones planteadas, citología convencional, citología en base líquida y pruebas de ADN-VPH, pero luego de encontrar la evidencia para esta última tecnología insuficiente, consideró prematuro generar recomendaciones sobre ésta, y únicamente generó recomendaciones sobre la citología, para casi todos los desenlaces de interés, excepto para el que corresponde a la estrategia de clasificación diagnóstica.
No obstante, las tablas de evidencia construidas en dicha GPC, respecto al interés de la presente guía, son presentadas como parte del bloque de evidencia.
La GPC de la OMS, WHO guidelines for screening and treatment of precancerous lesions for cervical cancer prevention (13), incluyó comparaciones para VIA, ADN-VPH y citología, y arrojó información para todos los desenlaces de interés a la presente GPC (13).
Sin embargo, los desenlaces fueron obtenidos a través del modelamiento matemático de datos de estudios de rendimiento diagnóstico, y las recomendaciones corresponden a estrategias de tamizar-tratar.
Frente a la necesidad de explorar nueva evidencia, más enfocada en las intervenciones propuestas en la presente guía
Se realizó una estrategia de búsqueda de la literatura con el propósito de obtener revisiones sistemáticas o metanálisis que evaluaran dichas estrategias de tamización, en mujeres que hayan iniciado actividad sexual.
Dos revisiones sistemáticas fueron seleccionadas, pero dada la ausencia de información para algunas intervenciones y desenlaces en estas revisiones, se realizaron nuevas estrategias de búsqueda para obtener estudios primarios. En esta fase, ensayos clínicos aleatorizados fueron también seleccionados para responder esta pregunta.
3.1.2.1 Calidad de la evidencia
Para la evaluación de la calidad de la evidencia se empleó la metodología GRADE. La evaluación formal de la calidad de las GPC fue realizado mediante el instrumento AGREE II por cuatro evaluadores independientes, identificando así las guías que podrían ser seleccionadas para este proceso.
La calificación del riesgo de sesgo de estudios integrativos y primarios, herramientas específicas para cada tipo de diseño (AMSTAR para RS y Cochrane para ensayos clínicos aleatorizados). Las revisiones sistemáticas de la literatura (RSL) de las GPC incluidas, también fueron evaluadas con el instrumento AMSTAR.
GPC
Solo las dos GPC incluidas lograron puntajes superiores a 60% en los dominios de rigor en la elaboración e independencia editorial (12, 13) y en general ostentaron puntajes superiores a 70% en la totalidad de los dominios, siendo mayores que 95% en los dominios de alcance y objetivo y de claridad en la presentación.
Las dos GPC que no superaron este proceso de evaluación de calidad, evidenciaron puntajes inferiores a 60% en el dominio de rigor en la elaboración (14, 15), y una de ellas también mostró baja puntuación en el de independencia editorial (14). La calidad de las revisiones sistemáticas de las dos GPC seleccionadas para responder. En general la calidad fue buena, con AMSTAR de 11/11 (12) y de 10/11 (13) dado a que no reportó la valoración de la probabilidad del sesgo de publicación.
Estudios integrativos
Las dos revisiones sistemáticas incluidas mostraron una calidad aceptable con AMSTAR de 8/11. Ninguna de las dos declaró el estado de publicación como criterio de inclusión ni incluyó un listado de los estudios incluidos y excluidos. Una de ellas además no declaró conflicto de intereses (16) y la otra no reportó la valoración de la probabilidad del sesgo de publicación (17).
Estudios primarios
Cuatro ensayos clínicos fueron seleccionados (7, 8, 18, 19). El riesgo de sesgo, evaluado con la herramienta de Cochrane, fue bajo para los tres primeros estudios y moderado para el último.
La generación de la secuencia fue bien reportada por los autores de los estudios, a excepción de uno en el que no se brindó información al respecto (19), en dos de ellos no se reporta información sobre el ocultamiento de la asignación.
En general ninguno de los estudios realizó cegamiento de las participantes, debido a que no era posible por la naturaleza de las intervenciones, y debido a la aleatorización por conglomerados realizada en dos de los estudios (7, 8).
En todos los estudios se realizó cegamiento de los evaluadores de los desenlaces, excepto en uno (19). Se reportaron pérdidas de aproximadamente 0% en tres estudios (7, 8, 19) y baja probabilidad de pérdida de información en otro estudio (18). Todos los estudios reportan resultados para la totalidad de los grupos comparados y se encontró bajo riesgo de otras fuentes de sesgo.
(Lea También: Confirmación Diagnóstica con Inmunohistoquímica)
3.1.2.2 Resumen de resultados
Recommendations on screening for cervical cancer Canadian Task Force on Preventive Health Care
Como se mencionó anteriormente la GPC de la CTFPHC no generó recomendaciones respecto a pruebas diferentes a la citología, sin embargo reportó que la mayoría de los estudios de pruebas de ADN-VPH han mostrado reducción en las lesiones pre-cancerosas, así como en incidencia y mortalidad por cáncer de cuello uterino.
Uno de los ensayos clínicos aleatorizados incluidos que reportó efectividad de las pruebas de ADN-VPH en reducción de la incidencia y la mortalidad por cáncer de cuello uterino estudió el efecto de una sola ronda de tamización en mujeres de la India, mayores de 30 años, quienes no tenían historia previa de tamización, por lo que estos resultados fueron considerados inciertos para la población canadiense.
Un segundo estudio de Finlandia, incluido en la GPC, no encontró reducciones más significativas en la incidencia de cáncer de cuello uterino con la prueba de ADN-VPH.
En relación específica a las comparaciones de interés a esta guía, respecto a la citología en base líquida comparada con la citología convencional, no encontró ningún estudio que evaluara los desenlaces de incidencia y mortalidad, y que cumplieran con los criterios de inclusión.
Respecto a las pruebas de ADN-VPH en comparación con la citología convencional
Se encontró un rendimiento significativamente mejor de las pruebas de ADN-VPH, con una reducción del riesgo de mortalidad de 41% sobre la citología, y del 37% del riesgo de incidencia de cáncer en estadios avanzados.
Combinados los resultados de los dos estudios incluidos en la GPC en mención, la prueba de ADN-VPH fue también superior a la citología en la reducción de incidencia de cáncer de cuello uterino, con un seguimiento que va desde los 3 a los 8 años (RR 0,78, IC 95% 0,62-0,99, p=0.04). Los estudios fueron calificados con calidad moderada de acuerdo al sistema GRADE.
Como prueba reflex, es decir como prueba de triage a la citología, en comparación con la citología, no encontraron estudios que cumplieran sus criterios de inclusión.
En relación a los eventos adversos y el sobrediagnóstico de la tamización con pruebas de ADN-VPH en comparación con citología, no encontraron estudios, ni para los eventos planteados, ni para los desenlaces de interés, por lo que una nueva búsqueda específica fue realizada por el grupo desarrollador de la GPC en mención.
Todos los estudios encontrados son de tipo observacional y carecen de comparación. Además se reporta alta heterogeneidad de los estudios por lo que no es posible emitir consideraciones al respecto.
La guía de la CTFPHC recomienda el uso de citología cervical convencional o en base líquida para mujeres sin síntomas de cáncer de cuello uterino, con vida sexual activa, independiente de la orientación sexual.
Mujeres menores de 20 años y mujeres de 20 a 24 años, no recomienda tamización de rutina. Para mujeres de 25 a 29 años y mujeres de 30 a 69 años, se recomienda tamización de rutina con un intervalo de 3 años.
Para mujeres de 70 años o mayores, quienes han tenido adecuada tamización (al menos 3 citologías negativas en los últimos 10 años) se recomienda finalizar la tamización. Las otras mujeres de 70 años o mayores se recomienda continuar la tamización hasta que tres resultados negativos sean obtenidos.
WHO guidelines for screening and treatment of precancerous lesions for cervical cancer prevention
La guía de la OMS desarrolló un flujograma de toma de decisiones para que los administradores de programas de tamización, puedan seleccionar una de las estrategias sugeridas, dependiendo del contexto donde serán implementadas.
A pesar de reconocer el hecho de que la mejor evidencia para valorar los efectos de una estrategia de tamizar-tratar proviene de ensayos clínicos aleatorizados, pocos estudios han evaluado estas estrategias y cuentan con desenlaces importantes para el paciente.
Los desenlaces en esta guía fueron obtenidos mediante un modelo matemático, calculando la proporción de resultados verdaderos positivos (VP), verdaderos negativos (VN), falsos positivos (FP) y falsos negativos (FN), para cada una de las pruebas, dadas las estimaciones combinadas de exactitud de las pruebas y la probabilidad pre-test de tener neoplasia intraepitelial cervical (NIC) en esa población.
Se calculó la probabilidad de desarrollar cualquiera de los desenlaces considerados críticos, que coinciden en su totalidad con los desenlaces planteados en la presente Guía, basados en los tratamientos que podrían recibir los pacientes, y la estimación combinada de la eficacia y las potenciales complicaciones de los diferentes tratamientos (crioterapia, conización con bisturí frío, y LEEP).
Para calcular una estimación global de los desenlaces, agregaron la probabilidad de desarrollar un desenlace por cada de una de las categorías (VP, VN, FP, FN) para las mismas pruebas de tamización y las opciones de tratamiento. Todo esto bajo diferentes supuestos que fueron agregados al modelo.
Esta guía tuvo en cuenta consideraciones importantes respecto al éxito de los programas de tamización basados en citología
En lugares donde los sistemas de salud no son robustos, los recursos son limitados, o el aseguramiento de la calidad es difícil de mantener. Asegurar la calidad de la citología permite resultados precisos y reproducibles, pero es más costoso en términos de recursos humanos y financieros, en comparación con otras estrategias, y debido a que los resultados de la citología no están disponibles de manera rápida, existe una gran probabilidad de perder a las mujeres en el seguimiento, reduciendo los beneficios de la tamización.
La citología seguida por colposcopia, con o sin biopsia, no mostró en esta revisión, mejores resultados que otras estrategias para la prevención del cáncer cervical. El uso de la citología, previa realización de pruebas de ADN-VPH no fue evaluado en esta revisión, ni modelado para las recomendaciones.
Todas las recomendaciones que genera la guía de la OMS corresponden a estrategias para un programa de tamización y tratamiento. Estas recomendaciones aplican para mujeres de 30 años y mayores debido a su alto riesgo de cáncer de cuello uterino, sin embargo la magnitud del efecto variará de acuerdo a grupos de edad y al riesgo de base de NIC 2 o mayor.
La prioridad debe ser tamizar mujeres de 30-49 años más que maximizar el número de pruebas en la vida de una mujer. La tamización, incluso una sola vez en la vida, es beneficiosa.
A continuación se presentan las recomendaciones dadas en la guía de la OMS:
- Primero, No se recomienda la conización con bisturí frío (CKC) como tratamiento en una estrategia de tamizar y tratar. Aunque los beneficios de CKC son similares comparados con crioterapia y LEEP, los efectos secundarios son mayores con CKC.
- Segundo, En donde los recursos lo permitan, se sugiere tamizar con pruebas de ADN-VPH y tratar con crioterapia (o LEEP cuando la paciente no sea elegible para crioterapia) sobre las estrategias de tamizar con VIA y tratar con crioterapia (o LEEP). En escenarios con recursos limitados, donde no es factible la implementación de las pruebas de ADN-VPH, se sugiere tamizar con VIA y tratar con crioterapia (o LEEP).
- Tercero, Se recomienda tamizar con VIA y tratar con crioterapia (o LEEP) por encima de tamizar con citología seguida de colposcopia (con o sin biopsia) y tratar con crioterapia (o LEEP).
- Cuarto, Se sugiere tamizar con pruebas de ADN-VPH y tratar con crioterapia (o LEEP cuando la paciente no sea elegible para crioterapia) sobre una estrategia de tamizar con pruebas de ADN-VPH seguido de colposcopia (con o sin biopsia) y tratar con crioterapia (o LEEP).
- Quinto, Se sugiere cualquiera estrategia, entre tamizar con pruebas de ADN-VPH seguido por VIA y tratar con crioterapia (o LEEP) o tamizar con pruebas de ADN-VPH y tratar con crioterapia (o LEEP).
-
Sexto, Se sugiere tamizar con pruebas de ADN-VPH seguido por VIA y tratar con crioterapia (o LEEP) sobre tamizar con VIA y tratar con crioterapia (o LEEP).
- Séptimo, Se sugiere tamizar con pruebas de ADN-VPH seguido por VIA y tratar con crioterapia (o LEEP) sobre tamizar con citología seguido de colposcopia (con o sin biopsia) y tratar con crioterapia (o LEEP).
- Octavo, Se sugiere tamizar con pruebas de ADN-VPH seguido por VIA y tratar con crioterapia (o LEEP) sobre tamizar con pruebas de ADN-VPH seguido de colposcopia (con o sin biopsia) y tratar con crioterapia (o LEEP).
Evidencia de estudios integrativos y estudios primarios
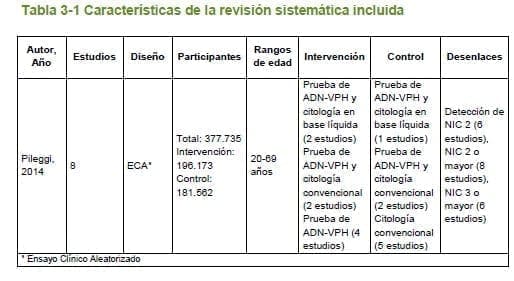
Las dos revisiones sistemáticas seleccionadas fueron analizadas en detalle en busca de evidencia para las intervenciones y desenlaces de la presente guía. Debido a que la revisión más reciente (16) incluyó los mismos estudios que la otra revisión seleccionada (17), y también estudios adicionales, para los mismos desenlaces, se tuvieron en cuenta solo sus datos en este bloque de evidencia.
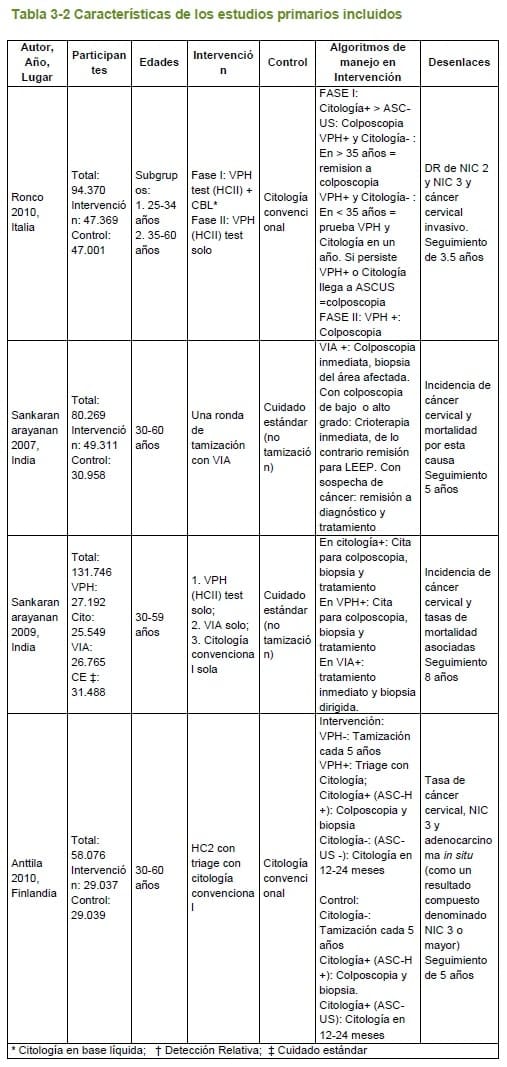
Adicionalmente, dos ensayos clínicos, incluidos en la revisión sistemática seleccionada, un ensayo producto de una búsqueda de estudios primarios, y un ensayo referido por expertos, fueron analizados de manera individual, dado a que estudiaron los desenlaces de interés. Las características de los estudios incluidos se presentan en las 3.1.1 y 3.1.2.
Comparación 1: Citología convencional versus citología en base líquida
La guía de la CTFPHC no encontró evidencia para esta comparación respecto a los desenlaces de incidencia y mortalidad, sin embargo refieren su similitud en cuanto a sensibilidad y especificidad, definida ésta desde la guía que le precede publicada en 2012, en la que además se basaron para recomendar, de acuerdo a la disponibilidad, el uso de cualquiera de las dos citologías, en su programa nacional.
Las revisiones sistemáticas seleccionadas tampoco diferenciaron el tipo de citología para sus comparaciones con otras tecnologías diferentes a citología.
Un estudio holandés publicado en 2009 (20), que comparó la citología en base líquida con la citología convencional, reportó que no existen diferencias significativas en las tasas de detección relativa, ni crudas ni ajustadas, para NIC 1+ (DR ajustada 1,01, IC 95% 0,85 a 1,19), para NIC 2 o mayor (DR ajustada 1,00, IC 95%, 0,84-1,20), para NIC 3 o mayor (DR ajustada 1,05, IC 95% 0,86-1,29), ni para carcinoma (DR ajustada 1,69, IC 95% 0,96-2,99).
Las razones del valor predictivo positivo (VPP) ajustadas, consideradas en varios puntos de corte citológicos y para varios resultados de NIC no difirieron significativamente, mostrando que la citología de base líquida no tiene mejor efectividad ni rendimiento que la citología convencional en la detección de lesiones precursoras de cáncer cervical.
Comparación 2: Citología (en base líquida o convencional) versus pruebas de ADN-VPH
La revisión sistemática seleccionada estudió esta comparación para los desenlaces de detección relativa de NIC 2 o mayor y NIC 3 o mayor.
Los resultados combinados de siete estudios, mostraron que las pruebas ADN-VPH presentan una detección significativamente más alta que la citología, de base líquida o convencional, tanto para NIC 2 o mayor como para NIC 3 o mayor, sin embargo debido a que una alta heterogeneidad entre los estudios fue reportada, un análisis de sensibilidad fue realizado.
Dado el pequeño número de estudios, este análisis solo pudo ser realizado para el desenlace de NIC 2 o mayor, excepto para edad que también pudo ser realizado para NIC 3 o mayor.
Al evaluar las diferentes fuentes potenciales de heterogeneidad, se encontró que pese a que la alta heterogeneidad persiste en todos los análisis, algunos resultados se mantienen estadísticamente significativos, para las siguientes variables:
– Edad > 30 años:
La detección relativa fue significativamente más alta con las pruebas de ADN-VPH que con la citología, tanto para NIC 2 o mayor (p=0,022) como para NIC 3 o mayor (p=0,02), en este grupo de edad.
En el grupo de edad de <35 años, las diferencias no fueron significativas (NIC 2 o mayor, p=0,05; NIC 3 o mayor, p=0,128), sugiriendo mayor beneficio de la tamización con pruebas de ADN-VPH en el primer grupo de edad.
– Intervalo de tamización de 5 años:
La detección relativa fue significativamente más alta con las pruebas de ADN-VPH que con la citología para NIC 2 o mayor (p=0,03), en este intervalo de tamización; en el intervalo de 3 años, las diferencias no fueron significativas (NIC 2 o mayor, p=0,143), sugiriendo mayor beneficio de la tamización en un intervalo de 5 años.
Resultados significativos a favor de las pruebas de ADN-VPH, en la detección de NIC 2 o mayor, fueron también encontrados en estudios de alta calidad (p=0,043), cuando se usan como pruebas ADN-VPH en el grupo de intervención captura de híbridos 2 (HC2) (p=0,049) y las pruebas de PCR (no se reporta valor p), cuando se usa en el grupo control citología convencional (p=0,027), y cuando se manejan las mujeres con resultados positivos en ambas pruebas, tanto en la prueba de ADN-VPH como en la citología, con colposcopia (p=0,014).
El ensayo clínico aleatorizado de Ronco y cols. (18)
Mostró adicionalmente una incidencia de cáncer de cuello uterino significativamente más baja en la segunda ronda de tamización para todas las edades, en el brazo de las pruebas de ADN-VPH en comparación con la citología (p= 0,004); esta reducción en incidencia a favor de las pruebas de ADN-VPH solo se mantuvo significativa para el grupo de 35 a 60 años (p=0,016), diferente que para el grupo de 25 a 34 años (p=0,50).
Tomando los datos de la fase 2 de este estudio, en la que se comparó prueba de ADN-VPH sola con citología convencional en la primera ronda de tamización, la detección de NIC 2, NIC 3 y adenocarcinoma in situ fue significativamente mayor en el brazo de pruebas de ADN-VPH, tanto en el grupo de 25 a 34 años, como en el de 35 a 60 años.
El ensayo de Sankaranarayanan y cols. (8), del que se presentó la comparación de citología versus pruebas de ADN-VPH dentro de la GPC de la CTFPHC, mostró beneficios estadísticamente significativos de la tamización con pruebas de ADN-VPH en comparación con no tamizar para los desenlaces de incidencia de cáncer cervical en estadios avanzados y mortalidad por esta enfermedad. Para la citología en cambio, no se encontraron beneficios significativos en estos mismos desenlaces en comparación con no tamizar.
Comparación 3: VIA versus citología y versus pruebas de ADN-VPH
La guía de la OMS ha sugerido, en ausencia de recursos para la implementación de pruebas de ADN-VPH, la tamización con VIA seguida de tratamiento inmediato con crioterapia, e incluso ha sugerido esta estrategia sobre la tamización con citología seguida de colposcopia, con o sin biopsia.
La revisión seleccionada no contempló esta tecnología dentro de sus comparaciones, pero uno de los ensayos clínicos aleatorizados incluidos en esta revisión, también comparó las pruebas de VIA con el escenario de cuidado estándar, es decir con no tamizar, y fue revisado como fuente de evidencia. Adicionalmente, otro estudio del mismo autor fue referido por un experto clínico del grupo desarrollador de la guía y fue también incluido.
El ensayo incluido en la revisión, estudio realizado en la India (8), no mostró reducción ni en incidencia de cáncer cervical en todos los estadios, ni en estadios avanzados con la tamización con VIA comparado con no tamizar en un seguimiento de 8 años.
En mortalidad mostró una reducción, pero no fue estadísticamente significativa. La citología mostro reducciones solo en incidencia de estadios avanzados y mortalidad, pero tampoco significativas. La prueba de ADN-VPH mostró reducciones en los mismos desenlaces que la citología, pero éstas si significativas.
Comparada directamente con citología, la tamización con VIA mostró
Reducciones en incidencia de todos los estadios y mortalidad, pero no significativas. Comparada directamente con ADN-VPH, se encontró reducción de incidencia de todos los estadios, de estadios avanzados y de mortalidad, todas a favor de las pruebas de ADN-VPH, y solo significativas en las dos últimas.
El estudio referido por un experto, también realizado en la India por el mismo autor (7), en donde solo se comparó la tamización basada en VIA con no tamizar, mostró reducciones significativas en un seguimiento de 6 años tanto en incidencia de cáncer cervical en todos los estadios como en mortalidad por esta enfermedad.
En estadios avanzados la reducción no es significativa. Adicionalmente en un análisis por subgrupos de edad se encontró que en el grupo de 30 a 39 años las reducciones en incidencia en todos los estadios, en estadios avanzados y en mortalidad, son mayores y estadísticamente significativas. En los grupos de 40 a 49 años, y de 50 a 59 años, también se observaron reducciones en los mismos desenlaces, pero ninguna estadísticamente significativa.
En nuestro escenario, las pruebas de inspección visual se realizan usando además del ácido acético, lugol para la emisión de un diagnóstico y la definición de tratamiento, definida ésta prueba como VIA-VILI.
Comparación 4: Pruebas de mARN-VPH versus citología, pruebas de ADN-VPH y VIA
No se encontró evidencia para esta comparación respecto a los desenlaces de interés, ni en revisiones sistemáticas, ni en estudios primarios. La evidencia existente solo reporta desenlaces sobre rendimiento de las pruebas de mARN.
Prueba de tamización definida
Teniendo en cuenta los resultados encontrados, tanto en datos combinados como en estudios primarios, se considera que existe evidencia suficiente a favor de la tamización con pruebas de ADN-VPH, y que la edad de inicio debe ser los 30 años, dados los resultados significativos encontrados a partir de esta edad. La edad de finalización en los estudios de los que se extrajo la evidencia no supera los 60 años, pero debe evaluarse el riesgo diferencial de NIC en edades mayores.
El intervalo de tamización en el que se lograron resultados significativos va de 3 a 5 años. La guía de la OMS también recomienda un intervalo de 5 años frente a resultados negativos de las pruebas de ADN-VPH.
Intervalo de tamización
Una cohorte europea (21) mostró resultados respecto al valor predictivo negativo de las pruebas de ADN-VPH en un seguimiento de 6 años. Mujeres con citología positiva y VPH negativo tuvieron una incidencia acumulada para NIC 3 o mayor de 2,7% (0,6%-6,0%); mujeres con citología negativa y VPH negativo tuvieron bajo riesgo de futuro NIC 3 o mayor (0,28%, 0,10%-0,47%).
A los seis años de seguimiento, la tasa de NIC 3 o mayor fue significativamente menor entre las mujeres negativas para VPH (0,27%, 0,12%-0,45%) que entre las mujeres con resultados citológicos negativos (0,97%, 0,53% y 1,34%). Una pequeña diferencia fue observada en las tasas de NIC 3 o mayor entre las mujeres con resultados negativos en ambas pruebas y mujeres negativas para VPH.
Comparación 5: Prueba de clasificación diagnóstica (triage) frente a resultados positivos de ADN-VPH
Ningún resultado específico sobre el triage de mujeres positivas fue reportado en revisiones sistemáticas. La guía de la OMS sugiere realizar triage de mujeres con resultados positivos de VPH con VIA y tratamiento inmediato sobre las estrategias de tamizar solo con VPH o con VIA y tratar inmediatamente.
Un ensayo clínico aleatorizado realizado en Finlandia fue seleccionado como evidencia sobre la prueba de triage adecuada
Para clasificar mejor a mujeres con resultados positivos de VPH (19, 22). Los resultados mostraron que hubo una tasa relativa significativamente mayor de NIC 3 o mayor, desenlace compuesto entre cáncer cervical, adenocarcinoma in situ y NIC 3, en el grupo de VPH y triage con citología, tanto al realizar el análisis en la totalidad de mujeres invitadas a la tamización, como al realizar el análisis solo con las mujeres que atendieron a la tamización.
La tasa relativa de cáncer cervical solo fue mayor en el grupo de VPH y triage con citología, entre las mujeres que fueron tamizadas, pero no significativamente, al igual que las tasas relativas de adenocarcinoma in situ, tanto en invitadas como en tamizadas.
La tasa relativa de NIC 3 fue significativamente mayor, tanto en invitadas como en tamizadas, en el grupo de VPH y triage con citología. Hubo más mujeres con resultados de NIC en la tamización en el grupo de pruebas de VPH y triage con citología que en el grupo de citología convencional (110 Vs 72), así como más mujeres con recomendación de siguientes pruebas de tamización como control (1244 Vs 1053).
Entre las mujeres con resultados negativos en la tamización, la tasa relativa de NIC 3 o mayor fue ligeramente menor en el grupo de VPH y triage con citología.
Estos resultados muestran que un programa bien establecido de tamización, basado en pruebas de VPH y triage con citología, es más sensible que la citología convencional en la detección de NIC 3 o mayor.
Un estudio que evaluó 14 estrategias de triage para mujeres VPH positivas en el 2012 (23)
Concluyó que la estrategia más atractiva era triage con citología al inicio del estudio, seguido por repetición de la citología a los 12 meses, con una tasa global de remisión a colposcopia de la población total de 1,70 (IC 95% 1,54–1,85) y un VPN del 99,3% (IC del 95%: 98,1-99,8%).
Otros estudios también soportan el uso de la citología como triage para las pruebas de VPH positivas, mostrando menor tiempo a la colposcopia (mediana de 11 meses) en comparación con solo citología (mediana de 3 meses) (24), y mostrando incrementos en la sensibilidad para NIC 3 o mayor hasta en un 30% comparado con citología sola (IC 95 9-54%), con un sostenimiento de un alto VPP (VPP relativo 0.87, IC 95% 0,60-1,26), y solo con un incremento del 12% en el número de pruebas de detección (25).
Un estudio comparó el uso de citología y VIA como pruebas de triage frente a resultados positivos de VPH y no encontró diferencias significativas en cuanto a remisión a colposcopia (62% y 59%, respectivamente, p=0,012), por lo que sugiere que la selección de una u otra prueba depende de la disponibilidad y asequibilidad en cada escenario (26).
3.1.3 De la evidencia a la recomendación
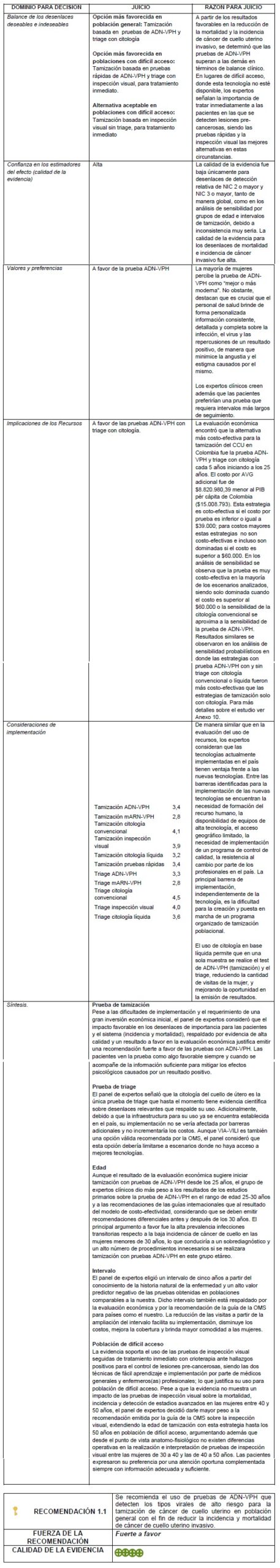
Detalles de la recomendación
La implementación de esta tecnología deberá realizarse dentro del marco de un programa organizado de tamización con cumplimiento de indicadores de cobertura, calidad y seguimiento, y un sistema de vigilancia de los mismos. Asimismo, debe garantizarse el acceso a la clasificación y confirmación diagnóstica y el tratamiento oportuno de las mujeres con resultados positivos.
No se sugiere hacer genotipificación para tipos virales específicos de alto riesgo.
No se sugiere hacer detección de tipos virales de bajo riesgo.
Las pruebas de ADN-VPH que se sugiere utilizar en la tamización son aquellas que cuenten con estudios de validación clínica.
Se debe realizar triage de resultados positivos independiente del reporte de genotipificación, dado que, sin importar el tipo viral, el manejo de los positivos debe ser el mismo.
Las pruebas de auto-toma pueden ser usadas como estrategia para incrementar la cobertura, cuando la toma por profesionales sea una barrera.
Cuando se utilicen técnicas de captura de híbridos, se deben utilizar los puntos de corte definidos por el fabricante para establecer positividad en las pruebas de ADN-VPH para tipos de alto riesgo.
Necesidades de investigación
Las nuevas pruebas de ADN-VPH a ser implementadas en el país deberán contar con validación clínica cuyo rendimiento iguale o supere a las tecnologías ya validadas.
Una vez puesta en marcha la recomendación se requieren estudios prospectivos para medir los desenlaces de las estrategias en nuestra población.
Se esperan los resultados a largo plazo de las cohortes de niñas vacunadas para conocer el impacto de esta estrategia de prevención primaria en la tamización.
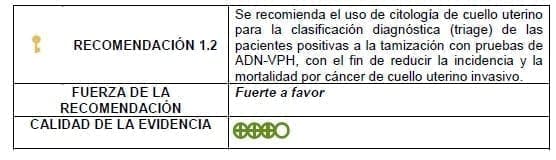
Detalles de la recomendación
Es aceptable el uso de citología convencional o, si está disponible, la citología en base líquida, las cuales se recomienda tomar en el mismo momento de la prueba ADN-VPH con el fin de disminuir el número de visitas; pero sólo se procesarán si la prueba de tamización es positiva.
Las mujeres positivas al triage deben ser referidas a colposcopia y biopsia según hallazgos, en unidades de patología cervical habilitadas.
Las mujeres negativas al triage deben tener recomendación de nueva prueba de ADN-VPH en 18 meses con el objetivo de evaluar persistencia de la infección.
Las citologías tomadas como pruebas de triage deberán ser incluidas en el sistema de control de calidad.
Debe garantizarse el acceso a la confirmación diagnóstica y el tratamiento oportuno de las mujeres con resultados positivos.
Se considera triage positivo un hallazgo citológico de ASC-US o mayor.
Necesidades de investigación
Una vez puesta en marcha la recomendación se requieren estudios prospectivos para medir los desenlaces de las estrategias en nuestra población.

Detalles de la recomendación
La tamización solo se deberá realizar en mujeres que hayan iniciado actividad sexual.
En mujeres mayores de 65 años, la finalización de la tamización debe estar condicionada a la verificación de una prueba de tamización negativa al menos en los últimos 5 años.
Necesidades de investigación
Una vez puesta en marcha la recomendación se requieren estudios prospectivos para medir los desenlaces de las estrategias en nuestra población.
Se esperan los resultados a largo plazo de las cohortes de niñas vacunadas para conocer el impacto de esta estrategia de prevención primaria en la edad de inicio de tamización.

Detalles de la recomendación
En el caso del uso de pruebas rápidas o auto-toma se deberá realizar la tamización cada tres (3) años ante resultados negativos.
Necesidades de investigación
Una vez puesta en marcha la recomendación se requieren estudios prospectivos para medir los desenlaces de las estrategias en nuestra población.
Se esperan los resultados a largo plazo de las cohortes de niñas vacunadas para conocer el impacto de esta estrategia de prevención primaria en los intervalos de tamización.
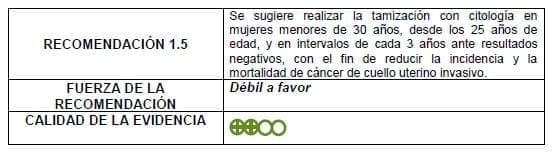
Detalles de la recomendación
No son claros los beneficios de iniciar tamización para cáncer de cuello uterino antes de los 25 años de edad. Teniendo en cuenta la muy baja incidencia de cáncer y lesiones precancerosas en estre grupo de edad, los expertos sugieren no realizar tamización como parte de un programa poblacional organizado, dejando a criterio del experto clínico ofrecer un diagnóstico de oportunidad con citología.
Es aceptable el uso de citología convencional para la tamización entre los 25 y 30 años de edad. El uso de la citología en base líquida es también aceptable donde la tecnología y los recursos para su implementación estén disponibles.
Se considera positivo a la tamización un hallazgo citológico de ASC-US o mayor.
El hallazgo de ASC-US en la citología debe ser confirmado con un prueba de ADN-VPH. Si esta es positiva, debe realizarse colposcopia, y si es negativa se continúa con el esquema de tamización de rutina para su grupo etáreo.
El hallazgo de LEI-BG o mayor en la citología debe ser confirmado directamente con colposcopia.
Si la citología es reportada como insatisfactoria, ésta debe repetirse en un tiempo no mayor a 30 días.
Debe garantizarse el acceso a la confirmación diagnóstica y el tratamiento oportuno de las mujeres con resultados positivos.
Necesidades de investigación
Una vez puesta en marcha la recomendación se requieren estudios prospectivos para medir los desenlaces de las estrategias en nuestra población.

Detalles de la recomendación
Cuando exista la disponibilidad de las pruebas rápidas de ADN-VPH, la tamización se realizará en primer lugar con estas pruebas, y ante un resultado positivo, se deben realizar inmediatamente (en la misma visita) las pruebas de inspección visual, que determinarán la realización o no de tratamiento inmediato.
Frente a resultados negativos, ya sea de las pruebas rápidas de ADN-VPH o de las pruebas de inspección visual, el intervalo de repetición de las pruebas no debe ser superior a 3 años.
Población mayor de 50 años, considerada como población de difícil acceso a los servicios de salud, deberá ser tamizada con citología cervico uterina o pruebas rápidas de ADN-VPH según disponibilidad y remisión a ginecología para tratamiento indicado, frente a resultados positivos.
Población menor de 30 años, considerada como población de difícil acceso a los servicios de salud, deberá ser tamizada con la mejor tecnología disponible, siguiendo las mismas recomendaciones definidas para población general.
Necesidades de investigación
Una vez puesta en marcha la recomendación se requieren estudios prospectivos para medir los desenlaces de las estrategias en nuestra población.
Referencias
- 1. Miller AB. Conundrums in screening for cancer. International journal of cancer Journal international du cancer. 2010;126(5):1039-46.
- 2. Quinn M, Babb P, Jones J, Allen E. Effect of screening on incidence of and mortality from cancer of cervix in England: evaluation based on routinely collected statistics. BMJ (Clinical research ed). 1999;318(7188):904-8.
- 3. Almonte M, Murillo R, Sanchez GI, Jeronimo J, Salmeron J, Ferreccio C, et al. [New paradigms and challenges in cervical cancer prevention and control in Latin America]. Salud publica de Mexico. 2010;52(6):544-59.
- 4. Cuzick J, Bergeron C, von Knebel Doeberitz M, Gravitt P, Jeronimo J, Lorincz AT, et al. New technologies and procedures for cervical cancer screening. Vaccine. 2012;30 Suppl 5:F107-16.
- 5. Schiffman M, Wentzensen N, Wacholder S, Kinney W, Gage JC, Castle PE. Human papillomavirus testing in the prevention of cervical cancer. Journal of the National Cancer Institute. 2011;103(5):368-83.
- 6. Cuzick J, Cadman L, Mesher D, Austin J, Ashdown-Barr L, Ho L, et al. Comparing the performance of six human papillomavirus tests in a screening population. British journal of cancer. 2013;108(4):908-13.
- 7. Sankaranarayanan R, Esmy PO, Rajkumar R, Muwonge R, Swaminathan R, Shanthakumari S, et al. Effect of visual screening on cervical cancer incidence and mortality in Tamil Nadu, India: a cluster-randomised trial. Lancet. 2007;370(9585):398-406.
- 8. Sankaranarayanan R, Nene BM, Shastri SS, Jayant K, Muwonge R, Budukh AM, et al. HPV screening for cervical cancer in rural India. N Engl J Med. 2009;360(14):1385-94.
- 9. INC. Recomendaciones para la tamización de neoplasias del cuello uterino en mujeres sin antecedentes de patología cervical (preinvasora o invasora) en Colombia. 2007.
Bibliografías
- 10. Cox JT, Castle PE, Behrens CM, Sharma A, Wright TC, Jr., Cuzick J. Comparison of cervical cancer screening strategies incorporating different combinations of cytology, HPV testing, and genotyping for HPV 16/18: results from the ATHENA HPV study. American journal of obstetrics and gynecology. 2013;208(3):184.e1-.e11.
- 11. Wiesner Ceballos C, Acosta Peñaloza JA, Díaz del Castillo A, Tovar Murillo S, Salcedo Fidalgo H. Efectos psicológicos y sociales que genera la prueba del virus del papiloma humano: un estudio exploratorio. RCCAN Revista Colombiana de Cancerología. 2009;13(3):145-56.
- 12. Dickinson J, Tsakonas E, Conner Gorber S, Lewin G, Shaw E, Singh H, et al. Recommendations on screening for cervical cancer. Cmaj. 2013;185(1):35-45.
- 13. WHO Guidelines Approved by the Guidelines Review Committee. WHO Guidelines for Screening and Treatment of Precancerous Lesions for Cervical Cancer Prevention. Geneva: World Health Organization Copyright (c) World Health Organization 2013.; 2013.
- 14. Wilkinson J, Bass C, Diem S, Gravley A, Harvey L, Hayes R, et al. Preventive services for adults. Institute for Clinical Systems Improvement. 2012.
- 15. Saslow D, Solomon D, Lawson HW, Killackey M, Kulasingam SL, Cain J, et al. American Cancer Society, American Society for Colposcopy and Cervical Pathology, and American Society for Clinical Pathology screening guidelines for the prevention and early detection of cervical cancer. CA Cancer J Clin. 2012;62(3):147-72.
- 16. Pileggi C, Flotta D, Bianco A, Nobile CG, Pavia M. Is HPV DNA testing specificity comparable to that of cytological testing in primary cervical cancer screening? Results of a meta-analysis of randomized controlled trials. Int J Cancer. 2014;135(1):166-77.
Fuentes
- 17. Murphy J, Kennedy EB, Dunn S, McLachlin CM, Fung Kee Fung M, Gzik D, et al. HPV testing in primary cervical screening: a systematic review and meta-analysis. J Obstet Gynaecol Can. 2012;34(5):443-52.
- 18. Ronco G, Giorgi-Rossi P, Carozzi F, Confortini M, Dalla Palma P, Del Mistro A, et al. Efficacy of human papillomavirus testing for the detection of invasive cervical cancers and cervical intraepithelial neoplasia: a randomised controlled trial. Lancet Oncol. 2010;11(3):249-57.
- 19. Anttila A, Kotaniemi-Talonen L, Leinonen M, Hakama M, Laurila P, Tarkkanen J, et al. Rate of cervical cancer, severe intraepithelial neoplasia, and adenocarcinoma in situ in primary HPV DNA screening with cytology triage: randomised study within organised screening programme. BMJ. 2010;340:c1804.
- 20. Siebers AG, Klinkhamer PJ, Grefte JM, Massuger LF, Vedder JE, Beijers-Broos A, et al. Comparison of liquid-based cytology with conventional cytology for detection of cervical cancer precursors: a randomized controlled trial. JAMA. 2009;302(16):1757-64.
- 21. Dillner J, Rebolj M, Birembaut P, Petry KU, Szarewski A, Munk C, et al. Long term predictive values of cytology and human papillomavirus testing in cervical cancer screening: joint European cohort study. BMJ. 2008;337:a1754.
- 22. Leinonen MK, Nieminen P, Lönnberg S, Malila N, Hakama M, Pokhrel A, et al. Detection rates of precancerous and cancerous cervical lesions within one screening round of primary human papillomavirus DNA testing: prospective randomised trial in Finland. BMJ. 2012;345:e7789.
- 23. Rijkaart DC, Berkhof J, van Kemenade FJ, Coupe VM, Hesselink AT, Rozendaal L, et al. Evaluation of 14 triage strategies for HPV DNA-positive women in population-based cervical screening. Int J Cancer. 2012;130(3):602-10.
Lecturas Recomendadas
- 24. Louvanto K, Chevarie-Davis M, Ramanakumar AV, Franco EL, Ferenczy A. HPV testing with cytology triage for cervical cancer screening in routine practice. Am J Obstet Gynecol. 2014;210(5):474.e1-7.
- 25. Naucler P, Ryd W, Törnberg S, Strand A, Wadell G, Elfgren K, et al. Efficacy of HPV DNA testing with cytology triage and/or repeat HPV DNA testing in primary cervical cancer screening. J Natl Cancer Inst. 2009;101(2):88-99.
- 26. Muwonge R, Wesley RS, Nene BM, Shastri SS, Jayant K, Malvi SG, et al. Evaluation of cytology and visual triage of human papillomavirus-positive women in cervical cancer prevention in India. Int J Cancer. 2014;134(12):2902-9.
- 27. Ferlay J, Soerjomataram I, Dikshit R, Eser S, Mathers C, Rebelo M, et al. Cancer incidence and mortality worldwide: Sources, methods and major patterns in GLOBOCAN 2012. Int J Cancer. 2014.
- 28. Vizcaino AP, Moreno V, Bosch FX, Muñoz N, Barros-Dios XM, Parkin DM. International trends in the incidence of cervical cancer: I. Adenocarcinoma and adenosquamous cell carcinomas. Int J Cancer. 1998;75(4):536-45.
- 29. Madeleine MM, Daling JR, Schwartz SM, Shera K, McKnight B, Carter JJ, et al. Human papillomavirus and long-term oral contraceptive use increase the risk of adenocarcinoma in situ of the cervix. Cancer Epidemiol Biomarkers Prev. 2001;10(3):171-7.
- 30. Sasieni P, Adams J. Changing rates of adenocarcinoma and adenosquamous carcinoma of the cervix in England. Lancet. 2001;357(9267):1490-3.
- 31. Smith HO, Tiffany MF, Qualls CR, Key CR. The rising incidence of adenocarcinoma relative to squamous cell carcinoma of the uterine cervix in the United States–a 24-year population-based study. Gynecol Oncol. 2000;78(2):97-105.
Referencias Bibliográficas
- 32. Tjalma WA, Fiander A, Reich O, Powell N, Nowakowski AM, Kirschner B, et al. Differences in human papillomavirus type distribution in high-grade cervical intraepithelial neoplasia and invasive cervical cancer in Europe. Int J Cancer. 2013;132(4):854-67.
- 33. Costales AB, Milbourne AM, Rhodes HE, Munsell MF, Wallbillich JJ, Brown J, et al. Risk of residual disease and invasive carcinoma in women treated for adenocarcinoma in situ of the cervix. Gynecol Oncol. 2013;129(3):513-6.
- 34. Kim ML, Hahn HS, Lim KT, Lee KH, Kim HS, Hong SR, et al. The safety of conization in the management of adenocarcinoma in situ of the uterine cervix. J Gynecol Oncol. 2011;22(1):25-31.
- 35. WHO Guidelines Approved by the Guidelines Review Committee. WHO Guidelines: Use of Cryotherapy for Cervical Intraepithelial Neoplasia. Geneva: World Health Organization World Health Organization.; 2011.
- 36. Wu YM, Wang T, He Y, Song F, Wang Y, Zhu L, et al. Clinical management of cervical intraepithelial neoplasia in pregnant and postpartum women. Arch Gynecol Obstet. 2014;289(5):1071-7.
- 37. He Y, Wu YM, Wang T, Song F, Wang Y, Zhu L. Perinatal outcomes of pregnant women with cervical intraepithelial neoplasia. Arch Gynecol Obstet. 2013;288(6):1237-42.
- 38. Schaefer K, Peters D, Aulmann S, Sohn C, Eichbaum MH. Value and feasibility of LLETZ procedures for pregnant women with suspected high-grade squamous intraepithelial lesions and microinvasive cervical cancer. Int J Gynaecol Obstet. 2012;118(2):141-4.
- 39. Preti VB, Hatschbach SB, Linhares JC, Guerreiro JA, Minari CL, Maestri CA, et al. [High-grade cervical intraepithelial neoplasia during pregnancy: experience in a service in southern Brazil]. Rev Bras Ginecol Obstet. 2009;31(12):604-8.
Fuentes Bibliográficas
- 40. Fambrini M, Penna C, Fallani MG, Pieralli A, Mattei A, Scarselli G, et al. Feasibility and outcome of laser CO2 conization performed within the 18th week of gestation. Int J Gynecol Cancer. 2007;17(1):127-31.
- 41. Kaplan KJ, Dainty LA, Dolinsky B, Rose GS, Carlson J, McHale M, et al. Prognosis and recurrence risk for patients with cervical squamous intraepithelial lesions diagnosed during pregnancy. Cancer. 2004;102(4):228-32.
- 42. Palle C, Bangsbøll S, Andreasson B. Cervical intraepithelial neoplasia in pregnancy. Acta Obstet Gynecol Scand. 2000;79(4):306-10.
- 43. Koh WJ, Greer BE, Abu-Rustum NR, Apte SM, Campos SM, Cho KR, et al. Cervical cancer, version 2.2015: Featured updates to the NCCN guidelines featured updates to the NCCN guidelines. JNCCN Journal of the National Comprehensive Cancer Network. 2015;13(4):395-404.