El camino al futuro para el tratamiento del cáncer de próstata avanzado comenzó muy recientemente. Ya que hasta los años 70 no se iniciaron los estudios para conocer los mecanismos moleculares que llevan a la hormonoresistencia.
Existía muy poco conocimiento de la genética tumoral prostática y la terapia antiangiogénica era en esos momentos vista como una posibilidad nula en el tratamiento de las entidades oncológicas. Las terapias inmuno-oncológicas no existían y la terapia génica apenas comenzaba su investigación.
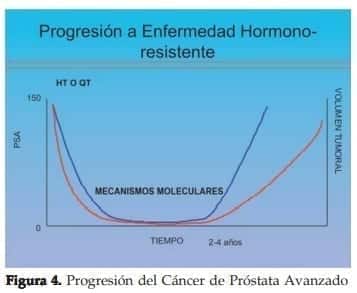
Estas son las alternativas de tratamiento que van a cambiar la historia natural de la enfermedad de alto riesgo y como se demuestra en la figura . A medida que podamos incluir estos esquemas de tratamiento en la historia natural de la progresión de la enfermedad. Podremos pasar la curva azul hacía la curva roja y así mejorar tanto la calidad de vida y sobrevida de estos pacientes.
Vitamina D
Calcitriol, la forma activa de la Vitamina D, tiene efectos importantes sobre células cancerosas, incluyendo inducción de diferenciación, arresto del ciclo celular y apoptosis. Basado en este perfil de actividades el calcitriol ha sido extensamente estudiado como agente único o en combinaciones en el tratamiento del CapHR.
Los trabajos iniciales tuvieron serios problemas de hipercalcemias. Pero con la adición de esteroides y administrándose en dosis intermitentes se disminuyeron estos efectos colaterales.
Los estudios fase II demostraron una mejoría del PSA en mas de un 50 % con la combinación de docetaxel mas calcitriol. Pero los estudios fase III, confirmatorios, aún no se han reportado15.
(Lea También: Argumento para una Preservación Selectiva de la Vejiga en Cáncer T2A de Alto Grado)
Terapia Antiangiogénica
Al Dr. Judah Folkman, le debemos el concepto que el crecimiento tumoral depende de los nutrientes que le aportan al tumor los vasos sanguíneos.
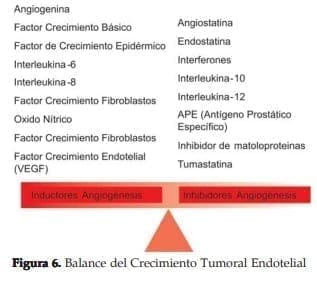
Con base en este concepto se desarrollaron las estrategias farmacológicas que inhibieran el desarrollo endotelial tumoral o la angiogénesis tumoral y así convertir el cáncer de próstata como ocurre en otras malignidades en una “enfermedad Crónica”. El balance de los factores angiogénicos y los antiangiogénicos nos permitirán manipular el crecimiento tumoral en varias fases de la enfermedad16. Figuras 5 y 6.
 |
 |
La terapia antiangiogénica tumoral prostática tuvo sus inicios con la inserción de la Talidomida en su metabolito activo como tratamiento complementario al Docetaxel, con resultados prometedores en estudios fase II, en donde se demostró mayor descenso del PSA en pacientes con CaPHR17.
Existen otras moléculas que han sido estudiadas en estudios pilotos, teniendo como premisa el balance mencionado en la figura 6, como la Trombospondina-I, Inhibidores del Receptor de Tirosina y los bloqueadores Alfa, todos logrando efectos en la inhibición del VEGF (factor de crecimiento endotelial) y del EGF (Factor de Crecimiento Epidermoide), factores que se expresan en mayores concentraciones en tejidos con CaPHR y así intentando lograr control de los pacientes en la fase de Hormonoresistencia18.
Moléculas que están siendo estudiadas en estudios Fase II y III en combinaciones con el Docetaxel o entre sí como el Atrasentan (Potente inhibidor de la Endotelina-I, el Bevacizumab (Avastin) y el MEDI 522 (Bloquea el receptor de Fibronectina) están demostrando mejorías en las cifras de sobrevida y control de los niveles de APE19,20,21.
Vacunas y Estimulantes Inmunológicos
Las alternativas inmunoterapéuticas están basadas en la premisa que si el sistema inmune se estimula o se moviliza adecuadamente, va a poder erradicar células malignas. Las estrategias de estimular el sistema inmune varían desde el uso de agentes inespecíficos como las Vacunas de Células Completas hasta agentes muy específicos como las vacunas contra la Prosterna, un tipo de APE.
En cuanto al a movilización del sistema inmune, también este varía desde el uso de células T y respuestas humorales inespecíficas hasta el uso de tipos celulares específicos como el uso de células dendríticas.
Los trabajos con este tipo de alternativas terapéuticas se enfrentan a tres grandes problemas: 1.) Las células prostáticas producen grandes cantidades de Factor Transformante de Crecimiento Beta, un potente inmunosupresor.
Los Antígenos de Histocompatibilidad tipo I, que son vitales para el reconocimiento de una respuesta inmune, son defectuosos en el tejido prostático maligno y por último 3.) Defectos en el receptor de la célula T se manifiesta en el tejido de pacientes con CaPHR22.
A pesar de estas dificultades técnicas propias de la enfermedad, existen trabajos en fase I y II con diferentes componentes como: GM-CSF (GVAX), Sipulevcel-T (Provenge), PROSTVAC y PROSTVAC-F TRICOM que como vacunas o estimulantes del sistema inmune están siendo estudiados como agentes únicos o como adyuvantes del Docetaxel en pacientes en diferentes estadios de la enfermedad hasta la hormoresistencia23,24.
Terapia Génica
La Terapia Génica tiene como objetivo final el lograr un tratamiento oncológico altamente eficaz y específico, produciendo el menor daño en las células sanas del órgano comprometido. Esto se logra mediante la manipulación de Oncogenes y Genes Supresores, y así lograr destrucción tumoral utilizando vectores de transferencia.
La primera estrategia terapéutica génica es la terapia génica correctiva, en donde se intenta corregir genes defectuosos. Aunque todavía no hay estudios diferentes a los preclínicos que demuestren que la corrección de un solo gen pueda tener efectos benéficos en el tratamiento del Cáncer de Próstata.
La segunda estrategia es la de lograr destrucción tisular mediante el uso de virus oncolíticos. La tercera y última estrategia es la de inducir una respuesta inmune antitumoral en el huésped18.
El método ideal de transporte de esta terapia génica debería ser el transporte de esta información genética directamente al órgano afectado. Sin producir efectos colaterales serios en el paciente en casos de enfermedad localizada y de manera sistémica en casos de enfermedad metastásica.
La aplicación local de estas estrategias es relativamente fácil, debido al uso de la ecografía transrectal y la Resonancia Nuclear Magnética para tales fines. Cada Vía de administración tiene sus ventajas y desventajas y las investigaciones actuales están siendo dirigidas al mejoramiento de los sistemas de transporte de estos vectores25.
De todos los protocolos de Terapia Génica Oncológica inscritos actualmente, el 15% corresponden a protocolos para cáncer de próstata. Se tienen protocolos de terapia génica tanto correctiva y citoreductora.
Las estrategias futuras son las de lograr una adecuada multiplicación del véctor viral de transporte. La supresión del sistema inmune del huésped para así evitar la desactivación del vector viral, disminuir los tiempos terapéuticos para así lograr mejorar su eficacia y seguridad26.
Papel del Urólogo en el Tratamiento Futuro del Cáncer de Próstata
Es claro que el adecuado tratamiento actual del paciente con enfermedad de Alto Riesgo o Enfermedad Avanzada debe ser con grupos multidisciplinarios y dichos grupos deben ser liderados por nosotros los URÓLOGOS.
Este liderazgo deber estar marcado por el conocimiento perfecto de la historia natural de esta enfermedad desde su inicio hasta el desarrollo de la enfermedad hormonoresistente para referenciar los pacientes en el momento correcto a los especialistas de apoyo (Oncólogo Clínico, Radioterapeuta, Terapista del Dolor, Nutricionista, Psicólogo, etc).
Por último los urólogos nacionales debemos tener conocimiento de los diferentes protocolos de investigación internacionales para así poder tener la oportunidad de enrolar nuestros pacientes en estas novedosas alternativas terapéuticas.
Por último, frases de destacados Cirujanos Urólogos Oncólogos como la siguiente del difunto Dr. William Fair en el MSKCC de Nueva York en octubre del 2006: “Doctores Residentes, traten de realizar todas las prostatectomías radicales posibles, ya que en treinta años la dieta y la terapia génica acabará con el Cáncer de Próstata”, eran solo una advertencia del conocimiento que debemos tener sobre esta enfermedad para así mantenernos en la carrera por ser los líderes en su tratamiento.
Bibliografía
- 1. Jemal A, Murray T, Ward E, Cancer Statistics, 2005, Cancer 2005;55:10
- 2. D´Amico A, Kantoff P, et al, Report to the nation on Advanced Prostate Cancer, September 2005, Medscape-Hematology
- 3. Johanson Jan-Erik et al, Radical Prostatectomy Vs Watchful waiting in Localized prostate Cancer, N Engl J Med 2005;352:1977-1984
- 4. Thompson I.M., Goodman W, et al, The Influence of Finasteride in Developing Prostate Cancer, N Engl J Med 2003; 349:215-224
- 5. Gleave M, So A.I, et al, Effect of time of Castration and Tumor Volume and the developing of androgen resistance in th Shionogui Tumor Model BJU International, Vol 93, Pag 45, April 2004
- 6. Tannock IF, de Wit R, Berry WR, et al: Docetaxel plus prednisone or Mitoxantrone plus prednisone for advanced prostate cancer. N Engl J Med 351: 1502-1512,2004
- 7. Carducci P, Carroll P, et al: Multisciplinary Management of Advanced prostate Cancer: Changing Perspectives. UROLOGY 65 (Suppl 5A):18-22, 2005
- 8. Smith BR et al: Log Term Side Effects of Androgen Supresión; JCEM 87, 599-603, 2004
- 9. Bruchovsky N, Gleave M, Lange P, et al: Intermitent Androgen Supresión Delays Progresión to Androgen Independent Regulation en th LNCap prostate cancer model.J. Steroid, Biochemistry, and Molecular Biology, Vol 58, Issue 2, 139-146, 1996
- 10. Goldenberg L, et al: Intermitent Androgen Supresión in Advanced prostate Cancer Delays Progresión to Hormonoe refractory Disease a preliminary report; Urology, Vol 45, 839-44, 1995.
- 11. SWOG-9346, Southwest Oncology Group Stage IV Prostate Cancer-Intermitent Androgen Suppression Trial
- 12. Gilbert S, Mckierman J: The Role of Biphosphanates in Preventing Skeletal Complications of Hormonal Tharapy; Urol Clin N Am, 33 (2006) 191-199
Referencias
- 13. Petrilak Daniel: The Current Role of Chemotherapy in Metastatic Hormona-Refractory Prostate Cancer; UROLOGY 65 (Suppl 5A):3-8, 2005
- 14. Derek Raghavan-Chemotherapy for Advanced Prostate Cancer:State of the Art Lectur-AUA 2006
- 15. Beer TM et al., Weekly high dose calcitriol and Dpocetaxel in metastastati andorgen-independent prostate cancer, J.Clin. Oncology 21: 123-128, 2003
- 16. Folkman J. Tumor angiogenesis: therapeutic implications. N Eng J Med 1971; 285:1182
- 17. Dahut WL, et al: Randomized Phase II Trial of Docetaxel + Thalidomide in Hormone Refractary Prostate Cancer. J. Clin. Oncology 22: 2532-2539, 2004
- 18. Desai Patrick, et al, Future Innovations in treating Prostate Cancer, Urol. Clin. N Am., 33, 2006, 247-272
- 9. Picus et al., ASCO 2003 # 1578: Docetaxel + Bevacizumab: Phase II Trial
- 20. Ning et al, ASCO 2006 # 13037: Docetaxel + Bevacizumab + Thalidomide: Phase II Trial
- 21. Pratt et al, Study of Docetaxel + Placevo Vs. Docetaxel + Atrasentan in HRPC (SO421)
- 22. Smith M, Nelson J, Future Therapies in Hormone-refractory Prostate Cancer UROLOGY 65 (Suppl 5A) 9-17 2005
- 23. Prostate Cancer Vaccine Protocol G9803-NCI
- 24. Rini et al, GM-CSF alone alters PSA Kinetics in patients with rising PSa after definitive local therapy. J Clin Onology 21:99-105, 2003
- 25. Allay JA, Steiner MS, Zhang Y, et al. Adenovirus p16 gene therapy for prostate cancer. World J Urol 2000;18:111.
Enviado para publicación: Noviembre de 2006
Aceptado para publicación: Noviembre de 2006