Structural and functional aspects of vitamin E
Lilia Yadyra Cortés,1* Carlos Corredor,2* Ludis Morales.3*
Resumen
Aun cuando desde 1922 se reconoce a la vitamina E como nutriente esencial para el humano, solo hasta años recientes las investigaciones han demostrado que sus funciones van más allá de la capacidad antioxidante; modulan señalización celular y expresión génica.
El término vitamina E cobija 8 isómeros (4 tocoferoles y 4 tocotrienoles). Luego de ser absorbida a nivel intestinal, la vitamina E es transportada en los quilomicrones, sobre los cuales actúa la lipoproteína lipasa (LPL) librando parte de ella a los tejidos extrahepáticos.
Los remanentes de quilomicrón llevan la vitamina restante al hígado, en donde por acción de la proteína transportadora de a-tocoferol (a-TTP), este se incorpora a las VLDL. La vitamina E se metaboliza de forma similar a los xenobióticos: inicialmente es w-oxidada por el citocromo P450, luego sufre varias b-oxidaciones; y por último, conjugada y excretada. Como resultado, las concentraciones de vitamina E son finamente reguladas evitando efectos de toxicidad.
Palabras clave: Vitamina E, tocoferol, tocotrienol, a-TPP, metabolismo.
Abstract
Although Vitamin E has been known as an essential nutrient since 1922, only recently has research shown that its functions go beyond antioxidation: it also modulates cell signaling pathways and gene expression.
The term vitamin E refers to eight isomers: four tocopherols and four tocotrienols. After intestinal absorption, vitamin E is transported in chylomicrons. Lipoprotein lipase (LPL) action on these chylomicrons frees part of the transported vitamins to be incorporated into extrahepatic tissues.
The remaining portion of the vitamins is transported to the liver where action of alpha-tocopherol transfer proteins (α-TPP) allows it to be incorporated into very-low-density-lipoproteins (VLDL). Similar to xenobiotics, vitamin E is metabolized through initial ω-oxidation by cytochrome P450, and then undergoes several rounds of β-oxidation after which it is conjugated and excreted. As a result, liver vitamin E concentrations are closely regulated, limiting potential toxic effects of vitamin E.
Key words: Vitamin E, tocopherol, tocotrienol, α-TPP, metabolism.
Introducción
La vitamina E fue descubierta hace casi 100 años y se le conoce como uno de los principales factores alimentarios necesarios para el buen funcionamiento del organismo, y en la prevención de numerosas patologías.
Sin embargo, la principal acción que se le ha atribuido es la de funcionar como un escudo protector de las membranas celulares para evitar el deterioro por los radicales libres que contienen oxígeno y que pueden resultar tóxicos y cancerígenos.
La vitamina E no se presenta en una sola estructura química sino como dos conjuntos de compuestos formados por una estructura básica, que difieren en el número y posición de los sustituyentes del anillo aromático y en la saturación de su cadena lateral.(1)
Son precisamente las características estructurales las que hacen que la actividad biológica y la capacidad antioxidante de la vitamina E no sean iguales para las diversas formas.
Por tener una estructura altamente hidrofóbica y en consecuencia ser liposoluble, esta vitamina necesita un sistema de transporte en los sistemas acuosos como plasma y líquidos corporales. Y por lo tanto se transporta en las lipoproteínas, particularmente asociada a lipoproteínas de baja densidad.
Formas esterificadas de la vitamina E
Todas las formas esterificadas de la vitamina E son casi completamente hidrolizadas antes de su absorción en el tracto gastrointestinal, y las sales biliares juegan un papel fundamental en esta absorción, que es casi del 50%. El resto es degradado, absorbido y transportado a través de la sangre o excretado en las heces fecales.
La deficiencia de la vitamina E es debida a causas asociadas a metabolitos que no pueden ser sintetizados por el organismo, como son: el no consumo de alimentos que lo contengan o la mala absorción; en este caso, de las grasas.
Se ha observado que un déficit de vitamina E produce distrofia muscular, pérdida de fertilidad y anemia, entre otros. Su exceso, no obstante, al parecer no produce efectos tóxicos masivos.
A pesar del número creciente de artículos en la literatura científica acerca de la vitamina E, sin duda, no es fácil encontrar en un mismo documento información actualizada sobre esta.
Mucho se desconoce aún sobre aspectos tales como utilización y transporte, mecanismos regulatorios de los mismos, así como detalles del mecanismo antioxidante que utiliza en la protección y antienvejecimiento celular.
Esta revisión tiene como propósito recopilar aspectos estructurales y funcionales de la vitamina E, y en particular, la relación entre su compleja estructura y su actividad.
Algo de historia
En 1922, Evans y Bishop describieron un nuevo factor nutricional indispensable para la reproducción normal. El Factor X, como fue denominado inicialmente por ellos, y luego acuñado como vitamina E, fue descubierto luego de alimentar en forma accidental a ratas hembras con grasa rancia y de observar que su deficiencia causaba reabsorción fetal.(2)
La gran diversidad en la vitamina E se empezó a describir en 1936, cuando Evans y Emerson caracterizaron y aislaron dos compuestos con “actividad de vitamina E” del aceite de germen de trigo. Estos compuestos fueron designados como a y b tocoferol, proveniente de la expresión griega tokos (nacimiento) y phorein (acarrear). Posteriormente, Klaus Schwart, en 1965, “redescubrió” la vitamina E llamándola factor 2, y le adjudicó propiedades antioxidantes junto con los aminoácidos azufrados (factor 1) y el selenio (factor 3).(3)
En los años siguientes, se describieron tanto los isó- meros d y g del tocoferol,(4,5) como los tocotrienoles.(6) En 1968, el American Food and Nutrition Board reconoció oficialmente a la vitamina E como un nutriente esencial para el ser humano.
(Lea También: Absorción, transporte, captación celular y metabolismo de la vitamina E)
Aspectos estructurales y propiedades físicas
A diferencia de otras vitaminas que presentan una sola estructura química, bajo el nombre de vitamina E se agrupan dos conjuntos de compuestos químicamente muy similares, que presentan en su estructura básica: tocol ó 2-metil-2-(4´,8´,12´-trimetiltridecil)-6- cromanol. Estos son los tocoferoles (TF) y los tocotrienoles (T3E).
Los tocoferoles poseen una cadena poliprenilo saturada de 16 carbonos y tres centros quirales con configuración R en las posiciones 2, 4´ y 8´ (figura 1).
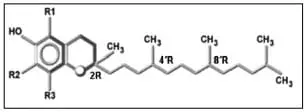
Figura 1. Estructura química del tocofero
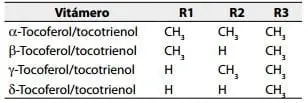
Los tocotrienoles, poseen una cadena isoprenoide con tres insaturaciones en las posiciones 3´, 7´ y 11´ (figura 2). Los miembros dentro de cada conjunto son denominados a, b, g, y d dependiendo del número y de la posición de los grupos metilo sustituyentes del anillo aromático (tabla 1).(7)
 Figura 2. Estructura química del tocotrienol.
Figura 2. Estructura química del tocotrienol.
Tabla 1. Sustituyentes del anillo aromático en la vitamina E. (Tomado de: IUPAC-IUB, 1982).(8)

Debido a que los tocoferoles poseen tres centros quirales, ellos pueden existir como ocho diasteroisómeros agrupados en cuatro pares de enantiómeros. En la naturaleza, el α-TF ocurre en la configuración 2R, 4´R, 8´R por lo cual se llama (2R, 4´R, 8´R)-α-tocoferol o RRR-α-tocoferol (d-α-TF). El diasteroisómero (2S, 4´R-, 8´R)-α-tocoferol fue llamado l-α-TF y, posteriormente, renombrado como 2-epi-α-TF.
En cuanto a los isómeros de los T3E, es importante aclarar que debido a la presencia de los dobles enlaces en las posiciones 3’ y 7’. Estos compuestos solo presentan isómeros de posición y, debido a que poseen un centro quiral en la posición 2, presentan dos estereoisómeros. Los T3E se manifiestan en los alimentos únicamente en la configuración 2R, 3´-trans, 7´-trans. (9)
La vitamina E es la excepción al paradigma de que una vitamina natural y una sintética (5,7-dimetiltocol) son idénticas. La forma presente en la naturaleza, RRRα-tocoferol o d-α-tocoferol, es solo uno de los posibles estereoisómeros. Por el contrario, la forma sintética de vitamina all–rac-α-tocoferol o dl-α-tocoferol como se llamó históricamente, desarrollada de manera comercial como producto de la reacción de trimetilhidroquinona (TMHQ) con isofitol, resulta en una mezcla con igual cantidad de los ocho posibles estereoisómeros (figura 3).(10) Cuatro de los estereoisómeros son formas 2R (RRR-, RSR-, RRS- y RSS-α-TF) y cuatro son 2S (SRR-, SSR-, SRS-, y SSS-α-TF).
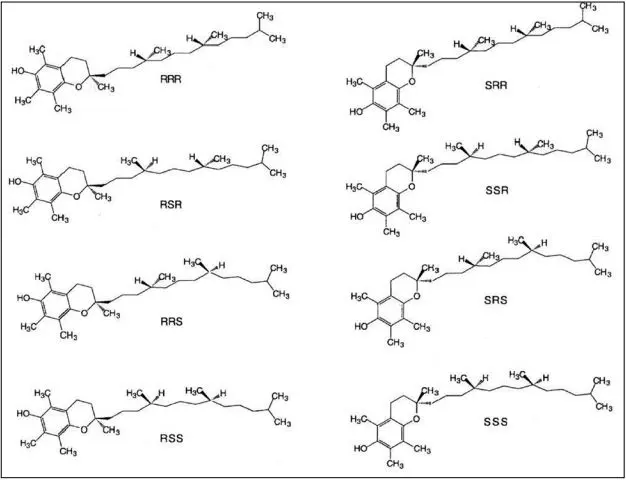
Figura 3. Estereoisómeros de a-tocoferol.
(Tomado de: https://www.nap.edu/openbook/0309069351/html/189.html)
Es importante recalcar que de los ocho estereoisómeros formados, solo 12,5% tiene la conformación encontrada en la naturaleza: RRR-α-TF. Esta forma tiene un punto de fusión de 2,5-3,5 °C, por la cual a temperatura ambiente, el compuesto es un aceite viscoso de color amarillo pálido, soluble en grasa, alcohol y solventes orgánicos no polares pero no en agua. La rotación óptica de estos compuestos es muy pequeña y depende de la naturaleza del solvente.(11) En etanol, su espectro UV muestra picos de absorción en el rango de 292-298 nm con valores de 292, 297, 298 y 298 nm para los isómero sα-, β-, γ- δ d- respectivamente.(9)
Aspectos funcionales
Es de esperarse que las diferencias estructurales conlleven a diferencias en la actividad. La primera actividad reportada para la vitamina E tuvo que ver con la acción biológica descrita como factor de fertilidad en los animales; posteriormente se describió su papel como antioxidante. Por esta razón, la actividad de la vitamina E se ha medido en forma separada en términos de tasa de reabsorción fetal conocida como “actividad biológica” y en términos de “actividad antioxidante”. De acuerdo con estudios de actividad biológica y de remisión de deficiencia en humanos,(12-14) la forma a-TF de la vitamina E es la que mayor actividad biológica presenta (tabla 2)(15) y es la más abundante en la naturaleza.(16)
Tabla 2. Actividad biológica relativa de la vitamina E natural y los estereoisómeros
sintéticos de a-acetato de tocoferilo. (Adaptada de: Azzi, 2000).
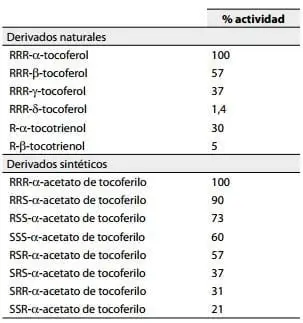
La actividad biológica y la capacidad antioxidante no son iguales para las diversas formas, así sean las producidas naturalmente por las plantas. Mientras que el g-TF forma abundante en la dieta humana, aproximadamente 50% de la capacidad antioxidante de la forma a, solo posee 10% de su actividad biológica.(1,17) Por otro lado, se ha descrito que las formas sintéticas del a-TF, aun cuando poseen diferencias marcadas en su actividad biológica, tienen una capacidad antioxidante similar.(7,18)
No todas las formas sintéticas tienen la misma actividad biológica; los esteroisómeros han sido evaluados utilizando ensayos de reabsorción fetal y se encontró gran diferencia entre su actividad.(10,19) Si se toma la actividad del RRR-a-acetato de tocoferilo como el 100%, las otras formas tienen actividades decrecientes desde 90% en la RRS hasta 21% en la SSR (tabla 2).
El ensayo de reabsorción fetal reportado en la tabla 2 muestra mayor actividad para la forma RRR-α-TF que es la más abundante en la naturaleza. A pesar de que los estereoisómeros sintéticos de α-TF deberían poseer, por lo menos en teoría, iguales propiedades antioxidantes, ellos han demostrado actividad biológica disminuida.
Esto indica que las características estructurales del RRR-a-TF son de vital importancia y que las propiedades antioxidantes de cada forma no reflejan necesariamente la actividad biológica de esta. Un ejemplo de este hecho es que los T3E tienen una capacidad antioxidante 40-60 veces mayor que los TF, pero su papel en la reabsorción fetal no es tan importante.
Actividad biológica de los isómeros de vitamina E
Así pues, las diferencias que se observan en la actividad biológica de los isómeros de vitamina E tienen correspondencia con su estructura. En particular con la presencia o ausencia de grupos metilo en el anillo cromanol, con la estereoquímica de los centros quirales así como con la ramificación o desaturación de la cadena lateral.(7)
Al observar la representación tridimensional de los epímeros R- y S- del a-TF (RRR-α- vs. SRR-a-) se puede ver por qué el cambio en configuración en la posición C2 que tiene un mayor impacto sobre la estructura tridimensional de la molécula (figura 4), se manifiesta como una disminución significativa en la actividad biológica (100% a 31%). La influencia de los otros centros quirales en las posiciones 4´R y 8´R es menos pronunciada y tiene un menor impacto sobre la actividad del correspondiente isómero (tabla 2).
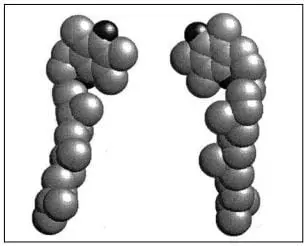
Figura 4. Modelo espacial de la forma RRR-a-tocoferol y su epímero 2S sintético SRR-a-tocoferol
(Tomado con autorización de: Azzi, 2000)
Por último, es importante anotar que la forma comercial de la vitamina E, por lo general, consiste de una mezcla de RRR-α-tocoferol, estereoisómeros sintéticos y sus ésteres. La esterificación se hace en el grupo hidroxilo (OH) presente en el anillo cromanol de la vitamina E y previene la oxidación de la vitamina permitiendo extender su vida útil, por lo cual estos son usados para suplementos y fortificación de alimentos. Al parecer, los ésteres (a-acetato de tocoferilo o a-succinato de tocoferilo) son hidrolizados y absorbidos de manera eficiente.
1 Lilia Yadyra Cortés. Nutricionista Dietista, Magíster en Nutrición clínica y normal, profesora asociada. Candidata a doctorado.
2 Carlos Corredor. Doctor en Bioquímica, profesor titular.
3 Ludis Morales. Química, Doctor en Ciencias, profesora asociada.
* Departamento de Nutrición y Bioquímica – Pontificia Universidad Javeriana, Colombia.
Correspondencia: ycortes@javeriana.edu.co
Recibido: noviembre de 2009
Aceptado para publicación: enero de 2010
RMNC 2010; 1(1): 46-56

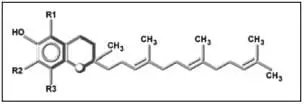 Figura 2. Estructura química del tocotrienol.
Figura 2. Estructura química del tocotrienol.