Herpes Virus como posible Responsable de un Caso de Neumonía, Discusión
La historia clínica anotada muestra la evolución de un paciente con alteración severa de la inmunidad celular, tal como es observada en los pacientes VIH positivos, en los cuales, el deterioro progresivo de su sistema inmune lleva a la presentación de infecciones pulmonares por diversos gérmenes oportunistas como P. carinii, pseudomonas, diversos hongos, virus como Citomegalovirus y herpes y micobacterias como M. tuberculosa o M. avium complex.
Existen dos tipos de Herpes simplex, el tipo I (HSV-1), el cual clásicamente compromete cabeza y cuello y el tipo II (HSV-2) que afecta la región ano-genital. El HSV-1 es muy común y usualmente se disemina por contacto oral; el HSV-2 es de transmisión sexual1. La gran mayoría de infecciones herpéticas suelen ser asintomáticas o asociadas a mínima morbilidad2.
El compromiso pulmonar usualmente ocurre en el terreno de un pulmón previamente lesionado por diferentes causas y generalmente el huésped presenta algún grado de inmunocompromiso como desnutrición crónica, malignidad subyacente, terapia inmunosupresora crónica, SIDA, o quemaduras extensas; puede existir una historia previa de tabaquismo o intubación oro-traqueal prolongada. Las lesiones mucocutáneas preceden o coinciden con las lesiones pulmonares.
Las infecciones diseminadas en adultos son casi siempre fatales y refractarias a la terapia antiviral2. La coinfección – como en el presente caso- es un hecho frecuente y ensombrece aún más el pobre pronóstico de estos pacientes2.
Macroscópicamente los pulmones muestran áreas pálidas de pocos milímetros de diámetro. Desde el punto de vista histológico, el cuadro se caracteriza por la necrosis del tracto respiratorio, la cual puede extenderse desde la tráquea hasta los alvéolos.
Los focos de necrosis tienden a tornarse confluentes, principalmente alrededor de los bronquiolos. Estos focos suelen estar rodeados por infiltrado inflamatorio intersticial de tipo mononuclear. Además, en las áreas necróticas, puede
encontrarse exudado eosinofílico proteináceo, en el que se identifican detritus celulares y residuos de la cariorrexis de los neutrófilos. Las células epiteliales pueden exhibir un aspecto en “vidrio esmerilado”, o inclusive, pueden visualizarse las inclusiones eosinofílicas intranucleares llamadas cuerpos de Cowdrey tipo A, sin embargo estos hallazgos son muy difíciles de detectar en la presencia de lesiones con extensa necrosis4. El parénquima pulmonar aledaño puede exhibir cambios de daño alveolar difuso (DAD).
En los casos de viremias generalizadas, el compromiso puede involucrar diversos órganos o tejidos como hígado, cerebro, glándulas suprarrenales, orofaringe, esófago, pulmón y globo ocular2.
La identificación de las partículas virales solo puede hacerse con estudios complementarios de microscopía electrónica. Las técnicas de hibridación in-situ también permiten la detección de anticuerpos específicos contra el HSV-1 y el HSV-25. El DNA viral puede ser detectado con técnicas de reacción en cadena de la polimerasa (PCR)6.
En nuestro caso no fue posible la tipificación del bacilo, pudiendo bien corresponder a M. tuberculosis o a las denominadas micobacterias atípicas, actualmente clasificadas como micobac-terias no tuberculosas. A continuación destacaremos los aspectos más importantes de ambas especies, en el contexto de la coinfección por VIH.
En cuanto a M. tuberculosis, es un hecho reconocido la frecuente coinfección con VIH, con porcentajes que varían según las series; en el hospital Simón Bolívar de Bogotá se observa hasta en un 20% de los pacientes infectados por VIH que se hospitalizan por diversas causas.
En la actualidad se reconoce como una de las complicaciones más frecuentes en los individuos infectados con VIH, siendo además, de todas las infecciones que presentan estos pacientes, la única capaz de trasmitirse a los contactos inmu-nocompetentes, hecho de gran importancia desde el punto de vista epidemiológico y de bioseguridad. Su presencia en seropositivos define el diagnóstico de sida.
Debe sospecharse en todo paciente infectado con VIH que presente tos, aún en ausencia de alteraciones en la radiografía de tórax. Las manifestaciones clásicas, tanto clínicas como radiológicas, varían en proporción inversa al conteo de CD4, siendo más frecuentes los infiltrados basales y las adenopatías hiliares o mediastinales, en la medida que progresa la inmunodeficiencia.
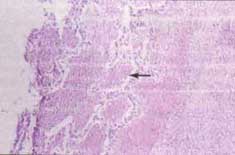
Figura No. 1 Vista panorámica del pulmón donde se observan los cambios necróticos extensos, con preservación de algunos septos alveolares y depósito de abundante material fibrinoide eosinofílico (flecha), (H/E, 10x).
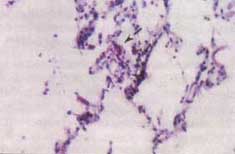
Figura No. 2 Áreas pulmonares no necróticas con septos alveolares preservados y presencia de numerosos bacilos ácido alcohol resistentes (flecha), (ZN, 40x).
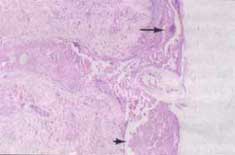
Figura No.3 Panorámica de las lesiones cutáneas donde se observa la formación de vesículas intraepi-dérmicas con marcados cambios acantolíticos (flecha corta), además hay balonización y multinucleación secundarios a la infección viral (flecha larga), (H/E, 10x).
El diagnóstico se confirma con la positividad del Bk de esputo, la cual es mayor mientras menor grado de inmunocompromiso exista. En presencia de tos pero ausencia de expectoración, deberá recurrirse a la solución salina hipertónica o a la realización de fibrobroncoscopia.
La baciloscopia deberá practicarse, al igual que el cultivo, a cualquier material orgánico donde se sospeche la presencia del bacilo. En lo posible deberá acudirse a la tipificación y a las pruebas de resistencia.
El hemocultivo, al igual que las biopsias de ganglio, hígado o medula ósea, constituyen otros auxiliares diagnósticos. Para el tratamiento, se cuenta con esquemas específicamente normados por el Ministerio de Salud para ser aplicados en nuestro medio, insistiendo siempre en la educación del paciente respecto a sus posibles efectos secundarios y cumplimiento del mismo.
La quimioprofilaxis solo está recomendada en casos de prueba de tuberculina positiva, una vez excluída enfermedad tuberculosa y ante la absoluta seguridad que el paciente cumplirá con la prescripción, ya que de lo contrario se puede incurrir en monoterapia, con la consiguiente resistencia secundaria, hecho catastrófico en el manejo de esta enfermedad13.
Las infecciones por micobacterias no tuber-culosas en los pacientes con sida son casi todas debidas a microorganismos del complejo CMA, el cual incluye al M. intracellulare, al M. scrofulaceum y al M. avium, siendo este último el responsable de casi todas las infecciones.
Antes de la aparición del SIDA, solo se habían reportado 37 casos documentados de infección diseminada por MAC, sin embargo, a partir de la segunda mitad de la década de los 80, su incidencia ha venido en franco aumento, al punto de constituir, en los pacientes con SIDA, la causa más común de infección bacteriana diseminada8, siendo el M. avium el responsable de la mayoría de los casos.
Otra condición que ha favorecido este incremento es la mayor sobrevida de personas sometidas a terapia inmunosupresora prolongada por diversas causas, como tumores malignos, transplantes, o enfermedades autoinmunes2.
La infección por MAC puede adoptar formas localizadas o formas diseminadas. Los casos de infección localizada se presentan en individuos con conteos de CD4 mayores de 50; son raros en comparación con las formas diseminadas y pueden manifestarse como abscesos cutáneos, lesiones endobronquiales, enfermedad pulmonar localizada, ileitis terminal y diarrea crónica.
La forma diseminada, que es la presentación más frecuente, debe sospecharse en todo paciente con recuentos de CD4 menores de 50, quien además acuse fiebre, sudoración nocturna, pérdida de peso o dolor abdominal, manifestaciones hasta cierto punto inespecíficas, ya que pueden confundirse con las generadas por el mismo sida.
El diagnóstico de la forma diseminada se establece mediante hemocultivos, los cuales tienen ventaja sobre las biopsias de hígado, ganglio linfático o medula ósea, confirmando la enfermedad en un 86 a 98% de los casos.
Los resultados positivos de los cultivos de esputo o de heces indican más colonización que enfermedad, aunque en pacientes con infección por VIH y conteos de CD4 menores de 50 esta colonización puede presagiar una enfermedad diseminada en corto plazo13.
Desde el punto de vista microscópico, en los pacientes inmunocomprometidos, se observa una pobre respuesta inflamatoria, con presencia de granulomas pobremente formados, hecho explicado por el déficit en la inmunidad celular que ellos presentan10.
El hallazgo histológico más constante es la presencia de colecciones de histiocitos espumosos, con citoplasma amplio, (similares a las células típicas encontradas en la enfermedad de Gaucher); con las coloraciones especiales para la detección de bacilos ácido alcohol resistentes, estos pueden ser identificados en el citoplasma de tales células12.
Los hallazgos en la radiografía de tórax son muy escasos. La presencia de adenopatías retroperito-neales en la TAC abdominal es un hallazgo sensible más no específico de la enfermedad.
El tratamiento, aunque no se dispone de datos definitivos, se basa actualmente en uno de los nuevos macrólidos, asociado a una o más drogas como etambutol, rifabutina, clofazymine, ciprofloxacina o un aminoglucósido.
La rifabutina o la claritromicina se constituyen además en agentes profilácticos efectivos contra las formas diseminadas de MAC, haciendo la salvedad que en países de escasos recursos, cada caso debería ser evaluado particularmente antes de generalizar estas medidas13.
La infección por Herpes simplex ocurre en adultos jóvenes de ambos sexos, el compromiso es principalmente a nivel muco-cutáneo (oral y genital). La infección por el virus zoster ocurre frecuentemente en niños y en forma muy ocasional en adultos, el compromiso se da al nivel de los dermatomas7.
Clínicamente las lesiones pueden ser pápulas, vesículas, vesículas costrosas y pústulas. El curso clínico es usualmente corto, menos de dos semanas, especialmente si el paciente presenta algún grado de inmunocompromiso2.
Los hallazgos histopatológicos dependen del tiempo de evolución de la lesión; en las que están completamente desarrolladas, se encuentra infiltrado inflamatorio de predominio perivascular, constituido por linfocitos y neutrófilos, además se reconoce fibrina en las paredes de las vénulas.
A nivel de la epidermis, los cambios más característicos son la balonización y multinucleación de los queratinocitos, secundario a estos cambios, se identifica la formación de vesículas intraepidérmicas con presencia de células acantolíticas. En fases tardías hay áreas de necrosis confluentes con erosión y ulceración7.
Los cambios histopatológicos causados por la infección de Herpes simplex, zoster y varicella son indistinguibles entre sí, y solo las características clínicas de la enfermedad ayudan a establecer el diagnostico diferencial2,7.
Bibliografia
- Hasleton PS.: Viral infections. In: Hasleton P.S., editor. Spencer´s pathology of the lung. Fifth Edition. International Edition: McGraw-Hill, 1996: 139-177.
- Khalifa MA, Lack EE.: Herpes Simplex Virus Infection. In: Connor D.H, et.al. editors. Pathology of Infectious Disease Vol. I. 1ª Edition. Appleton & Lange, 1997: 147-152.
- Tuxen DV, Cade JF, McDonald MI, Buchanan RC., Clark RJ, Pain MCF.: Herpes simplex virus of the lower respiratory tract in adult respiratory distress syndrome. Am Rev Respir Dis, 1982, 126: 416-419.
- Katzenstein A-L.: Infection I. Unusual Pneumonias. In: Katzenstein A-L.,editor. Katzenstein and Askin´s Surgical Pathology of Non-Neoplastic Lung Disease. Third Edition. Major Problems in Pathology Vol 13. W. B. Saunders Company, 1997: 247-85.
- Strickler JG, Manivel JC, Copenhaver CM, Kubic VL.: Comparison of in situ hybridization and immunohis-tochemistry for detection of Cytomegalovirus and Herpes simplex virus. Hum Pathol, 1990, 21:443 -8.
- Geradts J, Warnock M, Yen T.S.: Use of the polymerase chain reaction in the diagnosis of unsuspected Herpes simplex viral pneumonia: Report of a case. Hum Pathol, 1990, 21: 118-21.
- Ackerman A.B.: Herpesvirus infection. In: Ackerman A.B. et.al., editors. Histologic Diagnosis of Inflammatory Skin Diseases. Second Edition. Williams & Wilkins, 1997: 442-3.
- Nash G.: Respiratory system. In: Nash G. And Said J.W., editors. Pathology of AIDS and HIV Infection. First edition. Major Problems in Pathology Vol 26. W. B. Saunders Company, 1992: 60-100.
- Murray JF, Felton CH, Garay SM, et.al.: Pulmonary complications of the acquired immune deficiency syndrome: Report of a National Heart, Lung, and Blood Institute Workshop. N Engl J Med, 1984, 310: 1682 – 1688.
- Farhi DC, Mauson UG., Horsburgh C.R. Jr.: Patho logic findings in disseminated Mycobacterium avium-intracellulare infection. Am J Clin Pathol, 1986, 85: 67-72.
- Klatt EC, Jensen DF, Meyer PR.: Pathology of Mycobacterium avium-intracellulare infection in acquired immune deficiency syndrome. Hum Pathol 1987, 18: 709 – 714.
- Armstrong D, Gold JWM, Dryjanski J, et.al.,: Treatment of infection in patients with acquired immune deficiency syndrome. Ann Intern Med 1985, 103: 738-43.
- Chin D. Hopewell P. Mycobacterial complications of HIV infection. In: White D. Stover D. eds. Clinics In Chest Medicine. W. B. Saunders, 1996:697-712.
CLIC AQUÍ Y DÉJANOS TU COMENTARIO