Marcelo A. Beltrán
Palabras clave: síndrome de Zollinger-Ellison; gastrinoma; gastrinas; neoplasia endocrina múltiple; úlcera péptica.
Resumen
El síndrome de Zollinger-Ellison se caracteriza por la presencia de úlceras pépticas resistentes al tratamiento que se deben a la hipersecreción ectópica de gastrina por un tumor neuroendocrino, que es el gastrinoma y que resulta en la hipersecreción de ácido clorhídrico en el estómago. Este síndrome se presenta en forma esporádica y también se asocia al síndrome de neoplasia neuroendocrina múltiple de tipo 1.
Se describen ambas presentaciones clínicas, así como también la fisiopatología, el diagnóstico, el estudio, el tratamiento y el pronóstico, enfatizando en los detalles técnicos de la cirugía. El pronóstico de los gastrinomas cuando son identificados precozmente es bueno, aun en aquellos casos malignos, por lo que la sospecha clínica asociada al estudio específico y al tratamiento de estos pacientes es fundamental. Dada la tecnología diagnóstica disponible en la actualidad, la identificación de estos tumores será cada vez más frecuente, por lo que el conocimiento de los detalles esenciales para su tratamiento es importante para el cirujano.
Introducción
La hipergastrinemia es la consecuencia de la producción anormal de gastrina por tumores que se originan de las células gastrointestinales secretoras de gastrina o células G. Estos tumores constituyen la tercera neoplasia neuroendocrina gastroenteropancreática después de los tumores carcinoides y los insulinomas. Desde la descripción original de esta condición patológica 1, el diagnóstico y las estrategias terapéuticas han evolucionado radicalmente, desde la cirugía destinada a remover el órgano blanco hasta el manejo médico de la hipersecreción de ácido gástrico secundaria a la hipergastrinemia y, principalmente, la cirugía específica del tumor.
Existen dos entidades asociadas a la hipergastrinemia secundaria al gastrinoma. La más frecuente es el desarrollo esporádico de tumores secretores de gastrina, que constituye el síndrome de Zollinger-Ellison; la segunda es el desarrollo de estos tumores en el contexto de la neoplasia endocrina múltiple de tipo 1. El síndrome de Zollinger-Ellison se caracteriza principalmente por la presencia de úlcera péptica resistente al tratamiento. En todos los pacientes con gastrinomas esporádicos o asociados a neoplasia endocrina múltiple de tipo 1, se tienen dos objetivos terapéuticos: el primero es lograr el control de la hipersecreción ácida y el segundo es el tratamiento quirúrgico del tumor.
En el presente artículo se revisa el conocimiento actual sobre los gastrinomas, delineándose los métodos de diagnóstico y la conducta terapéutica apropiada.
Anatomía
Anatomía del gastrinoma esporádico
Los tumores neuroendocrinos se presentan con mayor frecuencia en el páncreas y con menor frecuencia en el estómago, el duodeno y el intestino delgado. En el páncreas, se desarrollan en las células de los islotes de Langerhans y pueden ser funcionales o no funcionales. Entre los tumores funcionales, se encuentran los gastrinomas que causan hipergastrinemia 2.
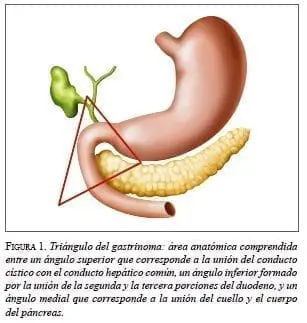
Los gastrinomas se localizan con mayor frecuencia en el duodeno (70 a 90 %). El páncreas constituye la segunda localización anatómica más frecuente y es donde se encuentran, aproximadamente, 30 % de estos tumores (10 a 40 %). Más del 90 % de los gastrinomas se localizan en el denominado ‘triángulo del gastrinoma’, que es el área anatómica delimitada por la vía biliar, el duodeno y el páncreas 3 (figura 1). Los tumores que se encuentran hacia la izquierda de la arteria mesentérica superior son malignos con mayor frecuencia que aquellos que se encuentran dentro del triángulo del gastrinoma. Se han descrito localizaciones ectópicas y anecdóticas de los gastrinomas, incluyendo ovarios, antro gástrico, hígado, epitelio biliar, hilio esplénico, mesenterio y ventrículos cardiacos, y como parte del tumor pulmonar de células pequeñas.
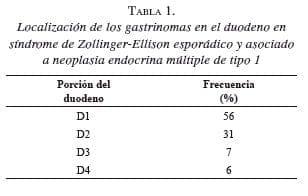
Localización de los gastrinomas en pacientes con neoplasia endocrina múltiple de tipo 1
En pacientes con síndrome de Zollinger-Ellison asociado a neoplasia endocrina múltiple de tipo 1, entre el 65 y el 100 % de los gastrinomas se encuentran en la primera y segunda porción del duodeno (tabla 1). Entre 0 y 15 % se localizan en el páncreas. Habitualmente, son múltiples y pequeños (menos de 1 cm). Los gastrinomas duodenales son principalmente submucosos, habitualmente malignos, de curso lento y se asocian a metástasis linfáticas en 34 a 85 % de los casos. Las metástasis hepáticas son infrecuentes y se presentan solo en 2 a 14 % de todos los pacientes.
Gastrinomas primarios que se originan en ganglios linfáticos
Se considera que alrededor del 10 % de todos los gastrinomas se originan en los ganglios linfáticos del triángulo del gastrinoma 4-6, aun cuando la existencia de gastrinomas primarios que se originan en los ganglios linfáticos no es de consenso y permanece controversial. Se define como gastrinoma primario de ganglio linfático al que se presenta en un paciente en el que el único gastrinoma extrahepático se encontró en un ganglio linfático y que después de la cirugía se consideró libre de enfermedad 4. Se acepta que un gastrinoma se origina en los ganglios linfáticos cuando cumple los criterios descritos en la tabla 2.
Gastrinomas asociados a tumores neuroendocrinos del estómago
La hipergastrinemia causada por el gastrinoma en pacientes con neoplasia endocrina múltiple de tipo 1 estimula la proliferación de células enterocromafines (células de Kulchitsky), produciendo hiperplasia. Si el estímulo persiste, se desarrollan tumores neuroendocrinos hasta en 23 % de los pacientes 7,8, 20 a 30 % los cuales son malignos 7-12. Los tumores neuroendocrinos gástricos derivados de las células enterocromafines se clasifican en tres tipos; el de tipo 2 es el que se presenta en el síndrome de Zollinger-Ellison esporádico y, principalmente, en el asociado a neoplasia endocrina múltiple de tipo 1 5-10. Estos tumores son múltiples, frecuentemente funcionales, liberan histamina y secretan gastrina, y se localizan en el cuerpo y el fondo del estómago 10-12. En estos pacientes, los gastrinomas asociados se localizan en el duodeno y son pequeños, midiendo entre 0,1 y 1,6 cm; ocasionalmente, pueden ser de mayor tamaño con metástasis a los ganglios linfáticos hasta en 30 % de los casos 5,7.

Epidemiología
Servicio de Cirugía, Hospital San Juan de Dios de La Serena; Facultad de Medicina, Universidad Católica del Norte, La Serena – IV Región, Chile.
Fecha de recibido: 2 de marzo de 2016
Fecha de aprobación: 5 de julio de 2016
Citar como: Beltrán MA. Síndrome de Zollinger-Ellison: revisión del conocimiento actual. Rev Colomb Cir. 2016;31:197-211.Gastrinoma esporádico
La incidencia anual de gastrinomas en los Estados Unidos de América se estima que varía entre dos y cuatro casos por millón de habitantes. Aproximadamente, 80 % de los gastrinomas ocurren esporádicamente, y del 20 al 25 % restante se asocia a neoplasia endocrina múltiple de tipo 1 6. Los gastrinomas esporádicos son únicos en 20 a 50 % de todos los casos y son múltiples en el restante 50 a 80 %. El síndrome de Zollinger-Ellison es la causa de 0,1 a 1 % de todas las úlceras pépticas. Aproximadamente, 0,4 % de todos los casos de úlcera péptica primaria y 2 % de todos los casos de úlcera péptica recurrente se asocian a gastrinomas. Los gastrinomas son más comunes en pacientes masculinos (60 %) y se presentan en cualquier edad, con mayor frecuencia entre los 20 y los 60 años 6-9.
Gastrinoma asociado a neoplasia endocrina múltiple de tipo 1
Los pacientes con neoplasia endocrina múltiple de tipo 1 representan entre el 10 y el 48 % de todos aquellos con síndrome de Zollinger-Ellison, siendo el gastrinoma el tumor endocrino funcional más común en estos casos 7,8. La asociación de estas dos enfermedades se presenta en pacientes jóvenes, alrededor de los 30 años de edad. Los tumores de la neoplasia endocrina múltiple de tipo 1 que se asocian a gastrinoma son, con mayor frecuencia, los paratiroideos (80 %), con menor frecuencia, los tumores de células o insulinomas (20 %) y, con una frecuencia menor de 5 %, el glucagonoma, el ‘VIPoma’ y otros 13,14. Los adenomas pituitarios se encuentran en 50 a 60 % y, los tumores suprarrenales, en 27 a 36 %; muchos de ellos no son funcionales 6. En la neoplasia endocrina múltiple de tipo 1, los pacientes con síndrome de Zollinger-Ellison tienen una elevada probabilidad de desarrollar tumores neuroendocrinos malignos originados en las células enterocromafines 15-17. La incidencia de malignidad de un gastrinoma en pacientes con neoplasia endocrina múltiple de tipo 1 puede llegar a 47 % de los casos y es mayor que la incidencia reportada para gastrinoma esporádico 14.
Historia natural
Gastrinoma esporádico
Los pacientes con síndrome de Zollinger-Ellison tienen una supervivencia general a cinco años que varía entre 62 y 75 %, a 10 años la supervivencia es de 50 %. En el momento del diagnóstico, algunos pacientes tendrán tumores muy pequeños y otros tendrán tumores avanzados con metástasis linfáticas hasta en 40 % de los casos, las que, junto con las metástasis hepáticas, influyen en la supervivencia. La cirugía tiene la capacidad de alterar la historia natural del síndrome de Zollinger-Ellison. Cuando se logra resecar los gastrinomas, los pacientes tienen una supervivencia de 60 a 100 % a 10 años; cuando el tumor es metastásico o no es posible su resección, la supervivencia a cinco años es de solo 40 % 15-19.
Gastrinoma asociado a neoplasia endocrina múltiple de tipo 1
En el síndrome de Zollinger-Ellison asociado a neoplasia endocrina múltiple de tipo 1, la supervivencia a 10 años es de 83 % como promedio, comparada con los casos del síndrome esporádico en los que la supervivencia a 10 años es de 40 a 65 %, con un promedio de 50 %. La supervivencia en pacientes con la asociación de ambas enfermedades, es de 90 a 96 % a cinco años, a 10 años es de 75 a 95 % y a 20 años es de 58 a 90 % 7. La mortalidad en estos pacientes se debe a que el tumor se torna maligno y desarrolla metástasis en 10 % de los casos de gastrinomas esporádicos y en 45 a 85 % de los gastrinomas asociados a neoplasia endocrina múltiple de tipo 1 14,15. Las causas más importantes de mortalidad en el síndrome de Zollinger-Ellison son las complicaciones de la hipergastrinemia, como hemorragia digestiva, perforación de la úlcera, estenosis esofágica y desnutrición grave 6,13.
El factor más importante que determina la supervivencia en pacientes con gastrinomas asociados a neoplasia endocrina múltiple de tipo 1 es el desarrollo de metástasis hepáticas, las que tienen un comportamiento muy agresivo comparadas con las metástasis linfáticas, las cuales tienen un comportamiento más benigno 13-17. Finalmente, se ha demostrado que los gastrinomas pueden tener comportamientos muy agresivos en su presentación o pueden comportarse como tumores benignos o poco agresivos. En la neoplasia endocrina múltiple de tipo 1, solo 14 % de los tumores tienen un comportamiento agresivo, comparados con el 24 % de los tumores en el síndrome de Zollinger-Ellison esporádico 7.
Presentación clínica
Gastrinoma esporádico
El síndrome de Zollinger-Ellison se presenta habitualmente en la quinta década de la vida; puede hacerlo desde la infancia hasta la senectud, pero el 90 % de los casos se diagnostican entre los 20 y los 60 años de edad. La sintomatología actual del síndrome de Zollinger-Ellison no es exactamente la que fue descrita originalmente. El cambio se debe al diagnóstico relativamente más temprano de esta enfermedad y al uso indiscriminado de inhibidores de la bomba de protones.
La clásica descripción de Zollinger y Ellison incluía la triada de hipersecreción persistente de ácido gástrico, desarrollo de múltiples úlceras pépticas en localizaciones inusuales, como la segunda o la tercera porciones del duodeno y el yeyuno proximal, o úlceras recurrentes y tumores pancreáticos de células no-b del páncreas 1.
Actualmente, los síntomas de presentación del síndrome de Zollinger-Ellison incluyen diarrea (71 a 80 %), dolor epigástrico (65 a 83 %), reflujo gastroesofágico y sus complicaciones, tales como esofagitis (6 a 13 %), náuseas, desnutrición y pérdida de peso 9,17. La diarrea es, posiblemente, la forma de presentación más común y se describe hasta en 80 % de los casos 6,9. Debido a la naturaleza inespecífica de estos síntomas, el diagnóstico correcto del síndrome de Zollinger-Ellison, aun en la actualidad, no es precoz.
El diagnóstico inicial más común en esta enfermedad es el de úlcera péptica idiopática, en 75 % de los casos, y el de síndrome diarreico, en 20 %. El promedio de tiempo para llegar al diagnóstico correcto desde el inicio de los síntomas es de 5,9 a 6,4 años 6-8. Este promedio de tiempo se ha mantenido constante durante los últimos 30 años, sin embargo, el uso actual de inhibidores de la bomba de protones, que producen una efectiva supresión de la secreción ácida gástrica, podría diferir aún más el diagnóstico correcto.
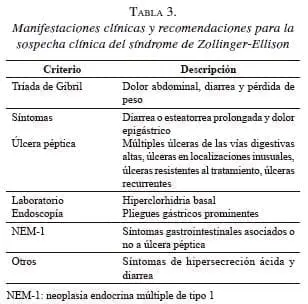
Debido al continuo retraso en el diagnóstico, se han propuesto algunas recomendaciones y se han identificado algunos factores que, cuando están presentes, deben despertar la sospecha del síndrome (tabla 3). En general, se debe sospechar un síndrome de Zollinger-Ellison en cualquier paciente que se presente con una úlcera péptica negativa para Helicobacter pylori, resistente al tratamiento y en localizaciones no habituales, o en aquellos con una enfermedad endocrina, como hiperparatiroidismo o neoplasia endocrina múltiple de tipo 1 9.
Gastrinoma asociado a neoplasia endocrina múltiple de tipo 1
Los pacientes con neoplasia endocrina múltiple de tipo 1 desarrollan el síndrome de Zollinger-Ellison a una edad más temprana que aquellos con la forma esporádica; la edad promedio de presentación varía entre los 33 y los 39 años (figura 2).
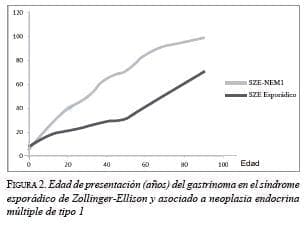
La presentación clínica de la neoplasia endocrina múltiple de tipo 1 es similar a la del síndrome de Zollinger-Ellison esporádico, siendo la diarrea el síntoma más frecuente (66 a 76 %), además de dolor epigástrico, pirosis, náuseas, vómito y pérdida de peso; la principal diferencia se encuentra en la presencia de hipercalcemia y nefrolitiasis (47 %) causada por hiperparatiroidismo 7.
Aun cuando se conoce la elevada frecuencia de síndrome de Zollinger-Ellison en casos de neoplasia endocrina múltiple de tipo 1, el diagnóstico en estos pacientes tampoco es precoz. El diagnóstico inicial correcto en esta última es de 5 %. El periodo de retraso en su diagnóstico es similar al que se presenta en el síndrome de Zollinger-Ellison esporádico (5,5 años) 7.
Estudio de laboratorio
Gastrina sérica en ayunas
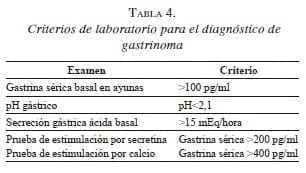
El estudio de laboratorio debe comenzar con una muestra de gastrina sérica en ayunas y la demostración de hipersecreción gástrica ácida (tabla 4).
La hipersecreción ácida con niveles séricos elevados de gastrina es crucial para confirmar el diagnóstico de gastrinoma. Aproximadamente, 97 a 99 % de todos los pacientes con gastrinoma tendrán una secreción basal de gastrina elevada mayor de 100 pg/ml 8,9,20. Aquellos en tratamiento con inhibidores de la bomba de protones deben suspenderlos, por lo menos, 72 horas a una semana antes del examen y aquellos en tratamiento con bloqueadores de los receptores H2 deben suspenderlos, por lo menos, 48 horas antes. El valor absoluto de gastrina sérica no permite el diagnóstico definitivo: en 99 % de los pacientes el nivel basal será mayor de 100 pg/ ml y en 60 % será mayor de 500 pg/ml 17-22.
Secreción gástrica ácida basal y pH gástrico
En el síndrome de Zollinger-Ellison, la secreción gástrica ácida basal será mayor de 15 mEq/hora o, en promedio, de 37,5 mEq/hora 17. En estos casos, el pH gástrico será igual o menor de 2; un pH mayor de 3,5 descarta la presencia de hipersecreción gástrica 6.
Prueba de estimulación por secretina
La prueba de estimulación por secretina es el método de referencia para el diagnóstico bioquímico del síndrome de Zollinger-Ellison 18. Todos los pacientes con sospecha de este síndrome deben someterse a una prueba de estimulación por secretina 19-22, porque confirma el diagnóstico de hipergastrinemia y puede ser útil, sobre todo, cuando los resultados de las gastrina sérica basal en ayunas y los valores de secreción gástrica ácida no son concluyentes; sin embargo, es positiva solo en 85 % de los casos. No es necesario suspender el tratamiento médico antisecretor para este examen, por lo cual también es útil en aquellos que no pueden suspender su tratamiento.
Esta es una prueba de provocación en la que se inyecta por vía venosa un bolo de 2 U/kg de peso o 0,4 mg/kg de peso, de secretina, y se miden los niveles de gastrina sérica a los 0, 2, 5, 10, 15 y 30 minutos. Un aumento de la gastrina sérica mayor de 200 pg/ml hace el diagnóstico de síndrome de Zollinger-Ellison. Se ha reportado una tasa de falsos negativos para esta prueba de 1,5 %.
En 44 a 47 % de los pacientes con neoplasia endocrina múltiple de tipo 1, el síndrome de Zollinger-Ellison produce la primera manifestación clínica 7. Por esta razón, se recomienda que en el estudio por sospecha de síndrome de Zollinger-Ellison esporádico, se midan los niveles séricos de calcio, fósforo, hormona paratiroidea y prolactina durante la primera evaluación y, posteriormente, en el control y seguimiento del paciente.
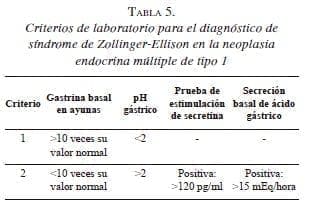
Gastrina sérica en ayunas, prueba de estimulación de secretina, secreción de ácido gástrico y pH gástrico en la neoplasia endocrina múltiple de tipo 1
En pacientes con neoplasia endocrina múltiple de tipo 1 sometidos a paratiroidectomía, la gastrina sérica basal y la secreción de ácido gástrico pueden ser normales y la prueba de estimulación de secretina puede ser negativa 9. Consecuentemente, se han sugerido los criterios descritos en la tabla 5 para el diagnóstico de síndrome de Zollinger-Ellison en casos de neoplasia endocrina múltiple de tipo 1 8,20.
Endoscopia
La endoscopia de vías digestivas altas no ha demostrado su utilidad para demostrar los gastrinomas duodenales 17. El estudio endoscópico forma parte del estudio general de la sintomatología epigástrica y es habitualmente el primer estudio en pacientes con gastrinoma.
Las características endoscópicas principales son los pliegues gástricos prominentes (95 %), la úlcera péptica activa (65 %) y, en algunos casos, una úlcera con signos de hemorragia reciente (7 a 12 %). Durante el estudio y tratamiento del síndrome de Zollinger-Ellison, la endoscopia es útil en el diagnóstico y control de las úlceras y sus complicaciones, y en la medición del pH gástrico.
Estudios imaginológicos
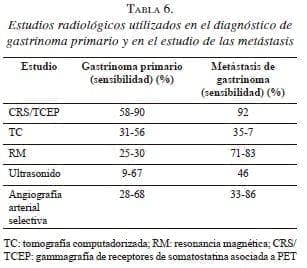
Los estudios imaginológicos que han demostrado una mayor utilidad en el diagnóstico y estadificación de los gastrinomas son la gammagrafía de receptores de somatostatina, que utiliza el octeótrido como radiomarcador, en conjunto con la tomografía computadorizada de emisión de positrones (Positron Emission Tomography, TEP) 4,9. Otros estudios habitualmente utilizados son la endosonografía, la tomografía computadorizada (TC) abdominal, la resonancia magnética (RM) abdominal y la angiografía arterial (tabla 6).
El uso combinado de endosonografía, TC y RM tiene una sensibilidad de 40 a 70 % para el diagnóstico de gastrinomas; ninguna de estas técnicas puede diagnosticar gastrinomas menores de 5 mm, y pueden visualizar solo 15 a 30 % de los gastrinomas pancreáticos entre 1 y 3 cm.
Otra técnica que no se encuentra ampliamente disponible es la prueba de inyección arterial selectiva con secretina o calcio, con la cual se pueden diagnosticar gastrinomas mayores de 1 mm. Actualmente, aun con toda la tecnología radiológica disponible, la localización preoperatoria de los gastrinomas se logra en 60 a 80 % de los casos.
Gammagrafía de receptores de somatostatina, sola y asociada a TEP
La sensibilidad de estas dos técnicas combinadas ha demostrado ser igual o mayor que todas las otras modalidades combinadas 9,23,24. Este estudio puede demostrar tumores en localizaciones ectópicas y su sensibilidad depende del tamaño del tumor. Detecta 30 % de los gastrinomas menores de 1 cm, 64 % de aquellos entre 1 y 2 cm, y 96 % de los mayores de 2 cm, pero no detecta 33 % de los menores de 1 cm que se localizan principalmente en el duodeno 23. Aun así, es el mejor examen actualmente disponible para el estudio y el diagnóstico de los gastrinomas primarios y metastásicos 24,25 (tabla 6).Endosonografía
En pacientes con tumores pancreáticos, el ultrasonido tiene una sensibilidad promedio de 85 % (75 a 100 %) para la detección de gastrinomas pancreáticos; es más efectivo que otros exámenes radiológicos disponibles. Cuando los tumores son duodenales o en el estudio de metástasis hepáticas, su utilidad es menor (sensibilidad 25 a 63 %, promedio 43 %).
TC abdominal
La TC abdominal tiene la ventaja de proveer mayor información anatómica que la gammagrafía de receptores de somatostatina con TEP, pero tiene una sensibilidad menor para demostrar los gastrinomas. En este estudio, 52 % de los tumores se manifiestan como masas endolu minales polipoides 26. Cuando la tomografía se encuentre contraindicada, la alternativa es la RM, la cual provee la misma información anatómica.
Algoritmo diagnóstico
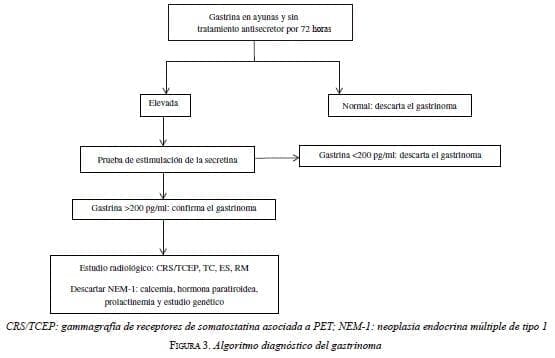
El diagnóstico de síndrome de Zollinger-Ellison requiere la demostración de hipergastrinemia en ayunas asociada a hiperclorhidria 20. Asociados a estos criterios, se encuentran otros hallazgos clínicos, de laboratorio y radiológicos 7-20. El estudio diagnóstico debe iniciarse con una muestra sérica para gastrina en ayunas, por lo menos, 72 horas después de la suspensión del tratamiento antisecretor. Si el valor basal de la gastrina es normal, la prueba se considera negativa. Cuando el valor de la gastrina es elevado, se puede medir la secreción de ácido gástrico, lo cual podría ser opcional.
A continuación se debe hacer una prueba de estimulación de secretina; si el valor de la gastrina sérica es mayor de 200 pg/ml, se considera que el paciente tiene un gastrinoma; algunos autores consideran positiva esta prueba con un valor de gastrina sérica mayor de 110 pg/ ml. Cuando el diagnóstico bioquímico de gastrinoma está confirmado, se continúa con estudios radiológicos para localizar el tumor.
Finalmente, en todo paciente con síndrome de Zollinger-Ellison se debe estudiar y descartar la neoplasia endocrina múltiple de tipo 1 (figura 3).
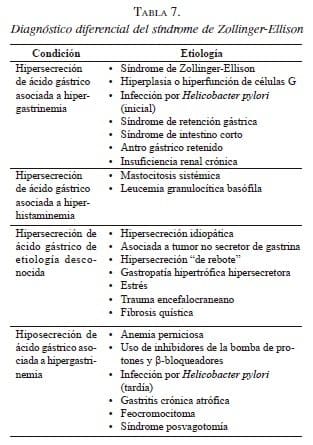
Diagnóstico diferencial
El diagnóstico diferencial de gastrinoma se establece con diversas condiciones patológicas. Desde el punto de vista de los exámenes de laboratorio, existen enfermedades y diversas condiciones clínicas que producen hipergastrinemia con producción excesiva o normal de ácido gástrico. En la tabla 7 se detallan las enfermedades que deben considerarse en el diagnóstico diferencial en pacientes con sospecha de gastrinoma.
Tratamiento
Los dos objetivos principales del tratamiento del síndrome de Zollinger-Ellison son el control de la producción de ácido gástrico y sus secuelas, y el tratamiento del tumor productor de gastrina, el cual es potencialmente maligno. La cirugía es la única modalidad terapéutica que puede ofrecer la curación de la enfermedad al paciente. Aun cuando en el estudio preoperatorio no se identifiquen tumores en pacientes con diagnóstico bioquímico de gastrinoma, estos deben someterse a la exploración quirúrgica en busca del tumor, porque hasta en 90 % de estos casos es posible encontrar el gastrinoma.
Tratamiento médico
El objetivo del tratamiento médico es controlar la hipersecreción de ácido gástrico. Los inhibidores de la bomba de protones, tales como el omeprazol y otros fármacos similares, son muy efectivos en lograr la supresión de secreción ácida 6,8,9,17,19-22. La dosis habitual para lograr este objetivo es de 40 a 60 mg cada 12 horas y, en algunos casos, se pueden utilizar dosis de hasta 180 mg al día 20.
El adecuado control de la hipersecreción gástrica de ácido se confirma mediante la medición del pH gástrico, el que debe ser mayor de 4 cuando la dosis es adecuada, también, se puede medir la secreción de ácido clorhídrico, la cual debe ser menor de 10 mEq/ hora durante la última hora antes de la siguiente dosis de inhibidores de la bomba de protones 8. En numerosos estudios se ha demostrado que el tratamiento prolongado con inhibidores de la bomba de protones es seguro y debe acompañarse de suplemento con ácido fólico y vitamina B12 9,27.
Es importante estar consciente de que los pacientes pueden desarrollar complicaciones secundarias a la hipersecreción gástrica muy rápidamente 20; consecuentemente, el rol del tratamiento médico en el síndrome de Zollinger-Ellison debe ser el de prevenir las posibles complicaciones, y estabilizar y mantener al paciente con una mínima sintomatología durante el estudio y diagnóstico definitivo hasta el momento de la cirugía.
Tratamiento quirúrgico
El tratamiento quirúrgico de los gastrinomas ha evolucionado desde la gastrectomía total hasta la cirugía tumoral específica 27-50. Su principal objetivo es lograr la curación o el control del tumor, y prevenir su diseminación y metástasis 28-50.
Aun con toda la tecnología diagnóstica actualmente disponible, la localización preoperatoria de los gastrinomas no llega al 100 % de los casos y, por esta razón, es que solo la adecuada exploración quirúrgica tiene el potencial de localizar el 100 % de los tumores 29-47,49,50. Se ha estimado que, aproximadamente, entre 60 y 90 % de todos los gastrinomas son malignos.
La progresión tumoral y el desarrollo de metástasis son los principales factores determinantes para la supervivencia. Consecuentemente, solo la cirugía ofrece al paciente la oportunidad de curación 31-50. Se ha demostrado y establecido que la exploración quirúrgica rutinaria incrementa la supervivencia a largo plazo. En 2006, Norton, et al., publicaron un estudio que demostró el significativo aumento de la supervivencia en los pacientes operados, con una supervivencia libre de enfermedad de 98 % a 15 años, comparada con el 74 % de supervivencia en aquellos no operados 40. Este estudio y otros, confirman la necesidad de realizar la exploración quirúrgica rutinaria en estos pacientes 40-47,39,50.
Indicaciones de cirugía en síndrome de Zollinger-Ellison esporádico
Todos los pacientes con diagnóstico de laboratorio de síndrome de Zollinger-Ellison esporádico tienen indicación de exploración quirúrgica debido a que hasta 30 % de los gastrinomas no son diagnosticados mediante los estudios radiológicos 29-50. Aun cuando la mayoría de los gastrinomas crecen muy lentamente, 60 a 90 % son malignos y, de estos, 25 % crecen muy rápidamente 31,42. La incidencia de metástasis linfáticas en gastrinomas duodenales se ha reportado hasta en 40 % de los casos; los gastrinomas pancreáticos presentan metástasis hepáticas con mayor frecuencia 41,42.
Debe tenerse en cuenta que hasta 15 % de los gastrinomas no identificados en estudios radiológicos tampoco se identifican durante la exploración quirúrgica 42. La cirugía puede lograr la curación definitiva del gastrinoma en 51 a 60 % de los casos en el posoperatorio inmediato, en 40 % de los casos a los cinco años y en 34 % de los casos a los 10 años después de la operación 40,42.
Gastrinomas duodenales y detalles de la técnica quirúrgica
El duodeno es el sitio de localización más frecuente de los gastrinomas 9,16,34. Se encuentran hasta en 60 % de los pacientes en los que se practica duodenotomía como parte de la exploración quirúrgica. En gastrinomas esporádicos, los tumores primarios se localizan en la primera y la segunda porciones del duodeno y, con menor frecuencia, en la tercera y la cuarta 34. Solo mediante una duodenotomía con eversión de la mucosa es posible la minuciosa exploración duodenal, mediante inspección, transiluminación endoscópica, palpación y ecografía intraoperatoria, que permite diagnosticar tumores mayores de 5 mm 26,29,35,39,40,41 (figura 4).
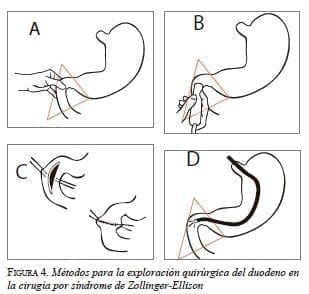
El uso rutinario de la duodenotomía en la cirugía por gastrinoma incrementa las tasas de curación a corto y largo plazo, debido a que permite la identificación y resección de un mayor número de gastrinomas duodenales 4,29,35,39,40,42. Si se identifica un tumor, debe resecarse localmente y someterse a biopsia rápida por congelación para confirmar el diagnóstico 41,42. Se debe practicar la linfadenectomía regional, debido a que se presentan metástasis linfáticas hasta en 60 % de los casos, habitualmente en los ganglios linfáticos cercanos al tumor 34.
Se debe palpar el páncreas en busca de otros gastrinomas primarios; el uso de ecografía intraoperatoria en la exploración del páncreas es de suma utilidad 4,39,41.
Gastrinomas pancreáticos y detalles de la técnica quirúrgica
Aproximadamente 30 % de los gastrinomas se encuentran en el páncreas. Para identificarlos se debe exponer el páncreas mediante la maniobra de Kocher extendida, y la movilización de la cola y el cuerpo; estas maniobras permiten la palpación del páncreas en busca de nódulos sospechosos 19,42. La completa movilización del páncreas permite, además, practicar una ecografía intraoperatoria, la cual es primordial para localizar tumores pequeños 4,7,19.
El hallazgo de un tumor pancreático no descarta la existencia de un tumor duodenal, por lo que la duodenotomía para explorar el duodeno debe ser rutinaria. Los tumores de la cabeza, el cuerpo o la cola del páncreas, menores de 2 cm, pueden ser enucleados. Los tumores de la cabeza del páncreas o de la segunda porción del duodeno adyacente a la cabeza del páncreas mayores de 2 a 4 cm, los tumores múltiples o aquellos que comprometen el conducto pancreático principal localizados en la cabeza del páncreas, requieren pancreatoduodenectomía para su adecuado tratamiento 19,42. Los tumores localizados en el cuerpo y la cola se encuentran adyacentes al conducto pancreático principal, por lo que la pancreatectomía distal con conservación del bazo o sin ella puede ser la opción más segura.
La linfadenectomía regional debe ser practicada sistemáticamente, resecando los ganglios linfáticos peripancreáticos, periduodenales y portohepáticos 4,40,42.
En caso de metástasis hepáticas, estas deben resecarse con un margen mayor de 1 cm; si esto no es posible, se deben practicar segmentectomías o lobectomías según el compromiso tumoral hepático.
Indicaciones de cirugía y técnica quirúrgica en síndrome de Zollinger-Ellison asociado a neoplasia endocrina múltiple de tipo 1
La cirugía en pacientes con esta asociación es controversial 31,32. La cirugía no es curativa en la mayoría de los casos y el porcentaje de curación alcanza solo al 11,3 % 19,21,47. Esto se debe a que los gastrinomas en la neoplasia endocrina múltiple de tipo 1 se localizan principalmente en el duodeno, son múltiples y pequeños, con frecuencia microscópicos y, consecuentemente, son difíciles de encontrar 41. En 50 a 86 % de los casos se asocian a metástasis linfáticas 16. Por esta razón, se ha informado curación en 77 a 100 % de estos pacientes cuando son sometidos a pancreatoduodenectomía; sin embargo, la opinión de los expertos es que, debido al bajo potencial maligno de los gastrinomas duodenales, el riesgo de esta cirugía es mayor que el potencial beneficio 7,8,51.
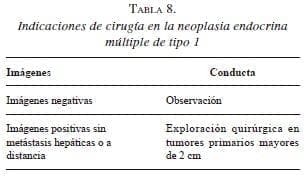
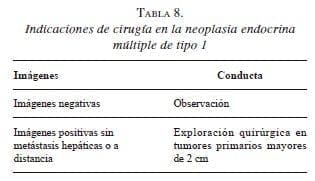
En la neoplasia endocrina múltiple de tipo 1, la necesidad de cirugía se determina mediante los estudios imaginológicos; está indicada en tumores mayores de 2 cm (tabla 8). Se ha descrito una supervivencia de 100 % a 15 años en pacientes con gastrinomas menores de 2 cm 7.
El principal objetivo de la cirugía en esta enfermedad es prevenir las metástasis. La extensión de las metástasis hepáticas es el principal factor determinante de supervivencia; estas no se desarrollan cuando el gastrinoma primario es operado 19,42. El riesgo de desarrollar metástasis se incrementa con el tamaño del gastrinoma primario. La frecuencia de las metástasis varía según el tamaño de los gastrinomas: en menores de 1 cm, es de 4 %; cuando miden entre 1 y 3 cm, es de 28 %, y cuando son mayores de 3 cm, es hasta de 61 % 21. Por estas razones, se recomienda la cirugía en todos los pacientes con gastrinomas mayores de 2 cm 42.
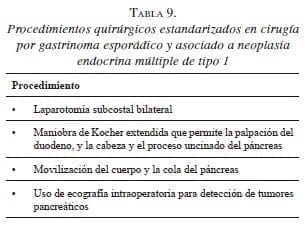
Otro aspecto que se debe tomar en consideración es la secuencia del tratamiento quirúrgico. Debido a que la mayoría de los pacientes con neoplasia endocrina múltiple de tipo 1 tienen hiperparatiroidismo primario, la paratiroidectomía debe practicarse antes de la cirugía del gastrinoma, debido a que así se reducen los niveles séricos de gastrina al remover la estimulación continua por la hipercalcemia 19,22,42. La técnica quirúrgica actualmente recomendada en casos de gastrinoma esporádico y asociado a neoplasia endocrina múltiple de tipo 1, se resume en la tabla 9 32,33,42.
Técnica quirúrgica estándar
Se aborda el abdomen a través de una laparotomía subcostal bilateral con maniobra de Kocher extendida, explorando la cavidad abdominal con especial énfasis en hígado, estómago, duodeno, intestino delgado, me mesenterio, páncreas, pelvis y regiones retroperitoneales del abdomen superior, además de la cuidadosa palpación del duodeno, la cabeza del páncreas y el proceso uncinado, tratando de identificar nódulos 16,26,42. Luego se procede a la apertura del ligamento gastrocólico y la movilización del ángulo esplénico del colon, para lograr la adecuada movilización del cuerpo y la cola del páncreas para permitir la palpación bimanual del órgano 14-16,19,26,42.
La ecografía intraoperatoria es útil en la identificación de pequeños nódulos pancreáticos y puede localizar tumores de hasta 5 mm de diámetro 16,19,26. El duodeno se transilumina mediante endoscopia, la que también permite identificar tumores submucosos 26,40,41.
Los tumores de la cabeza del páncreas deben ser enucleados o tratados mediante pancreatoduodenectomía; las lesiones del cuerpo y la cola pueden ser tratados mediante enucleación o pancreatectomía distal 8,39,40,42. Se debe practicar una duodenotomía lateral longitudinal de 3 cm de longitud, en la unión de la primera y la segunda porciones del duodeno, porque es el método más efectivo para identificar lesiones duodenales por inspección y palpación 29,42.
La duodenotomía puede ampliarse proximal y distalmente; esta incisión permite identificar mediante palpación todos los nódulos sospechosos 16,30,35,42 (figura 4). Finalmente, se debe proceder a la linfadenectomía regional de todos los ganglios linfáticos en el triángulo del gastrinoma 4,8,9,40,42.
Algunos autores recomiendan la medición rutinaria de gastrina sérica durante la cirugía y antes del cierre de la laparotomía 40,41,43,44.
Las opciones de tratamiento para las metástasis hepáticas son la resección quirúrgica, la ablación por radiofrecuencia, la embolia y quimioembolia de la arteria hepática, el trasplante hepático, la quimioterapia, la bioterapia y la terapia radiomarcada con somatostatina 9,22. La resección quirúrgica de las metástasis mejora la supervivencia de los pacientes a 5 años en 70 a 100 % de los casos. Los factores de mal pronóstico en estos casos son la edad mayor de 50 años y la presencia de metástasis múltiples en ambos lóbulos.
Cirugía laparoscópica en síndrome de Zollinger-Ellison
El tratamiento quirúrgico laparoscópico en el síndrome de Zollinger-Ellison no se encuentra completamente establecido y es controversial. La cirugía laparoscópica debe replicar la cirugía abierta y se deben realizar pasos y maniobras propias de la cirugía del gastrinoma que revisten gran dificultad técnica, además de requerir tecnología que no se encuentra ampliamente disponible. Consecuentemente, el tratamiento laparoscópico de los gastrinomas debe considerarse cuando la cirugía propuesta es una pancreatectomía distal o una pancreatoduodenectomía, o cuando se propone una enucleación en tumores únicos y localizados. Seguramente, cuando se trata de tumores múltiples en localizaciones diversas o en tumores metastásicos, el abordaje quirúrgico debe ser a través de una laparotomía.
La primera pancreatectomía distal laparoscópica para tumores neuroendocrinos del páncreas fue descrita por Michel Gagner en 1992. Una posterior publicación sobre su experiencia incluyó únicamente dos pacientes con gastrinomas sometidos a pancreatectomía laparoscópica distal, los que se complicaron con hemorragia en un caso y, en ambos casos, con fístulas pancreáticas 36. Existen otras publicaciones en forma de casos clínicos o pequeñas series de pacientes en conjunto con otros tumores neuroendocrinos pancreáticos, sobre resección laparoscópica de gastrinomas distales; ninguna de ellas informa seguimiento o resultados a largo plazo 37.
Técnica quirúrgica de la pancreatectomía laparoscópica distal en síndrome de Zollinger- Ellison
Con el paciente en posición ginecológica y en posición de Trendelenburg inverso, se aborda el abdomen con cuatro o cinco trocares. Se expone el cuerpo y la cola del páncreas a través de una ventana en el ligamento gastrocólico; mediante ecografía laparoscópica, se explora el páncreas en busca de los tumores para identificarlos y evaluar las opciones para su resección, enucleación o pancreatectomía distal. La enucleación se hace guiada por la ecografía, seccionando el parénquima pancreático alrededor del tumor; los vasos sanguíneos son coagulados o controlados con clips. Es recomendable aplicar algún tipo de fibrina para reforzar el sellado de la cavidad o podría también utilizarse epiplón para este fin. La pancreatectomía distal se practica mediante liberación y movilización del bazo y sección del cuerpo mediante grapadora lineal laparoscópica y refuerzo de la línea de sutura con sutura manual o fibrina selladora; como alternativa, se puede intentar la conservación del bazo manteniendo la irrigación a través de los vasos gastroesplénicos o liberando la arteria y la vena esplénicas del páncreas 36,38.
Controversias del tratamiento quirúrgico
Las controversias actuales del tratamiento quirúrgico del síndrome de Zollinger-Ellison son las siguientes.
1. Realización de procedimientos quirúrgicos durante la cirugía por gastrinoma para la reducción de la secreción ácida gástrica, como la vagotomía de células parietales 51. Este procedimiento reduce efectivamente la producción de ácido gástrico y la necesidad de uso prolongado de inhibidores de la bomba de protones en pacientes con enfermedad persistente o recurrente. Como consecuencia de la inhibición prolongada de la secreción ácida gástrica se produce aclorhidria que lleva a deficiencia de vitamina B12 y hierro 42; además, en pacientes con neoplasia endocrina múltiple de tipo 1, puede llevar al desarrollo de tumores neuroendocrinos gástricos malignos.
2. La curación quirúrgica de pacientes con síndrome de Zollinger-Ellison asociado a neoplasia endocrina múltiple de tipo 1 varía entre 0 y 10 %, cuando son operados mediante la técnica estándar 37,49.
La pancreatoduodenectomía es controversial debido al elevado potencial de morbilidad y mortalidad que tiene esta cirugía y al buen pronóstico general que tienen aún los gastrinomas malignos metastásicos a ganglios linfáticos, con una supervivencia demostrada de 52 % a 15 años 31,32,39,47,49,51. En la neoplasia endocrina múltiple de tipo 1, algunos estudios han demostrado curación hasta en 77 % de los casos un año después de la pancreatoduodenectomía 51. Los gastrinomas duodenales se presentan hasta en 90 % de los casos de neoplasia endocrina múltiple de tipo 1, por lo que algunos autores recomiendan la pancreatoduodenectomía como la cirugía de elección.
Otras indicaciones para esta cirugía son: un tumor muy grande en la cabeza del páncreas o el duodeno que no puede ser enucleado; múltiples tumores duodenales o de la cabeza del páncreas asociados a múltiples ganglios linfáticos regionales metastásicos, o recurrencia del gastrinoma después de la cirugía habitual con enucleación 39,37,51.
3. El manejo quirúrgico de las metástasis hepáticas del gastrinoma mejora la supervivencia hasta en 85 % a los cinco años de la cirugía. La recomendación actual es que se debe intentar la resección de las metástasis, siempre y cuando por lo menos el 90 % del tumor pueda ser resecado 42,51.
4. La cirugía laparoscópica del gastrinoma es un procedimiento complejo que se ha intentado en numerosas ocasiones, pero que tiene un elevado índice de conversión debido a la naturaleza propia del gastrinoma, y a tumores múltiples duodenales y en otras localizaciones extrapancreáticas frecuentemente asociados a metástasis.
Seguimiento
El seguimiento de los pacientes sometidos a tratamiento quirúrgico por síndrome de Zollinger-Ellison debe ser anual 42. Debe incluir estudios radiológicos tales como TC, ultrasonido, RM y la gammagrafía de receptores de somatostatina asociada a la PET; además, estudios funcionales de laboratorio para evaluar la posible recurrencia, como los de secreción de ácido gástrico, gastrina sérica en ayunas y prueba de estimulación de secretina; también, evaluación del estatus endocrino con pruebas de función paratiroidea, pituitaria y suprarrenal 4.
Resultados finales y pronóstico
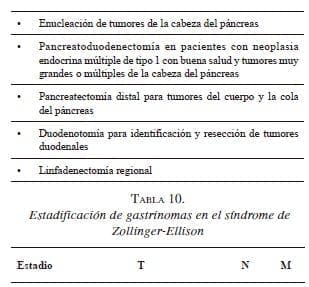
La estadificación para los pacientes con síndrome de Zollinger-Ellison esporádico y asociado a neoplasia endocrina múltiple de tipo 1 se detalla en la tabla 10.
Un paciente se considera libre de enfermedad cuando, después del tratamiento quirúrgico, los niveles de gastrina sérica en ayunas son normales, la prueba de estimulación de secretina es negativa y en los estudios radiológicos no se evidencian tumores 4.
Se considera que hay recurrencia del gastrinoma, cuando el paciente se encontraba libre de enfermedad después del tratamiento quirúrgico y, en el seguimiento, se encuentra elevación de la gastrina sérica en ayunas, la prueba de estimulación de secretina es positiva o se demuestran metástasis 4,7.
El principal factor que determina la supervivencia de los pacientes con gastrinoma es la presencia de metástasis hepáticas 8,9.
La cirugía resulta en la curación de aproximadamente 35 a 60 % de los pacientes con gastrinomas esporádicos. A los cinco años de la cirugía, el promedio de curación en estos casos es de 40 %. Los pacientes con gastrinoma asociado a neoplasia endocrina múltiple de tipo 1 raramente logran la curación de la enfermedad 47,49,51. La supervivencia en casos de gastrinomas de ganglios linfáticos después de cinco años de la resección quirúrgica, es comparable a la de pacientes con gastrinomas duodenales o pancreáticos 4,42,48,51. La cirugía tiene un impacto importante en la progresión de las metástasis hepáticas. En grandes series de pacientes operados, la supervivencia a 15 años es de 98 %, comparada con una supervivencia de 74 % en los no operados 42.
Conflicto de intereses: no existe ninguno.
Zollinger-Ellison syndrome: review of current knowledge
Abstract
Zollinger-Ellison syndrome is characterized by peptic ulcers refractory to treatment secondary to ectopic gastrin hypersecretion by a neuroendocrine tumor called gastrinoma resulting in gastric hydrochloride acid hypersecretion. This syndrome occurs sporadically and is also associated to Multiple Neuroendocrine Neoplasia type 1. The present article describes their clinical presentations, as well as their pathophysiology, diagnosis, study, treatment and prognosis, emphasizing the surgical technical details. Early diagnosis of gastrinoma carries a good prognosis, even in those malignant cases. Consequently, clinical suspicion associated to specific study leading to diagnosis and treatment is fundamental for these patients. Due to the available current technology, the diagnosis of these tumors should be more common, as a consequence the knowledge of important details within their management is important for the surgeon.
Key words: Zollinger-Ellison syndrome; gastrinoma; gastrins; multiple endocrine neoplasia; peptic ulcer.
Referencias
1. Zollinger RM, Ellison EH. Primary peptic ulcerations of the jejunum associated with islet cell tumor of the pancreas. Ann Surg. 1955;142:709-23.
2. Kent RB, van Heerden JA, Weiland LH. Nonfunctioning islet cell tumors. Ann Surg. 1981;193:185-90.
3. Stabile BE, Morrow DJ, Passaro E. The gastrinoma triangle: Operative implications. Am J Surg. 1984;147:25-31.
4. Norton JA, Alexander HR, Fraker DL, Venzon DJ, Gibril F, Jensen RT. Possibly primary lymph node gastrinoma: Oc¬currence, natural history, and predictive factors. Ann Surg. 2003;237:650-9.
5. Klöppel G, Clemens A. The biological relevance of gastric neuroendocrine tumors. Yale J Biol Med. 1996;69:69-74.
6. Hirschowitz BI. Pathobiology and management of hypergas¬trinemia and the Zollinger-Ellison syndrome. Yale J Biol Med. 1992;65:659-76.
7. Metz DC, Jensen RT. Gastrointestinal neuroendocrine tumors: Pancreatic endocrine tumors. Gastroenterology. 2008;135:1469-92.
8. Osefo N, Ito T, Jensen RT. Gastric acid hypersecretory sta¬tes: Recent insights and advances. Curr Gastroenterol Rep. 2009;11:433-41.
9. Jensen RT, Berna MJ, Bingham DB, Norton JA. Inherited pancreatic endocrine tumor syndromes: Advances in molecu¬lar pathogenesis, diagnosis, management, and controversies. Cancer. 2008;113(Suppl.):1807-43.
10. Bordi C, D’Adda T, Azzoni C, Ferraro G. Pathogenesis of ECL tumors in humans. Yale J Biol Med. 1998;71:273-84.
11. Waldum HL, Brenna E, Sandvik AK. Relationship of ECL cells and gastric neoplasia. Yale J Biol Med. 1998;71:325-35.
12. Burkitt MD, Varro A, Pritchard DM. Importance of gastrin in the pathogenesis and treatment of gastric tumors. World J Gastroenterol. 2009;15:1-16.
13. Doherty GM, Olson JA, Frisella MM, Lairmore TC, Wells SA, Norton JA. Lethality of multiple endocrine neoplasia type 1. World J Surg. 1998; 22:581-7.
14. Veldhuis JD, Norton JA, Wells SA, Vinik AI, Perry RR. Surgical versus medical management of multiple endocrine neoplasia (MEN) type 1. J Clin Endocrinol Metab. 1997;82:357-64.
15. Lopez CL, Waldmann J, Fendrich V, Langer P, Kann PH, Bartsch DK. Long-term results of surgery for pancreatic neu¬roendocrine neoplasms in patients with MEN-1. Langenbecks Arch Surg. 2011;396:1187-96.
16. Jkerström G, Stjlberg P, Hellman P. Surgical management of pancreatic-duodenal tumors in multiple endocrine neoplasia syndrome type 1. Clinics. 2012;67:173-8.
17. Wolfe MM, Jensen RT. Zollinger-Ellison syndrome – Cu¬rrent concepts in diagnosis and management. N Engl J Med. 1987;317:1200-9.
18. Feldman M, Schiller LR, Walsh JH, Fordtran JS, Richardson CT. Positive intravenous secretin test in patients with achlor¬hydria-related hypergastrinemia. Gastroenterology. 1987;93: 59-62.
19. Andersen DK. Current diagnosis and management of Zollinger- Ellison syndrome. Ann Surg. 1989;210:685-703.
20. Ito T, Cadiot G, Jensen RT. Diagnosis of Zollinger-Ellison syndrome: Increasingly difficult. World J Gastroenterol. 2012;18:5495-503.
21. Rehfeld JF, Gingras MH, Bardram L, Hilsted L, Goetze JP, Poi¬tras P. The Zollinger-Ellison syndrome and mismeasurements of gastrin. Gastroenterology. 2011;140:1444-53.
22. Poitras P, Gingras MH, Rehfeld JF. The Zollinger-Ellison syn¬drome: Dangers and consequences of interrupting antisecretory treatment. Clin Gastroenterol Hepatol. 2012;10:199-202.
23. Alexander HR, Fraker DL, Norton JA, Barlett DL, Tio L, Benjamin SB, et al. Prospective study of somatostatin receptor scintigraphy and its effect on operative outcome in patients with Zollinger-Ellison syndrome. Ann Surg. 1998;228:228-38.
24. Gibril F, Reynolds JC, Lubensky IA, Roy PK, Peghini PL, Doppman JL, et al. Ability of somatostatin receptor scintigraphy to identify patients with gastric carcinoids: A prospective study. J Nucl Med. 2000;41:1646-56.
25. Levy AD, Sobin LH. Gastrointestinal carcinoids: Imaging features with clinicopathologic comparison. Radio Graphics. 2007;27:237-57.
26. Sugg SL, Norton JA, Fraker DL, Metz DC, Pisegna JR, Fis¬hbeyn V, et al. A prospective study of intraoperative methods to diagnose and resect duodenal gastrinomas. Ann Surg. 1993;218:138-44.
27. Thompson NW, Vinik AI, Eckhauser FE. Microgastrinomas of the duodenum: A cause of failed operations for the Zollinger- Ellison syndrome. Ann Surg. 1989;209:396-404.
28. McCarthy DM. The place of surgery in the Zollinger-Ellison syndrome. N Engl J Med. 1980;302:1344-47.
29. Harmon JW, Norton JA, Collin MJ, Krudy AG, Shawker TH, Doppman JL, et al. Removal of gastrinomas for control of Zollinger-Ellison syndrome. Ann Surg. 1984;200:396-403.
30. Thomson AB, Sauve MD, Kassam N, Kamitakahara H. Safety of the long-term use of proton pump inhibitors. World J Gas¬troenterol. 2010;16:2323-30.
31. Norton JA, Fraker DL, Alexander R, Venzon DJ, Doppman JL, Serrano J, et al. Surgery to cure the Zollinger-Ellison syndrome. N Engl J Med. 1999;341:635-44.
32. Laimore TC, Chen VY, DeBenedetti MK, Gillanders WE, Norton JA, Doherty GM. Duodenopancreatic resections in patients with multiple endocrine neoplasia type 1. Ann Surg. 2000;231:909-18.
33. Norton JA, Alexander HR, Fraker DL, Venzon DJ, Gibril F, Jensen RT. Comparison of surgical results in patients with advanced and limited disease with multiple endocrine neoplasia type 1 and Zollinger-Ellison syndrome. Ann Surg. 2001;234:495-506.
34. Zogakis TG, Gibril F, Libutti SK, Norton JA, White DE, Jensen RT, et al. Management and outcome of patients with sporadic gastrinoma arising in the duodenum. Ann Surg. 2003;238:42-8.
35. Norton JA, Alexander HR, Fraker DL, Venzon DJ, Gibril F, Jensen RT. Does the use of routine duodenotomy (DUODX) affect rate of cure, development of liver metastases, or survi¬val in patients with Zollinger-Ellison syndrome? Ann Surg. 2004;239:617-26.
36. Assalia A, Gagner M. Laparoscopic pancreatic surgery for islet cell tumors of the pancreas. World J Surg. 2004;28:1239-47.
Pierce RA, Spitler JA, Hawkins WG, Strasberg SM, Linehan DC, Halpin VJ, et al. Outcomes analysis of laparoscopic
resection of pancreatic neoplasms. Surg Endosc. 2007;21: 579-86.
38. Fernández-Cruz L, César-Borges G. Laparoscopic strategies for resection of insulinomas. J Gastrointest Surg. 2006;10:752-60.
39. Norton JA. Surgery for primary pancreatic neuroendocrine tumors. J Gastrointest Surg. 2006;10:327-31.
40. Norton JA, Fraker DL, Alexander HR, Gibril F, Liewehr DJ, Venzon DJ, et al. Surgery increases survival in patients with gastrinoma. Ann Surg. 2006;244:410-9.
41. Imamura M, Komoto I, Ota S. Changing treatment strategy for gastrinoma in patients with Zollinger-Ellison syndrome. World J Surg. 2006;30:1-11.
42. Morrow EH, Norton JA. Surgical management of Zollinger- Ellison syndrome: State of the art. Surg Clin North Am. 2009;89:1091-103.
43. Imamura M. Recent standardization of treatment strategy for pancreatic neuroendocrine tumors. World J Gastroenterol. 2010;16:4519-25.
44. Imamura M, Komoto I, Ota S, Hiratsuka T, Kosugi S, Doi R, et al. Biochemically curative surgery for gastrinoma in multiple endocrine neoplasia type 1 patients. World J Gastroenterol. 2011;17:1343-53.
45. Fendrich V, Bartsch DK. Surgical treatment of gastroin¬testinal neuroendocrine tumors. Langenbecks Arch Surg. 2011;396:299-311.
46. Norton JA, Harris EJ, Chen Y, Visser BC, Poultsides GA, Kunz PC, et al. Pancreatic endocrine tumors with major vascular abutment, involvement, or encasement and indication for resection. Arch Surg. 2011;146:724-32.
47. Norton JA, Jensen RT. Resolved and unresolved controversies in the surgical management of patients with Zollinger-Ellison syndrome. Ann Surg. 2004;240:757-73.
48. Vargas CC, Castaño R. Tumores neuroendocrinos gastroente¬ropancreáticos. Rev Colomb Gastroenterol. 2010;25:165-76.
49. Epelboym I, Mazeh H. Zollinger-Ellison syndrome: Clas¬sical considerations and current controversies. Oncologist. 2014;19:44-50.
50. Zhang IY, Zhao J, Fernández-del-Castillo C, Braun Y, Razmdjou S, Warshaw AL, et al. Operative versus nonoperative manage¬ment of nonfunctioning pancreatic neuroendocrine tumors. J Gastrointest Surg. 2016;20:277-83.
51. Norton JA, Alexander RH, Fraker DL, Venzon DJ, Gibril F, Jensen RT. Comparison of surgical results in patients with ad¬vanced and limited disease with multiple endocrine neoplasia type 1 and Zollinger-Ellison syndrome. Ann Surg. 2001;234: 495-506.
Correspondencia: Marcelo A. Beltrán, MD
Correo electrónico: Beltran_01@Yahoo.Com
La Serena – IV Región, Chile
