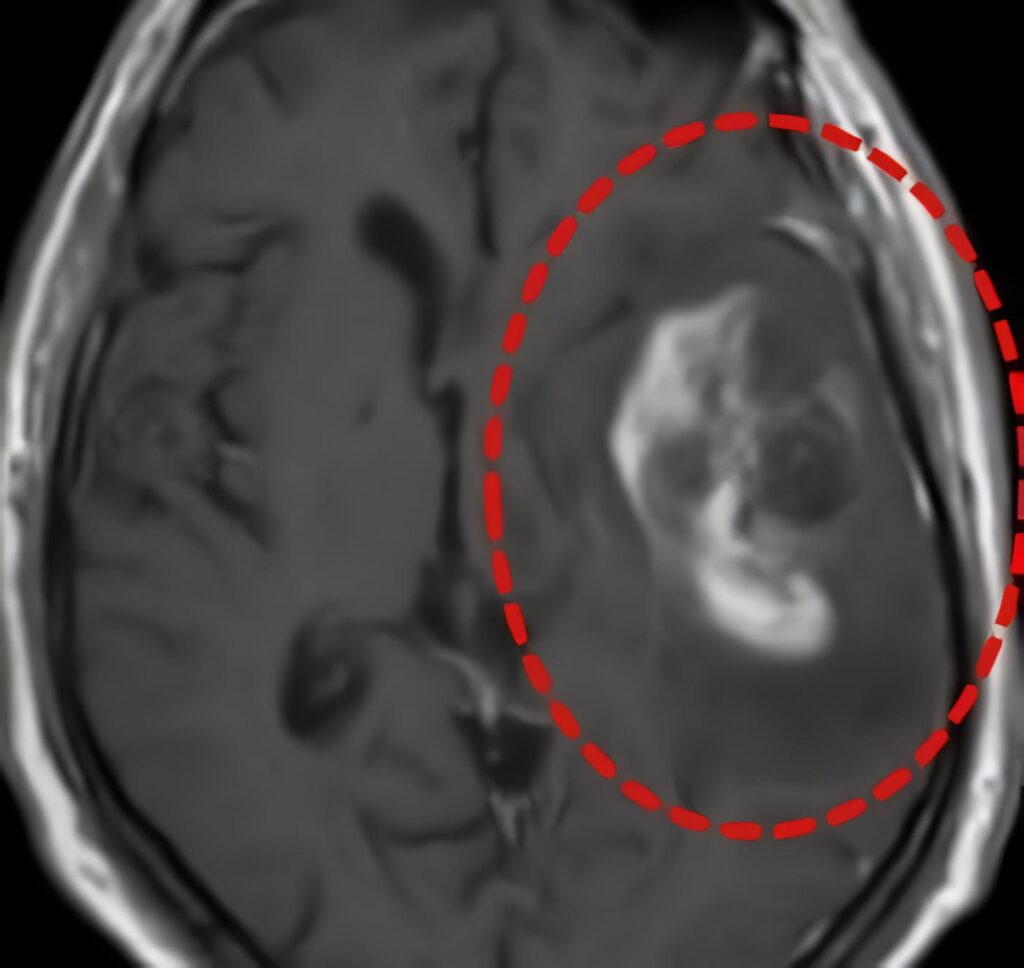
Pacientes con Gliobastoma Multiforme
En cuanto a la pregunta, si el volumen tumoral está asociado con la sobrevida? Es importante comentar que el astrocitoma anaplasico y el glioblastoma multiforme tienen la tendencia característica de infiltrar microscopicamente tejido cerebral perilesional y es claro que la tomografía cerebral y la resonancia magnética no pueden fácilmente diferenciarla.
La mayoría de estudios no ha mostrado efecto directo del volumen tumoral y el pronóstico.
Un alto nivel de vascularizacion ha sido reconocido como indicador de potencial maligno, puesto que este refleja el grado de angiogenesis tumoral, reflejando la relación entre angiogenesis y la habilidad del tumor para alimentarse y aumentar la masa tumoral. En los tumores de alto grado, la proliferación de células endoteliales es un evento clave, en los gliomas de bajo grado este suceso es más bien raro.
La densidad de microvasos, un medidor histologico de la vascularidad, ha sido estudiada y se ha demostrado que en los gliomas de bajo grado fue un indicador de sobrevida. En dicho estudio se incluyeron Pacientes con Gliobastoma Multiforme de alto grado.
A pesar del tratamiento agresivo multimodal que comprende la resección quirúrgica, quimioterapia local y sistémica, la sobrevida media está en el rango de los doce meses, se ha encontrado un grupo de pacientes, aunque pequeña con sobrevida de mas de 36 meses, que son conocidos como los sobrevivientes a largo plazo.
Resulta interesante mencionar a los sobrevivientes a largo plazo, los cuales son raros, y en donde se han identificado diversas variables tamaño del tumor y localización, edad de presentación, estado funcional (Karnofsky) al momento del diagnóstico, hallazgos histológicos, factores genéticos y moleculares. Solo el 2% de los pacientes logra vivir hasta tres años. (35)
Sobrevida postoperatoria
Diversos estudios han mostrado una relación negativa entre la edad avanzada y la sobrevida postoperatoria, algunos estudio han revelado que los pacientes menores de 40 años sobrevivirán alrededor de 34% a los 5 años comparados con los pacientes mayores de 40 años. (36)
En relación a los Pacientes con Gliobastoma Multiforme ancianos, ésta ejerce una fuerte influencia negativa sobre la sobrevida, la cual es realmente pobre. Analizando datos del registro de tumores cerebrales en los estados Unidos se revela que las tasas de sobrevida a 1 año están alrededor del 16.9 % en pacientes entre los 65 y 74 años de dad y en 8.2 % en pacientes mayores de 75 años.
A los 2 años la tasa de sobrevida disminuye a 2.7 % y 1.3% respectivamente.
Un trabajo reciente propone que los Pacientes con Gliobastoma Multiforme manejados con medicamentos antiepilépticos inductores enzimáticos sobreviven más tiempo, además de ocurrir de manera interesante un enlentecimiento de la progresión de la enfermedad que cuando se comparan con pacientes manejados con otros drogas antiepilépticas, estos inductores enzimáticos son el fenobarbital, fenitoína, carbamazepina y la primidona, los cuales modulan enzimas microsomales como la P450 que mejoran la función de los agentes quicioterapéuticos, siendo este un factor predictivo independiente de superviviencia libre de progresión en gliomas de alto grado.
Se ha conceptualizado también que pacientes con mayores puntajes de Karnosfky pueden tener mejor pronóstico.
En importante definir un concepto reciente conocido como pseudoprogresión, el cual denota la aparente progresión después del tratamiento incluido radioterapia y temozolamida y es mayormente definido por la resonancia magnética posradioterapia. (31, 32, 33).
La pseudoprogresión fue inicialmente descrita por Hoffman y Cols. en Pacientes con Gliobastoma Multiforme diagnosticado de primera vez y en tratamiento de radioterapia con o sin carmustina.
Progresión de la enfermedad
De los Pacientes con Gliobastoma Multiforme observados experimentaron progresión de la enfermedad después de radioterapia 28 a 51% y del 38 al 33% revelaron mejoría o estabilización de la enfermedad. (34)
Conclusiones
Finalmente, es importante mencionar la utilidad de estudios de imágenes como la tomografía por emisión de positrones en el manejo de gliomas, esta técnica usa radiotrazadores de vida media corta, a concentraciones micro o nanomolares para obtener información cuantitativa sobre procesos de transporte, metabolismo y expresión de receptores como también el efecto de fármacos sobre los tejidos humanos.
Esta técnica se puede fusionar con la resonancia magnética obteniéndose imágenes en 3D.
Trazadores como la 18 F-Desoxiglucosa son capaces de diferencias gliomas de bajo y alto grado y la C 11- metionina es capaz de mejorar el contraste de la imágenes para determinar la extensión de los gliomas y es mejor para determinar la actividad cerebral normal cuando se compara con la18 F-desoxiglucosa. (22, 23, 24, 25, 26, 27, 28).
Conflictos de Intereses:
ninguno que declarar.
Financiación:
Recursos propios de los autores.
Referencias Bibliográficas
- 1. Lacroix M, Abi-Said D, Fourney DR, et al. A multivariate analysis of 416 patients with glioblastoma multiforme: prognosis, extent of resection, and survival, J Neurosurg, 2001;95:190–98.
- 2. Stewart LA, Chemotherapy in adult high-grade glioma: a systematic review and meta-analysis of individual patient data from 12 randomised trials, Lancet, 2002;359:1011–18
- 3. O’Reilly SM, Newlands ES, Glaser MG, et al., Temozolomide: a new oral cytotoxic chemotherapeutic agent with promising activity against primary brain tumours, Eur J Cancer, 1993;29A:940–42
- 4. Stupp R, Dietrich PY, Ostermann Kraljevic S, et al. Promising survival for patients with newly diagnosed glioblastoma multiforme treated with concomitant radiation plus temozolomide followed by adjuvant temozolomide, J Clin Oncol, 2002;20:1375–82.
- 5. Stummer W, Reulen HJ, Meinel T, Pichlmeier U, Schumacher W, Tonn JC, Rohde V, Oppel F, Turowski B, Woiciechowsky C, Franz K, Pietsch T; ALA-Glioma Study Group.Neurosurgery. Extent of resection and survival in glioblastoma multiforme: identification of and adjustment for bias.2008 Mar;62(3):564-76; discussion 564-76
- 6. Glioblastomas: correlation between oligodendroglial components, genetic abnormalities, and prognosis. Pinto LW, Araújo MB, Vettore AL, Wernersbach L, Leite AC, Chimelli LM, Soares FA. Virchows Arch. 2008 May;452(5):481-90.
- 7. Stupp R, Mason WP, van den Bent MJ, et al. Radiotherapy plus concomitant and adjuvant temozolomide for glioblastoma, N Engl J Med, 2005;352:987–96.
- 8. Westphal M, Hilt DC, Bortey E, et al., A phase III trial of local chemotherapy with biodegradable carmustine (BCNU) wafers (Gliadel wafers) in patients with primary malignant glioma, Neuro Oncol, 2003;5:79–88.
- 9. Vredenburgh JJ, Desjardins A, Herndon JE II, et al., Phase II trial of bevacizumab and irinotecan in recurrent malignant glioma, Clin Cancer Res, 2007;13:1253–9.
- 10. Maxwell JA, Johnson SP, Quinn JA, et al., Quantitative analysis of O6-alkylguanine-DNA alkyltransferase in malignant glioma, Mol Cancer Ther, 2006;5:2531–9.
- 11. Therasse P, Arbuck SG, Eisenhauer EA, Wanders J, Kaplan RS, Rubinstein L, et al. New guidelines to evaluate the response to treatment in solid tumors. European Organization for Research and Treatment of Cancer, National Cancer Institute of the United States, National Cancer Institute of Canada. J Natl Cancer Inst. 2000;92:205-16.
- 12. Walker MD, Alexander E Jr, Hunt WE, MacCarty CS, Mahaley MS Jr, Mealey J Jr, et al. Evaluation of BCNU and/or radiotherapy in the treatment of anaplastic gliomas. A cooperative clinical trial. J Neurosurg. 1978;49:333-43.
- 13. Brada M, Thomas DG, Bleehan NM, Roberts JT, Senanayake F, Abram P, et al. Medical Research Council (MRC) randomized trial of adjuvant chemotherapy on high grade glioma (HGG)-BR05. Proc Am Soc Clin Oncol. 1998;17: A1543.
- 14. Levin VA, Silver P, Hannigan J, Wara WM, Gutin PH, Davis RL, et al. Superiority of postradiotherapy adjuvant chemotherapy with CCNU, procarbazine, and vincristine (PCV) over BCNU for anaplastic gliomas: NCOG 6G61 final report. Int J Radiat Oncol Biol Phys. 1990;18:321-4.
- 15. Cavazos CM, Keir ST, Yoshinari T, Bigner DD, Friedman HS. Therapeutic activity of the topoisomerase I inhibitor J-107088 [6-N-(1-hydroxymethyla-2-hydroxyl) ethylamino- 12,13- dihydro-13-(beta-D-glucopyranosyl) -5H-indolo [2,3-a]-pyrrolo[3,4-c]-carbazole-5,7(6H)- dione]] against pediatric and adult central nervous system tumor xenografts. Cancer Chemother Pharmacol. 2001;48:250-4.
- 16. Hegi ME, Diserens AC, Gorlia T, Hamou MF, de Tribolet N, Weller M, et al. MGMT gene silencing and benefit from temozolomide inglioblastoma. N Engl J Med. 2005;352:997- 1003.
- 17. Pech IV, Peterson K, Cairncross JG. Chemotherapy for brain tumors. Oncology. 1998;12:537- 43.
- 18. Williston Park.Russell D, Rubinstein L. Pathology of Tumors of the Central Nervous System. 5th ed. Baltimore, Williams & Wilkins, 1989, p. 1012.
- 19. Helseth A, Mark SJ. Neoplasms of the central nervous system in Norway: III. Epidemiological characteristics of intracranial gliomas according to histology. A.P.M.I.S. 1989; 97: 547–55.
- 20. Wong ML, Prawira A, Kaye AH, Hovens CM. Tumour angiogenesis: its mechanism and therapeutic implications in malignant gliomas. J Clin Neurosci. 2009 Sep;16(9):1119-30.
- 21. Chang SM, Parney IF, McDermott M, et al. Perioperative complications and neurological outcomes of first and second craniotomies among patients enrolled in the Glioma Outcome Project. J Neurosurg. 2003; 98(6): 1175-81.
- 22. Beany RP. Positron emission tomography in the study of hu-man tumors. Sem Nucl Med 1984;14:324-41.
- 23. Silverman DHS, Hoh CK, Seltzer MA, Schiepers C, Cuan GS Gambir SS, et al. Evaluating Tumor Biology and Oncological Disease with Positron Emission Tomography. Seminars in Ra- diation Oncology 1998;3:183-96.
- 24. Hawkins RA, Hoh C, Dahlbom M, Choi Y, Glaspy J, Tse N, et al. PET cancer evaluations with FDG. J Nucl Med 1991;32(8): 1555-8.245
- 25. Rigo P, Paulus P, Kaschten BJ, Hustinx R, Bury T, Jerusalem G, et al. Oncologic applications of positron emission tomo-graphy with fluorine-18 fluorodeoxyglucose. Eur J Nucl Med 1996;23:1641-74.
- 26. Heiss WD, Wienhard K, Wagner R, Lanfermann H, Thiel A, Herholz K, et al. F-Dopa as an amino acid tracer to detect brain tumors. J Nucl Med 1996;37(7):1180-2.
- 27. Inoue T, Koyama K, Oriuchi N, Alyafei S, Yuan Z, Suzuki H, et al. Detection of Malignant Tumors: whole-body PET with fluorine 18 alpha-methyl tyrosine versus FDG-preliminary study. Radiology 2001;220:54-62.
- 28. Weber WA, Wester HJ, Grosu AL, Herz M, Dzewas B, Feld- mann HJ, et al. O-(2-[18F] fluoroethyl)-L-tyrosine and L-[methyl-11C]methionine uptake in brain tumours: initial results of a comparative study. Eur J Nucl Med 2000;27(5):542-9
- 29. Cairncross JG, Ueki K, Zlatescu MC, et al. Specific genetic predictors of chemotherapeutic response and survival in patients with anaplastic oligodendrogliomas. J Natl Cancer Inst 1998;90:1473–1479
- 30. Madajewicz S, Chowhan N, Tfayli A, Roque C,et al. Therapy for patients with high grade astrocytoma using intraarterial chemotherapy and radiation therapy. Cancer. 2000 May 15;88(10):2350-6
- 31. Robins HI, Lassman AB, Khuntia D.Therapeutic advances in malignant glioma: current status and future prospects. Neuroimaging Clin N Am. 2009 Nov;19(4):647-56.
- 32. Brandes AA, Franceschi E, Tosoni A, et al: MGMT promoter methylation status can predict incidence and outcome of pseudoprogression after concomitant radiochemotherapy in newly diagnosed glioblastoma. J Clin Oncol 26:2192- 2197, 2008
- 33. Taal W, Brandsma D, de Bruin HG, et al: Incidence of pseudo-progression in a cohort of malignant glioma patients treated with chemoirradiation with temozolomide. Cancer 113:405- 4 1 0 , 2008
- 34. Hoffman WF, Levin VA, Wilson CB. Evaluation of malignant glioma patients during the postirradiation period. J Neurosurg 50:624-628, 1979
- 35. Scott JN, Rewcastle NB, Brasher PM, et al. Which glioblastoma multiforme patient will become a long-term survivor? A population-based study. Ann Neurol 1999 Aug;46(2):183–8.
- 36. Korshunov A, Sycheva R, Golanov A. The prognostic relevance of mo lecular alterations in glioblastomas for patients age < 50 years. Cancer 2005 Aug 15;104(4):825–32.