vZika y SGB
Dado el aumento de complicaciones neurológicas asociadas con el vZika, principalmente SGB y microcefalia, se hizo necesario establecer hipótesis que permitieran determinar las causas de dicha asociación, siendo las más plausibles el mimetismo molecular y la toxicidad directa del vZika sobre el sistema nervioso.
Por un lado, se propone que el mimetismo molecular entre glucolípidos, presentes en las capas de mielina y en el axolemma, y moléculas de superficie de agentes infecciosos puede explicar la mayoría de los casos de SGB precedidos por una infección, mientras que la toxicidad directa de vZika sobre las células neuronales se ha planteado como un mecanismo por el cual vZika induce la microcefalia. Sin embargo no se descarta que dicho mecanismo pueda estar también relacionado con el SGB (26).
VZika y retos en el diagnóstico
Un reto importante en relación con la infección tiene que ver con el diagnostico, ya que la mayoría de los casos reportados han sido diagnosticados por sospecha clínico-epidemiológica y no por laboratorio.
Adicional a esto, varios protocolos de reacción en cadena de la polimerasa con transcriptasa inversa (RT-PCR) han sido descritos y pueden generar resultados diversos y hasta contradictorios. Así mismo, existen varias pruebas serológicas comerciales para la detección de anticuerpos contra el virus que deben ser utilizadas con precaución dada la alta reactividad cruzada con otros arbovirus.
En este sentido, no hay que olvidar que en Colombia, existe la circulación simultánea de otros arbovirus que también pueden causar SGB y que deben ser considerados en el diagnóstico diferencial (27,28). (Ver también: La Inmunomodulación inducida por los Helmintos)
vZika y trombocitopenia
La evidencia de trombocitopenia autoinmune ha sido confirmada en varios reportes de caso y estudios descriptivos (7). Sin embargo, los mecanismos fisiopatológicos se desconocen. No obstante, esta observación permitió realizar una revisión de la literatura.
Se encontraron 14 artículos que evidenciaron la presencia de trombocitopenia relacionada con la infección por vZika. A partir de estos estudios, se describieron menos de 25 casos (al menos dos casos se informaron dos veces).
En todos los casos excepto en uno, los niveles de trombocitopenia fueron inferiores a 100.000/uL. Aunque se reportaron algunos casos fatales, la mayoría de los pacientes respondieron bien al tratamiento inmunomodulador (29).
vZika y SGB en Colombia
Una revisión sistemática sobre la situación del SGB en Colombia, previo a la epidemia del vZika, evidenció que la mayoría de los pacientes fueron hombres (67%). Adicionalmente, se encontró que un gran porcentaje de los casos fueron pacientes menores de 50 años (94%), y cerca del 70% tenían menos de 20 años.
Igualmente, se documentó que el subfenotipo más frecuente de GBS en Colombia corresponde a la polineuropatía desmielinizante aguda idiopática (AIDP). Por otro lado, el antecedente de infección previa al inicio del SGB se obtuvo en el 31% de los casos reportados.
Finalmente, en relación con los manejos instaurados, los artículos publicados antes de 1980 describieron enfoques de tratamiento que incluían asistencia respiratoria y tratamiento sintomático, hormona adrenocorticotrópica intravenosa o corticoides. Artículos posteriores describieron el tratamiento con inmunoglobulinas intravenosas o plasmaféresis, junto con asistencia respiratoria (30).
Conociendo la situación del SGB en Colombia y observando un aumento de los casos de este síndrome en el país (Figura 2), se decidió realizar un estudio multidisciplinario en Cúcuta, Norte de Santander, una de las ciudades más afectadas por infecciones transmitidas por arbovirus (6), con el fin de evaluar la respuesta autoinmune en aquellos individuos infectados por vZika (13,14).
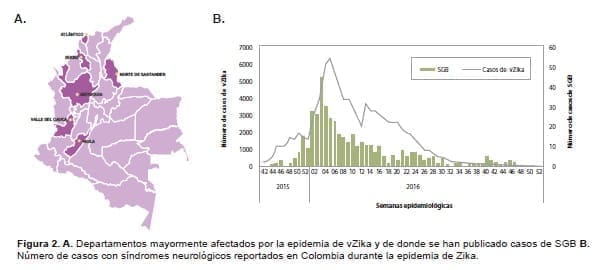
Se utilizaron datos de pacientes con enfermedad de vZika notificados al sistema de vigilancia poblacional nacional para calcular el número de reproducción básica (Ro) y las tasas de ataque, es decir el número de personas que presentaron la enfermedad por vZika en relación con el número de personas expuestas al riesgo de sufrir dicha enfermedad en un período limitado de tiempo durante la epidemia. Los pacientes con síndromes neurológicos fueron contactados y sus diagnósticos fueron confirmados (6).
El valor estimado del Ro osciló entre 2,68 (IC del 95%: 2,54-2,67) a 4,57 (IC del 95%: 4,18-5,01). La tasa de ataque fue 1306 por 100.000 mujeres y 552 por 100.000 hombres. Se observó una interacción no lineal entre la edad y el sexo en las tasas de ataque (6).
Se realizó un estudio de asociación basado en casos y controles en el que se incluyeron 29 pacientes con SGB asociado con vZika que fueron comparados con 74 controles pareados por género, edad y barrio, con antecedente de infección por vZika, sin manifestaciones neurológicas. Se evaluaron anticuerpos contra arbovirus y otras infecciones que pudieran desencadenar SGB (6).
Los resultados del estudio mostraron durante la epidemia ocasionada por el vZika en Cúcuta, el SGB aumentó más de 4 veces, y que el bajo nivel socioeconómico, vivir cerca de zonas de alta contaminación e infecciones previas favorecieron el desarrollo del síndrome.
En particular, el antecedente de haber cursado con M. pneumoniae aumentó cerca de cuatro veces el riesgo de desarrollar SGB en personas infectadas por vZika; un hallazgo que está siendo confirmando en otras ciudades. Además del SGB, el vZika puede ocasionar compromiso de la médula espinal (mielitis), del cerebro (encefalitis) y de nervios craneales (parálisis facial) (6).
El subfenotipo AIDP fue diagnosticado en el 70% de los pacientes. El 40% de los nervios de pacientes con AIDP mostraron una participación desmielinizante distal prevalente, pero este patrón no es específico de la AIDP asociaciada al vZika (31).
Adicionalmente, se observó que la presencia de disautonomía en el GBS asociado a vZika fue el principal indicador de mal pronóstico. Se encontró que los pacientes con SGB asociado al vZika tuvieron una mayor frecuencia de disautonomía (75,9%) en comparación con el SGB asociacado a otras infecciones.
Estos hallazgos motivaron la realización de un estudio de asociación en el que se pudo observar que los pacientes con el antecedente de infección por vZika sin compromiso neurológico evidente presentaron puntajes más altos de disautonomía (medidos por medio del COMPASS-31, instrumento validado para la evaluación de síntomas asociados a disfunción autonómica), que aquellos controles sin antecedente de infección por vZika (9).
vZika y otros síndromes neurológicos en Colombia
Trece pacientes fueron diagnosticados con otros síndromes neurológicos diferentes al SGB (6 con MT, 3 con encefalitis, 3 con parálisis facial periférica y uno con mielopatía toraco-lumbosacra) (6). Los datos confirmaron una mayor transmisión del vZika en Cúcuta, y mostraron la asociación entre síndromes neurológicos severos relacionados con la infección por vZika.
Las formas complejas por las cuales las infecciones previas y el estatus socioeconómico interactúan para aumentar el riesgo de SGB en las personas infectadas por vZika deben ser investigadas más a fondo.
VZika y autoinmunidad tiroidea y reumatológica
Se realizó un análisis de autoinmunidad tiroidea y reumatológica mediante un estudio de asociación basado en casos y controles en el que se evaluó, mediante inmunoensayo, la presencia de un panel de 14 autoanticuerpos en los pacientes con SGB (Figura 3).
Aunque algunos pacientes presentaron autoinmunidad reumatológica y tiroidea, no se observaron diferencias entre los pacientes con SGB-vZika y los pacientes con infección por vZika sin síndromes neurológicos. Además, no se encontraron diferencias entre la presencia de auto-anticuerpos en pacientes con enfermedad por vZika y controles sanos (29).

Plausibilidad genética
El proyecto RAIZ permitió la realización del primer análisis del genoma completo en pacientes con infección por vZika que desarrollaron SGB post-viral, mediante un estudio de asociación en el que se examinó la cohorte de 116 pacientes con infección por vZika y 1.536 controles no afectados (32).
La confirmación de la infección por vZika se realizó mediante la prueba de neutralización por reducción en placas, ELISA e inmunofluorescencia, tal como descrito (31). Las muestras fueron genotipificadas mediante el “Affymetrix Axioma Genoma-Wide LAT 1 Array 4”.
Después del control de calidad, 380.599 polimorfismos de nucleótido simple fueron evaluados en 95 casos y 1.366 controles. Los análisis estadísticos se realizaron en el programa PLINK (http://pngu.mgh.harvard.edu/ purcell/plink/). El análisis de componentes principa les se utilizó para detectar y cuantificar la estructura genética de las poblaciones. La imputación se realizó utilizando IMPUTE2 (33).
Los datos fueron ajustados mediante control genético y la tasa de falsos descubrimientos. Para cada polimorfismo se calcularon las ra- zones de disparidad (OR) y los intervalos de confianza del 95% (IC95%). El nivel de significancia establecido fue 5.0E-08.
Un primer análisis reveló tres polimorfismos asocia- dos con la infección por ZIKV, en los genes MYEOV2, KCNQ3 y C12orf40, ubicados en los cromosomas 2, 8 y 12, respectivamente. Un segundo análisis, que inclu- yó sólo pacientes con SGB post-viral, predijo un poli- morfismo stop-gain en el gen APOBEC3G, en 22q13.1 (OR: 2,06, IC95%: 1,17-3,61, p=8,01E-08) (Figura 4).
MYEOV2, también conocido como subunidad 9 del complejo de signalosoma COP9, tiene 2 isoformas altamente expresadas en el sistema nervioso central. KCNQ3 codifica una proteína que participa en la regu- lación de la excitabilidad neuronal. C12orf40 (Chromo-some 12 Open Reading Frame 40) es un gen codifica- dor de proteína, cuya función aún no se conoce bien.
APOBEC3G es un miembro de la familia APOBEC3 (del inglés apolipoprotein B mRNA editing enzyme, catalytic polypeptide-like 3), cuya proteína tiene ca- pacidad antiviral. APOBEC3G se expresa, particular mente, en linfocitos T, macrófagos, células dendríticas mieloides y células dendríticas plasmocitoides. Futuros estudio de replicación y meta-análisis son necesa- rios para confirmar estos resultados.
 Conclusiones y perspectivas A pesar de que en el SGB predomine una respuesta hu-moral sobre aquella mediada por células T, al menos en la fase progresiva de la lesión del nervio y en las formas axonales, los mecanismos de interacción entre los facto- res infecciosos y del hospedero que conducen a una res- puesta autoinmune no son completamente conocidos.
Conclusiones y perspectivas A pesar de que en el SGB predomine una respuesta hu-moral sobre aquella mediada por células T, al menos en la fase progresiva de la lesión del nervio y en las formas axonales, los mecanismos de interacción entre los facto- res infecciosos y del hospedero que conducen a una res- puesta autoinmune no son completamente conocidos.
Por lo tanto, en los casos de SGB será importante dis- tinguir entre la neurotoxicidad del vZIKA, demostrada desde su descubrimiento, y la generación de respuesta autoinmune por mimetismo molecular (u otro). Es posible que la inmunidad poblacional proteja contra una nueva epidemia por cerca de una década.
Sin embargo, dadas las secuelas a largo plazo de este y otros arbovirus, así como la posibilidad de nuevas epidemias trasmitidas por el mismo vector, la investigación tras- lacional y la colaboración nacional e internacional deben ser una prioridad permanente de las entidades académicas y gubernamentales, con el fin de mejorar la calidad de la misma y ofrecer respuestas a proble- mas nacionales con repercusión regional y mundial.
Los resultados aquí resumidos del proyecto RAIZ son, por lo tanto, de utilidad para el diseño de políticas públicas, medidas de prevención y predicción de patologías asociadas al vZika, así como para el desarrollo de estrategias científicas ante futuras epidemias.
Conflicto de intereses
Ninguno
Financiación
Este proyecto fue financiado por la Universidad del Rosario (ABN011), y Colciencias (747-2016), Bogotá, Colombia.
Agradecimientos
Los autores expresan su gratitud y reconocimiento a todos los miembros del Centro de Estudio de Enfermedades Autoinmunes (CREA), a los colegas que han participado en el desarrollo de los estudios sobre autoinmunidad asociada al vZika y a la Alcaldía de Cúcuta por su apoyo y contribuciones al presente trabajo. Los autores declaran no tener ningún conflicto de interés.
Referencias
1. Dick GWA, Kitchen SF HA. Zika virus. I. Isolations and serological specificity. Trans R Soc Trop Med Hyg 195. 1952;46(5):509–20.
2. ICTV. International comittee on taxonomy of viruses. Vi¬rus taxonomy. 2014. Release 2015.
3. Duffy M. Chen T.Hancock T. Powers A. Kool J. Lan¬ciotti R. Pretrick M. Zika Virus Outbreak on Yap Is¬land, Federated States of Micronesia. N Engl J Med. 2009;360:2536–43.
4. Lessler J, Chaisson LH, Kucirka LM, et al. Assess¬ing the global threat from Zika virus. Science. 2016 Aug;353(6300):aaf8160.
5. Cao-Lormeau V-M, Blake A, Mons S, Lastère S, Roche C, Vanhomwegen J, et al. Guillain-Barré Syn¬drome outbreak associated with Zika virus infection in French Polynesia: a case-control study. Lancet. 2016 Apr;387(10027):1531–9.
6. Anaya J-M, Rodríguez Y, Monsalve DM, Vega D, Ojeda E, Gonz Alez-Bravo D, et al. A comprehensive analysis and immunobiology of autoimmune neurological syn¬dromes during the Zika virus outbreak in Cúcuta, Co-lombia. J Autoimmun. 2016;77:123–38.
7. Karimi O, Goorhuis A, Schinkel J, Codrington J, Vreden SGS, Vermaat JS, et al. Thrombocytopenia and subcu¬taneous bleedings in a patient with Zika virus infection. Vol. 387, Lancet. England; 2016. p. 939–40.
8. Carteaux G, Maquart M, Bedet A, Contou D, Brugières P, Fourati S, et al. Zika Virus Associated with Meningo-encephalitis. N Engl J Med. 2016 Apr;374(16):1595–6.
9. Rodriguez Y, Monsalve D, Acosta-Ampudia Y, Mola¬no-González N, Ramírez-Santana C, Anaya JM. Dis-autonomia en pacientes con infección por virus Zika. VII Simp Nac y III Congr Latinoam Virol. 2017; DOI: 10.16925/greylit.2097 (enviado a publicación)
10. Pinto-Diaz CA, Rodriguez Y, Monsalve DM, Acosta-Ampu¬dia Y, Molano-Gonzalez N, Anaya J-M, et al. Autoimmunity in Guillain-Barre syndrome associated with Zika virus infec¬tion and beyond. Autoimmun Rev. 2017 Apr;16(4):327–34.
11. Chalela JA. Pearls and pitfalls in the intensive care man¬agement of Guillain-Barré syndrome. Semin Neurol. 2001;21(4):399–405.
12. Willison HJ, Jacobs BC, van Doorn PA. Guillain-Barre syndrome. Lancet. 2016 Aug;388(10045):717–27.
13. Jasti AK, Selmi C, Sarmiento-Monroy JC, Vega DA, An¬aya J-M, Gershwin ME. Guillain-Barre syndrome: caus-es, immunopathogenic mechanisms and treatment. Ex¬pert Rev Clin Immunol. 2016 Nov;12(11):1175–89.
14. Anaya J, Ramirez-Santana C, Salgado-Castaneda I, Chang C, Ansari A, Gershwin M. Zika virus and neu-rologic autoimmunity: the putative role of gangliosides. BMC Med. 2016;14.
15. Anaya J-M. The autoimmune tautology. A summary of evidence. Joint, bone, spine.2017;84: 251–3.
16. Anaya J-M, Ramirez-Santana C, Alzate MA, Mola¬no-Gonzalez N, Rojas-Villarraga A. The Autoimmune Ecology. Front Immunol. 2016;7:139.
17. Paixao ES, Barreto F, Teixeira M da G, Costa M da CN, Rodrigues LC. History, Epidemiology, and Clinical Man¬ifestations of Zika: A Systematic Review. Am J Public Health. 2016 Apr;106(4):606–12.
18. Mesci P, Macia A, Moore SM, Shiryaev SA, Pinto A, Huang C-T, et al. Blocking Zika virus vertical transmis¬sion. Sci Rep. 2018;8(1):1218.
19. Zanluca C, de Noronha L, Duarte Dos Santos CN. Ma¬ternal-fetal transmission of the zika virus: An intriguing interplay. Tissue barriers. 2017 Nov;e1402143.
20. Musso D, Nilles EJ, Cao-Lormeau VM. Rapid spread of emerging Zika virus in the Pacific area. Clin Microbiol Infect. 2014;20(10):595–6.
21. Dupont-Rouzeyrol M, O ’connor O, Calvez E, Daures M, John M, Grangeon J-P, et al. Co-infection with Zika and Dengue Viruses in 2 Patients, New Caledonia, 2014. Emerg Infect Dis. 2015;21:381–2.
22. Pyke AT, Daly MT, Cameron JN, Moore PR, Taylor CT, Hewitson GR, et al. Imported zika virus infection from the cook islands into australia, 2014. PLoS Curr. 2014;6:1–7.
23. Wæhre T, Maagard A, Tappe D, Cadar D, Schmidt-Chan¬asit J. Zika Virus Infection after Travel to Tahiti , Decem¬ber 2013. Emerg Infect Dis. 2014;20(8):8–10.
24. Tognarelli J, Ulloa S, Villagra E, Lagos J, Aguayo C, Fasce R, et al. A report on the outbreak of Zika vi¬rus on Easter Island, South Pacific, 2014. Arch Virol. 2016;161(3):665–8.
25. Zanluca C, Melo VC, Mosimann AL, Santos GI, San¬tos CN, Luz K. First report of autochthonous transmis-sion of Zika virus in Brazil. Mem Inst Oswaldo Cruz. 2015;110(4):569–72.
26. Bukrinsky M. Yeast help identify cytopathic factors of Zika virus. Cell Biosci. 2017;7:12.
27. Acosta-Ampudia Y, Monsalve DM, Rodríguez Y, Gunturiz ML, Ramirez-Santana C, González-Bravo DC, et al. Au¬toinmunidad Neurológica En Los Tiempos Del Zika. Rev Med. 2016;38(2):187–200.
28. Acosta-Ampudia Y, Monsalve D, León-Ramos C, Anaya JM, Ramírez-González JD. Diagnóstico de la infección por el virus Zika: retos y dificultades. VII Simp Nac y III Congr Latinoam Virol. 2017; DOI: 10.16925/greylit.2097
29. Monsalve DM, Pacheco Y, Acosta-Ampudia Y, Rodri¬guez Y, Ramirez-Santana C, Anaya J-M. Zika virus and autoimmunity. One-step forward. Autoimmun Rev. 2017 Dec;16(12):1237–45.
30. Mahecha MP, Ojeda E, Vega DA, Sarmiento-Monroy JC, Anaya J-M. Guillain-Barre syndrome in Colombia: where do we stand now? Immunol Res. 2017 Feb;65(1):72–81.
31. Uncini A, González-Bravo DC, Acosta-Ampudia YY, Oje¬da EC, Rodríguez Y, Monsalve DM, et al. Clinical and nerve conduction features in Guillain-Barré syndrome associated with Zika virus infection in Cúcuta, Colom-bia. Eur J Neurol [Internet]. [cited 2017 Dec 21]; Avail¬able from: http://onlinelibrary.wiley.com/doi/10.1111/ ene.13552/full/#.WjvHYZQeVss.mendeley
32. Anaya JM, Sun C, Acosta-Ampudia Y, Monsalve DM, Rodríguez Y, Ramírez-Santana C, Nath S. Plausibilidad genética de la infección por el virus del Zika y el sín¬drome de Guillain-Barré. VII Simp Nac y III Congr Lati¬noam Virol. 2017; DOI: 10.16925/greylit.2097 (enviado a publicación).
33. Howie BN, Donnelly P, Marchini J. A flexible and accu¬rate genotype imputation method for the next generation of genome-wide association studies. PLoS Genet. 2009 Jun;5(6):e1000529.