Se procesaron 694 muestras de orina, que se dividieron en 4 grupos: las orinas cuyos recuentos fueron >100.000 UCF/mL (216 casos), de 10.000 a 90.000 UCF/mL (107) casos de 100.000 UCF/mL fueron: en mujeres de 1 a 10 años 3% (5 casos), entre 20 y 39 años 33%, entre 40 a 59 años 27% y mayores de 60 años 37% (69 de 187).
Con respecto a los hombres hubo en total 16 casos, 3 fueron en niños menores de 1 año, 1 caso de 10 a 19 años, 1 de 20 a 39 años, 9 de 40 a 59 años y 2 casos de pacientes mayores de 60 años.
Estandarización del inóculo para antibiogramas con la nueva técnica de enriquecimiento
Inicialmente se comparó el caldo Schaedler con el caldo triptona soya. Incubando orina con caldo triptona soya por varias horas se obtuvieron antibiogramas similares al inóculo de la escala de McFarland obtenidos con la técnica estándar.
Con el caldo triptona soya, a las 2 horas dio cuantificaciones similares en un 70.4% (69 de 98) y con el caldo Schaedler del 66.6% (70 de 105), con el caldo triptona soya a las 3 horas de incubación dio 80% (124 de 155) y a las 4 horas 92% (46 de 50). (Lea: Medicina, Dos Nuevas Técnicas Manuales Rápidas para Antibiogramas Urinarios en 6 a 18 horas)
Comparación de las dos nuevas técnicas con la estándar
Del primer grupo (>100.000 UCF/mL) se analizaron 216 casos, de los cuales 130 muestras sirvieron para compararlas con la técnica estándar, pues no en todos los casos hubo crecimiento bacteriano en los antibiogramas de las nuevas técnicas. Por lo general las lecturas de los halos de inhibición siempre dieron mayores a los de la técnica estándar.
Se analizó por separado cada antibiótico, pues observamos que no todos se comportan de igual manera. En todos los casos se obtuvo una confiabilidad del 99% (un chi-cuadrado de p>0.900) pues entre las nuevas técnicas y la estándar no hay diferencia.
Con la técnica directa se obtuvieron zonas de inhibición en promedio de 2 a 4 mm mayores que con la estándar, y con la nueva técnica de enriquecimiento entre 1 a 2 mm (Figura 2). Los diámetros más cercanos a los de la técnica estándar fueron con la nueva técnica de enriquecimiento con 4 horas de incubación.
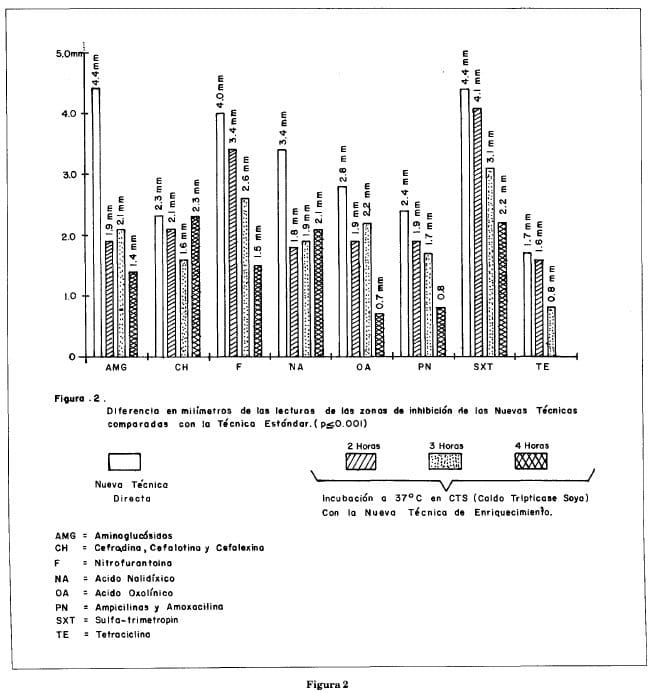
Con orinas de 3 cruces de bacterias en el parcial de orina se obtuvo crecimiento pero el antibiograma no da un inóculo uniforme y por lo tanto no se puede interpretar.
Discusión
El objeto de tener resultados rápidos es: primero, darle al médico una información lo más pronto posible para que pueda formular el medicamento preciso; segundo, evitar la resistencia bacteriana por el uso indiscriminado de antibióticos (26).
Tercero, disminuir costos al laboratorio para que no se procesen orinas para los recuentos de colonias; cuarto, reducir gastos al paciente evitándole comprar drogas que no tienen eficacia terapéutica (26, 27), en cambio con las nuevas técnicas se descartan en 6 horas cuando una droga no sirve.
Quinto, con nuestras nuevas técnicas podemos informar el antibiograma en casos urgentes a las 6 horas (24) para la directa o con la de enriquecimiento a las 8, 10, 12 o a las 22 horas.
Las técnicas que propongo son prácticas para los casos agudos o sea cuando es más necesario saber el antimicrobiano más eficaz.
Ninguna técnica manual se acerca tanto como la descrita en nuestra investigación, pues las técnicas de otros autores dan un 63% (28), un 65% (29), y un 77% (30) de confiabilidad y aún las técnicas semiautomatizadas dan 77% de correlación, como los sistemas automatizados, Autobac, que dan un 93% pero requieren de aislamiento bacteriano (31,32).
El comité de Estados Unidos NCCLS (National Committee for Clinical Laboratory Standards) (21) recomienda el agar Mueller Hinton, pero otros autores en Europa (22, 23, 33) trabajan la técnica de difusión en disco con agar Diagnostic Sensitivity test, agar Sensitest o agar Iso-Sensitest, porque el agar Mueller Hinton presenta variabialidad entre lote y lote (21).
Personalmente hemos observado una mayor nitidez en las lecturas con el agar Iso- Sensitest, y por ello hicimos nuestro trabajo con este medio, ya que no hay diferencias en sus halos de inhibición.
En conclusión, la técnica que recomiendo para emplear en los casos de orina con bacterias Gram negativas, incontables, y nitritos positivos en el parcial de orina es, en especial, la nueva técnica de enriquecimiento con 4 horas de incubación,
Se puede reportar el mismo día o al día siguiente, En el caso de un antibiograma con la nueva técnica directa, cuando utilizamos una cefradina y la zona es de 20 mm (sería por el método estándar “sensible”) (15), pero por la directa es mejor interpretarla como un halo de 16 mm o sea “intermedio”, pues Barlett recomienda hacer errores “menores” y no “mayores” (16).
Estas nuevas técnicas no se aplican para bacterias Gram positivas tales como Listeria, Lactobacillus, Enterococcus, Streptococcus y en algunos casos Staphylococcus aunque haya un recuento >100.000 UCF/mL.
Agradecimientos.
Un padre mi, de el cardiologo Y PROFESOR J. Remando Ürdóñez valiosas por todas SUS Observaciones; ya mi esposo Gustavo Danies Silva por el Desarrollo de los Programas de computador.
Referencias.
1. PEZZLO, MT, WETKOWSKI, M., PETERSON, E., y MAZA, L. Detección de bacterias y piuria dentro de dos minutos. J. Clin. Microbiol. 21 (4): 578-581, 1985.
2. BIXLER-Forell, E., BELTRÁN, M., y Bruckner, D. Evaluación clínica de tres métodos rápidos para la detección de bacteriuria significativa. J. Clin. Microbiol. 22 (1): 62-67, 1985.
3. LATHAM, R, RUNNING, K y STAMM, WE Infecciones del tracto urinario en mujeres adultas jóvenes por causada por Staphylococcus saprophyticus. JAMA. 250 (22): 3063-3066, 1983.
4. STAMM, infección WE Diagnóstico ofcoliform de forma aguda en mujeres dysuric. N. Engl. J. Med. 307: 463-468, 1982.
5. BERG, AO, HEIDRICJ, FE, Fihn, SD, BERGMAN, JJ, MADERA, R W., STAMM, WE, y Holmes, KK se establece la causa ofgenitourinary síntomas en las mujeres en una práctica familiar. JAMA. 251 (5): 620-625, 1984.
6. WEINSTEIN, MP Evaluación ofli, conservantes quid y liofilizados para urocultivo. J. Clin. Microbiol. 18 (4): 912-916, 1983.
7. Traub, WH, SPORHR, M., Arnold, M., y KLOTZ, la actividad bactericida de M. medicamentos antimicrobianos en muestras de orina simuladas a diversas temperaturas ofincubation. Zentralbl. Bakteriol. Mikrobiol. Hyg. [A] 255 (4): 494-502, 1983.
8. Komaroff, A L. Análisis de orina y urocultivo en mujeres con disuria. Anales oflnternal Medicina. 104: 212-218, 1986.
9. LIPPMAN, R W. Examen de orina y su Interpretación. 3a. ed. Salvat Ed. Barcelona. p. 3-54, 1982.
10.KAMOUN, P., y Frejaville, JP Guía de Exámenes de laboratorio. Salvat Editores, Barcelona, p. 53-56, 1981.
11. SHAW, ST, SELINA, y. P., y Wong, análisis de orina de rutina ET. ¿Es suficiente la varilla? JAMA. 11 (253): 1596-1600, 1985.
12. SZWED, JJ, y Schaust, C. La importancia de examen microscópico de la Am sedimento urinario. J. Med. Technol. 48 (2): 141-143, 1982..
13. CHOU, S., y Merigan, la detección y cuantificación rápida TC ofhuman citomegalovirus en la orina a través de la hibridación de ADN. N. Engl. J. Med. 308 (16): 921-925, 1983.
14.NICHANDER, KK, SANHOLTZER, CJ, y PETERSON, tubos de transporte de la cultura L.RUrine: efecto de un volumen de muestra sobre la toxicidad bacteriana del conservante. J. Clin. Microbiol. 15 (4): 593-595, 1982.
15. Koneman, EW, ALLEN, SD, DOWELL, Jr., V. R, y Sommers, HM Diagnostic Microbiology, JB Lippincontt Compañía. Philadelphia, 3-244, 1979.
16. BARLETT, R C., et al. Clínica, Microbiología. Aseguramiento de la Calidad en Microbiología Clínica. 16U.S. Departamento de Educación para la Salud y el Bienestar del Servicio de Salud Público, US A 926-936, 1978.
17. TANNER, E., y Bullin, la infección por C. Escherichia coli timidina-dependiente y SORNE asociado problemas de laboratorio. J. Clin. Sendero. 27: 565-568, 1974.
18. BAUER, A W., KIRBY, MM, Sherris, JC, y camiones, M. pruebas de sensibilidad a los antibióticos por un método de disco único estandarizado. Am. J. Clin. Pathol. 45 (4): 493-496, 1966.
19. METZLER, CM, y DeHaan, R M. prueba de susceptibilidad de las bacterias anaerobias sta consideraciones estadís- y clínicos. J. Infect. Dis. 130 (63): 588-594, 1974.
20. ORDOÑEZ SMITH, M. Generalidades de las pruebas de susceptibilidad a antimicrobianos Agentes y su Control De Calidad. Memorias del I Simposio Internacional de Microbiología Clínica. Bogotá, p. 1-32, 1983.
21. Comité Nacional para Estándares de Laboratorio Clínico NCCLS. Estándares Para Las pruebas de susceptibilidad en discotecas antimicrobianos / pruebas de susceptibilidad. 3a. ed. Vol. 4 No. 16: 1-24, 1984.
22. SNELL, ofresults JJS, BROWN, DF, y Gardner, de la comparación de PS de dos ensayos de pruebas de susceptibilidad a los antibióticos que formaron parte del esquema de evaluación externa de la calidad nacional del Reino Unido. J. Clin. Pathol. 37: 321-328, 1984.
23. Reller, LB, SCHOENKNECHT, D, KENNY, M. A, y Sherris, JC pruebas de sensibilidad a los antibióticos de Pseudomonas aeruginosa: Selección de un formagnesium cepa de control y el contenido de calcio en los medios de comunicación. J. Infect. Dis. 130: 454-463, 1974.
24. WADKE, M., McDONNELL, C., y ASHTON, procesamiento de J. K rápida ofurine especímenes de orina y sistemas de detección automicrobic. J. Clin. Microbiol. 16 (4): 668-672, 1982.
25. PARKER, R E. Estadística párrafo BioLogos. Ediciones Omega. Barcelona. p. 48-52, 1976.
26. ALVAREZ MESTRA, R. Combinación de antimicrobianos. Tribuna Médica. Colombia 854. Tomo LXXIII (2): 25-27, 1986.
27. Pfaller, M., y KOONTZ, F. Uso ofrapid pruebas de detección en el procesamiento de las muestras de orina por la cultura convencional y Sistema Automicrobic. J. Clin. Microbiol. 21 (5): 783-787, 1985.
28. BARRY, AL, JOYCE, LJ, ADAMS, AP, y Brenner, determinación CJ rápido ofantimicrobial susceptibilidad para situaciones clínicas urgentes. Am. J. Clin. Pathol. 59: 693-699, 1973.
29. ROSSIGNOL, D., BARTHEZ, JP, et SOUESME. J. antibiograma urinaire directo La Nouvelle Presse Médicale, 8 (39): 3127-3129, 1979.
30. PERRIN, P., GILLE, Y., DURAND, L., et VICENT, la infección por P. L’urinaire en urologie. Diario d’Urologie et de Nephrologie. No. 7-8: 499-507, 1977.
31. BINFORD, J., BINFORD, LF, y ADLER, P. Un método microcalorimétricas semiautomático de pruebas de sensibilidad a los antibióticos. Am. J. Clin. Pathol. 59: 86-94, 1973.
32. HEINZE, P., Thrupp, L., y ANSELMO, C. Un sistema rápido (4-6 h) orina de cultivo para la identificación directa y la prueba directa de susceptibilidad antimicrobiana. Am. J. Clin. Pathol. 71: 177-183, 1979.
33. NEUSSELL, H., y LINZENMEIER, G. Un nuevo medio semidefined para las pruebas de sensibilidad a los antibióticos. Comunicación. Todos. Octavo Congreso de Antibiot. Y Chemotherp. Atenas, 1973.

