Edmond J. Yunis, M.D.
* Profesor de Patologia Escuela de Medicina
Universidad de Harvard Boston, MA, U.S.A.
Jefe División de Inmuno-genética, Dana- Farber
Cancer Institute.
Miembro Honorario
Eduardo Egea, M.D.
* Profesor Facultad de Medicina Universidad del Norte Barranquilla, Colombia
Research Fellow de la División de Inmunogenética, Dana-Farber Cancer Institute.
Introducción
El sistema inmunitario juega un papel importante en el mantenimiento de la salud en general. Esta actividad requiere de refinados mecanismos regulatorios de naturaleza genética, que permiten las interacciones celulares, para la expresión de una respuesta inmunitaria.
Esta revisión, tiene por objeto presentar evidencias que permitan establecer una línea de estudio de los genes de la respuesta inmunitaria (R.1)en poblaciones colombianas. Para ello y con resultados previos, deseamos enfocar este diseño, hacia dos líneas de trabajo en enfermedades de gran prevalencia e importancia médica, en Colombia; estas líneas son:
- A) Aspectos inmunogenéticos de la Hepatitis B (HB) en poblaciones colombianas;
- B) Marcadores genéticos de susceptibilidad al asma bronquial.
La base de nuestra investigación es la identificación de variantes de glicoproteínas del complejo mayor de histocompatibílidad (CMH) de la clase II. Estas moléculas están involucradas en gran parte con la respuesta inmunitaria.
Por esto es necesario hacer primero una breve descripción de la respuesta inmunitaria y del papel primordial que juega el CMH en esas respuestas.
Explicaremos que existen muchas clases de estas glicoproteínas, cada una de ellas, haplotipos extendidos, (alelos)con variantes, que pueden estar ligadas no al azar en bloques dt ADN a nivel de la población. La identificación de estas regiones cromosómicas, en las poblaciones colombianas, servirán de base para estudios genéticos del control de la respuesta inmunitaria.
Como se discutirá más adelante, en poblaciones caucásicas y en japoneses, existen haplotipos específicos, los cuales sirven de marcadores para la respuesta inmunitaria contra alérgenos y haplotipos que identifican individuos los cuales no responden inmunológicamente a la vacuna de la hepatitis B.
La respuesta inmunitaria
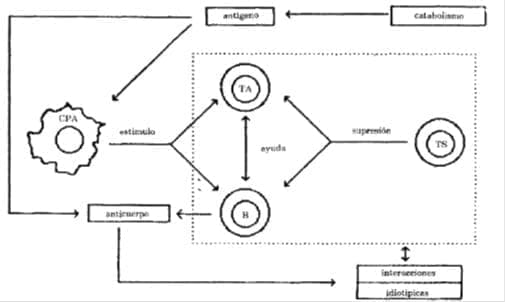
La respuesta inmunitaria es principalmente mediada por tres tipos de células. Los linfocitos T (LT), los linfocitos B (LB) y los macrófagos (Mo).Los linfocitos B en respuesta a un Ag. específico, se diferencian hacia células plasmáticas, productoras y secretantes de Ab. Esta respuesta de anticuerpos se encuentra genéticamente determinada (1-2)y está regulada por varias poblaciones celulares (3)(Figura 1).
Las otras células importantes en la producción de Ab son las diferentes subpoblaciones de los LT, así como los macrófagos y granulocitos. Todos ellos derivan de una célula pluripotencial presente en el hígado fetal y en la médula ósea (4).
Las células T interactúan con otras células para regular la respuesta inmunitaria. Esto conlleva a la producción de Ab y tiene por objeto la eliminación de microorganismos, células y sustancias extrañas en el organismo (4-5).
Los dos tipos de células T mejor caracterizadas son los linfocitos T cooperadores y los linfocitos T con función citotóxica o con función supresora (6). Estas dos poblaciones de células son reconocidas por la presencia de glicoproteínas de membrana celular, las cuales se identifican con el uso de anticuerpos monoclonales.
El fenotipo de la célula T colaboradora, CD4, detectado con un monoclonal Anti-T4 (anti-Ieu3) tiene un peso molecular de 55KD. La función de la población citotóxica o la población supresora porta un fenotipo CD8 con 32KD, ella se determina con un anticuerpo monoclonalAnti-T8 (anti-Ieu2a)(7).
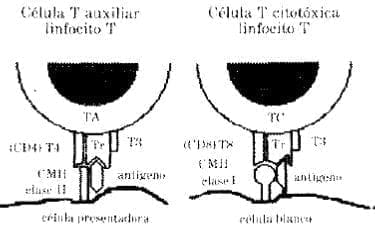
Los linfocitos CD4 participan en el reconocimiento de los antígenos cuando éstos son presentados por las moléculas de clase ndel CMH, mientras que las células con el fenotipo CD8 reconocenel Ag. en asociocon las moléculasclase 1del sistema HLA (8l (Figura 2). (Lea también: Complicaciones neurológicas de la enfermedad por descompresión de los buceadores)
Sinapsis del complejo mayor de histocompatibilidad
La regulación del sistema inmunitario está dada, por lo menos en parte, por moléculas codificadas por genes denominados genes R.I, algunos de los cuales se encuentran ubicados en un complejo genético denominado complejo mayor de histocompatibilidad (CMH) (Figura 3). En el humano éstos están localizados en el brazo corto del cromosoma 6 y se les denomina el sistema HLA (9,10).
Inhibición por Retroalimentación
 Figura 1
Figura 1
Regulación de la respuesta inmune: un modelo mínimo de controles por anticuerpo, por células y por catabolismo del antígeno.
ePA = célula presentadora de antígeno (célula adherente, i.e. macrófago)
TA = célula auxiliar (linfocito T)
B = linfocito B
TS = célula supresora (linfocito T)
 Figura 2
Figura 2
Hipótesis para explicar el reconocimiento del antígeno por células T. La molécula CMI-I de clase 11 con un antígeno es reconocida por la molécula CD4en unión del complejo T3 con el receptor de tal modo que existe restricción. En cambio la célula citotóxi la estimulada por una célula blanco reconoce a la molécula CM H clase l en unión con antígeno por medio de la molécula CD8 unida al complejo T3 con el receptor, produciendo restricción inmunológica.
Estos genes controlan la respuesta inmunitaria en tres niveles:
– Durante la presentación del Ag. por el Mo.
– En la interacción celular que conlleva a la producción de Ab.
– En la producción de mediadores solubles con función supresora o auxiliadora.
El sistema HLA representa 111000 del total del genoma humano. Los locus HLA-A, B YC codifican los Ag. de clase I los cuales se expresan en la superficie de la mayoria de las células nucleadas y las plaquetas.
Los loci de la región HLA-D (Figura 3) codifican para los determinantes antigénicos de la clase 11, los cuales se expresan en la superficie celular del linfocito B, monocitos y las células progenitoras de la médula ósea. Estos Ag. también se expresan en los LT activados (10).
En la región HLA hay otros grupos moleculares denominados Ag. de clase 111, los cuales están codificados por los genes estructurales para los componentes del complemento; C2, Bf, C4A, C4B, además hay genes estructurales para las enzimas 21-hidroxilasa y linfotoxinas (l0,11).
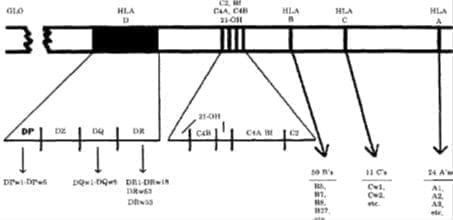
Estudios recientes, utilizando técnicas de genética molecular, han establecido que el orden de los genes del complemento y de la 21-hidroxilasa en el cromosoma 6 es: C2, Bf, C4A, 21OHA, C4B, 21OH-B (Figura 3).
 Figura 3
Figura 3
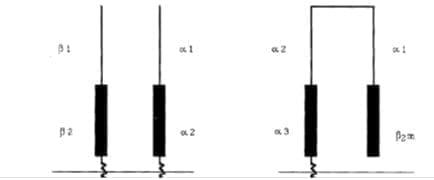
El complejo genético HLA comprende una región pequeña con una frecuencia de recombinación de los genes de esta región muy baja, de tal forma que este complejo puede considerarse como una sola unidad genética, pudiendo así heredarse de conjunto como bloque. El término haplotípo se utiliza para describir los alelos particulares del HLA·A, HLA-B, HLA-C y HLA-DR, DP, DQ, en cada uno de los cromosomas homólogos heredados por un índividuo. Los dos haplotipos conforman el genotípo, y los antígenos constituyen el fenotipo.
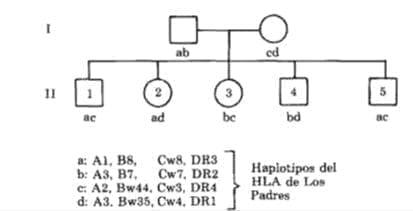
Los productos genéticos de cada uno de los locus HLA de clase 1 y de clase 11 se expresan en forma codominante en la superficie celular. Los haplotipos son transmítidos en forma codominante, así que cada hijo expresa un haplotipo materno y otro paterno (Figura 4).

Figura 4
ab; ed; ae; ad, be, db = genotipos
La mayoría de las personas son heterozígotos para cada uno de los loci de este complejo. Sin embargo, se pueden encontrar individuos homozígotos cuando los padres poseen el mismo alelo en uno de sus haplotipos.
La estructura de los Ag. de la clase 1 consísten de dos cadenas polipeptídicas (12).Una de las cadenas es codificada por el CMH y tiene un peso molecular de 44.000 daltons y está unída a una cadena más pequeña de 12.000 daltons que no está codificada por el CMH, c conocida como B2-microglobulina (B2m) (131.
La estructura de estas proteínas de membrana incluyen 3 dominios extracelulares de aproximadamente 90 aminoácidos cada una, además una región hídrofóbíca de 25 aminoácidos y una región íntracitoplasmática de 30 aminoácidos.
Los 4 dominios extracito plasmáticos (incluyendo B2m) están dispuestos de manera simétrica, semejantes a los dominios de la inmunoglobulina, así mismo, la secuencia de aminoácidos demuestra que el dominio Alfa 3 (el primero extracitoplasmátíco) tiene homología con la región constante de las inmunoglobulinas. Los dos dominios externos son muy polimórficos, y son responsables de la inmunogenecídad de las moléculas siendo los sitios reconocidos por las células citotóxicas y por los anticuerpos (13).
Los mapas genéticos que se obtienen utilizando ADN recomo binan te, han demostrado que existen entre 25 y 30 genes para la clase 1 (14,15). Tres tipos de moléculas distintas correspondientes a la clase 11en el humano han sido definidas dentro de este complejo y son denominadas DR, DQ, y DP (Figura 2) (16,17).
Se sabe que el locus DR está a un centimorgan del locus HLA-B. El locus HLA-DP:
Se localiza entre el HLA-DR y GLO-I. Ellocus HLA-D inicialmente se definió usando técnicas celulares (cultivo mixto de linfocitosl, mientras que los Ag. DR fueron definidos usando métodos serológicos (18).
Los Ag. de clase 11 del CMH están formados por dos cadenas de glicoproteínas unidas con enlaces no covalentes (18) ligadas a la membrana por una porción intracelular. A estas cadenas se les llaman cadena Alfa y cadena Beta. La cadena Alfa tiene un peso molecular de 34.000 y la cadena Beta entre 27.000 y Membrana Celular
 Figura 5
Figura 5
Los dominios de las cadenas α. Y β de los antígenos de la clase 1 y 11que se encuentran cercanos a la membrana celular, se conservan. Ellos tienen similitud a las inmunoglobulinas. Los dominios o: 1,f3 1 de la clase II yoc 2 yex: 1 de la clase I, los cuales en la figura se encuentran dibujados como líneas) son variables y por lo tanto contienen la secuencia de aminoácidos que son reconocidas por los anticuerpos y por las células T.
30.000 daltons (las diferencias de peso molecular entre ambas cadenas se debe a diferencias en su glicosilación, en donde la cadena Alfa contiene dos unidades de carbohidratos mientras la cadena Beta sólo posee una).
La cadena Beta consiste de dos dominios siendo una de ellas variable (Bl), mientras que la cadena Alfa tiene dos dominios constantes (Figura 5). En el caso de HLA-DQ, las cadenas Alfa y Beta tienen regiones variables, pero en el caso de HLA·DP sólo la cadena B tiene regiones variables.
Función del CMH en el mecanismo de restricción antigenica
Quizás ésta sea la función más importante de este complejo genético. Ya se conoce la naturaleza molecular de esta función biológica, en la que el receptor de la célula T reconoce al Ag. Extraño en el contexto de los Ag. de clase I y II del CMH, existen varios trabajos que muestran que el reconocimiento de las proteínas extrañas por los linfocitos T colaboradores, está dirigido a un número limitado de epitopes dentro de estos Ag. (19-22).
Estos estudios se basaron en la utilización de fragmentos proteicos o péptidos sintéticos en vez de Ag. Nativos para presentarlos a los LT. Estos péptidos inmunogénicos interactúan sobre la membrana del Mo (o de las células presentadoras de Ag.) con las moléculas del CMH para producir complejos, los cuales sirven como ligan tes, para interactuar con el receptor de LT (22, 23) (Figura 2).
Se sabe que después que el Ag. es catabolizado por las células presentadoras de Ag., su producto final se adhiere a una región de una cadena de la molécula del CMH de clase n. El péptido inmunogénico de la proteína tiene porciones de secuencias de aminoácidos las cuales pueden aparear posteriormente con un segmento receptor de una molécula clase II. Por otro lado, el receptor T puede reconocer todos los péptidos que tengan un buen ligamiento con un segmento dado de la molécula n a nivel de la región variable de dicha molécula.
Esta última determina:
Las diferencias entre alelos de cada locus de los genes Ir. El receptor T de un linfocito reconoce exclusivamente una configuración Ag.-glicoproteína clase II. Este fenómeno se denomina restricción inmunológica y esta célula T activada y su progenie solo reconocerá la misma configuración cuando se encuentre de nuevo con ella (24,25).
Resulta importante resaltar que las regiones variables de las glicoproteinas clase II son reconocidas por una proporción de células T colaboradoras, sin necesidad de estar combinada con el Ag., produciéndose la alorreactividad.
Individuos idénticos en las regiones variables de la clase II no producen activación de las células T colaboradoras, en cambio, una diferencia Ag. de la clase II provoca diferenciación de las células T colaboradoras. El reconocimiento del fenómeno de alorreactividad sugirió que las moléculas clase II en el humano, codificada por la región HLA-D, contienen los genes de la respuesta inmune del hombre.
Polimorfismo genético y desequilibrio de enlace genético
Los genes del complejo mayor de histocompatibilidad poseen el mayor polimorfismo dentro de los mamíferos. Los más polimórficos son los del locus B con 50 alelos definidos hasta la fecha. Le siguen los del locus HLA-A con 24 alelos. Solo se conocen 11 alelos del locus HLA-C. Los genes que codifican para los Ag. de clase III representan también un extenso sistema polimórfico que ocupa el segundo lugar solo después dellocus HLA-B. El mayor polimorfismo de los genes del CMH de la clase Il existe en el HLA-DR con 18 alelo s (Fig. 3).
El polimorfismo genético es el fenómeno por el cual dos o más alelo s se presentan en una población en frecuencias que no podrían mantenerse por el solo proceso de mutación. Uno de los mecanismos que generan polimorfismo es la mutación genética o las inserciones de secuencias nucleotídicas de loci vecinos (conversiones genéticas).
El mecanismo de tan extenso polimorfismo dentro el CMH no se conoce. Se ha encontrado que los Ag. HLA varían ampliamente de una población a otra, un ejemplo se encuentra en el HLA-A30., el cual es predominantemente de la raza negra (28%) comparada con la raza blanca (5%); no se encuentra en los japoneses.
El desequilibrio de enlace genético se da cuando alelos de dos o más loci se presentan juntos en la población, en el mismo haplotipo, con una frecuencia mayor de la esperada, si su asociación fuera determinada al azar.
Un ejemplo de lo anterior se encuentra en el haplotipo A1,B8:
El cual tiene una frecuencia de 6.8% en la población blanca americana, comparada con la frecuencia esperada que es de 2% (10). Otro ejemplo de este fenómeno se presenta con los diferentes alelos de los genes del C’ (Bf, C2, C4A, C4B). Estos son loci que se encuentran ubicados entre HLA-B y HLA-DR. Estos genes son todos codificados por un segmento de ADN no mayor de 120KB (26).
Los alelo s de estos genes no están asociados al azar a nivel de la población, del tal forma que la combinación de 4 alelos de ellos se pueden usar como marcadores individuales. Estos marcadores han sido enominados complotipos. Los estudios de familias realizados en caucásicos normales han establecido por lo menos una docena de complotipos (Tabla 1) (27-30).
Tabla 1
COMPLOTIPOS EN CAUCASICOS NORMALES
| SC31 SC01 FC31 SC30 SC42 SC61 SC21 FC(3,2)0 SC02 SC33 FC01 SB42 |
0.389 0.127 0.112 0.064 0.050 0.031 0.028 0.022 0.022 0.020 0.016 0.016 |
Toda esta región que contiene los genes que codifícan para HLAB, complotipos y HLA-DR, tiene una distancia de solo un centimorgan. Estudios anteriores han demostrado que hay desequilibrio de enlace entre alelo s de los loci HLA-B, los complotipos y la región HLA-DIDR.
Al conjunto de alelos heredados en bloque, que se expresan como una sola unidad genética, provenientes de cada una de estas regiones, se les denominan APLOTIPOS EXTENDIDOS (29). Las combinaciones más frecuentes de éstos se muestran con la tabla 2.
Tabla 2
HAPLOTIPOS EXTENDIDOS EN CAUCÁSICOS
| Haplotipos Extendidos | Frecuencia |
| [HLA-B8, DR3, SC01] [HLA-B7, DR2, SC31] [HLA-B44, DR4, SC30] [HLA-B44, DR7, FC31] [HLA-B57, DR7, SC61] [HLA-B35, DR1, FC(3,2)0] [HLA-B62, DR4, SC33] [HLA-B18, DR2, S042] [HLA-B14, DRl, SC2(1,2)] [HLA-B38, DR4, SC21] |
0.0762 0.0700 0.0311 0.0295 0.0171 0.0112 0.0109 0.0109 0.0109 0.0080 |
Podemos entonces decir que para muchos haplotipos extendidos, parece que los alelo s en varios locus son los mismos, y se comportan como si ellos hubieran sido “congelados” en el mismo punto, durante la evolución del hombre.
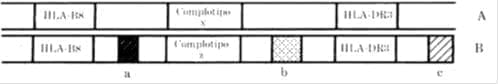
El concepto del haplotipo extendido está ilustrado esquemáticamente en la Figura 6. Si dos individuos poseen cromosomas del tipo A (con regiones asociadas en desequilibrio de enlace genético) y no como el tipo B (con regiones asociadas al azar) se puede asumir que las porciones de ADN intercaladas entre las regiones conocidas son idénticas. Las regiones a, b y c del cromosoma tipo B serán diferentes porque el complotipo es diferente (30).
De los resultados provenientes de estudios en otras especies mamíferas, se ha concluido por analogía, que los genes de la respuesta inmunitaria están en el humano, en los locus de las regiones del genoma que codifican para HLA-DR, DP y DQ y que la selección a través de la evolución de estos alelo s es la que ha determinado el desequilibrio de enlace genético (31,32).
Asociación de HLA y enfermedad
Existe un cierto número de entidades clínicas que muestran asociación con alelos del CMH (31,32). La tabla 3 ilustra algunas enfermedades, además se puede observar la fórmula para calcular el riesgo relativo de componentes de los haplotipos extendidos.
En la tabla 4 se resumen los haplotipos extendidos que se han descrito como marcadores de algunas enfermedades. Está claro también el componente de predisposición genética demostrada por la incidencia de ellos en gemelos homozigotos y un mayor riesgo de prevalencia en los miembros familiares comparados con la población general (32).
Se han propuesto una serie de mecanismos para tratar de explicar el papel de los alelos del sistema HLA en el establecimiento de la susceptibilidad a las enfermedades (32,33,34) entre otras:
 Figura 6
Figura 6
Ejemplo de desequilibrio de enlace y su representación esquemática. Las regiones identificadas con rectángulos pertenecen a regiones reconocidas por marcadores HLA-B8, complotipo x y HLA-DR3 del cromosoma A de un individuo. Ellos existen en asociación no aleatoria. Si dos de los tres marcadores son iguales como en el cromosoma B la presencia de un complotipo diferente (z) puede predecir que otras regiones del cromosoma B (a,b,c)pertenecen a polimorfismos diferentes no identificados en el presente.
Tabla 3
ALGUNAS ASOCIACIONES ENTRE ALELOS DEL “MHC” Y ENFERMEDADES
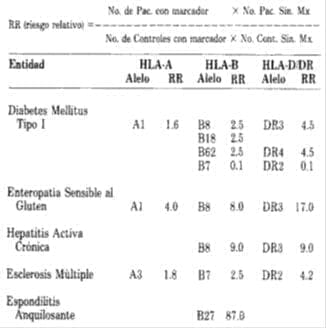
Tabla 4
HAPLOTIPOS ASOCIADOS A ENFERMEDAD

– La hipótesis de la similitud molecular, la cual trata de explicar el fenómeno por la reactividad cruzada entre el microorganismo patógeno y un Ag. del sistema HLA dado.
– La falta de respuesta a un Ag. Especifico la cual estará genéticamente controlada por genes R.I de un individuo.
En el contexto de este marco teórico, describiremos a continuación un modelo de estudio para nuestras poblaciones. Un campo de trascendental importancia lo constituyen las enfermedades infecciosas, por ello nuestro interés es iniciar una línea de trabajo en la inmunogenética de estas entidades.
La asociación de los haplotipos extendidos y la falta de respuesta a la vacuna de la hepatitis B
En un intento de estudiar e identificar marcadores del CMH en la respuesta inmune especifica contra el virus de HB, se realizó la tipificación de los antígenos de la clase I, II YIII en personas que recibieron la vacuna de la hepatitis B.
Los resultados mostraron que las personas que no respondieron a la vacunación, tenian un incremento de la frecuencia de dos haplotipos extendidos; HLA-B8, DR3, SC01 y HLA-B44, DR7, FC31, lo que sugiere que los genes que controlan la falta de respuesta inmunitaria contra la vacuna de la hepatitis B pudieran estar presentes en el mismo haplotipo extendido.
En estos estudios no solamente se encontraron estos haplotipos que pudieran predecir la pérdida a la respuesta de la vacuna de la hepatitis B, sino que se han inmunizado prospectivamente individuos homozigotos y en ellos no se provoca respuesta alguna (34).
Al parecer la respuesta inmunitaria contra el HBS-Ag. del HBV está controlada genéticamente, esto ha sido documentado en el modelo murino (35) y recientemente se han iniciado estudios en el humano (36,38-401).
Por esta razón, deberíamos considerar el estudio de la regulación genética de la respuesta inmunitaria a la vacuna de la hepatitis B y el estudio de la respuesta en individuos receptores a la vacuna HB para justificar o descartar con bases moleculares, biológicas e inmunológicas, la implementación de un programa de inmunización contra la HB en nuestro país.
Cayzer:
(Estudios no publicados, Abstracts-Simposio Internacional de Hepatitis B, mayo 1986, Londres, Pág. 89A) de la Universidad de Quesland, Bridbane, Australia, ha encontrado una relación dosis-efecto con el sistema HLA en la respuesta a la vacuna de la hepatitis B en el hombre, todos sus pacientes respondedores tuvieron uno o más de los siguientes alelos: B7, B8 o B44, Al, A2, A3, mientras que en los respondedores se encontró la presencia de DR4 y DR7.
En las mismas condiciones T. Sasazuki del Departamento de Genética de la Universidad de Kyushu, en el Japon, al estudiar la relación falta de respuesta a la vacuna de la hepatitis B y haplotipos, encontró que todos los individuos, quienes fueron positivos para: HLA-Bw54; DR4; DR53; DQw4, fueron no respondedores al HBS-Ag.
Ninguno de los linfocitos de sus pacientes no respondedores mostró un buen manejo de la respuesta in vitro al HBS-Ag.; sin embargo, si se hacia depleción de las células T-CDS de las muestras de sangre periférica, de los pacientes no respondedores, se observaba un incremento en la producción de Ab. (Tabla 5).
Tabla 5
GENES DE INMUNOSUPRESION (ls) EN EL MHC
ASOCIADOS A LA FALTA DE RESPUESTA
– A LA VACUNA DEL HB-V –

Estudios de regulación genética de la respuesta humoral HBSAg. en el modelo murino (35-37), indican que esta respuesta está regulada por genes localizados en el CMH en el ratón. Los mecanismos celulares responsables para la falta de respuesta al HBS-Ag. o a la vacuna de la hepatitis B no se han delineado muy bien.
Por lo anterior, decimos que la respuesta inmune a un Ag., en particular el HBS-Ag., fallaría si el macrófago no procesa el Ag. y/o lo presenta en forma inadecuada a las células T. Por otro lado, las células B pueden perder los receptores necesarios para la interacción con las células T o pudiera ser que estas deficiencias se deban a la ausencia de una clase de clono de células T, el cual potencialmente reaccionaría con un epitope y éste pudiera ser tan similar a la región variable de los genes de la clase Il, haciendo que las células T lo reconocieran como propio.
En este orden de ideas se haría un estudio de familias en poblaciones de áreas endémicas, con la finalidad de encontrar ha- plotipos extendidos, asociado a la falta de respuesta a la vacuna, para lo cual se compararía la frecuencia de estos haplotipos extendidos en los altos respondedores y no respondedores y se determinaría la relación con la vacuna.
Tabla 6
GENES R.I e IS ASOCIADOS AL CHM
(ALERGIA A LA AMBROSIA’RAGWEED’)

Todo lo anterior, aunado a ensayos de inmunorregulación en la misma muestra, arrojarán resultados que podrán aplicarse a los programas de salud en nuestro país.
La asociación de los haplotipos extendidos con la respuesta atopica
Un segundo aspecto de nuestro modelo, toca la asociación de las enfermedades atópicas y los haplotipos extendidos. Permítanos hacer una breve introducción a la genética y a las bases inmunológicas de la respuesta atópica.
La IgE, una glicoproteína con funciones de anticuerpo, tiene dos cadenas pesadas y dos livianas; es la inmunoglobulina con menor concentración en el suero, (entre 0.1 0-0.40 ug/mll. La propiedad biológica más destacada de esta molécula es la de sensibilizar tejidos homólogos, (41) a través de su capacidad de unirse a la membrana de basófilos y C. cebadas (42).
Los mastocitos son la mayor fuente de histamina y otros mediadores preformados que participan en los estadios iníciales de los procesos alérgicos.
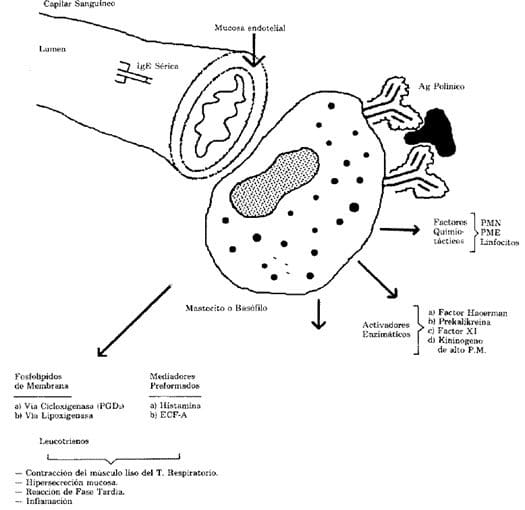
La reacción alérgica por excelencia se lleva a cabo cuando un alergeno interactúa con dos moléculas de IgE sobre la membrana del linfocito, desencadenando toda una secuencia de eventos bioquímicos y enzimáticos que determinan a la postre, los cambios fisiológicos que expresa el cuadro clínico.
Los eventos anteriormente descritos se resumen en la figura 7 (43,44). Las enfermedades atópicas, entre ellas el asma bronquial alérgica, son el resultado de la interacción de múltiples factores, tales como la funcionalidad del sistema inmunitario, la fisiopatología del árbol traqueo bronquial y los mecanismos genéticos y endocrinos comprometidos en ellas.
El control genético del asma es complejo; podemos decir que existen evidencias para considerar la implicación de varios genes asociados al CMH. El fenotipo de la enfermedad también puede ser regulada por niveles de IgE determinados genéticamente; esto puede ser la resultante del balance entre los genes de la respuesta inmune (1rl y los genes de inmunosupresión (1s), (localizados en el cromosoma 6) y los genes del IgE total localizados en cromosomas diferentes al 6.
Los primeros estudios del carácter hereditario del asma fueron realizados por Cooke y Vandzer Yeer en 1916 (3S-40).
Ellos y otros más, esclarecieron su predisposición genética (46-50). Más recientemente se ha venido estudiando la relación de marcadores genéticos con los posibles mecanismos de herencia de las enfermedades atópicas.
Al respecto, los investigadores han enfocado sus estudios hacia el sistema HLA; sin embargo, los resultados en la asociación CMH y enfermedad hasta el momento son polémicos, (4S-51l yen su mayoría fueron estudios de población. En contraste, los estudios de familia (52) mostraron segregación entre un haplotipo del HLA con la sensibilización al Ag.
RaE de la ambrosía; otros estudios también han aportado los mismos resultados (53-55). Por otro lado, la respuesta IgE específica al Ag. Ra5 de la ambrosía se encuentra altamente asociado con el DR2 y Dw2 (57,5S).
 Figura 7
Figura 7
Los genes I.R e Is que controlan la respuesta IgE específica al Ra5 de la ambrosía, se hallan con frecuencia en el haplotipo HLA-B7,SC31,DR2,DQwl y probablemente se heredan de manera recesiva, produciendo el asma bronquial. Pero la respuesta baja al mismo antigeno, se asocia con el haplotipo HLABB, SCOl,DR3,DRw52,DQw2, y se hereda dominantemente para producir rinitis (tabla 6).
No sabemos cuál molécula del CMH, clase II, por ejemplo, es la responsable de estas respuestas. Su identificación indicaría que algún subtipo aún desconocido se encontraría en desequilibrio de enlace en estos haplotipos.
Cuando se describan los haplotipos extendidos que contengan esta clase de genes en poblaciones colombianas, también será necesario identificar los subtipos que explicarán las bases moleculares de las respuestas inmunitarias en Colombia.
En estudios inmunogenéticos recientemente realizados en Colombia, analizando familias con varios hermanos con asma alérgica, se ha observado ligamiento genético entre la región HLAA, B, C, DR y esta manifestación atópica, sin que haya sido posible todavía establecer una relación definitiva entre un alelo o grupos de alelos específicos y dicha enfermedad (L. Caraballo, Com. personal).
Lo anterior nos ha dado pie a plantear la hipótesis que la expresión clínica de la enfermedad, puede estar regulada genéticamente, lo que explicaría la asociación de ciertos haplotipos extendidos con una enfermedad alérgica dada. El modelo de estudio por excelencia en el cual el fenómeno anterior se podría estudiar, lo constituye la triada clínica: asma, rinitis alérgica y eccema atópico, en la que generalmente una de las tres enfermedades predomina.
En todos estos pacientes propondríamos conocerles su fenotipo y seleccionar un grupo de ellos, para hacer estudios de familias, con la posibilidad de encontrar estos marcadores genéticos.
Una vez evidenciado lo anterior, tratar de establecer la presencia de un gen de susceptibilidad para cada expresión clínica utilizando la tecnologia de genética molecular y más explícitamente, la del polimorfismo de la longitud de los segmentos de restricción.
Además de los aportes que estos resultados puedan dar al entendimiento de la patogénesis de las atopías, ellos por sí mismos, por ser marcadores de atopía, podrían en conjunción con la determinación de los niveles de IgE sérica, en los lactantes, establecer un diagnóstico precoz que apoyara científicamente programas de prevención de estas enfermedades en poblaciones con estigma atópico.
Resumen
Basados en nuestra experiencia, es posible estudiar factores genéticos del complejo mayor de histocompatibilidad (CMH) en varias enfermedades inmunológicas, o también factores genéticos que influyen en la falta de respuesta inmunitaria a vacunas como la hepatitis B. Los alelos de diferentes loci del CMH sirven por sí mismos para identificar riesgos para enfermedades o falta de respuesta a vacunas.
El bloque de genes del CMH, que pueden existir al nivel de la población, en desequilibrio de enlace genético, es un mayor marcador para estudiar la susceptibilidad genética a enfermedades como las atopías así como también la falta de respuesta a vacunas.
Nosotros proponemos que un estudio inmunogenético de poblaciones colombianas, podría utilizarse como control para identificar susceptibilidad genética para el desarrollo de atopías a los ácaros del polvo y a los hongos (mohos), que son alergenos comunes en Colombia.
También, la existencia de una gran susceptibilidad para la hepatitis delta en la región norte de Colombia, indica que un estudio inmunogenético de identificación de haplotipos colombianos asociados con la falta de respuesta a la vacuna contra la hepatitis B serían muy útiles. La identificación de individuos
que no responden a vacunas comunes, sugeriría que ellos son más susceptibles a adquirir la hepatitis. En consecuencia, será necesario desarrollar otras vacunas con diferentes ntígenos para proteger a esa población.
Agradecimientos
Expresamos nuestros agradecimientos a Ada Watson por su ayuda con el material gráfico.
Referencias Bibliograficas
- 1. Reinherz, E.L., and Schlossman, S. (1980). The differentiation and function of human T Iymphocytes. Cell 19:821-826.
- 2. Bronet, J.C. (1983). The origin of human B and ‘1’ cells from multipotent stem cells. A study of the TN syndrome. Eur. J. Immunology. 13:350-355.
- 3. Moller, G. (1981).Ontogeny of human Iymphocyte function. Immunology Rev. 57:1-10;
- 4. Rosenthal, A.S. (1978).Determinant selection and macrophage function in genetic control of the immune response. Immunological Rev. 40:136-152.
- 5. Geha, RS., Milgrom, H., Broff, M., Alpert, S., Martin, S., and Yunis, E.J. (1979). Effect of anti-HLA antisera on macrophage-T-cell interaction. Proc. Nat!. Acad. Sci. 76(8):4038-4041.
- 6. Cantor, H., and Boyse, E.A. (1975). Functional subclases of ‘1’Iymphocytes bearing different Ly antigens 11. Cooperation between subclasses of Ly and Ly + cells in the generation of killer activity. J. Exp. Med. 141:1390.
- 7. Nomenclature Committee IUIS/WHO (1984). Leukocyte differentiation antigens. In: Leukocyte Typing. pp 133, Barnard, A., Bounsell, L., et al. (Eds.) Springer-Veriag, Berlin.
- 8. Flomenberg, N., and Naito, K. (1983).AlIocytotoxic ‘1’cell clones: Both Leu 2+3 and Leu 2-3+ ‘1’cell recognize class I histocompatibility antigens. Eur. J. Immunol. 13:905-907.
- 9. Klein, J. (1982). The major histocompatibility complex. In: Immunology, the science of self and nonself discrimination. A. Wiley, Inter-Science Pub!., John Wiley and Sonso
- 10. Yunis, E.J., Dupont, B. (1987).The HLA system. In: Hematology of infancy and childhood. Nathan and Oski (Eds.). Saunders.
- 11. Schneider, P.M. (1986).Polymorphism of the human complement C4 and steroid 21-hydroxylase genes. J. Clin. Invest. 78:650-657.
Otras Referencias Bibliográficas
- 12. Cresswell, P., Springer, T., Strominger, J.L., Turner, M.J., Grey, H.M. and Kubo, R.T. (1974). Immunological identity of the small subunit of HLA-A antigens and B-2 microglobulin and its turnover on the cell membrane. Proc. Natl. Acad. Sci. USA. 71:2123-2127.
- 13. Tragardh, L., Wiman, K. R, and Peterson, P.A. (1979). Fragmentation of the human transplantation heavy chain by limited proteolysis, acid cleavage and cyanogen bromide treatment. Biochemistry. 18:1322-1328.
- 14. Terhorst, C., Parham, P., Mann, D.L., and Strominger, J.L. (1976). Structure of HLA antigens amino-acid and carbohydrate compositions and NH2-terminal sequence for four antigen preparations. Proc. Nat!. Acad. Sci. USA. 75:3390-3394.
- 15. Shackelford, D.A., Kaufman, A.J., and Strominger, J.L. (1982). HLA-DR antigens: Structure separation of subpopulations gene cloning and function. Immuno!. Rev. 66:133-137.
- 16. Reinsmoen, N., and Yunis, E. (1977). Inheritance of recombinant HLA-GLO haplotype suggesting the gene sequence. Nature. 267:276.
- 17. Thorsby, E., Albrechtssen, D.L., Hirschberg, H., Kaakinen, A., and Solheim, B.G. (1977).MLC-Activating HLAD detenninants; identification, Tissue Distribution and Significance. Transplantation Proceedings. 9:393-400.
- 18. Schwartz, B.D., and Cullen, S.E. (1978).Chemical characteristics of la antigens. Springer Sem. Immunopath. 185-190.
- 19. Finnegan, A., Smith, M., Smith, J., Berzofsky, J., Sachs, D., and Hodes, R (1986).The ‘1’cell repertoire for recognition of a phylogenetically distant protein antigen. Peptide specificity and MHC restriction of staphlococcal nuclease-specific ‘1’cell clones. J. Exp. Med. 164:897-910.
- 20. Schwartz, R, Fox, B.S., Fraga, E., Chen, C.H., and Singh, B. (1985). The ‘1’Iymphocyte response to cytochrome C. J. Immuno!. 135: 2598-2608.
Fuentes Bibliográficas
- 21. Berkower, l., Matis, L.A., Buckenmeyer, G.K., Gurd Frank, RN., Longo, D.L., and Berzofksy, J.A. (1984). Identification of distinct predominant epitope recognized by myglobin-specific ‘1’cells under the control of different Ir genes and characterization of representative ‘1’cell clones. J. Immunol 132: 1370-1378.
- 22. Babbit, B.P., AlIen, P.M., Matsueda, G., Haber, E., and Unanue, E.R (1985). Binding of immunogenic peptides to la histocompatibility molecules. Nature. 317: 359•361.
- 23. Babbit, B.P., Matsueda, G., Haber, E., Unanue, E.R, and AlIen, P. (1986). Antigenic competition at the level of peptide-Ia binding. Proc. Nat!. Acad Sci. USA. 83: 4509-4513.
- 24. Buus, S., Colon, S., Smith, C., Freed, J.H., Miles, C., and Grey, H.M. (1986). Interaction between a “processed” ovalbumin peptide and la molecule. Proc. Nat!. Acad. Sci. USA. 83: 3968-3971.
- 25. Guillet, J., Ming-zong, L., Brinner, T.J., Buus, S., Sette Alexander Grey, H.M., Smith, J.A., and Gefter, M.L. (1986). Immunological self, nonself discrimination. 235: 865-870.
- 26. Alper, C.A., Awdeh, Z.L., and Yunis, E.J. (1986). Com- ‘plotypes, extended haplotypes, male segregation distortion and disease markers. Human Immunology. 15: 366-373.
- 27. Alper, C.A., Raum, D., Karp, S., Awdeh, Z.L., and Yunis, E.J. (1983). Serum complement “Supergenes” of the major histocompatibility complex in man (complotypes). Vox Sango 45: 62-67.
- 28. Alper, C.A., Awdeh, Z.L., Raum, D.D., and Yunis, E.J. (1985).Possible human analogs of the murine T/t complexo Exp!. Clin. Immunogenet. 2: 125-136.
- 29. Awdeh, Z.L., Raum, D., Yunis, E.J., and Alper, C.A. (1983a).Extended HLA complement allele haplotype: Evidence for T/t-like complex in mano Proc. Nat!. Acad. Sci.USA. 80: 259-263.
Otras Fuentes Bibliográficas
- 30. Alper, C.A., Awdeh, Z.L., Raum, D.D., and Yunis, E.J. (1982). Extended major histocompatibility complex haplotypes in man: Role of allelos analogous to murine T mutants. Clin. Immunology and Immunopathol. 24: 276-285.
- 31. Bodmer, W.F., and Bodmer, J.G. (1978). The HLA system; Introduction. Br. Med. BuI!. 34: 309-316.
- 32. Amos, D.B., Pool, P., and Grier, J. (1980). HLA-A, HLAB, HLA-C and HLA-DR In: Manual of clinical immunology. Rose, N.R, Friedman, H. (Eds.). pp. 978. American Society for Microbiology.
- 33. McFarlane, 1.G. (1984). Autoimmunity in liver disease. Clin. Sci. 67: 569-578.
- 34. Craven, D.E., Kunches, L.M., Dienstag, J.L., Werner, B.C., Alper, C.A., Yunis, E.J., Awdeh, Z.L., Polk, B.F., Snydman, D.R, Platt, R., Crumpacker, C.S., and Grady, G.F. (1986).Non-responsiveness to hepatitis B vaccine in health care workers; results of revaccination and gene tic typings. An. Int. Med. 105: 356.
- 35. Vento, S. (1984).Antigen specific suppressor cell function in autoimmune chronic active hepatitis. Lancet. 1200-1204.
- 36. Walker, M.E., Szmuness, W., Stevens, C.E., and Rubinstein, P. (1981). Genetics of anti-HBs responsiveness: 1. HLA-DR7 and non-responsiveness to hepatitis vaccination (abstract). Transfusion. 21: 601.
- 37. Milich, D., Leroux-Roels, G.G., and Chisari, F.V. (1983). Genetic regulation of the immune response to hepatitis B surface antigen HBsAg; n. Qualitative characteristic of the humoral immune response to the A, D, and Y determinants of HBsAg. J. Immuno!. 130: 1395-1400.
- 38. Usonis, V., Kuhn!, P., Rede, H.D., and Doerr, H.W. (1986). Humoral immune response after hepatitis B-vaccination: Kinetics of anti-HBs antibodies and demonstration of HLA antigens. Zentra (b) Bacterio!. Microbio!. Hyg. (a). 262(3): 377-384.
Referencias
- 39. Penichi, G., Cappellaccis, Mola, A., Morellini, M., Lulli, P., and Pescini, A. (1986). HLA and hyporesponsibility to anti-HBV vaccination (genetic study of non-responder subjects to anti•hepatitis B viral vaccine). Boll Inst. Sieroter Milan. 65(6): 459-463.
- 40. Gorzynski, T.J., and David, C.S. (1983). Immune response gene-associated antigens Ia/DR: structure and function in immunologically related diseases. Mayo Clin. Proc. 58: 457-466.
- 41. Cars, RM., and Anderson, R.R (1968).The disappearance rate of skinsensitivity antibody. J. Allergy. 42:29.
- 42. Ishizaka, K., and Ishizaka, T. (1978).Irnmunology of IgEmediated hypersensitivity in allergy-principles and practice. Vo!. 1. Middleton, Jr., Redd, C.H., and Ellis, Eds. pp. 52-78.
- 43. Bennich, H., and Johansson, S.G.O. (1971). Structure and function of human immunoglobulin E. Adv. Immuno!. 13:1.
- 44. Katz, D.H., and Marcelleti, J.F. (1983). Regulation of the IgE antibody system in human s and experimental animal. Progress in Immunology V. (Yamura and Tada, Eds.). V. Intern Congress of Immunology. pp. 465-482.
- 45. Scheleimer, RP., MacGlashan, D.W., Peters, S.P., Naderio, R., Proud, D., Adkinson, N.F. and Lichenstein, L.M. (1984).Inflammatory mediators and mechanism of release from puritied human basophils and mast cells. J. Allergy Clin. Immuno!. 4-473.
- 46. Smith, J.M. (1983). Epidemiology and natural history of asthma, allergic rhinitis and atopic dermatitis. In: Middleton, E., Reed, C., Ellis, E. (Eds.). Allergy; Principals and Practice. Sto Louis, C.V. Mosby company. pp. 771.
- 47. Blumenthal, M., Mendell, N., and Yunis, E. (1980). 1mmunogenetics of atopic diseases. J. All. Clin. Immunol. 65: 403-4G5.
- 48. Vaughn, W., and Black, J.H. (1954). Heredity in practice of allergy, 3rd ed. C.V. Mosby Co. pp. 74.
Bibliografías
- 49. Deweck, A., Blumenthal, M., Yunis, E.J., and Jeannet, M. (1977). HLA and allergy. In: Dausset, J., Svejgaard, A, (Eds.). HLA and Disease, Baltimore. The Williams and Wilkins Company.
- 50. Blumenthal, M., Namboodiri, K., Mendell, N., Gleich, G., Elston, R.C., and Yunis, E. (1981). Genetic transmission of serum IgE levels. J. Med. Genet. 10: 219-228.
- 51. Hopp, R, Coleman, R., Bewerta, A., and Townley, R. (1984). Methacholine inhalation challenge as a potential genetic marker. American Academy of Pediatrics, section on allergy and immunology.
- 52. Levine, E., Stember, R, and Fotino, M. (1972).Ragweed, hay fever, genetic control and linkage to HLA-A haplotypes. Science. 178: 1201.
- 53. Blumenthal, M., Amos, D., Noreen, H., Mendell, N., and Yunis, E.J. (1974). Genetic mapping of Ir locus in mano Linkage to second locus of HLA. Science. 184: 1301.
- 54. Mendell, N.R, Blumenthal, M., Amos, D.B., Yunis, E.J., and EIston, R.C. (1978). Ragweed sensitivity. Segregation analysis and linkage to HLA-B. Cytogenetics. 22: 330-334.
- 55. Blumenthal, M.N., Yunis, E.J., Mendell, N.R, and Amos, D.B. (1977). HLA and ragweed allergy. Monographs in Allergy. 11: 83-88.
- 56. Marsh, D., Hsu, S.H., and Roebber, M. (1982). HLADw2- A genetic marker for human immune response to short ragweed allergen RA5 1 response resulting primarily from natural antigenic exposure. J. Exp. Med. 155: 1439-1451.
- 57. Marsh, D., Meyers, D., and Freidhoff, L. (1982). HLADw2- A genetic marker for human immune response to short ragweed allergen RA5; n response after ragweed immunotherapy. J. Exp. Med. 155: 1452-1463.