Epidemiología
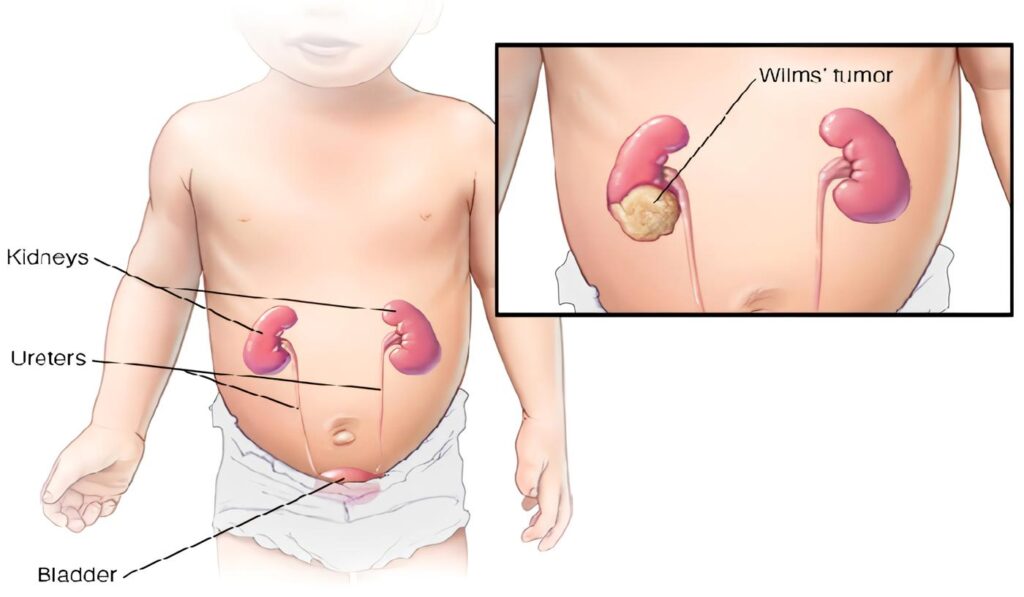
El tumor de Wilms es la neoplasia maligna renal más frecuente en niños. Su incidencia es de 8,1/1.000.000 en menores de 15 años. Representa del 5% al 6% de los tumores malignos en oncología pediátrica. El tumor se presenta a una edad más temprana en varones, con una edad media al diagnóstico, en tumores unilaterales, de 41 meses, comparado con 47 meses en las niñas. El promedio de edad de tumores bilaterales es de 20 meses para los niños y 33 meses para las niñas.
Las anomalías congénitas asociadas ocurren en el 12% al 15% de los casos, incluyendo anhiridia, hemihipertrofia, criptorquidia e hipospadias. Lo niños con pseudohermafroditismo o con enfermedad renal (glomerulonefritis, síndrome nefrótico), que desarrollan tumor de Wilms pueden presentar el síndrome de Denys-Drash: tumor de Wilms, aniridia, malformación genitourinaria y retardo mental. La hemihipertrofia puede ocurrir como anormalidad aislada o puede ser parte del síndrome de Beckwith – Wiedemann, que incluye: macroglosia, onfalocele y visceromegalia.
Etiopatogenia
Estudios realizados en pacientes con tumor de Wilms han encontrado, en algunos casos, deleción en el brazo corto del cromosoma 11 en la banda p13. Existe además un segundo locus en el cromosoma 11 p15 designado como WT2, que puede explicar la asociación de este tumor con el síndrome de Beckwith-Wiedemann.
Cuadro Clínico
La mayoría de los niños con tumor de Wilms son traídos a consulta médica por aumento en el perímetro abdominal o por tumoración abdominal palpable. Generalmente, esto es detectado por un familiar mientras bañan o visten al niño. El dolor abdominal, la hematuria macroscópica y la fiebre son otros de los síntomas frecuentes al diagnóstico. La hipertensión arterial se presenta en cerca del 25% de los casos y ha sido atribuida a un aumento en la actividad de la renina.
Durante el examen físico, el médico deberá anotar la localización y el tamaño de la tumoración abdominal. También es importante la búsqueda de signos, que forman parte de los síndromes asociados con este tumor, tales como aniridia, hemihipertrofia parcial o completa y anomalías genito-urinarias como hipospadias y criptorquidia, las cuales deben ser consignadas en la historia clínica. El varicocele secundario a la obstrucción de la vena espermática, puede estar asociado con la presencia de un trombo tumoral en la vena renal o en la cava inferior.
Clasificación Histopatológica
La histología del tumor de Wilms tiene un impacto importante en el pronóstico y el tratamiento. Se divide en tumores con histología favorable y con histología desfavorable. En este último grupo están los niños con anaplasia difusa o con anaplasia focal. La anaplasia está presente en 4,5% de los casos y ha sido relacionada con la edad del paciente. Es rara en los primeros 2 años y aumenta hasta el 13% en pacientes de 5 años o mayores.
Mientras que el sarcoma de células claras del riñón y el tumor rabdoide maligno del riñón fueron inicialmente agrupados dentro de los tumores de Wilms, actualmente son considerados y entidades distintas.
Criterios histopalógicos para el diagnóstico de anaplasia
Macroscópicamente se evalúan:
- Peso y tamaño del riñón y del tumor.
- Invasión capsular o pseudo-capsular.
- Invasión del seno renal. · Ruptura quirúrgica.
- Compromiso tumoral de la vena renal. · Implantes tumorales extra-renales.
- Compromiso ganglionar metastásico.
- Metástasis a distancia.
- Compromiso tumoral renal bilateral.
- Distancia de los bordes de sección quirúrgico.
Microscópicamente, se debe hacer al menos un corte por cada centímetro de diámetro mayor tumoral, en el que se represente ampliamente la periferia capsular tumoral y la interfase tumor-riñón. Los tumores de Wilms o nefroblastomas se subdividen en: tumores de histología favorable o desfavorable, evaluando principalmente anaplasia nuclear, en cualquiera de los componentes celulares blastomatosos, mesenquimales o epiteliales.
Definición y criterios de anaplasia:
Anaplasia: puede distribuirse en forma focal o difusa en el tumor primario o en las metástasis; se observa más frecuentemente en niños mayores de 5 años (hasta en 13%) y de raza negra; es rara en niños menores de dos años, encontrándose en el 4,5% de los casos. Usualmente el compromiso difuso confiere un peor pronóstico. Aparentemente, la histología desfavorable en tumores estado I, no tiene esta implicación pronóstica.
La histología desfavorable se define bajo estos criterios:
1. Agrandamiento nuclear marcado, mayor de 3 veces el tamaño de los núcleos vecinos, en cualquiera de los tipos celulares, excepto en las células de tipo muscular estriado.
2. Hipercromasia de los núcleos grandes.
3. Mitosis atípicas, multipolares.
Otros parámetros microscópicos a tener en cuenta incluyen: invasión linfática tumoral intra y extra-renal y compromiso tumoral de bordes de sección.
La anaplasia, aunque sea solamente en uno o pequeños focos de tumor, es suficiente para que tenga un marcado impacto en un peor pronóstico. El centro de patólogos del Wilms Tumor Study National (NWTS) recomienda un mínimo de secciones generosas obtenidas por cada centímetro de diámetro de tumor, con atención meticulosa a los detalles de preservación de tejido y preparación de láminas. Pequeñas fallas en el procesamiento del tejido causan falsas interpretaciones.
Restos Nefrogénicos – Nefroblastomatosis
La presencia de restos nefrogénicos (tejido metanéfrico persistente en el riñón después de la semana 36 de gestación), ha sido asociada con la ocurrencia del tumor de Wilms. Estas lesiones son consideradas premalignas, pueden ocurrir en la localización perilobular o intralobular y pueden ser simples o múltiples. En niños con aniridia o síndrome de Dennys-Drash, las lesiones son primordialmente intralobulares, mientras que en los niños con hemihipertrofia o síndrome de Beckwith-Wiedemann estas lesiones son predominantemente perilobulares. La presencia de restos nefrogénicos difusos o múltiples se denomina nefroblastomatosis.
Diagnóstico
Laboratorio
Deberá siempre incluir:
- Cuadro hemático, con plaquetas y recuento diferencial.
- Función hepática: bilirrubinas, transaminasas, fosfatasa alcalina.
- Función renal: nitrógeno ureico, creatinina, uroanálisis.
- Electrolitos: sodio, potasio y calcio sérico.
- Deshidrogenasa láctica.
- Estudios de coagulación (TP, TPT).
Imágenes Diagnósticas
Al ingreso del niño al hospital se deberán solicitar los siguientes estudios: ecografía abdominal total y exploración ecográfica de la vena cava inferior y de la aurícula derecha.
Radiografía de tórax (postero-anterior y lateral).
TAC torácica y abdominal con contraste, con el fin de valorar el riñón contralateral y el compromiso metastásico.
Gamagrafía ósea en caso de sarcoma de células claras.
Deberá además utilizarse la resonancia magnética cerebral o TAC cerebral en casos de tumor rabdoide o sarcoma de células claras.
Valoración Cardiológica
Esta valoración es necesaria en pacientes que van a recibir antraciclina. Se deben obtener los siguientes estudios:
Electrocardiograma, ecocardiograma y fracción de eyección ventricular por Medicina Nuclear.
Factores Predictores de Pronóstico
Los factores más directamente relacionados en el pronóstico de este tumor son: tamaño tumoral, edad del paciente, tipo histológico, metástasis a ganglios linfáticos e invasión vascular o capsular.
Con protocolos de tratamiento más efectivos, el significado pronóstico de los factores identificados inicialmente puede cambiar, como se ha observado en los estudios del NWTS. La supervivencia es mejor en niños menores de 2 años y varía de acuerdo con el estado clínico de la enfermedad así:
Estado I histología favorable 95% de supervivencia.
Estado II histología favorable >90% de supervivencia.
También, Estado III aproximadamente 90% de supervivencia con histología favorable.
Estado IV histología favorable, 80% de supervivencia.
La anaplasia es el más importante cambio citológico indicador de pobre pronóstico. Recaídas y muerte debidas a tumor en los estados I,II y III de niños con tumor anaplásico fueron de 47% en el NWTS 2, en contraste con solo 5% de los niños que no tuvieron anaplasia.
Los tumores bilaterales sincrónicos tiene mejor pronósticos que los tumores bilaterales metacrónicos.
Estadificación
Estado I
Tumor limitado al riñón y completamente resecado, cápsula renal intacta en la superficie externa el tumor. No se rompió si se tomó biopsia antes de extirparlo y no hay evidencia de tumor más allá de los márgenes de resección. Los vasos del seno renal están libres de tumor.
Estado II
El tumor se extiende más allá del riñón, pero fue completamente resecado. Hay extensión del tumor, con penetración a la cápsula renal, o invasión extensa del seno renal. Los vasos sanguíneos fuera del parénquima, incluyendo aquellos del seno renal, contienen tumor. Se tomó biopsia antes de la resección (excepto aspiración por aguja fina), o hay derrame de este antes o durante la cirugía, confinada al flanco y sin involucrar la superficie peritoneal. No hay evidencia de tumor más allá de los márgenes de resección.
Estado III
Tumor residual no hematógeno y confinado al abdomen, con alguno de los siguientes hallazgos:
- Presencia de ganglios linfáticos dentro del abdomen o de la pelvis, con compromiso tumoral del hilio renal, paraaórtico o más allá.
- Invasión tumoral a la superficie peritoneal, remanente tumoral, micro o macroscópico después de la cirugía.
- Tumor incompletamente resecado.
Estado IV
Extensión del tumor por metástasis hematógena (pulmón, hígado, hueso, cerebro, etc.) o metástasis a ganglios linfáticos fuera de la región abdominopélvica. En caso de detectar nódulos metastásicos solamente en la tomografía pulmonar, pero no en la radiografía simple de tórax, se sugiere confirmar por biopsia escisional.
Estado V
Compromiso renal bilateral al diagnóstico. En estos casos se debe intentar estadificar cada lado de acuerdo a los criterios establecidos, con base en la extensión de la enfermedad antes de la biopsia.
Tratamiento
Cirugía
El tratamiento inicial en todos los estados es la nefrectomía.
Procedimiento quirúrgico
Se recomienda utilizar una incisión grande transabdominal, transperitoneal, para una exposición adecuada. Se debe realizar una exploración completa del abdomen.
El riñón contralateral debe ser palpado y visualizado para descartar compromiso bilateral y se debe tomar biopsia a cualquier área sospechosa de compromiso bilateral.
Si el diagnóstico es todavía incierto en el momento de la laparotomía, la biopsia o punción del tumor debe ser evitada por el riesgo de siembras tumorales en el peritoneo.
Asignación del estado quirúrgico
El cirujano debe marcar el lecho tumoral (estado local-regional del tumor) de acuerdo con los hallazgos quirúrgicos. El uso de “clips” de titanio es recomendado para identificar tumor residual, margen de disección y áreas sospechosas. Los “clips” ferromagnéticos pueden interferir con la tomografía computarizada y no deben utilizarse.
Documentación de ganglios linfáticos
La presencia o ausencia de metástasis ganglionares en el hilio o metástasis regionales es muy importante para una adecuada estadificación y una terapia adecuada. Rutinariamente deben tomarse muestras de ganglios linfáticos de las áreas ilíacas, paraaórticas y celíacas, para una correcta estadificación. Los ganglios linfáticos sospechosos o comprometidos deben resecarse y marcarse cuidadosamente para examen microscópico.
Consideraciones intraoperatorias
Antes de movilizar el tumor primario, se debe intentar disecar, exponer y ligar los vasos renales, para disminuir el riesgo de diseminar las células tumorales cuando se retira el tumor. La ligadura preliminar no se deber realizar si es técnicamente difícil o peligrosa.
Vena renal/vena cava inferior
La ecografía prequirúrgica es recomendable para identificar la extensión intravascular del tumor. La vena renal y la vena cava inferior deben palparse cuidadosamente para descartar posible extensión tumoral a la luz de la vena. Si la extensión tumoral está presente, deberá removerse el tumor en “bloque” con el riñón, si es posible, antes de la ligadura de la vena.
Los pacientes con extensión del trombo tumoral por encima del nivel de las venas hepáticas deben recibir quimioterapia preoperatoria. Este manejo puede disminuir el trombo intravascular y facilitar el subsecuente procedimiento quirúrgico.
En tumores que comprometen las estructuras contiguas se deben tomar biopsias y definir el estado quirúrgico. La mayoría de estos tumores comprimen y adhieren el órgano adyacente, sin invadirlo. Estos pacientes pueden ser tratados con quimioterapia citorreductora y así permitir la nefrectomía con conservación de los órganos contiguos. Si se deja tumor residual, se debe identificar el sitio con “clips”.
La nefrectomía parcial no está indicada como procedimiento de rutina en el tumor de Wilms. Las excepciones incluyen pacientes con riñón solitario, niños con enfermedad bilateral sincrónica o metacrónica y otros pacientes con riesgo aumentado de neoplasias múltiples, como el síndrome de Beckwith- Wiedemann.
Derrame tumoral
El peritoneo debe considerarse contaminado si se ha realizado biopsia, si el tumor se ha derramado o si se ha roto.
Es importante para la adecuada estadificación, determinar la contaminación peritoneal por el tumor, pues es indispensable para la planeación de la radioterapia.
El derrame se refiere a la transgresión de la cápsula tumoral o sus extensiones durante la resección quirúrgica ya sea accidental, inevitable o espontánea.
Si el tejido tumoral fue cortado durante la resección de las estructuras adyacentes o durante la resección de los ganglios linfáticos, el cirujano debe indicar si la cavidad peritoneal fue sembrada por células tumorales local o difusamente.
Cuando el tumor se extiende dentro de la vena renal o de la vena cava inferior, debe hacerse una mención precisa de la técnica de resección y debe anotarse si el trombo tumoral fue resecado completamente y si hay evidencia de adherencia o invasión a la pared de la vena.
La ruptura se refiere a la ruptura espontánea o traumática del tumor, con diseminación de células tumorales a la cavidad peritoneal. El líquido peritoneal sanguinolento debe ser considerado un signo de derrame, ya sea que se encuentren o no en el examen microscópico células tumorales.
Tumores inoperables
Los tumores pueden ser inoperables a causa del tamaño, extensión dentro de la porción suprahepática de la vena cava inferior o por otras razones. La quimioterapia preoperatoria puede estar indicada para reducir el tamaño tumoral y facilitar la resección. En estos casos se debe evaluar nuevamente a la 5ª semana la posibilidad de resección quirúrgica.
Tumor de Wilms Bilateral
Antes de proceder a cualquier tipo de tratamiento deben tomarse biopsias bilaterales para confirmar la presencia de tumor en ambos riñones y definir su tipo histológico.
La nefrectomía parcial o la resección amplia pueden ser empleadas en la operación inicial, solamente si el tumor puede ser resecado con preservación de la mayoría del parénquima renal en ambos lados. Se deben tomar muestras de ganglios linfáticos sospechosos durante la cirugía.
La quimioterapia se administra de acuerdo al estado y la histología. La respuesta debe ser evaluada a la 5ª semana. Realizar la segunda cirugía con un control de tomografía computarizada antes de esta, para valorar la disminución del volumen tumoral y la posibilidad de resección parcial. Al tiempo de la segunda cirugía, deben realizarse nefrectomías parciales o resección amplia de los tumores, si es posible. Si durante la segunda cirugía no hay evidencia macro o microscópica de persistencia del tumor, el paciente debe continuar con quimioterapia. Los pacientes con persistencia de tumor intraabdominal deben ser valorados para cambios de la quimioterapia. La doxorrubicina esta indicada en caso de persistencia tumoral en la semana 6.
Debe valorarse nuevamente el paciente en la 12ª semana para posible resección quirúrgica. Si la exploración confirma persistencia tumoral el paciente debe ser valorado en junta interdisciplinario para posible tratamiento con radioterapia postoperatoria.
Quimioterapia
La quimioterapia debe iniciarse en el post-operatorio inmediato y no más allá del quinto día, en promedio en las primeras 72 horas del post-operatorio. Antes de iniciar cualquier esquema de quimioterapia deber hacerse un control hematológico completo.
La dosis se calcula por superficie corporal y debe disminuirse en un 50% en niños menores de 12 meses.
De acuerdo a los hallazgos histológicos se planea la quimioterapia así:
Estado I (histología favorable)
Edad menor de 24 meses y tumor que pesa menos de 550 g.
Nefrectomía. No requiere quimioterapia de acuerdo a las recomendaciones del NWTS.
Evaluación clínica mensual con radiografía de tórax, ultrasonido abdominal cada 3 meses, durante los primeros 2 años, después del diagnóstico.
Estado I (histología desfavorable)
Edad mayor de 24 meses, peso tumoral de 550 gramos y anaplasia focal o difusa:
Nefrectomía
Quimioterapia así :
Actinomicina D: 0,045 mg/kg/dosis IV. Se debe empezar dentro de los primeros 5 días post-nefrectomía y continuar en las semanas 3, 6, 9, 12, 15 y 18. La dosis de Actinomicina D, será de 1,35 mg/m2 para los pacientes que tengan un peso mayor de 30 kg y la dosis total no debe nunca exceder 2,3 mg.
Vincristina: 0,05 mgl/kg IV, (dosis máxima 2 mg), comenzando el día 7 post-nefrectomía, si la peristalsis se ha reestablecido. Se continúa semanalmente.
El tratamiento inicial de vincristina será de 10 dosis y luego se continuará con Vincristina: 0,067 mg/kg, IV, (dosis máxima 2,0 mg) con actinomicina en las semanas 12, 15, 18.
Estado II (histología favorable)
Nefrectomía
Quimioterapia así:
Actinomicina D: 0,045 mg/kg/dosis IV, (máxima dosis 2,3 mg), se debe empezar dentro de los primeros 5 días post-nefrectomía, es decir durante la semana 0, y continuar en las semanas 3, 6, 9, 12, 15 y 18.
La dosis de Actninomicina D se debe aumentar a 1,35 mg/m2 para los pacientes que tengan un peso mayor de 30 kg, pero esta dosis no debe exceder de 2,3 mg.
Vincristina: 0,05 mg/kg/dosis. Se debe empezar el día 7 post-nefrectomia (semana 1), si la peristalsis se ha reestablecido y continuarla semanalmente por un total de 10 dosis. Para los pacientes que pesen mas de 30 kg, la dosis de vincristina será de 1,5 mg/m2, sin exceder 2,0 mg. Luego se reajustará así la vincristina: 0,067 mg/kg, IV (dosis máxima 2,0 mg.) con actinomicina en las semanas 12, 15, 18, 21 y 24.
Estado III con histología favorable y estados II o III con anaplasia focal
Nefrectomía.
Radioterapia abdominal.
Quimioterapia así:
Actinomicina D: 0,045 mg/kg (dosis máxima 2,3 mg), comenzar en los primero 5 días post-nefrectomía y repetir durante las semanas 6, 12, 18 y 24. La dosis de Actinomicina D, deberá disminuirse en un 50% a partir de la sexta semana (0,0225 mg/kg/dosis), si el paciente va a recibir radioterapia abdominal total. Para pacientes con peso mayor de 30 kg, 1,35 mg/m2 (dosis máxima = 2,3 mg). Disminuir 50%, si recibe radioterapia concomitante.
Vincristina: 0,05 mg/kg, IV (máxima dosis 2 mg), comenzando en el día 7 postnefrectomía, si la peristalsis se ha establecido y continuar semanalmente por un total de 10 dosis. Luego se continúa con: Vincristina: 0,067 mg/kg. IV, (dosis máxima 2 mg) con actinomicina en las semanas 12, 15, 18, 21, 24.
Para pacientes que pesen mas de 30 Kg, la dosis de vincristina será de1,5 mg/m2 IV, pero no debe exceder 2,0 mg. Luego se continúa con dosis de 2 mg semanales
Doxorrubicina: 1,5 mg/kg, IV, administrada en las semanas 3 y 9. Posteriormente se continuará con doxorrubicina 1,0 mg/kg IV, en las semanas 15 y 21. La dosis de doxorrubicina se disminuirá en un 50% (0,75 mg/kg), si se administrado radioterapia abdominal.
Estado IV histología favorable o anaplasia focal
Nefrectomía, seguida de radioterapia abdominal y de acuerdo al estado local del tumor renal, se dará también radiación pulmonar bilateral, siguiendo los siguientes parámetros:
Los nódulos pulmonares no detectados en radiografía de tórax, pero visibles en tomografía computada del tórax, no requieren radioterapia pulmonar total. La decisión de administrar radioterapia pulmonar total deberá ser analizada por el grupo tratante. Se recomienda, biopsia escisional para confirmar estas metástasis.
La quimioterapia es igual a la utilizada en el estado III.
Estado V
Inicialmente se debe tomar biopsia del tumor bilateral. El tratamiento será de acuerdo a lo mencionado anteriormente en los otros estados. Una reevaluación 5 semanas después del diagnóstico es necesaria con el fin de considerar la posibilidad de segunda exploración. Posteriormente se hará una nueva reevaluación en la semana 27 después del diagnóstico.
Anaplasia difusa de estado II a IV
Nefrectomía, seguida de irradiación abdominal y radioterapia pulmonar total para pacientes con metástasis pulmonares. La quimioterapia se hace con vincristina, doxorrubicina, etopósido, ciclofosfamida y mesna, Además se utiliza profilaxis con trimetoprim sulfametoxasol 2,5 mg/kg dividido en dos dosis en 3 días consecutivos por semana, desde el comienzo del tratamiento y administrado por 6 meses después de terminada la quimioterapia.
Otros tumores renales:
Sarcoma renal de células claras estado I al IV
El tratamiento inicial será nefrectomía, seguida de radioterapia abdominal. Radioterapia pulmonar total para los pacientes con metástasis pulmonares y quimioterapia así:
Vincristina: 0,05 mg/kg, IV, comenzando 7 días posnefrectomía si la peristalsis está presente. Se continúa las semanas 2, 4, 5, 6. 7,8, 10 y 11. Esta dosis nunca será mayor de 2 mg. Se debe agregar doxorrubicina en las semanas 0,6, 12, 18 y 24. Para pacientes que pesen más de 30 kg, la dosis de vincristina será de 2 mg/m2. Luego se continuará Vincristina: 0.067 mg/kg IV, (dosis máxima 2 mg) en la semana 13 y vincristina 0,067 mg/ kg, IV, con doxorrubicina en las semanas 12, 18 y 24.
La dosis de doxorrubicina es de 1,5 mg/kg, IV. Sin embargo, debe disminuirse en la semana 6, en un 50%, si se ha administrado radioterapia abdominal o pulmonar total.
Ciclofosfamida: 14,7 mg/k/día, por 5 días, en la semana 3, 9, 15 y 21. Esta dosis se modificara a 440 mg/m2/día, por 3 días para los pacientes que pesen más de 30 kg.
Mesna, 3 mg/kg/dosis, por 4 dosis, en 10 ml. en infusión de 15 minutos, por 5 días, después de ciclosfosfamida en la semana 6, 12, 18 y 24. Esta dosis será de 90 mg/m2/ dosis, por 4 dosis, por 3 días, para los pacientes que pesen más de 30 kg.
Ciclofosfamida: 14,7 mg/kg/día, por 5 días, en las semanas 3, 9, 15 y 21, con Mesna por 5 días.
La ciclofosfamida se administrará primero que la doxorrubicina y que el etopósido.
Etopósido (VP-16) 3,3 mg/kg./día por 5 días, en las semanas 3, 9, 15 y 21. Para los pacientes cuyo peso sea de 30 kg o más, esta dosis será de 100 mg/m2/día, por 5 días.
Tratamiento de estados I a IV del tumor rabdoide renal
Nefrectomía, radioterapia y quimioterapia con ciclofosfamida, Mesna, etopósido y carboplatino.
Carboplatino: 16,7 mg/kg /día, por 2 días, durante las semanas 0, 3, 9. 12, 18, y 21 post-nefrectomia. La dosis de carboplatino se aumentara a 500 mg/m2/día, por 2 días, durante el mismo número de semanas, para los pacientes que pesen más de 30 kg.
Etopósido (VP-16) 3,3 mg/kg/día, por 3 días, en las semanas 0, 3, 9, 12, 18 y 21 después de la infusión de carboplatino. La dosis de etopósido será de 100 mg/m2, por 3 días, para los pacientes que pesen mas de 30 kg.
Ciclofosfamida 14,7 mg/kg/día, por 5 días, semanas 6,15 y 24. Para los pacientes que pesen más de 30 kg la dosis de ciclofosfamida será de 440 mg/m2/día, por 5 días.
Mesna 3 mg/kg/dosis, dosis por 4 dosis, en infusión de 15 minutos, por 5 días, será administrada después de la ciclofosfamida en las semanas 6, 15 y 24.
Radioterapia
El día de la nefrectomía será considerado el día 0. Según las recomendaciones recientes del NWTS, se debe empezar en los primeros 10 días después de cirugía.
Estado I, II de histología favorable, no necesita radioterapia postoperatoria.
Estado III de histología favorable, debe usarse radioterapia a dosis baja (1000 a 2000 cGy).
Recomendaciones
La radioterapia al flanco: Debe cruzar la línea media para incluir ganglios bilaterales paraaórticos en:
Compromiso ganglios linfáticos del hilio renal.
Enfermedad residual micro o macroscópica, confinada al flanco.
Compromiso de ganglios, linfáticos para-aórticos.
Dosis por fracción 1,5 – 1,8 GS, 5 días a la semana.
Dosis al lecho tumoral de 10,5 – 10,8 Gy.
Cuando el tumor es mayor de 3 cm de diámetro y hay enfermedad residual, se puede dar un refuerzo de 10,8 Gy, para una dosis total acumulada de 21,6 Gy.
Radioterapia abdominal total
En los casos de siembras peritoneales , enfermedad residual macroscópica, ruptura intraperitoneal preoperatoria, derrame operatorio difuso.
Dosis por fracción 1,5 – 1,8 Gy, 5 días a la semana.
Dosis 10,5 – 10,8 Gy, a todo el abdomen.
Cuando el tumor es mayor de 3 cm de diámetro y hay enfermedad residual, se puede dar una sobredosis adicional de 10,8 Gy para una dosis total acumulada de 21,6 Gy.
Estado IV de histología favorable
Tumor de Wilms estado IV con estado clínico I – II del riñón comprometido, solo radioterapia al lecho tumoral.
Dosis por fracción de 1,5 – 1,8 Gy, 5 días a la semana.
Dosis total 10,5 – 10,8 Gy al lecho tumoral.
Posteriormente de dará una sobredosis de 10,8 Gy para tumores mayores de 3 cm de diámetro, para una dosis total acumulada de 21,6 Gy.
Tumor de Wilms estado IV con estado clínico III del riñón comprometido: Se da radioterapia abdominal total.
Dosis por fracción 1,5 – 1,8 Gy, 5 días a la semana.
Dosis 10,5 – 10,8 Gy, a todo el abdomen.
De la misma manera Dosis adicional al lecho tumoral, para tumor residual mayor de 3 cm de diámetro: 10,5 – 10,8 Gy.
Estado IV con metástasis pulmonares
Campo pulmonar, técnica AP-PA. Dosis de 1,2 a 1,5 Gy por fracción, 5 días a la semana y un refuerzo al sitio local de enfermedad residual pulmonar hasta completar una dosis total acumulada de 30 Gy, si el volumen pulmonar lo permite.
La radioterapia también se utiliza para paliación de dolor, sangrado o procesos obstructivos secundarios a compromiso metastásico de otros órganos.
Pacientes con tumor anaplásico
Estado I no radioterapia postoperatoria.
Estado II, III igual que histología favorable estado III.
Y Estado IV igual que histología favorable estado IV.
Tumor de Wilms bilateral (Estado V)
Indicaciones para Radioterapia. Depende de los hallazgos quirúrgicos y se procederá de acuerdo con el estado, así:
Estado III histología favorable.
Estado II – III de tumor anaplásico.
Y Estado I – III de sarcoma de células claras y tumor rabdoide.
Cuando no se ha logrado la resección completa del tumor, aún con quimioterapia preoperatoria y una o dos cirugías: la radioterapia a dosis bajas 1,2 – 1,6 Gy puede producir citorreducción.
Sarcoma de Células Claras: Para menores de 6 meses de edad
Es necesario solicitar segunda opinión (Centros de referencia)
Estado I – III Igual que histología favorable estado III.
Estado IV Igual que histología favorable estado IV.
Tumor rabdoide renal
Estado I – II. No radioterapia abdominal
Estado III. Si al tiempo de la evaluación, en la semana 6 después del diagnóstico, en niños mayores de 6 meses de edad, hay evidencia radiológica de enfermedad residual, se dará radioterapia al lecho tumoral y otros sitios infradiafragmáticos necesarios. Todos los pacientes recibirán 10,8 Gy.
Estado IV. Aquellos con estado III del riñón comprometido, recibirán radioterapia si al tiempo de la evaluación de la enfermedad en la semana 6 hay evidencia radiológica de enfermedad residual.
Seguimiento
Estado I, II, III
Los pacientes deben ser examinados cada 3 meses por 5 veces, luego cada 6 meses por 2 veces y después anualmente.
Exámenes después de completar el tratamiento:
Examen físico con determinación de tensión arterial, cuadro hemático, TGP, fosfatasa alcalina, bilirrubina, creatinina, parcial de orina en cada control.
Evaluación por imágenes
Radiografía de tórax cada 3 meses por cinco veces; cada 6 meses por 3 veces, anualmente por 2 veces.
Ecografía abdominal:
Estado I (menor de 24 meses, tumor menor de 550 gr), cada 3 meses por 8 veces, cada 6 meses por 2 veces. Para evaluar el riñón contralateral el lecho tumoral, el hígado y otros sitios intraabdominales.
Estado I (niño mayor de 24 meses o tumor mayor de 550 gr), ecografía abdominal por tres años. Para evaluar el riñón contralateral, el lecho quirúrgico e hígado y otros sitios intraabdominales.
Estado II Ecografía abdominal anualmente, durante los primeros 3 años.
Estado III Ecografía abdominal cada 3 meses, por 5 veces. Luego cada 6 meses por 3 veces, y después cada año por 2 veces.
Estado IV: (Metástasis pulmonares)
Radiografía de tórax cada 3 meses por 5 veces, luego cada 6 meses por 3 veces y después anualmente por 2 veces. Ecografía abdominal cada 3 meses por 10 veces, luego cada 6 meses por 5 veces.
Estado V bajar Radiografía de tórax cada 3 meses por 5 veces, luego cada 6 meses por 2 veces y después anualmente por 2 veces. Ultrasonido abdominal cada 3 meses por 10 veces, luego cada 6 meses por 5 veces y después cada año por 5 veces.
Lecturas Recomendadas
- 1. FARIA P, BECKWITH JB, MISHRA K, ET AL. Focal versus diffuse anaplasia in Wilms tumor-new definitions with prognostic significance. A report form the National Wilms Tumor Study Group. Am J Surg Pathol 20:909, 1996.
- 2. GREEN DM, COPPES MJ, BRESLOW NE ET AL. Wilms’ Tumor. In: Pizzo PA, Poplack DG. (eds.) Principles and Practice of Pediatric Oncology. Philadelphia, Lippincott Raven, 1997.
- 3. GREEN DM, FERNBACH DJ, NORKOOL P, ET AL. The treatment of Wilms tumor patients with pulmonary metastases detected only with computed tomography: A report from the national Wilms’ tumor study. J Clin Oncol 9:1776, 1991.
- 4. HALPERIN EC, CONSTINE LS, TARBEL NJ, ET AL. In: Pediatric Radiation Oncology. Philadelphia, Lippincott– Raven, Williams & Wilkins, 343, 1999.