6.8 Síndrome de abstinencia neonatal a drogas de abuso
Marie Claire Berrouet Mejía. Médico Especialista en Toxicología Clínica Hospital General de Medellín Toxicóloga Clínica, Clínica Soma Medellín Docente de Farmacología y Toxicología Universidad CES, Medellín Miembro de la Asociación de Toxicología Clínica Colombiana – ATCC–
Ubier Eduardo Gómez. Calzada Médico Especialista en Toxicología Clínica Docente de Farmacología y Toxicología Universidad de Antioquia, Medellín Toxicólogo de Planta Hospital San Vicente Fundación de Medellín Miembro de la Asociación de Toxicología Clínica Colombiana – ATCC–
Diana Marcela Pava Garzón. Médico Línea Nacional de Toxicología Ministerio de Salud y Protección Social Miembro Grupo de Investigación sustancias psicoactivas Universidad Nacional de Colombia
Generalidades
El uso recreativo de las sustancias psicoactivas se convirtió en un problema de salud pública1. Es llamativo los pocos reportes del problema de las drogodependencias en una población especial como las gestantes, entendiendo los riesgos asociados para el binomio madre – feto2,3,4.
En Estados Unidos, para el año 2010, se encuentra que hasta el 92 % de las mujeres consumidoras se encontraban en edad reproductiva, 4,4 % de las mujeres en embarazo habían usado alguna sustancia nociva (tabaco 16,4 %, marihuana 11 %, alcohol 10,8 % y cocaína 1,1 %)5.
Según el “Informe Mundial sobre las Drogas” del 2015, emitido por la Oficina de las Naciones Unidas Contra la Droga y el Delito (UNODC), se estima que alrededor de 246 millones de personas, es decir 1 de cada 20 personas entre los 15 y 64 años, consumieron drogas ilícitas en el año 20136. Entendiendo que las mujeres en edad reproductiva están en este rango de edad es importante que el medico sospeche esta complicación en el neonato, reconozca los síntomas y que tanto la gestante consumidora como el neonato sean valorados por toxicología clínica y las otras especialidades pertinentes1-6.
Con el síndrome de abstinencia neonatal (SAN) se ha evidenciado un gran aumento en su incidencia en los últimos años10 en Estados Unidos la enfermedad aumento entre los años 2000 y 2009, puesto que pasó de 1,2 por cada 1000 nacimientos a 3,39 por cada 1000 nacimientos intrahospitalarios; esto causado en gran medida por un aumento en la prescripción de opioides de manera indiscriminada7. Para el año 2013, el 4% de los pacientes hospitalizados en unidad de cuidados intensivos neonatal (UCIN), era por causa de SAN12. Este tema ha causado gran preocupación en este país, llegándose incluso a hablar de una epidemia7,8.
Con relación a la epidemiologia del Síndrome de Abstinencia Neonatal en Colombia:
Preocupa el hecho de que los reportes son insuficientes, datos hasta la fecha proviene del Observatorio de Drogas de Colombia, con registro de mujeres gestantes en SUICAD por sustancia consumida -2011-2016 con un total de 80 casos, lo cual evidencia un amplio subregistro con respecto al tema y la necesidad de contar con estadísticas más amplias en nuestro país donde se muestren datos sobre el tema; sin embargo, según el estudio nacional de sustancias psicoactivas del 2013, se puede inferir que existe un factor de riesgo para el desarrollo de SAN13.
La fisiopatología exacta del síndrome de abstinencia neonatal, aún no está claramente comprendida puesto que muchos factores intervienen en la evolución del síndrome14. Entre ellos se destacan la gran variedad de sustancias abusadas licitas como ilícitas; entre ellas las bebidas alcohólicas, opiáceos, cocaína, cannabis, benzodiacepinas, fenieltilaminas inhalables, cafeína entre otros14,15 y sus diferentes propiedades químicas14,15.
Para entender la fisiopatología del SAN, es necesario tener en cuenta la capacidad de las diferentes sustancias al cruzar la barrera placentaria. Donde encuentran transportadores, bombas y diferentes enzimas de la familia de la citocromo P450, siendo las más importantes la CYP1, CYP2,CYP3 las cuales participan en la fase uno del metabolsimo en las reacciones REDOX , y de la fase dos del metabolismo se destacan: glutatión S transferasa, sulfotransfersas, epoxidohidrolasas y N-acetiltransferasa16,17. Dentro de los transportadores se resaltan los transportadores de serotonina y noradrenalina puesto están encargados de regular la concentración de monoaminas y al ser blancos de drogas de abuso explican algunos efectos adversos asociados a sustancias como cocaína y anfetaminas16,17,18.
Toxicocinética y toxicodinámica
En términos generales al suspender abruptamente la sustancia consumida por la madre hay desregulación de diferentes sistemas de neurotransmisores como dopamina, serotonina, acetilcolina y noradrenalina. El SAN está más estudiado con los opioides; pero debido al policonsumo son muchas las sustancias a las que se expone el feto hijo de madre consumidora, llevando a alteraciones en el sueño, irritabilidad, ansiedad, hiperfagia, alteraciones autonómicas, temblor y convulsiones entre otros. Dentro de los factores protectores para el SAN está el hecho de ser pretérmino entendiendo que hay menor tiempo de exposición, menos paso por barrera placentaria y los receptores están inmaduros.
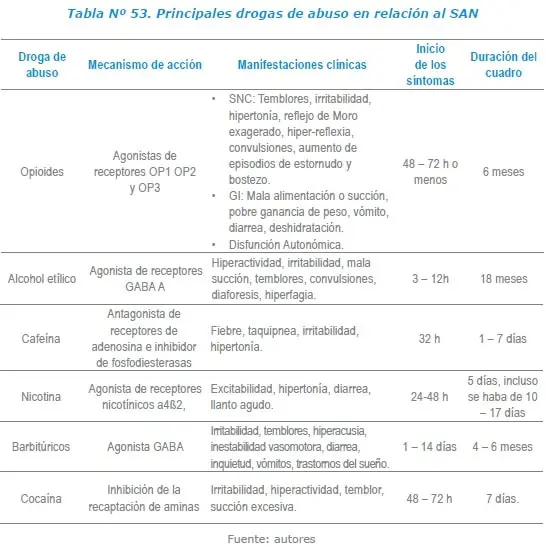
A continuación se explicará brevemente las alteraciones que se pueden ver con los diferentes grupos de sustancias, sin embargo como se puede observar es difícil diferenciar y en términos generales se puede afirmar que hay riesgos neurológicos, autonómicos, metabólicos, hidroelectrolíticos y gastrointestinales dentro de los que están: movimientos anormales, convulsiones, irritabilidad, vómito, hiperactividad adrenérgica, alteraciones en la alimentación, alteraciones en la ganancia de peso y alteraciones en el tono muscular20,21,22.
Opioides
Son compuestos lipofílicos, característica que les permite una buena absorción y un paso rápido por membranas biológicas20. Sus efectos clínicos son explicados por el agonismo de receptores opioides, OP1 (delta), OP2 (kappa), y OP3 (mu)19,20. Los principales cambios celulares por el agonismo de receptores son:
reducción en la producción de Adenosin Monofosfato Cíclico (AMPc) encargado de catalizar la fosforilación de varios substratos proteicos como los canales iónicos, produciendo un estado de hiperpolarización celular20, 21.
En embarazo es importante destacar que la heroína puede acumularse en líquido amniótico, y por la falta de mecanismos de biotransformación explica el alto riesgo de abstinencia para el neonato. La abstinencia en el recién nacido se caracteriza por hiperactividad adrenérgica, temblor, vómito e irritabilidad22.
Los síntomas se pueden presentar en las primeras dos semanas, pero son más frecuentes entre el tercer y cuarto día, por lo tanto, la vigilancia debe ser muy estrecha en los hijos de madres consumidoras, adicionalmente debe evitarse la lactancia por el riesgo de empeorar los síntomas, con respecto al síndrome de abstinencia a los opioides es importante reconocer la vida media de cada una de ellos 22.
Alcohol y otras sustancias lícitas
Se ha asociado el alcohol etílico al síndrome alcohólico fetal, constituido por retraso del crecimiento extra e intrauterino; alteraciones del sistema nervioso central (retraso mental, irritabilidad disminución del tono muscular), anomalías craneofaciales (macro, micro o hidrocefalia, etc.) y otras malformaciones congénitas, especialmente a nivel cardíaco y en menor grado en genitales y aparato urinario. El síndrome de abstinencia se puede evidenciar en las primeras 24 horas de vida, con temblores, irritabilidad, hipertonía, hiperventilación, movimientos anormales y convulsiones23,24,25,26.
Benzodiacepinas (BZD) y otros hipnosedantes, se asocian a manifestaciones similares a los opioides, también se han reportado manifestaciones musculares como hipotonía (Floppy baby)26,27.
La abstinencia a nicotina en el neonato también se ha reportado con irritabilidad hipertonía, diarrea, llanto agudo y puede parecer en las primeras 48 horas 28.
Con respecto a otros estimulantes como la cafeína en la literatura se han descrito pocos casos de SAN por cafeína u otras metilxantinas, sin embargo, es una etiología probable y se debe sospechar sobretodo en gestantes con consumos iguales o superiores a 450mg/día en gestación pues esto favorece el paso placentario de esta, y el síndrome de abstinencia al igual que el de otros estimulantes se caracteriza por fiebre, taquipnea, irritabilidad, hipertonía29,30,31.
Algunos estudios han mostrado que el tabaquismo se asocia a mayor frecuencia de abortos, restricción del crecimiento y parto pre-término, aumentando la morbilidad para el recién nacido. Con respecto al síndrome de abstinencia, se caracteriza por irritabilidad, hipertonía, diarrea, llanto agudo y puede aparecer en las primeras 48 horas32,33,34.
Cocaína
Los mecanismos de toxicidad del clorhidrato de cocaína, y sus derivados se explican por la estimulación de los receptores adrenérgicos α y β, y la inhibición de la recaptación de aminas. El consumo de cocaína en embarazo se asocia a crisis hipertensivas, perdidas fetales, parto pre término y al nacimiento se han reportado mayor frecuencia de signos y síntomas como irritabilidad, temblor, succión excesiva e inestabilidad en las primeras 72 horas35.
Marihuana
El mecanismo de acción es explicado por su acción en receptores endocanabinoides como CB1 y CB2. Luego del nacimiento, el SAN se caracteriza por temblor e irritabilidad; en la primera infancia se han hecho asociaciones con irritabilidad, déficit de atención, alteraciones en la memoria y gastrosquisis (es un tipo de defecto en la pared abdominal, en el cual los intestinos y otros órganos se desarrollan fuera del abdomen del feto, a través de una apertura de la pared abdominal, casi siempre a la derecha del cordón umbilical). Es uno de los SAN que más frecuentemente se pueden pasar por alto debido a que la vida media del alcaloide es prolongada y sus manifestaciones clínicas pueden tardar en aparecer36,37,38.
Drogas de síntesis
Entre las cuales de destacan las feniletilaminas, los estimulantes de tipo anfetaminico, anfetaminas metanfetaminas, metilendoximetanfetamina 2CB (4-bromo-2,5-dimetoxianfetamina), DOB (4-Bromo-2,5-dimetoxifenil aminopropano ) y catinonas23. El mecanismo de acción de estas sustancias es explicado por la inhibición en la recaptación de serotonina23 y el agonismo de receptores de serotonina como: 5HT1A, 5HT2A, 5HT2C 23. Las complicaciones más reportadas son: parto pre-término, restricción del crecimiento intrauterino, disminución del perímetro cefálico, anomalías congénitas y síndrome de abstinencia el cual es caracterizado por temblor, alteraciones en el sueño, llanto excesivo y pobre alimentación22,25,39.
El evento fisiopatológico que explica el SAN a diferentes drogas es la suspensión abrupta del estímulo. Cuando el médico se enfrenta ante un posible caso de SAN, es necesario tener en consideración un nexo epidemiológico y la clínica soportado, por ciertos paraclínicos como lo son los tóxicos en matriz orina en periodo de ventana según si es consumo crónico o agudo40. Es importante sospechar el SAN cuando hay una historia clínica donde se incluya dentro de los antecedentes maternos el consumo de sustancias psicoactivas, ausencia o bajo número de controles prenatales, y en el examen físico que evidencie alteraciones como microcefalia, irritabilidad entre otros41.
Aunque específicamente no se incluyen dentro del SAN los hijos de madres con alteraciones del afecto a quienes se les está administrando antidepresivos tricíclicos, inhibidores selectivos de la recaptación de serotonina (ISRS), duales o atípicos, al ser suspendidos de manera abrupta pueden presentar un conjunto de signos y síntomas similares a un índrome de abstinencia; en los adultos específicamente para los ISRS a este conjunto de signos y síntomas se le denomina descontinuación, en los neonatos se puede observar temblor, mioclonias e irritabilidad.
(Lea También: Abuso de Anfetaminas)
Abordaje y diagnóstico clínico
Es importante el realizar un examen físico neonatal detallado a nivel neurológico en un ambiente tranquilo, y con factores externos adecuados como temperatura.
Cuando el medico se enfrenta ante un posible caso de SAN, es necesario tener en consideración un nexo epidemiológico y la clínica soportado, por ciertos paraclínicos como positividad de tóxicos en orina.
Se considera caso sospechoso cuando hay una historia clínica donde se incluya dentro de los antecedentes personales maternos consumo drogas, población vulnerable y ausencia de controles prenatales, aquellas que tengan signos de abstinencia o que reclaman medicamento con potencial adictivo frecuentemente y a mayores dosis de lo usual como por ejemplo el caso de los opioides y hallazgos clínicos del paciente como los mencionados anteriormente.
Con respecto a los paraclínicos, se utiliza un análisis de la orina o de meconio, siendo en nuestro país más utilizadas las pruebas semicuantitativas en orina para la madre y para el recién nacido.
Para valorar la severidad del SAN, existen diversas escalas como la Finnegan Modificada (escala MOTHER NAS), Neonatal Withdraw Inventory (NWI), the Lipsitz Neonatal Drug-Withdrawal Scoring System, entre muchas otras. Sin embargo, éstas tienen limitaciones, pues están diseñadas para abstinencias por opioides y en neonatos a término, excluyendo otro tipo de sustancias o prematuros. Los puntos en común que evalúan fundamentalmente son: irritabilidad, cambios en la alimentación, temblor y tono muscular43.
Los objetivos del tratamiento de SAN son dos principalmente:
- Restaurar las actividades del neonato (alimentación, sueño, ganancia de peso)
- Prevenir complicaciones asociado a SAN.
Es importante resaltar que lo ideal sería prevenir los casos del SAN, sin embargo, para esto es importante brindar asesoría preconcepcional en mujeres consumidoras, y un acompañamiento interdisciplinario de la gestación que incluya obstetra, toxicólogo y psiquiatra si es del caso.
Además se debe tener en cuenta que el síndrome de abstinencia no tiene como única etiología el ser hijo de madre consumidora y los niños en unidades de cuidados especiales con uso prolongado de sedoanalgesia (benzodiacepinas y opioides) desarrollan tolerancia y abstinencia. Algunos autores plantean frecuencias de hasta un 60%; otros plantean que hay dosis acumuladas de riesgo y por supuesto a mayor tiempo, mayor es la posibilidad de un síndrome de abstinencia y nuevamente la triada de signos y síntomas más frecuentes son alteraciones neurológicas y autonómicas en el SNC.

Como la escala Finnegan solo se debe utilizar en los dos o tres primeros meses, para los mayores se puede utilizar la escala Sophia (Observation Withdrawal Symptoms-scale) donde se evalúan 15 parámetros tiene una sensibilidad del 83% y una especificidad del 93% para un punto de corte igual o superior a 4.
Los signos y síntomas que evalúa son: taquicardia (>15% fc basal), taquipnea (> 15% fr basal), fiebre > 38’4ºc, sudoración, agitación, ansiedad, temblores, movimientos anormales, hipertonía, llanto inconsolable, gestos de malestar, insomnio alucinaciones, vómitos, diarrea44.
Los anexos Nº 3 y 4 incluyen diferentes tablas que sirven para evaluar la severidad del síndrome de abstinencia y definir la necesidad de medicación.
Guías de manejo de la Academia Americana de Pediatría (AAP)
Tratamiento
Como se planteó anteriormente la prevención es importante y es fundamental la asesoría preconcepcional donde se cuente con el acompañamiento de toxicología para las madres consumidoras. En los neonatos que desarrollan el SAN es importante el manejo (idealmente) en un nivel de atención de alta complejidad con un equipo multidisciplinario que cuente con pediatría, neonatología y toxicología. En el manejo hay dos pilares: las medidas no farmacológicas y las farmacológicas.
Dentro de las no farmacológicas están: evitar la irritabilidad, ubicar en área tranquila ligera/oscura, arropar, pañales confortables, arrullo, cargarlo, mecer, chupo para los de “succión excesiva”, posición anti-reflujo. Fórmulas hipercalóricas, la lactancia ha sido muy discutida, pero se plantea en madres que están estables con el tratamiento de metadona y buprenorfina.
Con respecto al tratamiento farmacológico del SAN por opioides la elección es la morfina y la metadona; son los agentes farmacológicos más usados.
La morfina se administra según el índice de severidad, desde 0.03-0.1mg/kg cada 6 horas con dosis máxima de 0.2mg/kg. Al hacer la disminución se recomienda 10-20% cada tres días vigilando la respuesta con escalas de severidad.
Con la metadona las dosis van desde 0.05mg/kg hasta 0.2mg/kg cada 6 horas idealmente debe ser con una formulación liquida y al realizar la dilución debe ser con especial cuidado pues por su vida media larga hay riesgo de depresión respiratoria. La dilución se puede hacer en agua destilada o solución salina al 0.9% hasta conseguir una puntuación menor o igual a 8. A partir de allí se inicia el descenso, aunque no está establecido el tiempo se sugiere 10-20% cada 5 días en caso de metadona.
En caso de niños que requirieron manejo con fentanilo es necesario tener en consideración la equivalencia de los opioides y la vida media de estos para la disminución de la dosis y el cambio de moléculas43,44,45,46.
El fenobarbital y la clonidina son terapias coadyuvantes, cuando se requieren dosis altas de opioides; así mismo, es importante resaltar que en el SAN no causado por opioides sino por otras sustancias (cocaína THC) sería la primera línea la clonidina y se administra dosis de 1-4 μg/K cada 6- 12 horas. Es importante recordar que necesita de suspensión lenta por el riesgo de hipertensión refractaria47,48.
El fenobarbital se usa por su efecto gabamimético en este síndrome, para el tratamiento del SAN por opioides y en otras drogas en las cuales el SAN presente un riesgo neurológico su dosis es de 6mg/ kg/dia47.
Los alfa dos agonistas son útiles ya que no sólo se asocian a sedación sino que disminuyen la hiperactividad adrenérgica, el aprobado por la FDA es la clonidina, sin embargo cada vez hay más estudios con dexmedetomidina que tiene más especificidad que la clonidina, y efectos simpaticolíticos, sedativos y analgésicos en dosis entre 10-300 μ/kg, sin embargo en nuestro país no tiene aún indicación INVIMA con estos fines49,50.
Referencias
- 1. Informe Mundial sobre las Drogas 2014. Disponible en: http://www.unodc.org/
- 2. Vélez M, Jansson L. Drogas y embarazo. Capítulo 58 en: Velásquez de P E, Olaya A, Castaño G, Castro S. Adicciones aspectos clínicos y psicosociales, tratamiento y prevención. Primera edición Editorial CIB. pa. 601-608
- 3. Vélez M, Jansson L. exposición prenatal a drogas: efectos en el niño y adolescente. Capítulo 59 en: Velásquez de P E, Olaya A, Castaño G, Castro S. Adicciones aspectos clínicos y psicosociales, tratamiento y prevención. Primera edición Editorial CIB.pag. 611-619.
- 4. Prouillac C, Lecoeur S. The role of the placenta in fetal exposure to xenobiotics: importance of membrane transporters and human models for transfer studies. Drug Metab Dispos. 2010 Oct; 38(10):1623–35.
- 5. Wendell AD. Overview and epidemiology of substance abuse in pregnancy. Clin Obstet Gynecol. 2013 Mar; 56(1):91-6.
- 6. Oficina de las Naciones Unidas contra la Droga y el Delito. Informe mundial sobre las drogas 2015 disponible en: https://www.unodc.org/documents/mexicoandcentralamerica/eventos/2015/WDD2015/ WDR15_ExSum_S.pdf
- 7. Hall ES, Wexelblatt SL, Crowley M, Grow JL, Jasin LR, Klebanoff MA, et al. Implementation of a Neonatal Abstinence Syndrome Weaning Protocol: A Multicenter Cohort Study. Pediatrics. 1 de octubre de 2015; 136(4): e803-10.
- 8. Hayes MJ, Brown MS. EPidemic of prescription opiate abuse and neonatal abstinence. JAMA. 9 de mayo de 2012; 307(18):1974-5.
- 12. Tolia VN, Patrick SW, Bennett MM, Murthy K, Sousa J, Smith PB, et al. Increasing Incidence of the Neonatal Abstinence Syndrome in U.S. Neonatal ICUs. N Engl J Med. 28 de mayo de 2015; 372(22): 2118-26.
- 13. Ministerio de Justicia y del Derecho, Observatorio de Drogas de Colombia. Reporte de Drogas de Colombia [Internet]. Bogotá, Colombia; 2015 nov [citado 25 de marzo de 2016] p. 223. Disponible en: http://www.odc.gov.co/Portals/1/publicaciones/pdf/odc-libro-blanco/OD0100311215_reporte_de_drogas_de_colombia.pdf
- 14. Kocherlakota P. Neonatal Abstinence Syndrome. Pediatrics. 1 de agosto de 2014;134(2): e547-61. Dipsonible en: http://pediatrics.aappublications.org/content/134/2/e547.
- 15. Solís Sánchez G, Sánchez S, L J, Díaz González T. Exposición prenatal a drogas y efectos en el neonato. Trastor Adict. 1 de octubre de 2001; 3(4):256-62.
- 16. Nishimura M, Yaguti H, Yoshitsugu H, Naito S, Satoh T. Tissue distribution of mRNA expression of human cytochrome P450 isoforms assessed by high-sensitivity real-time reverse transcription PCR. Yakugaku Zasshi. 2003 May; 123(5):369–75.
- 17. Šlamberová R. Drugs in pregnancy: the effects on mother and her progeny. Physiol Res. 2012; 61 Suppl 1: S123–135.
- 18. Behnke M, Smith VC, Committee on Substance Abuse, Committee on Fetus and Newborn. Prenatal substance abuse: short- and long-term effects on the exposed fetus. Pediatrics. 2013 Mar; 131(3): e1009–1024.
- 19. Sivasubramaniam SD, Finch CC, Billett MA, Baker PN, Billett EE. Monoamine oxidase expression and activity in human placentae from pre-eclamptic and normotensive pregnancies. Placenta. 2002 Mar; 23(2-3):163–71
- 20. Berrouet Mejia MC. Intoxicación por Opioides. En: El Paciente Urgente. Medellín, Colombia. CIB. p. 619-31.
- 21. Fujita W, Gomes I, Devi LA. Heteromers of μ-δ opioid receptors: new pharmacology and novel therapeutic possibilities. Br J Pharmacol. Enero de 2015; 172(2):375-87.
- 22. Lindsay MK, Burnett E. The use of narcotics and street drugs during pregnancy. Clin Obstet Gynecol. 2013; 56(1):133–141.
- 23. Lorenzo Fernández P. Drogodependencias: farmacología, patología, psicología, legislación. Buenos Aires; Madrid: Panamericana; 2009.
- 24. Streissguth AP, Bookstein FL, Barr HM, Sampson PD, O’Malley K, Young JK. Risk factors for adverse life outcomes in fetal alcohol syndrome and fetal alcohol effects. J Dev Behav Pediatr. 2004; 25(4):228–238.
- 25. Behnke M, Smith VC, Committee onSubstance Abuse, Committee on Fetus and Newborn. Prenatal Substance Abuse: Short- and Long-term Effects on the Exposed Fetus. Pediatrics. 1 de marzo de 2013; 131(3): e1009-24.
- 26. Solís Sánchez G, Sánchez S, L J, Díaz González T. Exposición prenatal a drogas y efectos en el neonato. Trastor Adict. :256-62.
- 27. Igarashi M. Floppy infant syndrome. J Clin Neuromuscul Dis. Diciembre de 2004;6(2):69-90.
- 28. Wikner BN, Stiller C-O, Bergman U, Asker C, Källén B. Use of benzodiazepines and benzodiazepine receptor agonists during pregnancy: neonatal outcome and congenital malformations. Pharmacoepidemiol Drug Saf. noviembre de 2007; 16(11):1203-10.
- 29. Jarosz M, Wierzejska R, Siuba M. Maternal caffeine intake and its effect on pregnancy outcomes. Eur J Obstet Gynecol Reprod Biol. febrero de 2012; 160(2):156-60.
- 30. Montes Bentura D, La Orden Izquierdo E, Álvarez Fernández B, Garín Fernández N, Ortiz Movilla R, Muro Brussi M. Síndrome de abstinencia neonatal debido a consumo materno excesivo de cafeína. An Pediatría. 1 de marzo de 2009; 70(3):300-1.
- 31. Martín I, López-Vílchez MA, Mur A, García-Algar O, Rossi S, Marchei E, et al. Neonatal withdrawal syndrome after chronic maternal drinking of mate. Ther Drug Monit. febrero de 2007; 29(1):127-9.
- 32. Samet JM. Los riesgos del tabaquismo activo y pasivo. Salud Pública México. 2002; 44: s144–s160.
- 33. Mund M, Louwen F, Klingelhoefer D, Gerber A. Smoking and Pregnancy — A Review on the First Major Environmental Risk Factor of the Unborn. Int J Environ Res Public Health. diciembre de 2013; 10(12):6485-99.
- 34. Benowitz NL, Gourlay SG. Cardiovascular toxicity of nicotine: implications for nicotine replacement therapy. J Am Coll Cardiol. junio de 1997; 29(7):1422-31.
- 35. Bustamante JFM, Mejía MCB. Cocaína y estado convulsivo. Rev CES Med. 2012; 26(2):215–221.
- 36. Minnes S, Min MO, Singer LT, Edguer M, Wu M, Thi P. Cocaine use during pregnancy and health outcome after 10 years. Drug Alcohol Depend. 1 de noviembre de 2012; 126(1-2):71-9.
- 37. Toledo E, Eugenia I, Mejía B, Claire M, Ramírez G, Mauricio D. Molecular Mechanism of Addiction to Marihuana. Rev Colomb Psiquiatr. marzo de 2009; 38(1):126-42.
- 38. Brown HL, Graves CR. Smoking and marijuana use in pregnancy. Clin Obstet Gynecol. marzo de 2013; 56(1):107-13.
- 39. Bolea-Alamanac BM, Green A, Verma G, Maxwell P, Davies SJC. Methylphenidate use in pregnancy and lactation: a systematic review of evidence. Br J Clin Pharmacol. enero de 2014; 77(1):96-101.
- 40. Lazic-Mitrovic T, Mikovic Z, Mandic V, Hajnal-Avramovic L, Cecez D, Stanimirovic A, et al. Neonatal abstinence syndrome: Diagnostic dilemmas in the maternity ward. Srp Arh Celok Lek. 2015; 143(9-10):573-7.
- 41. Barrero Virguetti MH, Escalera Solis C. Síndrome de abstinencia neonatal. Rev Médica Cochabamba. 2008; 19:54.
- 42. Salazar L, Rincon D, Uso de los antidepresivos en el embarzo y la lactancia. Universitas Médica 2006 vol. 47 disponible en: http://med.javeriana.edu.co/publi/vniversitas/serial/v47n2/7%20Uso%20de%20los%20antidrepresivos
- 43. Siu A, Robinson CA. Neonatal abstinence syndrome: essentials for the practitioner. J Pediatr Pharmacol Ther. 2014; 19(3):147–155.
- 44. Monitorizacion de analgesia y sedación. Protocolo de sedonalgesia SECIP
- 45. Brown MS, Hayes MJ, Thornton LM. Methadone versus morphine for treatment of neonatal abstinence syndrome: a prospective randomized clinical trial. J Perinatol Off J Calif Perinat Assoc. abril de 2015; 35(4):278-83.
- 46. Young ME, Hager SJ, Spurlock D. Retrospective chart review comparing morphine and methadone in neonates treated for neonatal abstinence syndrome. Am J Health-Syst Pharm AJHP Off J Am Soc Health-Syst Pharm. 1 de diciembre de 2015; 72(23 Suppl 3):S162-167
- 47. Hall ES, Wexelblatt SL, Crowley M, Grow JL, Jasin LR, Klebanoff MA, et al. A Multicenter Cohort Study of Treatments and Hospital Outcomes in Neonatal Abstinence Syndrome. Pediatrics. 1 de agosto de 2014; 134(2):e527-34.
- 48. Streetz VN, Gildon BL, Thompson DF. The Role of Clonidine in Neonatal Abstinence Syndrome A Systematic Review. Ann Pharmacother. 18 de enero de 2016;1060028015626438.
- 49. Rayner SG, Weinert CR, Peng H, Jepsen S, Broccard AF, Study Institution. Dexmedetomidine as adjunct treatment for severe alcohol withdrawal in the ICU. Ann Intensive Care. 23 de mayo de 2012; 2(1):12.
- 50. Whalen LD, Di Gennaro JL, Irby GA, Yanay O, Zimmerman JJ. Long-Term Dexmedetomidine Use and Safety Profile Among Critically Ill Children and Neonates*: Pediatr Crit Care Med. octubre de 2014; 15(8):706-14.