10.5 Preguntas de antecedentes
El GD desarrolló preguntas de antecedentes en relación con la gestión de sangre del paciente neonatal y pediátrico. Los puntos clave en relación con los pacientes neonatales y pediátricos son:
- Su composición corporal y fisiología cambiantes relacionadas con el desarrollo y el crecimiento. Lo que significa que los riesgos y beneficios para esta población pueden diferir de los que se aplican a los pacientes adultos
- El potencial de tener consecuencias para toda la vida por los tratamientos dados durante la infancia y la niñez
- Ciertos trastornos que son exclusivos de la infancia y la niñez.
Las preguntas de antecedentes 1 y 3 abordan la vulnerabilidad especial de los pacientes jóvenes. La primera pregunta se refiere a las circunstancias en las que el uso de componentes sanguíneos que se han seleccionado sobre la base de características específicas o que han sido tratados especialmente puede mejorar los desenlaces a corto o largo plazo.
La tercera pregunta se refiere al hecho de que la pérdida de sangre por flebotomía y líneas de muestreo pueden contribuir sustancialmente al riesgo de anemia e incidencia de transfusión en pacientes neonatales y pediátricos que se someten a hospitalización prolongada. Tienen alta severidad de enfermedad o tienen condiciones crónicas. La pregunta explora métodos para minimizar estas pérdidas.
La pregunta de antecedentes 2 se refiere a la transfusión fetal, que fue la primera forma de tratamiento fetal y sigue siendo uno de los más exitosos.
Las preguntas de antecedentes 4 y 6 cubren problemas que se han tratado como preguntas generales o específicas para otros módulos. Pero en los que existen diferencias sustanciales entre adultos y niños que conducen a incertidumbres sobre si la evidencia en adultos puede ser extrapolada. Debido a que hay bajos niveles de evidencia en relación con los niños, estas preguntas se han retomado en este módulo como preguntas de antecedentes.
Los problemas principales son el uso de agentes hemostáticos para prevenir la pérdida de sangre excesiva en pacientes neonatales y pediátricos sometidos a cirugía mayor (pregunta de antecedentes 4), y la necesidad de adaptar para pacientes pediátricos y neonatales el protocolo de transfusión masiva desarrollado en el Módulo 1 (pregunta de antecedentes 6). El protocolo de transfusión masiva ha sido renombrado aquí como un “protocolo de sangrado crítico” para reflejar más exactamente el problema clínico, en lugar de sólo una de las modalidades utilizadas para abordarla.
Los infantes y los niños tienen factores de riesgo específicos para la ADH. La pregunta de antecedentes 5 explora estos factores de riesgo y proporciona orientación sobre la terapia con hierro.
10.5.1 Selección de componentes sanguíneos
Pregunta de antecedente 1
Para los pacientes fetales, neonatales o pediátricos, ¿la selección de componentes sanguíneos específicos, en comparación con los productos sanguíneos de rutina, mejora los desenlaces?
10.5.1.1 Uso de GR “frescos” en pacientes fetales, neonatales o pediátricos
¿Para los pacientes fetales, neonatales o pediátricos, los GR “frescos” (≤7 días), en comparación con los GR más antiguos, ¿mejoran los desenlaces?
Estudios retrospectivos y prospectivos han planteado preocupaciones tales como que los pacientes que reciben sangre más vieja tienen un aumento de la mortalidad en comparación con los pacientes que reciben las unidades recién almacenadas.
El almacenamiento refrigerado da lugar a una “lesión de almacenamiento”, caracterizada por alteraciones metabólicas, cambios en la forma y reología de los GR, pérdida de carbohidratos de membrana, daño oxidativo a lípidos y proteínas, cambios en la afinidad y entrega del oxígeno. Aumento de la adhesión de los GR a las células endoteliales y reducción de la expectativa de vida (201).
También hay riesgos secundarios como el aumento de las concentraciones de potasio y de plastificante, y desprendimiento de proteínas activas, lípidos y microvesículas (201). Juntos, estos cambios relacionados con el almacenamiento podrían aumentar los riesgos y reducir los beneficios de la transfusión. Pero no está claro si tienen un efecto significativo en los desenlaces clínicos (202).
Las circunstancias en las que las guías han sugerido el uso de GR más frescos son aquellas en las que:
- Los efectos tóxicos pueden ser magnificados por la inmadurez del paciente o por el tamaño, rapidez o frecuencia de la transfusión
Incluso pequeños aumentos en la longevidad de los hematíes transfundidos pueden ser una gran ventaja
No hay pruebas suficientes sobre las cuales basar las recomendaciones más fuertes para el uso de GR “frescos” en pacientes fetales, neonatales o pediátricos.
Sin embargo, las circunstancias en las que se recomiendan los GR “frescos” en las guías anteriores incluyen:
- Transfusión fetal intrauterina (TIU) (203-205)
- Exanguinotransfusión y transfusión de gran volumen en recién nacidos y lactantes menores de un año de edad (e.j. > 25 ml/kg) (206-208).
- Infantes y niños sometidos a cirugía cardíaca mediante CEC
- Pacientes con transfusión crónica (209).
Para los infantes y niños sometidos a cirugía cardíaca con CEC, un estudio retrospectivo informó tasas más bajas de complicaciones mayores en aquellos en los que se utilizó sangre fresca (<4 días de edad) para purgar el circuito de CEC (209-210).
Para los pacientes neonatales sometidos a transfusión complementaria, un ensayo aleatorizado no encontró diferencias en la mortalidad o la disfunción aguda de órganos entre los recién nacidos que recibían GR almacenados durante <7 días (media 5,1 días) y los que recibían GR mayores (14,6 días) (211). En constraste, en estudios observacionales, la transfusión de GR más viejos en pacientes en Unidad de Cuidado Intensivo Pediátrico (UCI) se ha asociado con un aumento de la incidencia de falla multiorgánica y la duración de la estancia de la UCI (212-213).
En el paciente transfundido crónicamente, es deseable maximizar el tiempo de supervivencia in vivo de los GR. Se piensa que, transfiriendo glóbulos rojos nuevos. El GR durará más tiempo, potencialmente extendiendo el intervalo de transfusión (210-211, 214).

(Lea También: Uso de Componentes Sanguíneos Negativos Para Citomegalovirus)
10.5.1.2 Sistema antigénico de Kell
Los anticuerpos contra antígenos del grupo sanguíneo Kell (K) pueden causar reacciones transfusionales severas y la enfermedad hemolítica del feto y del recién nacido. Los anticuerpos anti-K se desarrollan como resultado de transfusiones de sangre (50-88% de sensibilizaciones) o durante el embarazo (215-216).
Evitar la sensibilización K relacionada con la transfusión de mujeres y niñas que pueden tener hijos es una prioridad importante. Siempre que sea posible. Se deben seleccionar GR K negativos para transfundir a todas las mujeres con potencial fertil que sean K negativas o cuyo estado de antígeno K no pueda determinarse antes de la transfusión.
Para reducir el riesgo de aloinmunización y las reacciones transfusionales, los pacientes (hombres y mujeres) crónicamente transfundidos (ejemplo: pacientes con hemoglobinopatías o anemia congénita) deben tener un fenotipo extendido (e.j. Rh, K, Kidd, Duffy y Ss) antes de su primera transfusión de GR. Las transfusiones deben ser rutinariamente compatibilizadas para los antígenos K, Rh (D, C, c, E, e) y -donde esté disponible- el fenotipo de GR) (209, 216).

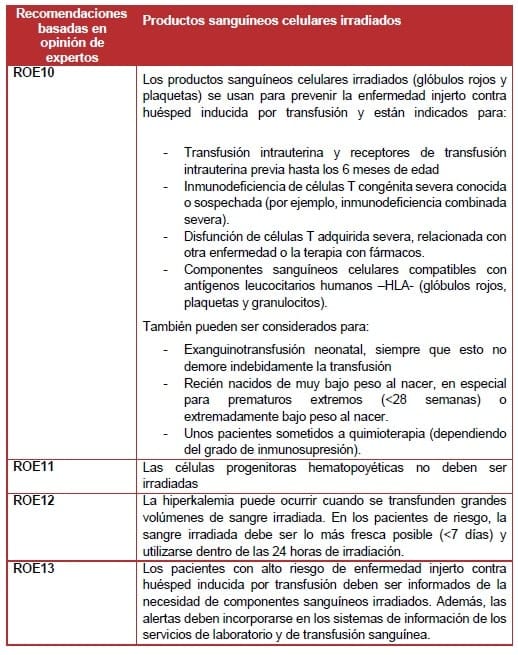
10.5.1.3 Uso de componentes sanguíneos celulares irradiados en recién nacidos y niños
La enfermedad injerta contra huésped asociada a la transfusión – EICH-AT- es una complicación rara y usualmente fatal de la transfusión de componentes sanguíneos celulares. Es causada por la falla en destruir los linfocitos T del donante, que luego proliferan y causan una respuesta inmune. La EICH-AT ocurre en receptores inmunocomprometidos. También puede ocurrir en receptores inmunocompetentes de componentes sanguíneos provenientes de un donante relacionado o HLA compatible.
La EICH-AT se previene usando componentes sanguíneos celulares irradiados (con radiación gamma de 25 Gy), la leucodepleción sola es insuficiente. No es necesario irradiar productos acelulares tales como PFC, crioprecipitado, IgIV, albúmina y concentrados de factor. Las células progenitoras hematopoyéticas no deben ser irradiadas para efectos del trasplante (ver Tabla 4).
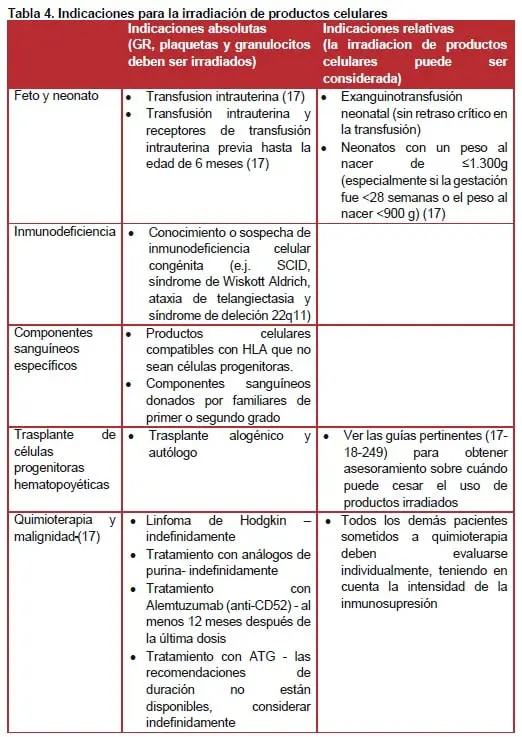
Circunstancias en las que no se requieren componentes sanguíneos irradiados
No se requieren componentes sanguíneos celulares irradiados en:
- Infección por VIH
- Inmunodeficiencia humoral
- Pacientes tratados con Rituximab
- Pacientes sometidos a trasplante de órganos sólidos.
Precauciones relacionadas con el uso de componentes sanguíneos celulares irradiados
La irradiación de los GR utilizados para la transfusión de gran volumen puede aumentar el riesgo de hiperpotasemia. Por lo tanto, el riesgo de EICH-AT debe ser balanceado contra este riesgo. Para minimizar el riesgo de hiperpotasemia en la transfusión de gran volumen. Los hematíes irradiados deben ser tan frescos como sea posible (<7 días de edad) y deben ser transfundidos dentro de las 24 horas de irradiación.