7.5 (Pregunta 5)
En pacientes con patología general, ¿con qué INR (PT/TTPa) para PFC, cuál nivel de fibrinógeno para crioprecipitado y cuál recuento de plaquetas para concentrados plaquetarios, deben transfundirse los pacientes para evitar riesgos de reacciones adversas significativas?
Evidencia
Hay controversia sobre el beneficio del uso de PFC, crioprecipitado y concentrados de plaquetas para mejorar la hemostasia tanto en los entornos procesales como no procedimentales.
En ausencia de evidencia de alta calidad, los clínicos han confiado tradicionalmente en los índices de laboratorio para tomar decisiones acerca de la transfusión de estos productos.
La revisión sistemática consideró los niveles de ‘transfusión-detonante’ de estos diversos índices. Excluyendo los estudios de pacientes con hemorragia masiva o que requirieran reversión de la warfarina.
La pregunta 5 fue originalmente definida como una pregunta de pronóstico. Se esperaba que la mejor evidencia relacionada con esta pregunta proviniera de estudios de cohorte grandes que estratificaban los resultados de acuerdo con los valores de base del INR, el fibrinógeno, y/o el recuento de plaquetas.
Sin embargo, la búsqueda bibliográfica para este módulo identificó una serie de ECA altamente relevantes que compararon diferentes detonantes transfusionales.
Por lo tanto, el GD decidió que esta pregunta se abordaría inicialmente como una pregunta de intervención, y luego como una pregunta de pronóstico si no se encontraba evidencia relevante del ECA.
Se encontró evidencia de alta calidad del ECA para la transfusión de plaquetas. Por lo tanto, esta parte de la pregunta fue tratada como una pregunta de intervención.
En contraste, los estudios relevantes para el uso de crioprecipitado y PFC fueron principalmente estudios de cohorte en los que los pacientes fueron estratificados por los valores de base del INR, PT/TTPa o fibrinógeno.
Por lo tanto, estas partes de la pregunta fueron tratadas como preguntas de pronóstico.
7.5.1 Parámetros de coagulación y transfusión de plasma fresco congelado
El objetivo de la revisión de la literatura fue determinar hasta qué punto la presencia de una elevación en INR/PT o TTPa representa un riesgo en situaciones no procedimentales, y si el nivel elevado debería desencadenar una transfusión de plasma para corregirla.
La revisión encontró varios estudios de cohorte prospectivos relevantes (nivel II) y retrospectivos (nivel III) que se centraron en pacientes en tres situaciones clínicas: enfermedad hepática, leucemia aguda y SCA.
En los pacientes con enfermedad hepática, todos excepto uno de los estudios de cohorte prospectivos incluidos encontraron que la coagulopatía era un factor de riesgo independiente para la mortalidad.
Un estudio identificó la proporción de protrombina de admisión como un predictor independiente de la mortalidad (129); otro encontró que el INR y TTPa sólo se asociaron con la supervivencia en el análisis univariado (130).
La revisión no identificó ningún estudio en pacientes con enfermedad hepática informando si la coagulopatía era un factor de riesgo independiente. Ya sea para los eventos de sangrado o la posterior transfusión de glóbulos rojos.
Aunque estos estudios sugieren una asociación entre los parámetros de la coagulación y la mortalidad. No proporcionan evidencia para seleccionar un umbral apropiado en el que debe ocurrir la transfusión.
Riesgo de hemorragia en la enfermedad hepática
Ninguna de las pruebas de uso común ha demostrado ser confiable como predictor de riesgo de hemorragia en la enfermedad hepática.
Las pruebas convencionales (ej. PT y TTPa) se correlacionan pobremente con el sangrado relacionado con procedimientos en estos pacientes. Ya que los niveles de proteína C, antitrombina y el inhibidor de la vía del factor tisular se reducen en paralelo con factores pro-coagulantes.
Por lo tanto, el equilibrio de pro y anticoagulantes puede ser normal, incluso cuando existe prolongación de PT y TTPa.
Sólo un estudio de cohorte retrospectivo en pacientes con leucemia aguda informó una asociación entre los parámetros de coagulación y la mortalidad (131).
Este estudio demostró que un INR ≥ 1,5 fue un factor de riesgo independiente para la hemorragia intracraneal fatal. Pero el TTPa no lo fue.
Sólo un estudio consideró el riesgo de hemorragia en la leucemia promielocítica aguda en relación con los índices de coagulación (132). Este estudio encontró que el PT ni el TTPa fueron factores de riesgo independientes para la mortalidad.

(Lea También: Transfusión de Glóbulos Rojos en pacientes Crónicamente Transfundidos)
7.5.2 Nivel de fibrinógeno y uso de crioprecipitado o concentrado de fibrinógeno
La hipofibrinogenemia adquirida puede surgir en diversos contextos clínicos.
Estos incluyen enfermedad hepática grave, insuficiencia hepática fulminante, coagulación intravascular diseminada (CID), post-trombólisis, pérdida de sangre masiva y transfusión, y después de terapia con L-asparaginasa para la leucemia linfocítica aguda.
El diagnóstico y manejo específicos de la CID no se han revisado específicamente en la búsqueda de literatura.
Aunque el PFC contiene algún fibrinógeno, la transfusión de crioprecipitado o concentrado de fibrinógeno es el medio más eficiente de reemplazo de fibrinógeno.
Estas intervenciones también pueden estar indicadas en pacientes con afecciones relativamente raras de afibrinogenemia hereditaria o disfibrinogenemia.
La revisión de la literatura excluyó a los pacientes en situaciones perioperatorias y aquellos con pérdida de sangre masiva o transfusión. Ya que estas poblaciones están cubiertas en otros módulos de esta guía.
En los pacientes con enfermedad hepática
La revisión encontró un estudio prospectivo de cohorte (nivel II) que observó a pacientes hospitalizados con cirrosis y empeoramiento de la insuficiencia hepática (130).
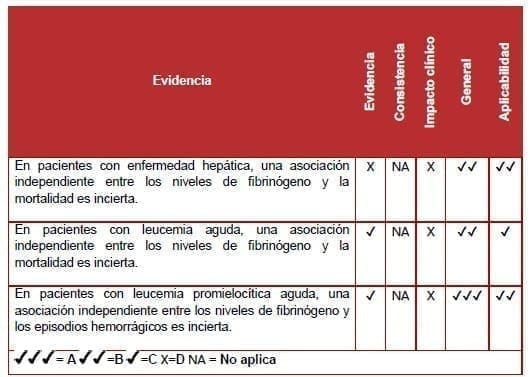
El nivel de fibrinógeno se asoció con supervivencia, pero sólo en el análisis univariado. Sin embargo, debido a la mala calidad de la evidencia, la asociación entre los niveles de fibrinógeno y la mortalidad sigue siendo incierta.
No se encontraron estudios que informaran si el nivel de fibrinógeno es un factor de riesgo independiente para el sangrado o para el riesgo de transfusión de glóbulos rojos en este grupo de pacientes.
Se encontraron dos estudios retrospectivos de cohorte relevantes (nivel III) en pacientes con leucemia aguda.
Un estudio de baja calidad observó a los pacientes que recibían quimioterapia de inducción para la leucemia promielocítica aguda (132).
El nivel de fibrinógeno no fue un factor de riesgo independiente para el sangrado en este contexto.
El otro estudio examinó el riesgo de hemorragia intracraneal fatal en pacientes con leucemia aguda. Pero no encontró asociación significativa entre el nivel de fibrinógeno y la hemorragia intracraneal fatal (131).
No se encontraron estudios de pacientes con leucemia aguda que informaran sobre una asociación entre el nivel de fibrinógeno y el riesgo de transfusión.
7.5.3 Recuento de plaquetas y transfusión profiláctica de plaquetas en pacientes sometidos a quimioterapia y trasplante de células progenitoras hematopoyéticas (CPH)
El uso de transfusiones profilácticas de plaquetas en pacientes que reciben quimioterapia mielosupresora o sometidos a trasplante alogénico de CPH es significativo.
En este contexto clínico -en ausencia de hemorragia aguda o la necesidad de un procedimiento invasivo- la transfusión profiláctica de plaquetas suele estar guiada por el recuento de plaquetas.
La revisión examinó los estudios relacionados con el recuento de plaquetas y el riesgo de hemorragia, junto con la intervención de transfusión de plaquetas. Pero excluyó los estudios en los escenarios de sangrado perioperatorio o agudo.
La revisión identificó cuatro ECA (nivel II) que compararon diferentes valores detonantes de la transfusión de plaquetas.
Tres estudios (134-136) compararon un umbral de transfusión de plaquetas de 10×109/L (10.000 cel/μL) con uno de 20×109/L (20.000 cel/μL). Otro estudio utilizó 30×109/L (30.000 cel/μL) como el mayor umbral (150). De estos estudios, tres (134,136, 137), no demostraron una diferencia significativa en la mortalidad entre los dos brazos del estudio.
Estos tres estudios informaron eventos hemorrágicos, pero ninguno observó una diferencia significativa en las tasas de hemorragia entre los dos brazos de estudio, ni en las tasas de hemorragia en relación con un umbral más restrictivo para la transfusión de plaquetas.
Las tasas de transfusión de glóbulos rojos se informaron en los cuatro estudios. Ninguno de los estudios demostró diferencias significativas en el número de unidades de GR transfundidas, o en el número de transfusiones, entre los brazos de estudio.
Pacientes sometidos a quimioterapia mielosupresora o trasplante alogénico de CPH
Basados en estos resultados, en los pacientes sometidos a quimioterapia mielosupresora o trasplante alogénico de CPH, la estrategia recomendada para la transfusión profiláctica de plaquetas es a un recuento de plaquetas <10×109/L (10.000 cel/μL) en ausencia de factores de riesgo, y en <20×109/L en presencia de factores de riesgo (ver recomendación R8).
No hay evidencia en este momento para apoyar un umbral más bajo para la profilaxis, o para la ausencia de profilaxis. Sin embargo, estas preguntas son el enfoque actual de dos importantes ECA internacionales.