Capítulo I
Profesor Rafael Gómez – Cuevas, MD
Control Central
Partimos de un hecho fundamental: todo organismo vivo precisa un aporte de nutrientes para el adecuado crecimiento, desarrollo y mantenimiento de sus tejidos, Dicho aporte es obtenido gracias a la ingesta alimentaria. Que a su vez depende basicamente del comportamiento alimentario, donde el apetito es factor principal.
Entonces el concepto de apetito debe ser entendido no simplemente como una elegante manera de traducir hambre sino desde un punto de vista mas complejo: debe ser estudiado en el campo psicobiológico.
En la conformación del sistema, las señales hormonales y neurológicas constituyen la parte biológica, mientras que los hábitos de alimentación y los aspectos socioculturales que rigen y regulan la ingesta alimentaria hacen la parte psicológica.
Estos mecanismos son vitales, ya que de ellos depende la supervivencia, y están delineados en particular para proteger al organismo contra la denutrición, impidiendo en cierto modo que disminuyan las defensas, y para luchar contra la sobrenutrición – que tambien puede convertirse en un factor nocivo-, lo que seguramente es parte de la explicación sobre las causas de la Obesidad.
El circulo puede comenzar en regulación biológica, a través del cerebro, con lo que se condiciona un comportamiento alimentario, hay una adaptación ambiental, previa al proceso de nutrición, se sigue entonces con una etapa metabólica, que cierra el círculo y conduce al campo de la regulación biológica nuevamente.
En conclusión:
El comportamiento alimentario se ajusta a las necesidades de regulación biológica y a la adaptación comportamental.
Hasta hace unos años, se valoraban exclusivamente los terminos de apetito y de saciedad, estaban identificados sus respectivos centros neurológicos y solo eran protagonistas un centro modulador y perifericamente una señal. Siguiendo a Blundell (1) hoy podemos ampliar el esquema en tres niveles:
La cascada de la saciedad, que consta de elementos cognitivos y sensoriales: El olfato y la vista constituyen señales que “abren” el apetito como acto preparatorio a la ingesta lo que comprende la llamada fase cefálica.
Los mecanismo fisiológicos intermediarios: a través del nervio vago el cerebro recibe información de los quimio y mecano – receptores del tracto gastrointestinal, que conforman en su conjunto los mecanismos de control postingesta.
Las vías cerebrales:
En la fase postabsortiva los distintos nutrientes son procesados y sus niveles en sangre se convierten -al regresar al cerebro por vía circulatoria- en señales de saciedad.
Este sencillo esquema explica entonces que el alimento ingresa al organismo gracias a la puesta en marcha del apetito, como señal indicadora, y que éste pasa entonces por una fase sensorial, cognitiva, postingesta y postabsorción, que marchan en forma decreciente, mientras simultáneamente la saciedad se va incrementando en forma inversa.
El díficil equilibrio entre apetito y saciedad – que finalmente va a regular cantidad y calidad de la ingesta alimentaria- se convierte entonces en un tema apasionante que seguiremos estudiando en las paginas siguientes.
Control Periférico
Kaufmann (2) quien ha revisado el tema recientemente nos recuerda un hecho fisiológico bien conocido: si bien la orden de iniciar la comida parte en principio del sistema nervioso central, del hipotálamo en particular, la continuación de mantener la ingesta de comida tiene su origen en señales o estímulos periféricos. Así, en el animal de experimentación- con una fístula esofágica que desvía al exterior toda la comida ingerida el impulso de comer es continuo y no aparece la saciedad, ya que no hay estímulo periférico que la provoque.
Hasta hace unos años el mecanismo propuesto era bien sencillo:
Luego de ingerir alimentos, estos pasan al estomago, luego al intestino, donde después del proceso digestivo habitual, son absorbidos y los nutrientes – uno de ellos la glucosa- pasan a la sangre.
Cuando la glicemia llega a un determinado nivel, el hipotálamo sería informado por vía sanguínea y la orden de detener la ingesta de comida era dada automáticamente.
Una sencilla explicación que sin embargo no encajaba en todos los casos. En los diabéticos por ejemplo, pese a tener elevados niveles de glicemia, el apetito persistía.
La observación sobre los distintos niveles de saciedad hizo participar en el mecanismo de control periférico del apetito a otros nutrientes y sustancias: se comprobó que el nivel de ácidos grasos también era importante y podía frenar la ingesta de comida, así como una información “global” del metabolismo celular que a través de la Leptina podía servir de informador al hipotálamo y producir saciedad.
Por otro lado a nivel del hígado hay receptores que informan sobre niveles de glucosa y su aprovechamiento (glucoreceptores) y hay que dar un papel relevante en el control periférico del apetito a las señales provenientes del estómago e intestino.
Recordemos que el apetito se puede frenar en los animales de experimentación si a estos se les introducen balones intragástricos que semejan la sensación de llenado post comida.
Finalmente los aspectos psicológicos son muy importantes:
Comer es uno de los placeres mas arraigados en el ser humano, es un instinto, una pulsión enlazada además con la conservación de la especie.
Sin embargo a manera de resumen conceptual podemos decir que los mecanismos de control periférico del apetito son definitivamente de origen mixto: es decir intervienen siempre en adecuada proporción señales humorales, mecánicas, sensoriales y psicológicas.
Si solo fuesen señales vehiculadas por la corriente sanguínea, sobre niveles de cualquier nutriente, el proceso de digestión gástrico, el de la absorción a nivel intestinal, luego el transporte de la señal bioquímica hasta el cerebro, sería un proceso tan largo que el impulso de comer sería también exagerado en el tiempo. Definitivamente es necesario valorar los principales elementos del sistema:
Mecanismo fisiológicos de control del apetito
Considerando que el control de la ingesta alimentaria o de energiía es de hecho un componente del balance calórico, el control del apetito tiene enorme influencia en su regulación, ya que si este balance se hace positivo, se produce sobrepeso u obesidad.
La expresion del apetito pude hacerse por mecanismos sensitivos que responden a la característica de un alimento determinado -aspecto hedónico-; respuesta fisiológica postingesta, porción absortiva del trato gastrointestinal traducida por señales que reflejan cantidad y calidad del alimento ingerido; señales postasortivas que se generan en el rápido turnover del alimento ingerido (glucógeno) y señales lipostáticas emanadas de la reserva adiposa.
En líneas generales se puede convenir entonces en que hay mecanismos de regulación a corto y largo plazo, así:
Mecanismos de regulación a corto plazo:
Cifra baja de niveles de glucosa en sangre, que “dispara” el apetito; descenso global del metabolismo celular, que actúa a nivel hipotalámico; información de los glucoreceptores hepáticos, de relativo valor y señales externas: gustatorias, visuales, olfativas, que cuando son agradables mantienen el deseo de comer y lo frenan y si son desagradables. (Lea También: Transtonos de la Conducta Alimentaria)
Mecanismos de regulación a largo plazo:
La insulinemia, que sabemos esta directamente relacionada con la proporción de tejido adiposo y los niveles de leptina. comando genético a distancia: se han descrito genes que a nivel de tejido adiposo con condicionan una información sobre niveles de grasa al hipotálamo.
Desde el punto de vista fisiológico, siguiendo el mismo esquema propuesto por Blundell podemos aceptar en reumen que puede situarse en tres niveles.
- Psicológico/comportamental
- Fisiológico/metabólico
- De interacción metabólica o neurotrasmisión cerebral.
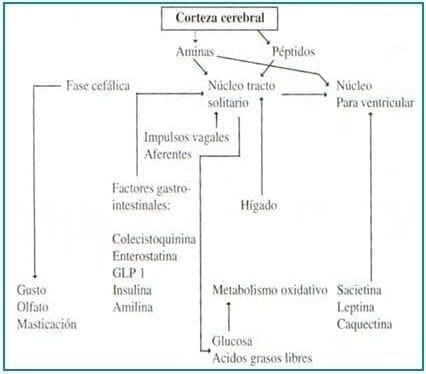
El apetito es entonces un reflejo de la actividad sincronizada de eventos en estos tres niveles, de acuerdo a la interacción de multiples factores siguiendo el esquema ya planteado, ver gráfica No. 1
Gráfica No. 1 Mecanismo de regulación del apetito
Modelos experimentales de regulación del apetito
De intento colocamos estos nuevos conceptos aún en el apartado de “experimental” ya que hasta ahora no se ha logrado reproducir exactamente lo encontrado en el laboratorio con los hallazgos en humanos.
Pero es verdad, en estos ultimos años, la investigación en animales ha abierto nuevos rumbos y aportado muevos elementos en este ajedrez de apetito /saciedad..
Ha sido fundamentalmente en roedores y en ciertas razas de ellos como por ejemplo los obesos (ob), los diabeticos (db) los “grasos” (fat) lo que ha permitido- decíamos- incluir nuevos actores como la leptina, que puede definirse como una sustancia hormonal que actúa como señal adiposa de saciedad, ejerciendo sus efectos sobre el sistema nervioso y sobre los niveles de insulina y glucagon, y cuyos receptores están situados en el hipotalamo.
La hipotesis actual sugiere que la leptina liberada por el tejido adiposo se liga a los receptores hipotalámicos y disminuye la actividad del NPY, potente estimulador de la ingesta alimentaria.
Se sabe tambien que otro gen el db codifica el receptor de la leptina, de ahí que se encuentren pacientes obesos con hiperleptinemia, dando lugar al llamado sindrome de resistencia a la leptina, en alguna forma parecido al de la resistencia insulínica.
Finalmente no debemos desconocer el aporte moderno de la neurofarmacología que ha despertado el interés en las aminas noradrenalina y serotonina, el neuropeptido Y y los opioides como importantes reguladores del apetito y la saciedad a través de su actividad dopaminergica entendida hoy como mesocorticolímbica, que en alguna forma pudiese explicar la etiología de anorexia y bulimia en particular como relacionadas con los niveles de serotonina.
Medicamentos que influyen en el control del apetito
La psicofarmacología ha tenido un importante desarrollo en el ultimo medio siglo, lo que ha permitido que tengamos una mayor experiencia en su uso y conozcamos mas sobre posibles efectos secundarios.
Y se ha observado, cómo al cabo de uno o dos años de tratamiento se encuentran incrementos entre 10 y 20 kilos Bernstein( 3), lo que en muchas ocasiones da lugar a que el paciente abandone precozmente la medicación, interrumpiendo el tratamiento, lo que ha conducido precisamente a buscar la relación entre psicofarmacos y obesidad.
Con respecto a los mecanismos para este no deseado incremento de peso, se consideran dos aspectos:
Este tipo ded sustancias – por su acción anticolinérgica- poseen la característica de incrementar la ingesta de hidratos de carbono para reducir los efectos secundarios típicos de boca seca, que producen, por lo que el paente apela a masticar chicles o chupar caramelos, dando lugar a una ingesta extra y continua de golosinas azucarads.
Además aumentan la sensación de sed conlo que se ingiere toda clase de bebidas, y siendo la más comunes y fáciles de tomar, las más populares (gaseosas dulces) se recibe aun otra cuota más de carbohidratos que descompensan cualquier plan nutricional restrictivo que haya sido aconsejado, y que incrementann la oferta de azúcares a niveles claramente hipercalóricos.
En segundo lugar, sabemos que estos pisicofarmacos alteran en alguna forma los mecanismos de control del apetito, seguramente a nivel de neurotrasmisores, o bien bloqueando receptores, con lo que se producen fenomenos de “down regulation” beta-drenérgicos.
Se ha encontrado dicha relación con los antidepresivos llamados triciclicos, con el litio y los antipsicóticos, en menor relación con benzodiazepinas.
Los antidepresivos tricíclicos:
Tienen clara tendencia a producir boca seca, y/o sed, y se ha comprobado que al cabo de uno o dos meses de su administración aumentan el apetito dando lugar a incremento de peso. Con respecto a su capacidad de aumento del apetito y sobre peso pueden clasificarse en principio así:
- Marcada actividad: Amitriptilina
- Mediana actividad: Imipramina, Nortriptilina, Doxepin,
- Escasa actividad: Amoxapina, Desipramina, Trazodone.
Paradójicamente se describe acción inhibidora del apetito para la fluoxetina y el bupropion (que carecen de actividad antihistamíbnica y efectos colinergicos)
Inhibidores IMAO.
Este tipo de sustancias entre las que se incluyen phenelizina, e isocarcarboxacitranylcipromina, claramente producen aumento del apetito y de la sensación de sed.
Posiblemente intervenga para estas sustancias otro efecto secundario: que se ha comprobado producen hipoglicemia, con lo que la necesidad de ingerir hidratos de carbono de facil absorción se hace perentoria, lo que obliga al paciente a buscar e ingerir comidas o bebidas dulces.
Litio.
Se trata de una sustancia, que para ser realmente útil, precisa de una administración a largo plazo, motivo por el cual, un efecto mínimo sobre los mecanismos de control del apetito se convierte en un severo problema posterior, de aumento de peso.
Se sabe, que el litio actúa a tres niveles: Incrementando la sensación de sed, en particular de bebidas dulces; disminuyendo el número de receptores cerebrales a la serotonina y bloqueando o reduciendo la acción de la tiroxina, produciendo un cuadro de hipotiroidismo, que nosotros observamos, y comprobamos casi en todas nuestras pacientes que reciben litio en forma crónica. Curiosamente lo vemos con mucha menor frecuencia en el sexo masculino.
Antipsicoticos.
Como prototipo se describe la clorpromazina, y se reportan cuantías de 4 a 5 kilos de aumento de peso, al cabo de 12 meses de su administración. Es marcada la sensación de boca seca y la apetencia por carbohidratos. Y se conoce tambien que inhiben receptores de serotonina, producen hipoglicemia y característicamente aumentan la ingesta de líquidos.
Pueden clasificarse por su grado de actividad para aumento de apetito, sed y peso así:
- Marcada actividad: Clorpromazina, thioridazina
- Mediana actividad: Trifluoperazyna, perphenazina.
- Baja actividad: Haloperidol, Loxapina
Se describen efectos contrarios es decir: reducción del apetito y de peso para el Molindone.
Señales de Saciedad
Son fundamentalmente inhibitorias, interrumpiendo el deseo de comer y provienen: del tracto gastrointestinal que está equipado con quimioreceptores especializados que envían información al cerebro a través del nervio vago.
Luego en la fase postabsortiva los nutrientes que atraviesan la barrera intestinal o son metabolizados constituyen otra serie de señales de saciedad. Intervienen también: la distensión gástrica postingesta y peptidos intestinales neurotrasmisores: GLP-1, CCK, amilina, enterostatina, bombesina, somatostatina y a nivel central NPY y Leptina.
Bombesina.
Trabajando en animales de experimentación se ha comprobado que si se conecta solo por vía sanguínea un estomago extra luego de una comida suficiente, hay alguna señal vehiculada a través de la sangre que hace que el animal receptor no tenga hambre.
Esta sustancia es la bombesina, que se considera realmente como un neuropeptido trasmisor que actúa sobre fibras aferentes vagales y espinales.
Colecistoquinina.
Es una “hormona” digestiva secretada por las celulas intestinales, que hace contraer la vesícula biliar, pero tambien lo hace a nivel gástrico, donde además favorece la contracción pilórica, dando lugar a sensación de llenado gástrico, con estimulación de los receptores vagales que como sabemos originan saciedad.