Dextrocardia por 46XX,+DER (13:14)(Q10)
Resumen
Se reporta la inusual presentación clínica de un neonato, de sexo femenino, con Síndrome de Patau por traslocación con escasas características dismórficas, en quien se documentó un hallazgo radiológico de dextrocardia; cursó con apneas, requirió ventilación mecánica, con evolución desfavorable hasta el exitus letalis a los 36 días. El cariotipo reportó 46XX, +der (13;14) (10q;10q),Síndrome de Patau por traslocación no balanceada.
Esta es una alteración severa con amplio espectro clínico, que se presenta con microcefalia, defectos del cuero cabelludo, holoprosencefalia y microftalmia, hendiduras orofaciales, defectos congénitos cardíacos, polidactilia y severo retardo mental, manifestaciones ausentes en nuestro paciente.
La sobrevida es corta y el riesgo de recurrencia es menor al 1% sin embargo, en los casos por traslocación, el riesgo de recurrencia depende de la fórmula cromosómica de los padres.
En el presente caso, al nacimiento, solo se observó retrognatia, pie equinovaro unilateral y pliegue palmar único, motivando su inclusión en el Estudio Colaborativo Latinoamericano de Malformaciones Congénitas (ECLAMC). Este reporte muestra la importancia de realizar estudios citogenéticos en pacientes que presentan un cuadro clínico inespecífico, con tres o más anomalías clínicas menores.
Palabras Claves
Dextrocardia, Síndrome de Patau, traslocación Robertsoniana, cariotipo, ECLAMC.
Abstract
We report the unusual clinical presentation of a female newborn, with Patau Syndrome due to traslocation with atypical clinical presentation consisting of micrognathia, single palmar crease and dextrocardia. She presented with apnea that required mechanical ventilation, with unfavorable evolution until exitus letalis 36 days after.
Cariotype reported 46,XX,+der(13;14)(10q;10q), Patau Syndrome by unbalanced translocation. This is a severe alteration with broad clinical features, as microcephaly scalp defects, holoprosencephaly, micropthalmy, orofacial clefts, congenital cardiac defects, polydactyly and severe mental delay, all of them absent in our patient.
The life span is short and the recurrence risk is lower than 1%, when Patau Syndrome is due to Robertsonian translocation, the recurrence depends on the parents cariotype. In the initial clinical examination retrognatia, single palmar crease and club foot were observed, which motivated its inclusion in the “Estudio Colaborativo de Malformaciones Congénitas “ (ECLAMC). This report evidence the importance of cariotyping patients who display unspecific clinical features, with three or more smaller clinical anomalies.
Key words
Dextrocardia, Patau Syndrome, Robertsonian translocation, cariotype, ECLAMC.
Caso Clínico – Caso de Síndrome de Patau por Traslocación Robertsoniana
El caso clínico reporta un recién nacido de sexo femenino de madre primigestante de 22 años de edad, con controles prenatales en los que se le administró sulfato ferroso desde el primer trimestre, cursó con infección de vías urinarias sin tratamiento al inicio de la gestación.
La ecografía con biometría fetal demostró hidroureteronefrosis derecha, en el último trimestre cursó con oligohidramnios y preeclampsia leve, que motivó su hospitalización para control, realizándose maduración fetal y posterior parto por cesárea, indicada por la hipertensión inducida por el embarazo y por presentación podálica del producto.
Al examen físico se encontró una Recién Nacida (RN), Pequeña para Edad Gestacional (PEG) con Retardo del Crecimiento Intrauterino (RCIU) asimétrico. Ballard de 36 semanas, talla de 44 cm. Peso de 1900 gr. y perímetro cefálico (PC) de 31 cm. Buena vitalidad APGAR 9/10 al minuto y 10/10 a los 5 minutos.
Silverman cero. RN con llanto inmediato, plagicefalia, micrognatia, orejas pequeñas de implantación baja con sobreplegamiento del hélix, pliegue palmar único derecho, pie equino varo izquierdo con reducción activa y pasiva, sobreposición del 4to dedo sobre el 3ro (bilateral) y sin déficit neurológico.[Figura 1]
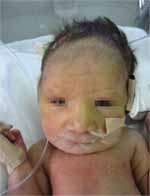
Figura 1. Se observa en la paciente una micrognatia como única malformación craneofacial presente en la
evaluación inicial. Posteriormente se describió talipes y pliegue palmar único.
Ingresó a la Unidad de Cuidados Intensivos Neonatales (UCIN) por prematurez, con una evolución caracterizada por polipnea en las primeras horas, cianosis perioral y signos de distress respiratorio. Se obtuvo una placa radiográfica de tórax que demostró dextrocardia con integridad del resto de las estructuras torácicas. La auscultación cardíaca no reveló presencia de soplos ni arritmias.
Posteriormente desarrolló alcalosis metabólica hiperoxémica y un cuadro hemático realizado reportó severa plaquetopenia.
Durante su hospitalización la ecografía abdominal confirmó la hidronefrosis derecha y el ecocardiograma reportó dextrocardia con situs solitus y foramen oval permeable, con adecuada función biventricular. La evolución llevó a la RN a sepsis neonatal + trombocitopenia, la que fue resuelta con antibióticoterapia para posterior alta.
A los pocos días retornó a la Unidad de Urgencias Pediátricas por trastornos en la deglución y se indicó su hospitalización por presunta broncoaspiración y antecedente de apneas frecuentes en el domicilio. La radiografía de tórax reveló infiltrados alveolares pulmonares y la valoración por Otorrinolaringología determinó una incoordinación velopalatina y reflujo gastroesofágico grado 4, luego de la realización de cinedeglución de vías digestivas altas.
La resonancia magnética nuclear cerebral fue normal, se realizó videolaringotraqueoscopía bajo anestesia general y trazado de sueño normal, sin embargo no se pudo demostrar que las apneas fueran de origen central.
La RN requirió ventilación mecánica y posteriormente se decidió suspender la misma y mantener oxígeno permanente, persistiendo los períodos de apnea, la paciente falleció a los 36 días de nacida. (Lea También: Falla Hepática, Sepsis, TBC vs. Linfoma, Infección Urinaria por Klebsiella)
Hallazgos Citogenéticos
El cariotipo fue realizado en cromosomas en metafase, la técnica de bandeo G fue empleada en cultivo de linfocitos de sangre periférica a las 72 horas.
El análisis de los cromosomas en 25 metafases mostró 46,XX,+13,der(13;14)(10q;10q) trisomía parcial del cromosoma 13 por traslocación con el cromosoma 14, sugiriéndose la realización del análisis cromosómico a los padres.
Las características del reporte citogenético correspondieron a un Síndrome de Patau por trisomía parcial por derivado del cromosoma 14 con traslocación no balanceada al brazo largo del cromosoma 13.
Síndrome de Patau – Trisomía 13
El síndrome de Patau es la tercera cromosomopatía en orden de frecuencia y a su vez la más letal de las trisomías autosómicas viables. La primera descripción clínica se realizó en 1657 por Bartholin1 sin embargo su identificación en laboratorio se remonta a 1960 cuando Patau logró demostrar la existencia de un tercer cromosoma 13 a través de las técnicas de citogenética.
Ese reporte publicado en Lancet hacía relación a un caso con un cromosoma acrocéntrico del grupo D, extra. En esa ocasión se registró microcefalia, anoftalmia o microftalmia, labio y paladar hendido bilateral y polidactilia; como parte del fenotipo correspondiente. 2
Otra fórmula cromosómica que corresponde al Síndrome de Patau por Traslocación Robertsoniana es la que comprende alteraciones estructurales que involucra dos cromosomas acrocéntricos, los cuales presentan puntos de rotura en o cerca de los centrómeros, ello determina la formación de un derivado cromosómico, como en el presente caso. (Ver: Comportamiento Clínico-Epidemiológico de Heridas por Mordeduras de Perro)
Presentación Clínica – Caso de Síndrome de Patau por Traslocación Robertsoniana
Un primer síntoma puede ser la historia de preeclampsia2 y la placenta puede ser anormal o mostrar cambios similares a una mola parcial.2,10 Las manifestaciones clínicas son características en este síndrome, sin embargo, estas pueden ser variables, se puede apreciar bajo peso, por debajo de 2600g. o 2480g.2,9
La trisomía 13 tiene un amplio espectro de manifestaciones clínicas que compromete diferentes sistemas, entre ellos el sistema cardíaco,3,6 músculo esquelético, genitourinario, sistema nervioso y defectos de la línea media con alteraciones en la conformación de las estructuras de la cara, entre ellas la cavidad oral y las órbitas con compromiso del globo ocular y estructuras perioculares,18 con o sin compromiso de la masa encefálica.
Se describieron casos con alteraciones gastrointestinales y vasculares.2 En el cuadro 1, se observan las alteraciones con su respectivo orden de frecuencia.
Malformaciones congénitas por sistemas descritas en el
Síndrome de Patau, frecuencia de presentación y hallazgos en el
presente caso.
| Cuadro 1 | ||
Malformaciones congénitas por
|
||
| Alteraciones craneales | ||
| Alteración | Frecuencia de presentación | Caso reportado |
| Microcefalia | >50% | Ausente |
| Plagicefalia | Rara | Ausente |
| Hendidura labial | 60 – 80 % | Ausente |
| Hendiduras palatinas | 60 – 80 % | Ausente |
| Anoftalmia | < 50 % | Ausente |
| Microoftalmia | < 50 % | Ausente |
| Micrognatia | Rara | Ausente |
| Aplasia cutis | < 50 % | Ausente |
| Alteraciones cardiacas | ||
| Persistencia de conducto arterioso | 80 % | Ausente |
| Defectos del septo ventricular | 80 % | Ausente |
| Defectos del septo atrial | 80 % | Ausente |
| Dextrocardia | 24 % | Ausente |
| Alteraciones abdominales | ||
| Onfalocele | Poco frecuente | Ausente |
| Hernias umbilicales | 67 % | Ausente |
| Arteria umbilical única | 40 % | Ausente |
| Hernia inguinal | 40 % | Ausente |
| Diástasis de rectos | Poco frecuente | Ausente |
| Alteraciones genitourinarias | ||
| Criptorquidia | 100 5 | Ausente |
| Hidronefrosis | 25 % | Ausente |
| Utero bicome | 12 % | Ausente |
| Riñón pliquistico | 70 % | Ausente |
| Duplicación de uréteres | 12 % | Ausente |
| Alteraciones musculoesqueléticas | ||
| Polidactilia postaxial | 76 5 | Ausente |
| Pliegue palmar único | 64 % | Ausente |
| Ectrodactilia | Rara | Ausente |
| Oligodactilia | Rara | Ausente |
| Talipes | 89 % | Ausente |
| alteraciones del SNC | ||
| Holoprosencefalia | 70 % | Ausente |
| convulsiones | 25 % | Ausente |
| Apnea | 58 % | Ausente |
El compromiso general de los pacientes con sospecha de trisomía 13 se aprecia con recién nacidos polimalformados con un compromiso severo de la línea media que se acompaña de hendiduras labiopalatinas4 de diverso grado.
Holoprosencefalia,1,2,9 en la cual el cerebro no se divide totalmente en dos hemisferios, es frecuente y se manifiesta por los defectos faciales de línea media los cuales incluyen: Hipotelorismo, microftalmia, anoftalmia. Agenesia o malformación de nariz o probóscide.
En las extremidades la polidactilia siempre es postaxial y puede afectar manos y/o pies y ser uni o bilateral2 Se han descrito pacientes afectados con ectrodactilia y oligodactilia5 y también talipes.
Las manifestaciones clínicas de las trisomías pueden verse drásticamente atenuadas si la alteración cromosómica es de tipo estructural y no numérica, en esos casos el espectro fenotípico contempla algunas anomalías menores que se acompañan de alguna anomalía mayor demostrable con procedimientos diagnósticos complementarios como resultado de alteraciones en la homeostasia de los pacientes afectados.
El ejemplo de nuestro caso reporte es claro, cuando se observaron alteraciones respiratorias que motivaron el empleo de una radiografía torácica y se encontró la dextrocardia como hallazgo radiológico. [Figura 2]
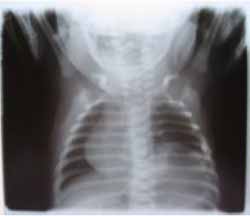
Figura 2. Placa radiográfica
Esto despertó la sospecha de alguna cromosomopatía implicada, debido a que se observaron elementos menores que motivaron la realización de un cariotipo diagnóstico, que posteriormente mostró las alteraciones ya mencionadas. [Figura 3]
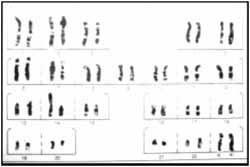
Figura 3. [* No se ha encontrado ningún filtro para la operación requerida. | En línea.{ ® *] Cariotipo Bandeo G en el que
se aprecia la traslocación Robertsoniana entre el cromosoma 13 y 14.
Pronóstico
El pronóstico de los afectados con Síndrome de Patau es malo, la gran mayoría tiene una sobrevida de pocos días, 8.5 días como promedio,7 algunos alcanzan los primeros meses de vida (11%), dependiendo de la severidad y número de las malformaciones.
Algunos pacientes sobreviven por encima del año y se relacionan con pacientes que presentan mosaicismo,12,14 ello determina una manifestación atenuada que permite alcanzar una expectativa levemente mayor; el retardo mental está presente en la mayoría de ellos y la literatura reporta un paciente que alcanzó la edad adulta portando esta cromosomopatía.
Aspectos Éticos
Se han considerado en cada intervención médica realizada en pacientes con Trisomía 13 universal o por traslocación, los costos y beneficios reales de llevar adelante diferentes tratamientos y se ha cuestionado su verdadera utilidad considerando el pronóstico ominoso que caracteriza a este síndrome.
En los hospitales se considera a través de un Comité de Ética la continuidad o no del manejo médico en pacientes diagnosticados con esta alteración, tales comités determinan en definitiva la actuación del equipo médico.
Otro aspecto ético está referido al diagnóstico prenatal del Síndrome de Patau; mediante la amniocentesis o el cultivo de vellosidades coriónicas se puede realizar un diagnóstico temprano en las primeras 12 a 15 semanas, aplicando técnicas de citogenética, convencional o citogenética molecular, sin embargo la decisión del curso de la evolución del embarazo debe ser considerado.
En nuestro medio la interrupción del embarazo no está amparada por las leyes y tal procedimiento no se practica de rutina en los Hospitales del sistema.
Frecuencia y Riesgo de Recurrencia
La frecuencia de la enfermedad es de 1 en 5000 nacidos vivos, 11 el Estudio Colaborativo de Malformaciones Congénitas (ECLAMC)13 resalta una frecuencia de 6.5 x 10.000. El estudio colaborativo de KOREA para amniocentesis diagnóstica mostró que de 11000 pacientes estudiados 6 casos fueron diagnosticados.15
La probabilidad de que una alteración cromosómica se repita es menor al 1%, esta aproximación corresponde a los casos de trisomías completas o universales.
Los riesgos de recurrencia para los miembros de la familia extendida aumentan cuando el síndrome de Patau ocurre debido a anormalidades cromosómicas estructurales.
El médico genetista debe evaluarlas en el paciente y ofrecer la prueba adicional a los miembros de la familia en riesgo. Los riesgos de la repetición para los embarazos futuros se deben tratar en todos los casos, si la aneuploidia o los cambios estructurales están implicados.
Se puede encontrar padres que son portadores de una traslocación Robertosniana balanceada sin manifestar un fenotipo alterado, que trasmiten a los hijos la alteración cromosómica, sin embargo en la progenie la alteración cromosómica es no balanceada y se manifiesta con el fenotipo del Síndrome de Patau.19
Conclusión – Caso de Síndrome de Patau por Traslocación Robertsoniana
Con respecto al presente caso se debe tener presente que la presentación de los casos de Síndrome de Patau puede ser variable, generalmente se presentan con las alteraciones clásicamente descritas, sin embargo, las formas atípicas pueden ser subevaluadas clínicamente, por ello el estudio citogenético es de gran utilidad.
Se debe considerar incluso que las formas atípicas de trisomía 13 por traslocación pueden ser variables clínicamente a pesar de tener un reporte de cariotipo similar, por ello el fenotipo con sus alteraciones funcionales pueden tener manifestaciones poco perceptibles en los primeros días posteriores al nacimiento y el médico examinador debe tener en cuenta la posibilidad de una alteración cromosómica al momento de evaluar clínicamente a un neonato.
Bibliografía – Caso de Síndrome de Patau por Traslocación Robertsoniana
- 1. Gorlin R. Cohen M. Levin S. Syndromes of the Head and Neck. 3º Edition.Oxford Univeristy Press.41-43
- 2. Tolmie. John.E Down Syndrome and other autosomal trisomies. In Principles and Practices of Medical Genetics. Emery and Raimonds. Vol 1. Churchill Livigstone. 4ta Ed. 2002. UK.
- 3. Teenstedt C. Chaoui R. Körner H. Dietel M. Spectrum of Congenital Heart Defects and Extracardiac Malformations associated with chromosomal abmormalities:results of a seven year necropsy study. Heart.1999(82):34-39
- 4. Perrotin F. Mabille L. Marret H.Paillet C. Lanasc J.Body G. Chromosomal defects and associated malformations in fetal lip with or without cleft palate. European Journal of Obstetrics and Ginecology and Reproductive Biology. 2001 (99):19-24
- 5. Martinez M. Villa A. Asero R. Ayala A. Calvo M. Bermejo E. Rodríguez L. Limb Defiencies in Infants with Trisomy 13. American Journal of Medical Genetics. 93:2000. 339-241.
- 6. Stromme P, Thaulow E, Geiran O.Cardiac surgery in a girl with trisomy 13. Cardiol Young. 2000;10(6):560.
- 7. Brewer C. Holloway S. Stone D. Carothers A. FitzPatrik D. Survival in Trisomy 13 and Trisomy 18 cases ascertained from populations based registers. Journal of Medical Genetic 2002(39):1-3
- 8. Kjær I. Keeling J. Fischaer B. Pattern of Malformations in the Axial Skeleton in Human Trisomy 13 Fetuses. American Journal of Medical Genetics. 1997(70):421- 426.
- 9. Jones K. Smith´s Recognizable Patterns of Human Malformation. 5th. Ed. Saunders Co. 1997.18-23.
- 10. Jauniaux E. Halder A. Partington C. A Case of Partial Mole associated with trisomy 13 Ultrasound Obstetric and Gynaecology.1998(11):62-64
Referencias – Caso de Síndrome de Patau por Traslocación Robertsoniana
- 11. Loughna S. Bennet P. Gau G. Nicolaides K. Blunt S. Moore G. Overexpression of sterease D in kidney from trisomy 13 fetuses. American Journal of Human Genetics. 1993;53(4):810-816.
- 12. Zoll B. Wolf J. Lensing-Hebben D. Pruggmayer M. Thorpe B. Trisomy 13 (Patau Syndrome) with an 11-year survival. Clinical Genetics.43(1):46-50
- 13. Zarante I. Castillo M. García N. Suarez F. Gutiérrez C. Umaña A. Análisis Clínico Epidemiológico de Factores Asociados a Malformaciones Congénitas ECLAMC-Hospital Universitario San Ignacio Junio- Dic de 2001. Universitas Médica.
- 14. Tunca Y, Kadandale JS, Pivnick EK. Long-term survival in Patau syndrome. Clin Dysmorphol 2001;10(2):149-50
- 15. Yang YH, Ju KS, Kim SB, Cho YH, Lee JH, Lee SH, Choi OH, Chun JH, Kim JI, Kim HJ, Sohn YS.The Korean collaborative study on 11,000 prenatal genetic amniocentesis. Yonsei Med J 1999;40(5):460-6
- 16. Delatycki M, Gardner RJ Three cases of trisomy 13 mosaicism and a review of the literature. Clinical Genetics 1997;51(6):403-7
- 17. Helali N, Iafolla AK, Kahler SG, Qumsiyeh MB. A case of duplication of 13q32—>qter and deletion of 18p11.32—>pter with mild phenotype: Patau syndrome and duplications of 13q revisited. Journal of Medical Genetics 1996;33(7):600-602
- 18. Koole FD, Velzeboer CM, van der Harten JJ. Ocular abnormalities in Patau syndrome (chromosome 13 trisomy syndrome). Ophthalmic Paediatric Genetics 1990;11(1):15-21
- 19. Peter A. et al. Two cases of Robertsonianas translocations in oligozoospermic males and their consequences for pregnancies induced by intracytoplasmic sperm injection. Human Reproduction 1997;12 (8)1642-1644.
Autores – Caso de Síndrome de Patau por Traslocación Robertsoniana
Dr. Igor Iván Salvatierra Frontanilla. MD. Residente de Genética Médica. Instituto de Genética Humana. Facultad de Medicina. Pontificia Universidad Javeriana
Dra. Gloria Ruiz. MD
Pediatra Neonatóloga. Jefe de la Unidad de Neonatología del Hospital Universitario San Ignacio Dr. Ignacio Briceño Balcázar. MD.Ph.D.
Médico Genetista. Profesor Asociado. Instituto de Genética Humana. Facultad de Medicina. Pontificia Universidad Javeriana