Dra. Susana Murcia de Onatra.
Unidad de Patología Pediátrica.
Departamento de Patología.
Facultad de Medicina, Universidad Nacional.
Hospital de la Misericordia, Santafé de Bogotá
Motivo de Consulta:
Lactante menor de 2 meses, sexo masculino, con tos seca, rinorea, fiebre de 39° C y dificultad respiratoria progresiva de 15 días de evolución.
Antecedentes: Madre de 18 años con historia de 5 compañeros sexuales y tres abortos, cuadro de infección urinaria en el primer trimestre, tratada con antibióticos. Parto eutócico de 300g, talla: 52cm, presentó ictericia en el primer mes, se desconoce la duración , tratado con fototerapia; alimentación con leche materna y NAN. Vacunas BCG y primera dosis de DPT y polio. Infección de vías respiratorias altas con otitis y sinusitis al mes de edad e infección de uña de grueso artejo.
Examen de Ingreso:
Paciente en malas condiciones , pálido, con leve tinte ictérico, sin dificultad respiratoria, FC: 130, FR: 30/min, peso: 5k, talla: 62 cm, secreción purulenta en ambos ojos, roncus en ambos campos, hepatomegalia de 9 cm, esplenomegalia hasta fosa ilíaca, petequias en piel de abdomen. El cuadro hemático mostró Hb: 7g/dl. Hto: 24, Blancos: 16100, N: 52, Linfos: 42, Cayados: 4, Metamiel: 2%, Reticuloc: 2.8%, Plaquetas: 22000, VSG: 39/h, Glicemia: 54, Bilirrubina total: 1.4, directa: 0.8, F alcalina: 250, TGO: 90, TGP: 52, Proteínas totales: 4.5, Albúmina: 1.5, Globulinas: 3.0, Na 131meq/l, LDH: 1045, TPT: 38.7, PPD: negativa, Rx de tórax infiltrados micronodulares paracardíacos derechos posteriores. Eco abdominal confirma víscemegalia rectificación de la Arteria. Mesentérica superior, sugestivo de adenomegalias retroperitoneales.
Al tercer día, presenta temperatura 39° C y deshidratación leve; se inician líquidos, oxacilina y ceftriaxona. Hace distensión abdominal, edemas y dificultad respiratoria. Se disminuye el volumen de líquidos, se estabiliza hemodinámicamente; resultado de hemocultivos negativo. Médula ósea normocelular ligera diseritropoyesis de línea granulocítica, mostrando todos los estados de maduración, presencia de granulaciones tóxicas y vacuolas. Perfil inmunológico: FTA negativo. HIV negativo. CMV y TOXOPLASMA: IgG e IgM positivos, Rubeola: IgM negativo. Niveles de IgG 1896 (N=190-670 mg/dl) IgM. Los estudios de pobalciones de linfocitos B y T, y los de fagocitosis y adherencia, no se alcanzaron a realizar.
Al 5o. día apariencia séptica, distensión abdominal, ruidos intestinales disminuidos, onda ascítica positiva presenta dificultad respiratoria progresiva, cianosis y fallece.
Diagnósticos Clínicos Finales:
Bronconeumonía, síndrome hepatoesplénico por TORCH, ¿enfermedad linfoproliferativa? ¿Inmunodeficiencia?
Hallazgos de Autopsia
Se encontró lactante en anasarca pálida ictérico, con abdomen globoso, protrusión del ombligo, Hidrotórax y ascitis de líquido citrino. Los pulmones, el hígado y el bazo estaban aumentados de tamaño con múltiples lesiones nodulares blanquecinas hasta de 0.5 cm. Los ganglios de todas las cadenas entre 1 y cm con centro necrótico, formando masas confluentes en especial en región celíaca e hilio pulmonar. Lesiones aisladas puntiformes, se vieron en riñon, intestino, páncreas y suprarenales.
El estudio histológico mostró múltiples granulomas incompletos, con muy escasa necrosis y con incontables bacilos ácido- alcohol resistentes libres, no fagocitados en estos órganos. No había compromiso cerebral. Los órganos del sistema inmune mostraron en los sitios conservados, un desarrollo adecuado, con una depleción del tejido linfoide y una involución tímica importante. Después del estudio de la necropsia, se le hizo Rx de tórax a la madre que fue normal. La prueba de HIV se le solicitó pero no se pudo establecer contacto con ella para conocer su resultado.
Diagnósticos Definitivos:
Tuberculosis miliar con compromiso multivisceral probablemente secundaria a diseminación de BCG.
Inmunodeficiencia secundaria, ver comentario:
A. Prueba de Elisa para HIV negativa en el niño, desconocida en la madre.
B. PPD negativa, elevación de inmunoglobulinas G, M y A.
C. Historia de múltiples infecciones desde el nacimiento.
D. Infección no activa por citomegalovirus y toxoplasma (anticuerpos positivos IgG e IgM).
E. Depleción linfoide de órganos linfohemopoyéticos.
Comentarios:
Este niño de dos meses de edad, presentó signos claros de una inmunodeficiencia como enfermedad de base: múltiples procesos infecciosos de vías respiratorias, de piel y una infección tuberculosa muy temprana y fulminante cuyo origen más probable fue una diseminación de bacilo de Calmet-Guerin, ya que había el antecedente de vacunación por BCG, con una respuesta granulomatosa muy poco activa con gran cantidad de bacilos-alcohol resistentes. Estos cuadros infecciosos, más un adecuado desarrollo de los órganos del sistema inmune, con cambios solamente secundarios de depleción linfoide, establecen el diagnóstico de una INMUNODEFICIENCIA SECUNDARIA, cuyas causas son múltiples y van desde procesos hereditarios por anomalías cromosómicas, disfunciones orgánicas y nutricionales, agentes inmunosupresores, enfermedades hematológicas e infiltrativas, trauma, cirugía, hasta múltiples enfermedades infecciosas virales bacterianas, micóticas o parasitarias1. Por la historia y los hallazgos de la necropsia el cuadro corresponde a un proceso secundario a infección. Los antecedentes maternos, hacen pensar como primera posibilidad etiológica, una infección por HIV.
En el niño, esta infección puede hacerse por transmisión vertical o perinatal (madre infectada-hijo): in útero, causada por pérdida de integridad de la barrera placentaria; intraparto, a través de las superficies mucosas en contacto con sangre contaminada (70% de los casos)2 o postparto, por alimentación con leche materna1,2,3. Ocasionalmente el contagio puede hacerse por transfusiones4. Entre el 15 y el 25% de los hijos de madres infectadas, desarrollan la infección por HIV3. A diferencia del adulto, que presenta en el 70% de los casos entre tres y seis semanas después de ña infección aguda, un cuadro parecido al de la mononucleosis, el niño tiene una progresión más rápida, el período de latencia es mar corto y las manifestaciones se relacionan con prematurez, retraso del desarrollo, infecciones congénitas (TORCH), micóticas recurrentes, por micobacterias, y otras bacterias encapsuladas (streptococo pneumonie, pseudomona, bordetella, pertusis, etc). Otras complicaciones frecuentes son la neumocitis carinii, encefalopatía, disfunción endocrina, hematológica, gastrointestinal y aparición de neoplasias tipo linfoma no Hodgkin de alto grado (primario del sistema nervioso, Burkitt o Ki-1), leiomiosarcomas, y menos frecuente, sarcoma de Kapossi2. La disminución de linfocitos CD4, clásica manifestación del SIDA, puede no ser evidente como en el adulto, hasta los 6 años de edad; cuando se presenta, se relaciona con infección por microbacterias2. La progresión de la enfermedad depende de la cantidad de inóculo viral, del tiempo en que ocurre la transmisión (más severa entre más temprana) y de la presencia de otros patógenos que pueden influir en la progresión del cuadro. Las pruebas diagnósticas incluyen determinación de anticuerpos IgG específicos contra HIV detectables por prueba de ELISA y confirmados por Western blot. La PCR detecta el genoma HIV-1 en sangre y los cultivos positivos del virus, en la primera semana de vida, son indicativos de mayor agresividad del cuadro; en algunos casos estas últimas pruebas pueden ser las únicas diagnósticas en los niños2.
Otros agentes infecciosos como los virus de inclusión citomegálica, herpes, Epstein Barr, etc, son causa de inmunodeficiencia secundaria. El citomegalovirus produce inhibición de los monocitos, que se vuelven incapaces de presentar antígenos, determinan una falla en la proliferación de linfocitos y causan un elevado número de células NK con actividad supresora1.
Muchas de estas características descritas anteriormente, pueden aplicarse a la historia del paciente y a sus hallazgos postmortem; teniendo en cuenta los criterios propuestos en 1994 por el sistema de clasificación para infección de HIV en niños menores de 13 años, del comité central de enfermedades de los Estados Unidos, (citado por Tudor-Williams). Podría catalogarse el caso, en la categoría C “Paciente severamente sintomático con estados patológicos asociados a severa inmunodeficiencia que aparecen frecuentemente en individuos infectados con HIV y con gran morbilidad y mortalidad” dentro de los cuales están entre otros múltiples, la infección extrapulmonar o diseminada por micobacterias; pero analizando otros aspectos como la negatividad de la prueba del HIV, y la posibilidad no comprobada de haber recibido la atención perinatal y de ser afectado (no mayor del 15-25%) se hace necesario pensar en otro factor etiológico de la inmunodeficiencia celular que presentó el niño y que podría ser la infección por citomegalovirus (niveles altos de IgG e IgM, sin lesión orgánica activa). Queda el interrogante si esta falla inmunológica, podría explicar también la falla en la respuesta al HIV o si por ella sola, causó la inmunosupresión y la diseminación del BCG.
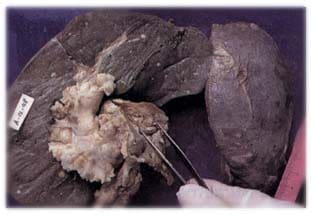
Figura No. 1. Lesiones miliares diseminadas en hígado y bazo y grandes adenomegalias.

Figura No. 2. Microfotografía de las lesiones tuberculosas

Figura No. 3. Timo con desarrollo normal con depleción del tejido linfoide. C. de Hassal normales.
Bibliografía
1. Sandberg ET, Kline MW Sheares WT. The secundary Inmunodeficiences in Stiehm. In: Inmunologic disorders in infants and Children 4th de WB Saunders 1996: 553.
2. Tudor-Williams G, Pizzo PA. Pediatric Human Inmunodeficiency Virus infection en Stiehm. In: Inmunologic disorders in infants and Children 4th de WB Saunders 1996: 510.
3. Chioddo F, Ricchie E, Costigliola P, et al. Vertical transmission of HTVL III Lancet 1986; 1: 739.
4. Anderson VM, Khan E, Greco MA. Pediatric AIDS pathology. Arch Path Lab Med 1993; 6: 313.
