Artículo corto
The emergence of “omic” sciences in nutrition: a current need
Sandra Perdomo, BSc, PhD,1 Diana Cárdenas, MD, MSc.2
Universidad El Bosque
Resumen
En la última década, la aproximación clásica de la investigación nutricional basada en aspectos fisiológicos y tendencias epidemiológicas le ha dado paso a la adquisición de plataformas de análisis genómico y a estudios moleculares de interacción entre nutrientes y expresión génica.
La investigación nutrigenómica se ha centrado, principalmente, en el estudio de enfermedades crónicas como el cáncer, la obesidad, la diabetes y la enfermedad cardiovascular. Se caracterizan por presentar redes biológicas y nutricionales disfuncionales, que involucran la regulación de múltiples genes.
La incorporación de nuevas tecnologías que permitan la aplicación de la genética, la genómica y la ciencia de la nutrición. Es un evento clave para promover el desarrollo de la investigación en el campo nutricional y para caracterizar la susceptibilidad genética de la población a las enfermedades crónicas relacionadas con la dieta así como las respuestas moleculares a factores dietéticos.
Palabras clave: Nutrigenómica, nutrición, genética (fuente: MeSH).
Abstract
In the last decade genomic analysis and molecular studies of the interactions among nutrients and of the interactions among processes of gene expression have begun to replace the classical perspective based on physiological and epidemiological aspects of nutrition.
Nutrigenomic research’s primary focus is the study of chronic diseases such as cancer, obesity, diabetes and cardiovascular diseases which are characterized by dysfunctional nutritional and biological pathways regulated by considerable numbers of genes.
The incorporation of new technologies which allow the application of genetics, genomics, and nutritional science is a pivotal event for promoting the development of nutritional research in characterizing genetic susceptibility to development of chronic diseases related to as well as research into molecular responses to dietary factors.
Key words: Nutrigenomics; nutrition; genetics.
Introducción
En los últimos diez años, la investigación en nutrición ha experimentado un cambio importante desde la aproximación epidemiológica y fisiológica hacia un abordaje desde la biología molecular y la genética.
Este cambio en el estudio nutricional, se debe principalmente al resultado de tres factores que han llevado a una creciente conciencia de que los efectos de la nutrición sobre la salud y la enfermedad no se pueden entender sin un profundo conocimiento de cómo los nutrientes actúan en el plano molecular: en primer lugar, los resultados de varios proyectos genómicos de gran escala han modificado las estrategias de investigación nutricional al resaltar la importancia de los genes en la nutrición humana y han proporcionado una gran cantidad de nueva información genética para ser explorada.
En segundo lugar, hay un creciente reconocimiento de la existencia de micronutrientes y macronutrientes que pueden comportarse como potentes señales dietéticas que influyen en la programación metabólica de las células y tienen un papel importante en el control de la homeostasis.
En tercer lugar, en el campo de la nutrición, los investigadores han comenzado a reconocer cada vez más que la predisposición genética puede ser un factor importante en el desarrollo de las principales causas de mortalidad que están vinculados con la dieta, tales como las enfermedades cardiovasculares, la diabetes tipo II y el cáncer.(1, 2)
Enfoque tradicional de investigación nutricional las ciencias Nutrigenómica
En contraste con el enfoque tradicional de investigación nutricional, las ciencias nutrigenómicas pretenden aplicar las últimas tecnologías para desarrollar un enfoque de investigación molecular y genético a problemas nutricionales.
Debido a la complejidad que representa abarcar el estudio de interacción entre genes y factores nutricionales y la complejidad de la alimentación y la nutrición, se han desarrollado tecnologías que son capaces de darnos nuevas ideas sobre el papel de los componentes de los alimentos en la regulación de la función tisular y el metabolismo humano y cómo estos procesos pueden estar implicados o alterados durante el desarrollo de trastornos metabólicos.
Estas tecnologías también son muy sensibles y capaces de detectar desviaciones relativamente pequeñas de homeostasis y leves efectos de factores dietéticos en la regulación de los niveles génicos o de metabolitos, por ejemplo.
Las herramientas “ómicas” más recientes son potencialmente capaces de cumplir con estos requisitos tecnológicos.
Bases teóricas del surgimiento de la Nutrigenómica
La dieta es un factor ambiental determinante del estado nutricional el cual participa de manera importante en la incidencia de enfermedades crónicas prevalentes. Actualmente, la nutrición y la genética unen esfuerzos y se integran en un área de estudio, la denominada genética nutricional y que abarca tanto la nutrigenómica como la nutrigenética.
Las diferencias fenotípicas del ser humano en salud y enfermedad se deben en especial a esta diversidad e individualidad genética propia de todos los miembros de la especie, y de forma igualmente importante a las diferentes experiencias ambientales de cada uno. La variabilidad genética interindividual es un determinante crítico de los distintos requerimientos nutricionales. El uso de diferentes técnicas moleculares ha permitido la identificación de marcadores de diferente tipo (polimorfismos en la longitud de los fragmentos de restricción RFLPS, marcadores de microsatélites, polimorfismos de un solo nucleótido), que frecuentemente se utilizan en la elaboración de los perfiles genómicos, y que van a permitir seleccionar individuos susceptibles a dietas específicas.(3)
Proceso nutricional se basa en la interacción
Esencialmente, cada proceso nutricional se basa en la interacción entre una multitud de proteínas codificadas por una multitud de moléculas de ARN mensajero expresada en un cierto tipo de células u órgano.
Alteraciones de los niveles de ARN mensajero y a su vez, de las proteínas correspondientes (aunque esto no necesariamente siempre cambia en paralelo) son parámetros críticos para controlar el flujo de un nutriente o metabolito a través de una vía bioquímica.
Nutrientes y componentes no-nutrientes de los alimentos pueden afectar la expresión génica ya sea directamente por interferencia con la maquinaria de control de la expresión de genes o en virtud de metabolitos o condiciones metabólicas inducidas (estado hormonal, estado redox celulares, etc.) que a su vez directa o indirectamente alteran los niveles de ARN mensajero y/o los niveles de proteína.
La aplicación de las tecnologías de la genómica y proteómica en estudios sobre nutrición, ya sea en cultivos celulares, animales o seres humanos, tiene el gran potencial para identificar marcadores específicos (biomarcadores) que respondan a determinados nutrientes, tratamientos o a una dieta.(4)
Estudios moleculares
Nuevas herramientas tecnológicas que han permitido realizar estudios moleculares cada vez más detallados en el campo de la nutrición también han ayudado a modificar el enfoque de esta área.
Cambios sutiles en la expresión génica, incluso en el plano de la sola célula, ahora pueden medirse por técnicas cuantitativas como PCR en tiempo real y análisis de alta densidad de microarrays.
Este último permite estudiar simultáneamente el transcriptoma nutricional, siendo este uno de los focos importantes del campo de la genómica nutricional o nutrigenómica.(5)
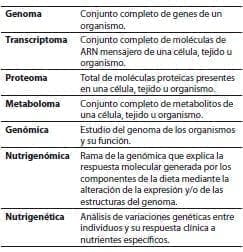
Progresos igualmente comparables en el análisis de la nutrición desde las perspectivas metabolómica y proteómica pronto deberían permitir el análisis de la respuesta de los nutrientes en las vías de señalización bioquímica y en la función metabólica, desde la expresión de genes hasta la condición fisiológica de los individuos (tabla 1).
Tabla 1. Definiciones (modificado de Gómez Ayala AE. 2007).(14)

Las tecnologías de “ómicas” son explotadas en estudios de intervención nutricional humana y los datos biológicos se usan sobre mecanismos importantes obtenidos en los diferentes modelos utilizando líneas celulares específicas así como modelos biológicos de ratón.
Mediante la combinación de herramientas de biología de sistemas ya existentes y algunos en proceso de desarrollo, se abriga la esperanza de identificar biomarcadores y su posible implicación en los eventos más relevantes que se desarrollan en las primeras etapas de los trastornos metabólicos.
De esta manera se obtendrá información sobre la forma como la nutrición puede prevenir el desarrollo de las enfermedades metabólicas más prevalentes como la diabetes de tipo II y las enfermedades cardiovasculares.
A pesar de que cada una de estas plataformas analíticas, desde la genómica a la proteómica y la metabolómica, proporcionan una información cada vez más exacta que describe un fenotipo determinado, es la integración de estas tecnologías la que proporciona los medios óptimos que revelan los efectos de un agente biológico en un organismo; así, el concepto de la biología de los sistemas (o del metabolismo integrado).(6)
De hecho, un acercamiento integrado del metabolismo vislumbra un futuro atractivo y emocionante para las comunidades farmacéuticas y alimenticias, y su búsqueda para mejorar salud y para prevenir enfermedad.
Estado del arte de las ciencias “ómicas ” en nutrición
En la actualidad existe un gran número de tecnologías que conforman la base experimental de la genómica nutricional.
Sin embargo, la aplicación de esta tecnología es aún limitada debido a la carente experiencia en su uso experimental y a una eficiente validación que permita su adopción rápida en disciplinas donde la genómica nutricional tiene un efecto medible como son la farmacéutica, la toxicología, la investigación clínica y la fármaco-genómica.
El mayor reto de la genómica nutricional está en el diseño de estudios significativos que apliquen estas metodologías, el desarrollo de investigaciones capaces de descifrar las complejas interacciones entre las diferencias genéticas individuales, la predisposición a las enfermedades y el componente de interacción genómica además de tratar de integrar los grupos que hayan o estén realizando estudios significativos en esta área.
Enfermedades que alcanzan proporciones epidémicas en la actualidad, tal como el cáncer, la obesidad, la diabetes y la enfermedad cardiovascular, se caracterizan por presentar redes biológicas y nutricionales disfuncionales, que involucran la regulación de múltiples genes (enfermedades poligénicas).
Los índices de incidencia y prevalencia de estas enfermedades en nuestro país se han incrementado en los últimos años. La Encuesta Nacional de la Situación Nutricional realizada en el año 2010 encontró que 51% de la población colombiana se encuentra con sobrepeso y obesidad.(7)
La Encuesta Nacional de salud del 2007 adicionalmente mostró la prevalencia de diabetes referida por entrevista en 3,51% para el ámbito nacional.(8)
Las cifras estimadas de incidencia de cáncer en Colombia y las de la base de datos Globocan 2002 muestran que las tasas de incidencia ajustadas de cáncer son de 186,6 en hombres y 196,9 en mujeres, convirtiéndose en una de las enfermedades más frecuentes en Colombia.
La obesidad y las patologías relacionadas están influenciadas por la ingesta total de energía:
Pero una ingesta subóptima de otros alimentos pueden también ser factores en la iniciación y el desarrollo de estas enfermedades.
Se ha comprobado cómo las deficiencias de ingesta y absorción de las vitaminas pueden también contribuir a la iniciación, a la severidad, y a las compli caciones de enfermedades crónicas en individuos.(9)
Tal vez una orientación más útil deberá considerar el genotipo de los individuos con un enfoque en polimorfismos genéticos comunes que alteran la biodisponibilidad de micronutrientes específicos, su metabolismo y la afinidad de enzimas clave involucradas en el metabolismo y síntesis de los cofactores de micronutrientes.
La suplementación de la dieta con vitaminas y minerales apropiados podría, en algunos casos, actuar como un modulador de riesgo.
Entre otros, se presta gran atención a los efectos potenciales de las dietas sobre genes implicados en la patogenia de las enfermedades cardiovasculares, la principal causa de mortalidad y morbilidad en todo el mundo.
En las últimas décadas, se ha centrado mucho la atención sobre la composición de la lipoproteína de plasma como uno de los factores de riesgo más importantes en el desarrollo de enfermedades cardiovasculares.
La variabilidad genética de los seres humanos para todos los genes relacionados con los lípidos conocidos y algunas variantes asociadas con una lipoproteína de metabolismo y perfiles de plasma de lípidos anormales se han estudiado extensamente.
La evidencia sugiere que una variación en los genes para apolipoproteína (apo) A – I, apo A – IV, apo B y apo E contribuye a la heterogeneidad en la respuesta de lípidos a la intervención dietética.(10)
estudio de la regulación metabólica
Por último, se ha generado gran expectativa en el estudio de la regulación metabólica y el desarrollo del cáncer. La carcinogénesis es un proceso integrado por múltiples etapas en las cuales tanto la expresión del gen, como la función de la proteína y del metabolito comienzan a funcionar de manera aberrante.
En la era posgenómica, los procesos celulares que median el inicio de la carcinogénesis, incluyendo aquellos mediados por factores dietéticos, han proporcionado información importante en nuestra comprensión de esta enfermedad.
El metabolismo observado en tumores es diferente a la de los tejidos normales de los que derivan los tumores.
Este fenotipo metabólico alterado permite a las células cancerígenas suplir demandas metabólicas crecientes y adaptarse a los cambios ambientales.
Por ejemplo, un metanálisis reciente de casi 2.000 estudios de microarrays en el que se analizaron 22 tipos diferentes de tumores.(11) Demostró que no hay una única mutación común de los genes responsables del inicio de estos tumores, pero que en su lugar existen vías funcionales de señalización incluyendo procesos metabólicos compartidos entre varios tipos de cáncer.
Así, la intervención dietética para prevenir el inicio de tales enfermedades es una meta compleja y ambiciosa que requiere no solo conocimiento de cómo un solo alimento puede afectar un sistema biológico. Sino también cómo una mezcla compleja (como es la dieta) de alimentos puede interactuar para modular las funciones biológicas.(12)
Alteraciones específicas en las rutas metabólicas pueden generar oportunidades para diseñar nuevos enfoques terapéuticos.
Perspectivas futuras
Dada la evidencia emergente que los requerimientos dietéticos de un individuo pueden depender de sus genes heredados, podemos anticipar que se lograrán importantes avances científicos en la comprensión de las relaciones entre el requerimiento dietético y los antecedentes genéticos para optimizar la estabilidad del genoma; y que el conocimiento acumulado sobre necesidades dietéticas para genotipos específicos se utilizará para orientar las decisiones por los profesionales de esta nueva rama de la medicina preventiva en lo que podría llamarse “Clínicas de Salud del Genoma”.(13)
Conclusiones
La integración y aplicación de la genética y la tecnología genómica en la investigación de la nutrición es necesaria para desarrollar programas de investigación en nutrición que estén encaminados a la prevención y el control de las enfermedades crónicas a través de intervenciones nutricionales basadas en la genómica.
De interés es la integración de métodos computacionales pertinentes en investigación genómica nutricional; la mejora de las herramientas aplicables a la biología de sistemas; y la difusión eficaz de información derivada de la genómica a los científicos, los responsables políticos y la comunidad.
En resumen, nuevos conocimientos, producidos a partir de la interfaz de la genética. La genómica y la ciencia de la nutrición son claves para promover el desarrollo de investigaciones que permitan caracterizar la susceptibilidad genética a las enfermedades crónicas relacionadas con la dieta y las respuestas moleculares a factores dietéticos.
Conflicto de intereses
Las autoras declaran ausencia de conflicto de intereses en la elaboración y publicación del artículo.
Referencias bibliográficas
- 1. Mutch DM, Wahli W, Williamson G. Nutrigenomics and nutrigenetics: the emerging faces of nutrition. Faseb J. 005; 19(12): 1602-16.
- 2. Yaktine AL, Pool R. Nutrigenomics and Beyond: Informing the Future-Workshop Summary, N.A.O. Sciences. Editor. Washington, DC: The National Academy Press. 2007.
- 3. Garcia-Canas V, Simo C, Leon C, Cifuentes A. Advances in Nutrigenomics research: novel and future analytical approaches to investigate the biological activity of natural compounds and food functions. J Pharm Biomed Anal. 2010; 51(2): 290-304.
- 4. Minieri M, Di Nardo P. Nutrients: the environmental regulation of cardiovascular gene expression. Genes Nutr. 2007; 2(2): 163-8.
- 5. Bochner BR. New technologies to assess genotype-phenotype relationships. Nat Rev Genet. 2003; 4(4): 309-14.
- 6. Kaput J. Nutrigenomics research for personalized nutrition and medicine. Curr Opin Biotechnol. 2008; 19(2): 110-20. 7. Instituto Colombiano de Bienestar Familiar. Encuesta Nacional de la Situación Nutricional en Colombia. ENSIN 2010.
- 8. Rodríguez J RF, Peñaloza E, Eslava J, Gómez LC, Sánchez H, Amaya JL, Arenas R, Botiva Y. Encuesta Nacional de Salud 2007. Resultados Nacionales. Bogotá: Fundación Cultural Javeriana de Artes Gráficas – Javegraf. 2009.
- 9. Silveira Rodríguez MB, Martínez-Piñeiro Muñoz y Carraro Casieri R. Nutrigenómica, obesidad y salud pública. Rev Esp Salud Pública 2007; 81(5): 475-87.
Fuentes Bibliográficas
- 10. Wise C, Kaput J. A strategy for analyzing gene-nutrient interactions in type 2 diabetes. J Diabetes Sci Technol. 2009; 3(4): 710-21.
- 11. Segal E, Friedman N, Koller D, Regev A. A module map showing conditional activity of expression modules in cancer. Nat Genet. 2004; 36: 1090-8.
- 12. Lamprecht SA, Lipkin M. Chemoprevention of colon cancer by calcium, vitamin D and folate: molecular mechanisms. Nat Rev Cancer. 2003; 3(8): 601-14.
- 13. Amir RE, Amir O, Paz H, Sagiv M, Mor R, Lewis BS. Genotypephenotype associations between chymase and angiotensin-converting enzyme gene polymorphisms in chronic systolic heart failure patients. Genet Med. 2008; 10(8): 593-8.
- 14. Gómez Ayala AE. Nutrigenómica y nutrigenética. La relación entre la alimentación, la salud y la genómica. Offarm. 2007; 26(4): 78-85.
Autores
1 Sandra Perdomo, BSc, PhD. Bachelor in Science de la Universidad George Mason, Doctorado en Biología Molecular de la Universidad de Salamanca. Coordinadora del Instituto de Investigación en Nutrición, Genética y Metabolismo, Escuela Colombiana de Medicina, Universidad El Bosque, Bogotá, Colombia.
Correspondencia: perdomosandra@unbosque.edu.co
2 Diana Cárdenas, MD, MS. Médica Universidad El Bosque, Magíster en Ciencias y en Nutrición Clínica de la Universidad de París VII. Directora del Instituto de Investigación en Nutrición, Genética y Metabolismo, Escuela Colombiana de Medicina, Universidad El Bosque, Bogotá, Colombia.
Correspondencia: cardenasdiana@unbosque.edu.co
Recibido: mayo de 2011
Aceptado para publicación: mayo de 2011
RMNC 2011; 2(1): 54-58.