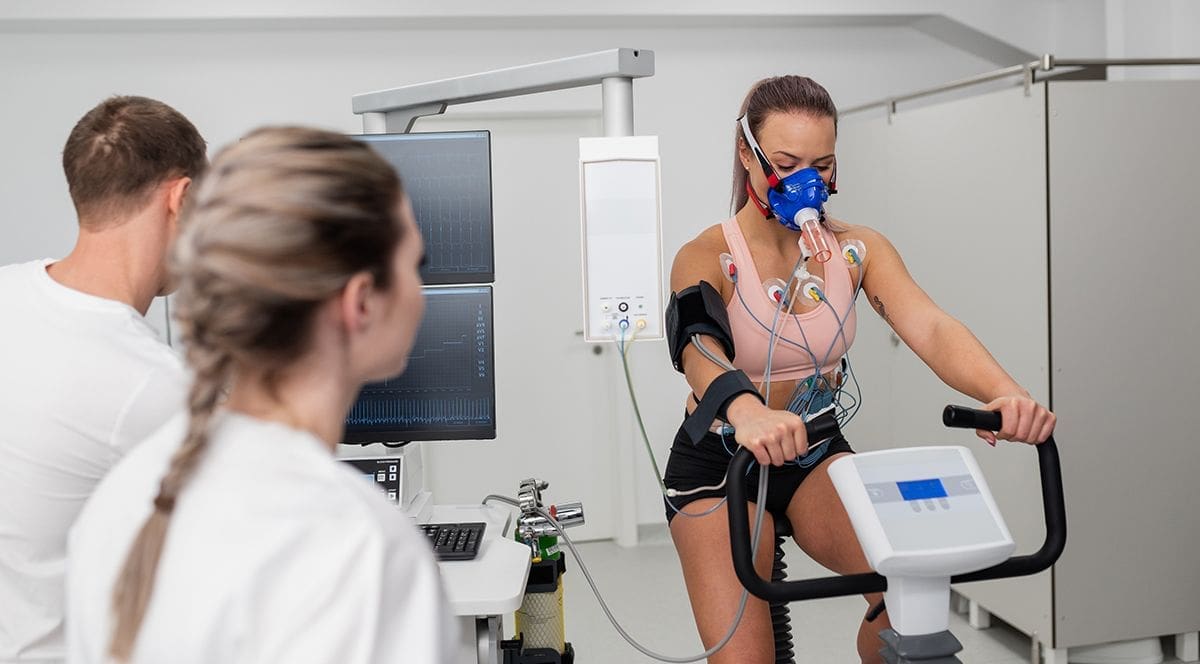
La ventilación con relación invertida (VRI) es una modalidad de soporte ventilatorio utilizada en el tratamiento de pacientes con insuficiencia respiratoria grave, especialmente en aquellos con síndrome de dificultad respiratoria aguda (SDRA). A diferencia de la ventilación convencional, en la cual el tiempo de inspiración es menor que el de espiración, en la VRI se invierte esta relación, prolongando el tiempo inspiratorio y acortando el espiratorio. Esta técnica permite mejorar la oxigenación al mantener los alveolos abiertos durante más tiempo, lo que reduce el colapso alveolar y ayuda a distribuir mejor el oxígeno en los pulmones. Sin embargo, la VRI es un método avanzado que debe ser manejado con precaución y experiencia, ya que aumenta la presión en las vías respiratorias y puede tener efectos secundarios importantes. (Lea también: Compromiso Neurológico y Síndrome de Dificultad Respiratoria Aguda en el Adulto)
María Fernanda Guzmán B., Ft.*, Marco Antonio Perafán C, MD*
* Docente Corporación Universitaria Iberoamericana
** Cardiólogo – Coordinador Cuidado Intensivo-Clínica Shaio, Bogotá
Historia de la ventilación con relación invertida
La ventilación extendiendo el tiempo inspiratorio ha sido utilizada en pacientes con Síndrome de Dificultad Respiratoria Agudo (S.D.R.A.) y en Síndrome de distress respiratorio neonatal con el objetivo de mantener un adecuado intercambio gaseoso minimizando la lesión pulmonar inducida por la aplicación de altas presiones.
El concepto de prolongar la fase inspiratoria fue investigado por primera vez en 1971 por Reynolds, quien investigó el efecto de múltiples alteraciones en el ventilador sobre el intercambio gaseoso en neonatos con membrana hialina.
En 1976 Fuelihan y cols. demostraron que en adultos con I.R.A. al adicionarse una pausa al final de la inspiración en cada ciclo mecánico, se disminuía la ventilación de espacio muerto y mejoraba la eficiencia ventilatoria.
Barotrauma e injuria pulmonar, ¿por qué IRV?:
En 1944 M.T. y C.C. Macklin describieron por primera vez la fisiopatología del barotrauma pulmonar, postulando que la ruptura alveolar ocurre cuando el gradiente de presión entre el alvéolo y el intersticio que lo rodea excede un nivel crítico.
El volutrauma afecta de 4 a 15% de todos los pacientes en ventilación mecánica, pero es más común en S.D.R.A., estatus asmático y neumonía aspirativa. Los factores de riesgo para neumotórax en S.D.R.A. aun son controvertidos, sin embargo se han considerado algunos como altos valores de Presión inspiratoria pico, presión plateau, PEEP y altos volúmenes intrapulmonares. (Vea también: Bases para el uso de broncodilatadores en lactantes)
Ventilación con presión positiva
Durante la ventilación con presión positiva la presión en la vía aérea no representa la presión en el sistema respiratorio; la presión que actúa para distender y potencialmente dañar el alvéolo es la presión transpulmonar definida como la presión alveolar (Palv) menos la presión pleural (Ppl).
Diferentes parámetros han sido utilizados como determinantes de la relación entre ventilación mecánica y volutrauma, entre ellos: PIP, PEEP, Presión plateau y VEI (volumen de fin de espiración).
Existen diversos estudios (Amato, Tharratt, Clevenger y otros) que sugieren que la PIP es el principal determinante de volutrauma, sin embargo sus resultados deben interpretarse con precaución debido a que en ellos no se menciona la magnitud del volumen corriente utilizado.
Una explicación para la relación variable entre presión en la V.A. y volutrauma es la distensión pulmonar mas que la presión aplicada en el sistema. Como resultado de este discernimiento (Polak y Adams, Hernández, Dreyfuss), se ha concluido que el volumen, más que la presión, daña el tejido pulmonar, así, el término volutrauma, más que el de barotrauma, describe en forma más exacta este efecto.
Mecanismos de lesión pulmonar inducida por ventilador
Los posibles mecanismos de la lesión pulmonar inducida por ventilador son:
1) daño producido por excesivo estiramiento de la pared alveolar,
2) disminución y/o alteración del surfactante,
3) permeabilidad capilar alta,
4) disminución de la presión perivascular intersticial asociada con la inflación pulmonar y
5) Aumento en la presión de filtración microvascular causada por incremento en la resistencia vascular pulmonar.
Principales factores que predisponen la lesión pulmonar inducida por ventilador
De lo anterior se pueden deducir los principales factores que predisponen a la lesión pulmonar inducida por ventilador:
1) PIP elevadas,
2) Presión plateau elevadas,
3) PEEP altos,
4) Altos volúmenes corrientes. Basado en estudios animales, el valor de umbral para el desarrollo de lesión del tejido se acerca a 25 a 30 cm H2O de presión de distensión (Pplat – PEEP),
5) Presión media en la vía aérea mayor de 12 mm Hg,
6) Curva de flujo cuadrada,
7) altos flujos y frecuencia respiratoria y tiempos inspiratorios cortos,
8) Altas FIO2,
9) Enfermedad pulmonar pre-existente.
La aproximación convencional a la hipoxemia refractaria en Lesión Pulmonar Aguda es el aumento progresivo del PEEP para lograr reclutamiento de unidades alveolares colapsadas y redistribución del agua pulmonar.
Extender tiempo inspiratorio
Extender el tiempo inspiratorio pretende manipular el patrón de presión aplicada para lograr reclutamiento alveolar sin sobredistensión de unidades pulmonares con constantes de tiempo normales.
Para evaluar la efectividad de esta estrategia es importante considerar la relación entre presión alveolar media (promedio de presión aplicada para provocar reclutamiento alveolar en contra de las fuerzas de retroceso elástico) y la presión que determina el volumen alveolar.
Aunque la presión alveolar no puede ser medida directamente, sí puede ser estimada a través de los cambios en la presión media de la vía aérea. Un incremento en la presión media de la V.A. puede reflejar aumento en la presión alveolar media en proporción variable dependiendo del volumen minuto y las diferencias relativas entre resistencia inspiratoria y espiratoria en la V.A.
En modelos animales se ha demostrado una relación lineal entre presión media de la V.A. y oxigenación en lesión pulmonar. La prolongación del tiempo inspiratorio puede elevar la Pva sin provocar cambios en la presión pico a V.C. y PEEP constantes.
Si el tiempo respiratorio es insuficiente la presión alveolar al final de la espiración puede aumentar por encima de la presión del PEEP particularmente en unidades con constantes de tiempo anormales.
Beneficio de prolongar el tiempo inspiratorio
Prolongar el tiempo inspiratorio puede mejorar el intercambio gaseoso por otros mecanismos diferentes a los cambios en la presión media.
Las unidades alveolares con constantes de tiempo anormales pueden no acercarse a la inflación completa durante el tiempo inspiratorio normal, adicionalmente alvéolos no ventilados pueden requerir períodos mayores de tracción para lograr su apertura; tiempos inspiratorios prolongados utilizando flujos inspiratorios promedio bajos al final de la inspiración logran disminuir el espacio muerto por mejoría de la ventilación colateral facilitando el intercambio gaseoso.
La disminución de la ventilación de espacio muerto permite la reducción del volumen minuto lo cual permite la utilización de volúmenes corrientes menores disminuyendo así la presión en el V.A.
Aunque la documentación acerca de los efectos del uso de curvas de flujo desaceleradas o de la adición de pausas al final de la inspiración aun no es concluyente, se ha observado que estos métodos tienden a mejorar la eficiencia ventilatoria en 10 a 20% con respecto a métodos convencionales (PEEP) aun cuando la relación Ti / Ttot permanezca constante. A este respecto es importante hacer notar que la IRV es diferente del PEEP el cual, para una Pva similar, tiende a acentuar la ventilación de espacio muerto.
En resumen, la IRV mejora la oxigenación a través de los siguientes mecanismos:
- Incremento en la Presión media de la V.A. y redistribución del agua pulmonar
- Mejora la ventilación de unidades previamente colapsadas
- Genera PEEPi previniendo el colapso alveolar
¿Cómo implementar ventilación con relación invertida?:
El método mas apropiado para incrementar el tiempo inspiratorio aun no se ha definido. Hasta el momento existen tres métodos: 1) Disminuir el flujo pico manteniendo un V.C. constante, 2) Pausa al final de la inspiración en ventilación controlada por volumen, 3) Flujo desacelerado.
Disminuir el flujo pico
Esta técnica puede desperdiciar la porción temprana de la inspiración permitiendo que unidades inestables se colapsen aun cuando se halla iniciado una nueva inspiración. Figura 1.
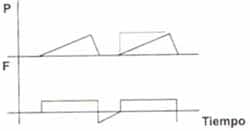
Figura No 1. El área punteada indica el inicio de la inspiración donde el lento incremento de la presión inspiratoria puede favorecer el colapso alveolar.
Pausa al final de la inspiración
Esta modalidad se utiliza cuando se desea extender el tiempo inspiratorio con modalidades controladas por volumen. Puede generar presiones pico altas, aumentando el riesgo de sobredistender unidades alveolares con constantes de tiempo normales antes de llegar a la fase estática del ciclo.
A su vez en esta última fase se debe asegurar que la presión crítica de apertura sea suficiente para mantener abiertas unidades inestables. Con este método se obtienen valores de presión media en la vía aérea superiores a los encontrados con cualquier otro método. Figuras 2 y 3b.
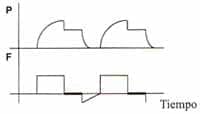
Figura No 2. Observando la morfología de la curva de flujo y las altas presiones en la parte inicial del ciclo se puede comprender el riesgo de ruptura de unidades alveolares con constantes de tiempo normales.
Flujo desacelerado
Este es el método utilizado durante la ventilación controlada por presión. El flujo es inicialmente alto como consecuencia del gradiente de presión entre la V.A. y el alveolo, a medida que el gradiente disminuye, de igual forma lo hace el flujo.
El flujo inspiratorio desacelerado resulta en una mejor distribución de la ventilación y mayor presión media alveolar a cualquier VC o Ti. La apropiada relación I:E y frecuencia respiratoria resulta en un “efecto de PEEP” donde cada nuevo ciclo se inicia antes de que finalice el flujo espiratorio.
Esta maniobra produce atrapamiento de gas e incrementa la CRF. Esta curva de flujo puede generar grandes fuerzas de cizallamiento al inicio de la inspiración aun cuando no sería así al finalizar la misma. Figuras 3a y 3b.
IRV por ventilación controlada por presión o por volumen
La IRV puede a su vez ser creada a través de ventilación controlada por presión o por volumen. La ventilación controlada por presión puede ser más segura que los modos ciclados por volumen. Puede ser mejor tolerada por el paciente y evita incrementos de la presión alveolar pico durante los períodos de respiración asincrónica o cambios en la relación I:E.
La principal ventaja es que conlleva el uso de curva de flujo desacelerada y facilita la manipulación del tiempo inspiratorio y de la relación I:E por ser un modo ciclado por tiempo.
En los modos controlados por volumen el Ti puede prolongarse aplicando una pausa inspiratoria, disminuyendo el flujo pico o utilizando curvas de flujo desaceleradas. La relación I:E no puede ser directamente programada ya que está en función del VC, flujo pico y frecuencia respiratoria.
La ventilación controlada por volumen utilizando un patrón de flujo desacelerado puede acercarse a las características de la ventilación controlada por presión pero garantizando un volumen corriente constante. El principal riesgo se deriva del monitoreo poco cuidadoso de la PIP la cual puede variar ampliamente según la impedancia del sistema o por la presencia de PEEPi.
Según lo mencionado, el método escogido para implementar IRV debe depender de:
1. Preferencias clínicas del operador para utilizar métodos que garanticen VC o limiten la PIP
2. Curva de flujo deseada
3. Familiaridad del equipo de trabajo con cada uno de los métodos
4. Tolerancia del paciente
Es relevante recalcar la importancia del uso de una adecuada sedación y/o relajación cuando se usa la relación invertida como estrategia ventilatoria. Los pacientes usualmente no toleran la IRV sin sedación porque esta no es compatible con un patrón ventilatorio normal, si se les permite respirar a una frecuencia mayor de la programada el compromiso hemodinámico y el riesgo de barotrauma aumentan en forma exponencial.
¿Hasta donde invertir la relación?
Se han utilizado con relativo éxito relaciones I:E de 1:1 hasta 4:1, sin embargo, para obtener los beneficios del Ti prolongado no siempre es necesario invertir completamente la relación. El uso de relaciones mayores de 3:1 no debe ser considerado hasta que no exista evidencia de seguridad clínica y eficacia.
Aunque la IRV ha sido tachada de peligrosa e innecesaria, ha probado ser ventajosa si se usa en forma cautelosa y monitorizando apropiadamente la presión alveolar, cuidando de mantenerla dentro de límites seguros. El uso conjunto de IRV e hipercapnia permisiva con bajos VC puede ser requerido para mantener un adecuado control sobre la PIP, presión alveolar y presión media de la VA.
¿Cuándo utilizar IRV?:
Debe considerarse en pacientes hemodiná-micamente estables con injuria pulmonar en quienes han fallado medidas tradicionales para mantener una adecuada oxigenación, es decir cuando se ha llegado a valores de PEEP mayores o iguales a 15 cm H2O, FIO2 mayor o igual a 70%, distensibilidad estática disminuida, PIP mayor de 65 cm H2O a pesar de sedación.
Es una estrategia que debe instaurarse antes de que se haga evidente un deterioro franco de la oxigenación. Puede observarse mayor hipoxemia cuando se inicia la IRV, al igual que ocurre cuando se cambia de modo ventilatorio.
Si se tiene en cuenta que uno de los principales mecanismos de acción de la IRV es el incremento del volumen pulmonar promedio reflejado a través de la presión media de la VA se explica el retardo (horas) que existe entre el momento de implementación de la IRV y el máximo beneficio reflejado en la PaO2.
Complicaciones de la IRV
1. Hiperinflación dinámica: La magnitud de la misma es difícil de predecir y puede variar de un paciente a otro. El grado de hiperinflación puede acentuarse en unidades con alta resistencia al flujo espiratorio. En patologías con marcadas diferencias regionales la medición del PEEPi puede no reflejar el grado real de atrapamiento de aire en algunas regiones pulmonares.
2. Excesivos valores de presión media alveolar pueden causar efectos deletéreos en el tejido pulmonar. El tiempo inspiratorio prolongado con o sin atrapamiento de aire puede exacerbar el riesgo de barotrauma.
3. El gasto cardíaco y el DO2 pueden disminuir a medida que el PEEPi y la presión media en la VA se incrementan. Diversos estudios concluyen que la incidencia de efectos hemodinámicos adversos relacionados con IRV pueden ser impredecible.
4. El uso de sedación y/o relajación prolongada conlleva por sí mismo el riesgo potencial de atrofia muscular y síndrome de desacondicionamiento.
5. En ventilación controlada por presión y relación invertida pueden presentarse atelectasias en presencia de bajas distensibilidades pulmonares.
Bibliografia
1. Amato MB, Barbas CS, Medeiros DM., et al. Beneficial effects of the “open lung approach” with low distending pressures in acute respiratory distress syndrome. Am J Respir Crit Care Med 1995;152:1835
2. Delgado E, Hoffman LA. Pressure control ventilation: Practical steps for patient management, Critical Care Alert, 2000;8:6-8.
3. Hyzy RC, Propovich J. Alternate modes of mechanical ventilation, Up to Date, Jan. 12, 1999.
4. Gurevitch MJ. Inverse ratio ventilation and the inspiratory/expiratory ratio. In: Stock MC, eds. Handbook Of Mechanical Ventilatory Support. 1997;165:172.
5. Kirton OC. Ventilatory support modes. In: Civetta JM, Taylor RW, Kirby RR, eds. Critical Care. 1997;49:755.
6. Marcy TW. Inverse ratio ventilation. In: Tobin MJ. Principles and practice of mechanical ventilation. 1994;319:331.
7. Marini JJ. Mechanical Ventilation and newer ventilatory techniques. In: Bone R. Pulmonary Critical Care 1998:745.
8. Sandur S, Stoller JK. Pulmonary complications of mechanical ventilation. Clinics in Chest Medicine 1999;20:223-47.