Ventajas y Desventajas de la Vía Traansdérmica
Introducción
Tradicionalmente los estrógenos usados en la terapia hormonal de reemplazo (THR) han sido dados por vía oral, y los diferentes estudios en el mundo han podido evaluar sus beneficios en el mejoramiento de los síntomas climatéricos, aparato cardiovascular y hueso, así como sus efectos secundarios sobre los cálculos y triglicéridos1.
La introducción de otras formas terapéuticas se inicia con el desarrollo por parte de laboratorios CIBA Pharmaceutical, Sumit NJ, del sistema transdérmico para los estrógenos (TTS) en 19882.
Estos primeros parches se desarrollaron en una matriz donde el 17-b-estradiol se encontraba en un medio alcohólico y una membrana con microporos que controlaba su liberación, recomendándose una aplicación dos veces por semana.
Posteriormente, se mejora esta forma farmacéutica utilizando una matriz más delgada, monolítica, en un medio no alcohólico, y un nuevo adherente como la bentonita, mejorando la absorción, adherencia y con menos irritación local, de Laboratorio Cilag de Suiza (System, Menorest), llamados los parches de la segunda generación3.
Ingresan recientemente dos nuevas formas farmacéuticas de aplicación del 17-b-estradiol. Una desarrollada en Argentina a través de los Laboratorios Wyeth-Ayerst International y Ciba Pharmaceutical Company (Climaderm)4 y la otra por los laboratorios Berlex, Wayne, NJ de los Estados Unidos (Climara-Lindisc)5, donde el reservorio se encuentra en una base de poliéster-polietileno.
Las diferentes características de estas formas terapéuticas transdérmicas se muestran en la Tabla 1.
Tabla 1. Características de las diferentes generaciones de parches transdérmicos
RESERVORIO MEMBRANA LIMITANTE |
MONOLÍTICO 2 GENERACIÓN |
MONOLITICO 3 GENERACION |
|
Composición |
alcohol |
bentonita |
polietileno poliester |
Adhesivo |
anular |
100% superficie |
100% superficie Publicidad |
Incremento |
volátil |
fijo |
fijo |
Permeación |
|||
Membrana |
si |
no |
no |
Limitante |
|||
Niveles plasmáticos |
fluctuantes |
fluctuantes |
constantes |
Recambio |
72-92 horas |
72-92 horas |
168 horas |
Desprendimiento |
15% |
10-5% |
5-3% |
Aspecto |
opaco |
transparente |
translúcido |
Area activa |
10 cm |
16 cm |
15 cm |
Efectividad de la vía transdérmica en el síndrome climatérico
Oleadas de Calor:
Se sabe que al llegar la menopausia los niveles de estrona (E1) y estradiol (E2) disminuyen a valores de 30-70 ng/L y 5-20 ng/l respectivamente, cuando en fase folicular oscilaban entre 170-200 y 200-400 ng/L.
Cuando dicha concentración de estradiol se encuentra por debajo de 30-20 ng/L aparecen el cortejo de síntomas descrito en el síndrome climatérico, que incluye oleadas de calor, resequedad de piel y mucosas, trastornos del comportamiento como irritabilidad, depresión, angustia, artralgias, disminución de la libido y modificaciones en el aparato genito-urinario.
Tanto la vía oral como la transdérmica han mostrado efectividad en disminuir en un 50% las oleadas de calor después de 3 semanas de tratamiento cuando los niveles de estradiol están por encima de 60 pg/ml, y cesan completamente cuando están por encima de 122 pg/ml, confirmado por análisis estadístico de regresión lineal6.
Otros autores han encontrado que no sólo disminuye las oleadas de calor después de tres meses, sino que mejora las alteraciones del sueño, la ansiedad y la irritabilidad.
Erkola y col, en un estudio abierto multicéntrico en 249 mujeres finlandesas después de 6 meses de tratamiento, las oleadas de calor disminuyeron de 85% a 5.7%7.
– Atrofia Urogenital:
La segunda causa como motivo de consulta es la resequedad vaginal y molestias al orinar debido a la atrofia de este tejido. La vía transdérmica a dosis de 50ug ha mostrado ser útil en la primera semana de uso.
Algunas mujeres necesitan aumentar la dosis a 100 ug o la ayuda con aplicación local8. Los estudios comparativos con la vía oral no han mostrado diferencia significativa y la citología vaginal funcional es un buen método de seguimiento en la respuesta terapéutica.
– Síntesis proteica hepática:
El que el estradiol en la vía transdérmica pase a la circulación general evitando el primer paso hepático, los efectos sobre las diferentes globulinas transportadoras no se modifican como: los sustratos de renina, globulina transportadora de hormonas sexuales (SHBG), globulina unida a la tiroxina (TBG) y la globulina unida al cortisol (CBG)9.
Estos datos permiten afirmar que esta vía no altera los patrones de tensión arterial y las hormonas podrán viajar en su forma libre.
– Tensión arterial:
Inicialmente las primeras investigaciones mostraban que no modificaban la T. Arterial; con estudios a largo plazo se ha visto una disminución tanto de la TA. sistólica como diastólica, con o sin acetato de medroxiprogesterona10-11.
Tabla 2. Porcentaje de cambios de las fracciones lípidas en un estudio comparitivo vía oral Vs transdérmicas*
|
|
VE2+ NETA ORAL |
TTS+MPA VALOR DE P |
TRANSDÉRMICO |
VALOR DE P |
COLESTEROL |
||||
HDL2 |
<17 |
<0.001 |
<6 |
p<0.05 |
HDL3 |
sin cambio |
|||
HDL2b |
<30 |
<0.001 |
||
HDL2a |
<26 |
<0.001 |
||
HDL3a |
<15 |
<0.001 |
<14 |
p<0.01 |
HDL3b |
<12 |
p<0.01 |
||
HDL3c |
<17 |
p<0.01 |
||
TRIGLICERIDOS |
||||
Apo AI |
<5 |
<0.05 |
sin cambio |
|
Apo AII |
sin cambio |
<8 |
p<0.001 |
|
Lp AI |
sin cambio |
<8 |
p<0.001 |
|
Lp AII |
sin cambio |
<5 |
p<0.05 |
|
Lipasa hepática |
<12% |
p<0.05 |
sin cambio |
|
Proteina transportadora |
||||
Ésteres de colesterol |
sin cambio |
sin cambio |
– Hidratos de carbono:
Al comparar la respuesta al test de glucosa después de 3 meses de tratamiento con 50 ug TTS y estrógenos conjugados, se evidencia una disminución de los niveles de insulina en ayunas y un incremento del péptido C con la vía transdérmica y no con la vía oral.
Estos datos demuestran que aumentan la depuración de insulina a nivel hepático12 y una mayor excreción a nivel renal13.
Tabla 3. Ventajas y desventajas de la vía transdérmica
VENTAJAS -1 |
DESVENTAJAS 22-23 |
|||
|
AREA sanguíneo |
EFECTO hormona natural |
EFECTO% local |
1G 24 |
3G 15 |
|
Intestinal |
< náusea |
eritema |
16 |
13 |
|
Hepático |
< inducc. proteinas |
sitémico |
20 6 |
10 4 |
|
Depuración |
Niveles estables |
otros |
– Lípidos:
inicialmente y a corto plazo (3 meses) la vía transdérmica no modifica los parámetros lipídicos, sinembargo, en estudios a largo plazo (48 meses) se observa una disminución de la LDL sin modificación ni en las HDL ni en los triglicéridos10.
Un estudio reciente en 60 mujeres post-menopáusicas durante 12 meses, compara la vía oral (Valerato de E2+Noretisterona (NETA) vs (TTS50 + MPA10 mg cíclico) y su efecto sobre las fracciones lipídicas14 tabla 2, y evidencia múltiples cambios en las subfracciones lipídicas donde se creía que la vía transdérmica no las modificaba.
– Factores de coagulación:
Dados los pocos efectos sobre las proteínas hepáticas, la vía transdérmica no modifica los factores de coagulación como Antitrombina III, Fibrinopéptido A ni el fibrinógeno de alto peso molecular. Sin embargo, un estudio comparativo por vía oral (estrógenos conjugados n= 9 vs TTS 50 n= 13 ) evaluando diferentes parámetros de coagulación durante 3 meses, demuestra que la TTS50 aumenta el fibrinopéptido A significativamente (p<0.001) con disminución de la Proteína C (p<0.05), sin cambios en la función plaquetario ni en la actividad fibrinolítica15.
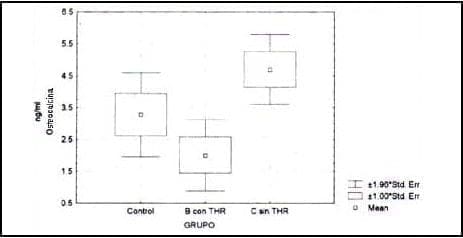
– Metabolismo óseo:
La pérdida de hueso después de la menopausia se ha calculado en 1% por año. La evaluación disponible se ha realizado sobre los marcadores de formación osteocalcina sérica, fosfatasa específica para hueso, propéptido colágeno I), de resorción (hidroxiprolina, piridinolina urinarias y fosfatasa tartrato resistente).
En el comportamiento del metabolismo óseo se ha tenido en cuenta la relación Calcio/creatinina urinaria o OH-Prolina piridinolina /creatinina urinaria, los que disminuyen a medida que pasa la edad.
Como métodos de mayor sensibilidad y especificidad han sido útiles las mediciones radiológicas por densitometría de Rx, de fotón simple o fotón dual16. Los estudios comparativos abiertos, aleatorizados, doble ciego o contra placebo han demostrado un aumento entre 1.5%-2.5% de cambios en la densidad mineral ósea a nivel lumbar y de fémur, con disminución de la relación calcio/creatinina urinaria o hidroxiprolina/creatinina urinaria17-18. Otros por el contrario no han evidenciado cambios ni en la fosfatasa alcalina ni en los parámetros urinarios9.
Recientemente, un estudio comparativo entre la vía transcutánea (gel), y la transdérmica a dosis TTS25-TTS50 en 44 mujeres postmenopáusicas menores de 67 años y 27 mayores de 67 años, durante 2 años, mostró su protección sobre la masa ósea, y las principales modificaciones se hallaron en el procolágeno tipo 1 que disminuyó al año de tratamiento con modificaciones variables en el procolágeno tipo III. Los niveles de estradiol alcanzados en ambas preparaciones oscilaron en los 83.8 pmol/l19.
– Endometrio:
Hay evidencia que dosis de TTS 5O produce proliferación a nivel endometrial. La recomendación del uso de un progestágeno en forma cíclica (MPA 5mg, NETA 1 mg, Medrogestone 5mg) reduce la hiperplasia de un 42% al 4%. En forma cíclica, la hemorragia se presenta en un 66.3%20.
– Experiencia en Colombia.
Existen dos estudios, uno como parte de un ensayo multicéntrico y aleatorizado, donde se compara: n=8, TSS50+MPA 5mg continuo VS n=11, NTTS (climaderm +MPA 5mg continuo) en mujeres postmenopáusicas durante un año.
Se evaluaron los principales síntomas y paraclínicamente química sanguínea, perfil lipídico y evaluación del metabolismo óseo, demostrándose a pesar del número pequeño de casos una disminución de las oleadas de calor en 50% a los 3 meses, una mejoría significativa en la citología vaginal funcional, una tendencia a disminuir el colesterol total, sin modificaciones en las HDL, LDL ni triglicéridos.
En el metabolismo óseo existe una tendencia a disminuir la fosfatasa alcalina y aumenta la D-oxipiridinolina sin ser significativa.
La densitometría mostró un aumento significativo en la densidad mineral ósea con ambos regímenes a nivel lumbar, trocanter y fémur. La biopsia endometrial no se modificó en los cambios proliferativos encontrados inicialmente21.
El otro estudio se encuentra en ejecución, multicéntrico, abierto, con una nueva matriz NTTS (menorest), donde se evalúa la aceptabilidad y comportamiento de algunos síntomas en mujeres postmenopáusicas.
Ventajas y desventajas
Las ventajas de la vía transdérmica se desprenden de su mecanismo de acción, al evitar el primer paso hepático influye sobre todo los procesos metabólicos: es el estrógeno natural, mínima dosis, mantiene niveles E2/E1 más estables que la vía oral, sin molestias gástricas, no incrementa los cálculos vesiculares, ni el sustrato renina -angiotensina y la aceptación es buena1.
Como desventaja, se anota tensión mamaria, hemorragia vaginal más en los tratamientos cíclicos (66%) que en los continuos (15%), con un promedio de 20% según el parche de 1 generación (1G) o de tercera generación (3G). La irritación local oscila en un 5-15% de acuerdo a la generación del parche22-23 Tabla 3.
El precio de esta forma terapéutica es alto en los diferentes países y en nuestro medio oscila entre $ 30.000 y $ 52.000/mes, por lo que sólo puede ser adquirido por una parte de la población productiva del país.
Bibliografía
- 1. Nachtigall L. Emerging delivery systems for estrogen replacement: aspects of transdermal and oral delivery. Am J Obstet Gynecol 1995; 173: 993-997.
- 2. Sitruk-Ware R. lnnovative technology for hormonal replacement therapy. Maturitas 1988; 10: 79-81.
- 3. System, Menorest.
- 4. Baracat E, Haidar M, Castelo A. et al. Comparative bioavaliability study of an once-a-week matrix versus a twice-a-week reservoir transdermal estradiol delivery systems in postmenopausal women. Maturitas 1996; 23: 285-291.
- 5. Gorden SF. Clinical experience with a seven-day estradiol transdermal system for estrogen replacement therapy. Am J Obstet Gynecol 1995; 173: 998-1004.
- 6. Steingold KA, Laufer Y, Chetkowski RJ et al. Treatment of hot flashes with transdermal estradiol administration. J Clin Endocrinol Metab 1985; 61: 627-632.
- 7. Erkkola R, Hollma P, Jarvi T et all. Transdermal oestrogen replacement therapy in a finnish population. Maturitas 1991; 13: 275-281.
- 8. Padwich MI, Endacott J, Whitehead Ml. Efficacy, acceptability and metabolic effects of transdermal estradiol in the management of postmenopausal women. Am J Obstet Gynecol 1985; 152: 1085-1091.
- 9. Selby PT, McGarrigle HHG, Peacock M. Comparison of the effects of oral and transdermal oestradiol administration on oestrogen metabolism, protein synthesis, gonadotrophin release, bone turnover and climateric symptoms in postmenopausal women. Clin Endocrinol 1989; 30: 214-249.
- 10. Pang SC, Greendale GA, Cedars MI, et al. Long-term effects of transdermal estradiol with and without medroxyprogesterone acetate. Fertil Steril 1993; 59: 76-82.
- 11. Akkad AA, Hallingan AW, Abrams K et al. Differing response in blood pressure over 24 hours in normotensive women eceiving oral or transdermal estrogen replacement therapy. Obstet Gynecol 1997; 89: 97-103.
Referencias
- 12. Cagnacci A, Soldani R, Camero PL et al. Effects of low doses of transdermal 17-b-estradiol on carbohydrate metabolism in post-menopausal women. J Clin Endocrinol Metab 1992; 74: 1396-1440.
- 13. Mueck AO, Seeger H, Armbruster FP et al. Urinary excretion of insulin after estradiol treatment of postmenopausal women. Clin Exp Obstet Gynecol 1997; 24: 11-13.
- 14. Tilly-Klesi M, Karl J, Pyorala T et al. Responses of HDL subclasses, Lp (A-l) and Lp (A-I: A-II) levels and lipolytic enzimes activities to continuous oral estrogen-progestin and transdermal estrogen with cyclic progestin regimens in postmenopausal women. Atherosclerosis 1997; 129: 249-259.
- 15. Pinto S, Bruni V, Rosati D et al. Effects of estrogen replacement therapy on thrombin generation. Thromb Res 1997; 85: 185-193.
- 16. Calvo MS, Eyre DR, Gundberg CM. Molecular basis and clinical application of biological markers of bone turnover. Endocrin Review 1996; 17: 333-369.
- 17. Stevenson JC, Cust MP, Gangar KF et al. Effects of transdermal versus oral hormone replacement therapy on bone density in spine and proximal femur in postmenopausal women. Lancet 1990; 336: 265-269.
- 18. Field CS, Ory SJ, Wahner HW et al. Preventive effects of transdermal 17b-estradiol on osteoporotic changes after surgical menopause: a two-year placebo controlled trial. Am J Obstet Gynecol 1993; 168: 114-121.
- 19. Sharp CA, Evans SF, Ristelli L et al. Effects of low and conventional dose transcutaneous HRT over 2 years on bone metabolism in younger and older postmenopausal women. Eur J Clin Invest 1996; 26: 763-771.
- 20. Clisham PR, Celdars MI, Greendale J et al. Long-term transdermal estradiol therapy: effects on endometrial histology and bleeding patterns. Obstet Gynecol 1992; 79: 196-201.
Fuentes
- 21. Onatra W, Sánchez J. Evaluación abierta, aleatoria de la eficacia y seguridad de una nueva matriz (NTTS – Climaderm) una vez por semana vs TTS50, dos veces por semana como terapia hormonal de reemplazo en mujeres postmenopáusicas. lnforme preliminar. (En prensa, Rev Col Men).
- 23. McCarthy T, Dramusic V, Ratnam S. Use of two types of estradiol-releasing skin patches for menopausal patients in a tropical climate. Am J Obstet Gynecol 1992; 166: 2005-2010.
- 24. Baracat E, Yamada S, Haidar M et al. Evaluation of skin tolerability in patients on a 7 day regimen of a new matrix transdermal estradiol delivery system an open label study. Curr Ther Res 1997; 58: 417-427.