Énfasis en la Menopausia
Recibido para publicación: mayo 2 de 2011. Revisado y aceptado: junio 12 de 2011
MARTHA CIFUENTES ACUÑA*, GUSTAVO GÓMEZ TABARES**
Nuevos hallazgos en el complejo circuito metabólico de la homeostasis de la energía han refinado nuestro entendimiento de la fisiopatología de la obesidad, basado en la identificación de nuevas funciones de péptidos que se descubrieron hace varias décadas.
El número de moduladores periféricos del apetito se ha incrementado rápidamente en la última década e incluye: leptina, ghrelin, colecistoquinina, péptido YY (PYY), insulina, polipéptido pancreático, péptido similar al glucagón 1 (GLP-1)65-72.
La leptina, una hormona de los adipositos, es un indicador de almacenamiento de energía y actúa en el hipotálamo para reducir la ingesta de alimentos y aumentar el gasto energético.
La ghrelin, el péptido YY, el polipéptido inhibidor gástrico, GLP-1, la colecistoquinina, el polipéptido pancreático y la amilina se liberan en la vía gastrointestinal y el páncreas en respuesta al consumo de nutrientes. Todos, menos dos, inhiben la ingesta. La dos excepciones son la grelin, que estimula el hambre, y polipéptido inhibidor gástrico, que puede promover el almacenamiento
de energía.
Se sabe que la hormona estimulante de los melanocitos (MSH), que es un péptido derivado de la Pro opio melanocortina y reconocida por su papel en la pigmentación de la piel a través de la actividad del receptor de la melanocortina1 (MC1R), disminuye la ingesta de alimentos y aumenta el gasto de energía a través de interacciones en el hipotálamo con otro receptor de la melanocortina, MN4R.
En el ratón la delección del gen de MC4R resulta en hiperfagia e hiperinsulinemia y reduce el gasto de energía. La delección de Mc3r, otro gen que codifica receptor de melanocortina y que está altamente expresado en el hipotálamo y el sistema límbico, también resulta en aumento de la adiposidad debido a la disminución del gasto de energía pero no causa hiperfagia.
Aunque la susceptibilidad a la obesidad común es poligénica, mutaciones en MC4R se encuentran en aproximadamente uno a siete por ciento de humanos con IMC de más de 40 y quienes llegan a una obesidad severa antes de los 10 años de edad.
Antagonismos de signos anorexigénicos (supresores del apetito) de la melanocortina es causada por péptidos orexigénicos (estimulan el apetito), como las proteínas agutí relacionadas y neuropéptido y que está coexpresado en un diferente subgrupo de neuronas dentro del hipotálamo.
La proteína agutí relacionada antagoniza la interacción entre la hormona estimulante de los melanocitos-y el MC4R, y el neuropéptido y disminuye la expresión del gene que codifica la proopiomelanocortina (POMC).
Varios polimorfismos en el gen que codifica la proteína agutí relacionada (AGRP) han sido asociados con protección contra la obesidad o con anorexia nervosa. El neuropéptido y también disminuye la síntesis de hormona liberadora de TSH y aumenta la síntesis de hormona concentrada de melanina, otro péptido orexigénico.
Las concentraciones circulantes de leptina e insulina influyen esos mecanismos centrales que controlan la ingesta de alimentos y gasto de energía.
La concentración de leptina en la sangre está altamente relacionada con la masa grasa total; las personas obesas tienen altas concentraciones de leptina El exceso de grasa corporal que resulta en una producción aumentada de leptina puede ser actualmente una corrección para un daño primario o secundario de señal de transducción hipotalámica inducida por la leptina.
La disminución de la grasa corporal que ocurre con pérdida de peso inducida por la dieta causa disminución de las concentraciones de leptina y dispara la respuesta que ayuda a conservar la grasa corporal. Al final, la masa de grasa corporal refleja avance a largo plazo entre el gasto de energía y la ingesta de energía. Esta última parece tener el papel predominante en mantener este balance.
¿Cómo decide el organismo cuándo y cuánto comer? Las señales a largo plazo asociadas con el almacenamiento de grasa corporal son dadas por la leptina y la insulina. Estas moléculas circulantes también modulan las señales a corto plazo que determinan el inicio y el final de la alimentación.
Las señales que proveen información a corto plazo acerca de hambre y saciedad incluyen hormonas intestinales, tales como colecistoquinina, ghrelin y péptido YY (PYY) y señales de neuronas vágales referentes dentro del tracto gastrointestinal que responden a deformación mecánica, macronutriente, pH, tonicidad y hormonas.
Los signos neurales y humorales se integran en regiones específicas del hipotálamo y tallo cerebral. Un estudio reportó que el PYY es un péptido secretado postrandialmente, en proporción a las calorías ingeridas, por las células endocrinas que tapizan el intestino delgado y el colon.
Los investigadores encontraron que la simple infusión de PYY, comparada con una infusión de solución salina, reduce el apetito y el consumo de alimentos en aproximadamente el 30% en un bufet, “todo lo que pueda comer”, provisto dos horas después de la infusión.
En el sujeto obeso, comparada con los sujetos delgados, la respuesta postprandial a PYY está disminuida aunque los sujetos obesos consumieron un mayor número de calorías. La infusión de PYY redujo el hambre en los grupos deobesos y delgados y no tuvo efecto en el sabor agradable de las comidas o sus sensaciones de náuseas.
La liberación inicial de PYY ocurrepoco después de la ingesta de la comida, presumiblemente a través de mecanismos neurales, antes de que los alimentos ingeridos lleguen a la porción distal del intestino delgadoy el colon. La liberación subsecuente de PYY es estimulada por los nutrientes, particularmente carbohidratos y lípidos, dentro del lumen de la porción distal de intestino delgado y el colon.
El PYY disminuye la ingesta de alimentos a través de la inhibición de la motilada intestinal (actuando como “freno ileal” para causar unasensación de saciedad) y por vía de neuronas vágales aferentes que ascienden del tracto gastrointestinal al cerebro posterior e interaccionan con receptores humorales en el hipotálamo.
En estudios animales el PYY inhibe el neuropéptido e hipotalámico –expresando neurona y proteínas gauti relacionadas– expresando neuronas a través de receptores y dos inhibitorios, desinhibiendo así las neuronas adyacentes que expresan proopiomelanocortina y disminuyendo la ingesta de alimentos FIG.
El estudio de Batteham y col. también mostró que la infusión de PYY disminuye las concentraciones en ayunas del péptido orexigénico ghrelin. Este es un péptido de 28 aminoácidos, asilado, secretado por células oxínticas en elfondo del estómago. La ghrelin actúa sobre los receptores secretagogos de la hormona del crecimiento (GH) para incrementar la liberación de GH por la pituitaria.
Recientemente, se ha identificado el papel putativo de la ghrelin en la homeostasis de la energía y, particularmente, cuando hay hambre y en la iniciación de la alimentación. Las concentraciones de ghrelin circulantes aumentan preprandialmente y disminuyen posprandialmente.
La ghrelin aumenta la ingesta de alimentos a través de la estimulación de receptores de ghrelin sobre el neuropéptido e hipotalámico, que expresa neuronas y proteínas gauti relacionadas.
Aunque la infusión de PYY reduce las concentraciones de ghrelin en sujetos delgados y obesos que están en ayunas y disminuye el aumento preprandial de ghrelin en sujetos delgados, no es claro si la extensión de tal supresión de ghrelin contribuye a la reducción en la ingesta de alimentos mediada por PYY, no es clara.
¿Podrán ser manipuladas las señales de hambre de ghrelin y las señales de saciedad de PYY?
Estudios de eliminación de genes en los ratones revelan que uno no puede fácilmente copar los mecanismos homeostáticos para mantener la grasa corporal; eliminación experimental del gen ghrelin, ag RP, y una doble eliminación de AgRP y Npy no están asociados con ningún efecto obvio sobre el metabolismo energético o la ingesta de alimentos.
En contraste, la mutación inactivante de POMC, el gen que codifica leptina y el receptor de leptina, y MC4R, producen profundo fenotipo obeso en ratones como también en humanos (figura 1).
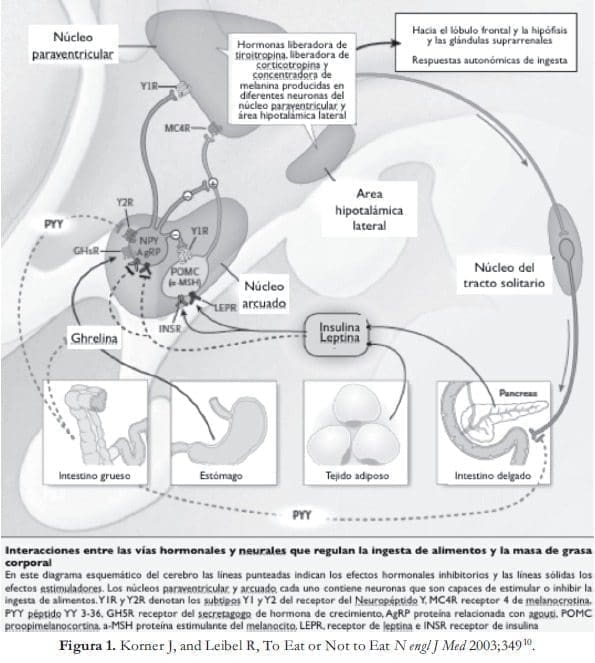
Parece que las vías orexigénicas son muy críticas para sobrevivir y la ausencia de un péptido es compensada por la acción de otros. Estudios de hormonas intestinales después de pérdida de peso por dieta o cirugía han dado algunas pistas sobre terapia con fármacos.
La pérdida de peso por restricción calórica está asociada con un aumento del hambre y concentraciones aumentadas de ghrelin. Después del bypass gástrico, el hambre disminuye, los niveles de ghrelin disminuyen y la concentración de PYY circulantes aumenta.
Los cambios hormonales después del bypass quirúrgico pueden, por lo tanto, jugar una parte en la supresión del hambre y el mantenimiento a largo plazo de la reducción de peso corporal.
Aunque inyecciones individuales de PYY intraperitoneales disminuyen la ingesta de alimentos por más de siete días en la ratas, los resultados de una simple infusión en humanos no se pueden extrapolar para predecir resultados a largo plazo.
El uso de PYY puede prevenir mecanismos contrarregulatorios de estimulación predominante de vías anoréxicas. Sin embargo, el desarrollo de anticuerpos o taquilaxis a través de “down regulation” del receptor puede limitar la eficacia de administración prolongada de PYY.
No parece que ninguna otra molécula derivada pueda proveer la acción mágica para inducir y mantener la pérdida de peso.
El tratamiento farmacológico exitoso para obesidad puede ser posible solamente actuando en varios objetivos y sistemas redundantes que conducen la ingesta de alimentos y actúan para resistirse a la pérdida grasa corporal.
La restricción calórica resulta en una rápida y profunda reducción de leptina circulante y gasto de energía y aumento del apetito73.
La compensación que los cambios de los mediadores del apetito provocan en la circulación para fomentar la recuperación del peso después de la disminución de peso inducida por la dieta no vuelve a los valores basales hasta dentro de los doce meses después de la reducción de peso inicial74,75.
Aspectos Nutricionales de la Obesidad
A todos estos cambios metabólicos que sufre la mujer en su etapa de menopausia, los cuales están directamente relacionados con el favorecimiento de la ganancia de peso y el desarrollo o agravamiento de la obesidad, se suman otras causas que igualmente facilitan esta ganancia de peso como son el desequilibrio en la ecuación de energía que introduce el proceso de envejecimiento, los inadecuados hábitos alimentarios y la reducción del gasto energético ligado a un estilo de vida sedentario.
Estos son importantes factores de riesgo de padecer o desarrollar sobrepeso u obesidad, independientes del hipoestrogenismo.
Un peso corporal no saludable se encuentra vinculado directamente con la mortalidad y, específicamente, una distribución inadecuada de la grasa (obesidad central o visceral), que se observa durante esta etapa de la vida de la mujer, se encuentra asociada a la insulinorresistencia; esta favorece, padecimientos crónicos como las cardiopatías, las dislipidemias, la hipertensión, el accidente cerebrovascular, la diabetes, las colecistopatías, la esteatosis hepática no alcohólica, la apnea del sueño, la artrosis y algunos tipos de cáncer hormono-dependientes.
Son varios los estudios que evidencian que la obesidad está relacionada con la mortalidad en mujeres1-6. Otros estudios han mostrado que un índice de masa corporal (IMC) entre 20,5 y 24,9 está relacionado con una mayor longevidad7-12.
Metabólicamente, la obesidad es considerada insana ya sea favoreciendo la aparición de varias patologías o empeorándolas en la medida que se incrementa el IMC a lo largo del ciclo de vida13-20. Así mismo la obesidad es igualmente un factor de riesgo para una mala cicatrización de las heridas y una mala respuesta de anticuerpos a la vacuna de la hepatitis B.
Los costos generados por el sobrepeso y la obesidad son muy altos, en Estados Unidos se estima que aproximadamente el 10% de los gastos médicos están derivados de ella, lo que equivale a 92.600 millones de dólares anuales21.
Igualmente el costo económico es muy significativo en otros países desarrollados como Francia, Países bajos y Australia22. A estos costos se les deben sumar los costos indirectos y los costos intangibles.
Los costos indirectos, que llegan a ser mucho mayores que los directos, incluyen los días de trabajo perdido, las visitas al médico, las pensiones por discapacidad y la mortalidad prematura. Los costos intangibles, como la menor calidad de vida, son también enormes.
En nuestro país, la Encuesta Nacional de la Situación Nutricional en Colombia23 indica que aumenta el exceso de peso en los colombianos adultos, en edades comprendidas entre 18 y 64 años. Se observó que uno de cada dos colombianos presenta exceso de peso.
Es preocupante como las cifras de exceso de peso (incluye sobrepeso más obesidad, es decir, IMC > de 25 kg/m2) aumentaron en los últimos cinco años en 5,3 puntos porcentuales (2005: 45,9% y 2010: 51,2%). Gráfico 1.
En las mujeres es mayor el exceso de peso frente a los hombres (55,2% frente a 46,5%). La mayor prevalencia de exceso de peso se presenta en el área urbana (52,5%), lo que supera el promedio nacional. Los departamentos con mayor prevalencia de exceso de peso son San Andrés y Providencia (65,0%), Guaviare (62,1%), Guainía (58,9%), Vichada (58,4%) y Caquetá (58,8%).
Respecto a la obesidad abdominal como factor de riesgo de enfermedades metabólicas y cardiovasculares, esta se encuentra presente en el 62% de las mujeres frente a un 39,8% en los hombres.
Esta proporción se incrementa a mayor edad y son más altas en la población de 50 a 64 años (84,1% mujeres frente a 60,1% hombres). En el grupo de las mujeres la prevalencia de obesidad abdominal fue mayor en el área rural. Los departamentos con mujeres con mayor prevalencia de obesidad abdominal fueron Tolima (72,9%), San Andrés y Providencia (72,1%), Cundinamarca (72,0%), Vichada (70,5%) y Arauca (69,9%). Gráfico 2.
Teniendo en cuenta todas las implicaciones que sobre la salud pública tienen el sobrepeso y la obesidad a nivel nacional, esta representa un desafío en aumento para la salud pública, lo cual ubica a la nutrición en un primer plano en las políticas y los programas de salud pública actuales.
Es imperativo generar políticas y estrategias que faciliten el logro de un peso corporal saludable a lo largo del ciclo de vida, en los seres humanos. Los objetivos de la Healthy People 2010 reconocen las implicaciones que tienen la obesidad y el sobrepeso sobre la salud pública y han determinado los objetivos nutricionales que fomentan el logro de un peso saludable y su consecuente reducción en el riesgo de desarrollar ECNT asociadas a la dieta y al peso.
Tendencias
La génesis de la obesidad es compleja, en ella se encuentran relacionados los estilos de vida, el medio ambiente y los genes. Aunque los factores genéticos pueden incrementar la susceptibilidad a la obesidad, es poco probable que esta se instaure si no existe un desajuste en el estilo de vida y la estructura genética.


El sobrepeso y la obesidad son la consecuencia de un desequilibrio entre la energía consumida y la que se gasta (alimentos consumidos y la práctica regular de actividad física).
La industrialización, la urbanización y la mecanización han impactado en forma negativa los estilos de vida de las diferentes sociedades a nivel mundial. Diferentes datos confirman que existe un cambio en los patrones de consumo sin observarse cambios en los patrones de actividad física.
Existe actualmente un periodo de transición nutricional en nuestro país, el cual se caracteriza por un consumo de dietas con muy alto valor calórico y baja densidad nutricional.
Favoreciendo incremento de la obesidad, la cual muchísimas veces se observa ligada a desnutrición crónica. Cada vez es mayor el consumo de raciones grandes de alimentos, el consumo de alimentos por fuera del hogar, mayor consumo de alimentos ricos en grasas y energía, sumado todo esto a estilos de vida sedentarios.
Estos regímenes no ofrecen un perfil nutricional adecuado, facilitando carencia de micronutrientes e igualmente no proporcionando un equilibrio entre los constituyentes de la dieta.
El cuadro 1 resume las recomendaciones dietarias para los americanos.
* Nutricionista Dietista de la Pontificia Universidad Javeriana, Hospital Universitario del Valle. Correo electrónico: martacifuentes@yahoo.es
** Ginecólogo, Endocrinología reproductiva, profesor titular y distinguido de la Universidad del Valle. Unidad de Medicina reproductiva,




