GUSTAVO GÓMEZ TABARES
La hiperprolactinemia más comúnmente resulta de condiciones fisiológicas o patológicas que causan hipersecreción de la células lactotropas hipofisiarias.
Hiperprolactinemia patológica se define como una elevación consistente de los niveles de PRL por encima de 20 ng/ mL1. Podríamos agregarle que depende de los valores de referencia del laboratorio donde se mida. Después de excluir efecto de drogas, hipotiroidismo, falla renal crónica, y cirrosis, los valores elevados de PRL sugieren fuertemente una patología hipotalámico-hipofisiaria.
Los estrógenos son responsables por mayores niveles de PRL en el suero, la respuesta aumentada de la PRL a los secretagogos y la mayor incidencia de prolactinomas en mujeres que en hombres. Por lo tanto la hiperprolactinemia ocurre más comúnmente en las mujeres de edad reproductiva, sus manifestaciones clínicas corresponden a las ocasionadas por la hiperprolactinemia más las resultantes del efecto de masa en el caso de los prolactinomas.
En general, cuanto mayor es el grado de hiperprolactinemia, mayor es la cantidad de anormalidades menstruales. Cuando se llega a un nivel de PRL cuatro veces por encima de lo normal, en general se produce amenorrea.
Cuanto mayor es el grado de HPRL, mayor es la probabilidad de que haya un prolactinoma subyacente y mayor en su tamaño. En contraste, el grado de hiperprolactinemia no tiene relación con la presencia o la severidad de la galactorrea.
Los cambios en la menstruación son proporcionales a los niveles de prolactina. Una HPRL moderada (hasta 40ng/mL) frecuentemente se manifiesta con deficiencias de fase lútea con ciclos cortos y “spotting” premenstrual. El cambio posterior, cuando los niveles de PRL se incrementan por encima de valores de alto riesgo de prolactinoma (por encima de 50 ng/mL), puede ocasionar anovulación, con ciclos oligomenorreicos y usualmente hipomenorreas. Casi en el 100% de los casos con niveles mayores de 100ng/mL hay amenorrea. Entonces, la alteración progresiva de la secreción de las gonadotropinas da como resultado un estado hipoestrogenizado, con amenorrea, infertilidad, dispareunia y, a largo plazo, osteoporosis. La progresión a través de estas diversas fases puede observarse en la mujer cuya HPRL se normalizó con un agonista de la dopamina que luego fue suspendido.
La galactorrea es el signo o síntoma sugestivo de hiperprolactinemia. No hay correlación entre la presencia o el grado de galactorrea y el grado de hiperprolactinemia. En el 30 al 80% de todas las mujeres con hiperprolactinemia se halla galactorrea. En el 75% de los casos la combinación de galactorrea y amenorrea se halla con un tumor hipofisiario.
En el hombre la sintomatología usualmente es más tardía y se debe a un adenoma generalmente de gran tamaño. Los síntomas van desde pérdida de la libido hasta impotencia en el campo sexual, cefalea, hemianopsia bitemporal y galactorrea. Generalmente hay trastornos del espermograma con bajo recuento, baja mortalidad, disminución de la viabilidad e infertilidad3.
Clasificación
Consideramos la hiperprolactinemia como de bajo y de alto riesgo de acuerdo a los niveles de PRL.
Los niveles de PRL elevados pero por debajo de 50 ng/ml se consideran de bajo riesgo. Usualmente se trata de efecto de medicamentos o hipotiroidismo.
Niveles de PRL mayores de 50 ng/ml, los consideramos de alto riesgo, con relación a la posible presencia de adenomas. En estos casos el TAC o la RNM pueden mostrar un prolactinoma.
La HPRL también se puede considerar como hiperprolactinemia fisiológica: embarazo, lactancia o hiperprolactinemia patológica que, a su vez, puede ser tumoral (prolactinoma) o no tumoral. La hiperprolactinemia patológica no tumoral puede resultar de varias causas rápidamente identificables que pueden interferir con la inhibición normal de la secreción PRL por la dopamina, drogas antagonistas de los receptores D2 dopaminérgicos, hipotiroidismo y otras causas (Figura 1)4.
 Figura 1. Causas de hiperprolactinemia
Figura 1. Causas de hiperprolactinemia
En algunos pacientes hiperprolactinémicos a pesar de una intensa búsqueda clínica, hormonal y neuroradiológica no se puede encontrar una causa y es lo que se denomina hiperprolactinemia idiopática5.
Un subgrupo de pacientes con HPRL puede tener microadenomas que no son detectados por técnicas de imágenes corrientes. Algunos de ellos se presentan con otra causa de HPRL llamada por Jackson y col.4 macroprolactinemia. Esta condición corresponde a la predominancia de la forma big big PRL que se ha postulado que representa un complejo con inmunoglobulinas anti PRL6. Muchos de estos pacientes con macroprolactinemia no presentan las típicas manifestaciones clínicas del síndrome de HPRL con la excepción de galactorrea7
Diagnóstico
El enfoque de la paciente con hiperprolactinemia debe contemplar:
1. Historia clínica y examen físico: deben descartarse inicialmente las causas fisiológicas (embarazo, lactancia, ejercicio, estrés, relación sexual antes del examen, sueño – menos de tres horas después de despertarse) y farmacológicas antes de continuar con una investigación más profunda. De la misma manera deben buscarse cuidadosamente estigmas clínicos de otras enfermedades endocrinas generales que se acompañan de hiperprolactinemia. La clínica de la hiperprolactinemia se resume en la Figura 2.

Figura 2. Clínica de la hiperprolactinemia
2. Determinación hormonal: el diagnóstico de un prolactinoma con frecuencia es obvio una vez que se ha evaluado al paciente, se ha medido el nivel sérico de PRL y se ha determinado la localización anatómica por medio de un TAC. Si embargo, debe procederse con cautela en cuanto al diagnóstico. El hecho de que en el 6 al 11% de la población normal se halle un microadenoma secretor de PRL en la necroscopsia, indica que un nivel sérico normal de PRL no descarta la presencia de un prolactinoma. Estos prolactinomas son clínicamente asintomáticos y parecen no tener ningún significado.
Un nivel de PRL sérica de 50 ng/ml indica un microadenoma secretor de PRL subyacente en el 25% de los pacientes; un nivel de 100 ng/ml se asocia con el diagnóstico de un microadenoma en el 50% de los casos, y un nivel de más de 200 ng/ml corresponde a un macroprolactinoma subyacente en el 99% de los pacientes sintomáticos. No es posible comparar macroadenomas con o sin extensión supraselar por el nivel de PRL.
Se recomienda, además, dosificaciones de FSH y LH como parte de la investigación de la reserva hipofisiaria y por la inhibición de la GnRH que se presenta en la hiperprolactinemia y determinación de TSH, T4: para descartarse hipotiroidismo primario.
Otros estudios extensos de la función hipofisiaria sólo se recomienda realizar si están clínicamente indicados.
3. Pruebas dinámicas: se han ideado diversas pruebas de estimulación y supresión dinámicas de la PRL en el intento de identificar prolactinomas subyacentes; hasta la fecha ninguna prueba única o conjunto de ellas permite diferenciar en forma práctica un prolactinoma de las causas no adenomatosas de la HPRL.
La más común es la prueba de estimulación con TRH y la medición de PRL a los 30, 60 y 120 minutos; una respuesta plana se interpreta como la posibilidad de un adenoma en un paciente con una silla turca normal.
Los pacientes que tienen un tumor hipofisiario secretor de PRL de gran tamaño corren el riesgo de desarrollar hipopituitarismo, y es esencial asegurar que tienen la secreción adecuada de cortisol tanto de base como después de una situación de estrés, si no se está planificando su intervención quirúrgica. Es necesario realizar una prueba de estimulación hipofisiaria posoperatoria para detectar cualquier hipopituitarismo residual.
4. Estudios imagenológicos: los problemas anatómicos subyacentes se definen por medios radiológicos. Los métodos actualmente más usados son la tomografía axial computarizada (TAC) y la resonancia nuclear magnética (RNM).
Tomografía axial computarizada (TAC): el TAC coronal directo con incremento por medio de la infusión rápida de una sustancia de contraste es el método más sensible para detectar un adenoma en la hipófisis. La demostración de un prolactinoma es menos confiable en los cortes axiales. El TAC se emplea para ver una lesión focal (y así diagnosticar un microadenoma) o una masa grande y también se utiliza en forma longitudinal para el seguimiento de los pacientes o para controlar los resultados del tratamiento.
Resonancia nuclear magnética (RNM): el papel de la RNM no está claro. Todavía no se ha determinado si la RNM puede ser superior al TAC, pero ambas técnicas parecen tener una sensibilidad similar. El TAC tiene una ventaja, por cuanto puede revelar la presencia de erosiones óseas y áreas focales de calcificación dentro de la lesión, mientras que la RNM es mejor para definir la diseminación extraselar9-10.
Estudios oftalmológicos: el examen de los campos visuales se documenta en forma objetiva utilizando la perimetría de Goldmann. Debe haber una prolongación supraselar para obtener una compresión quiasmática. Si bien pueden producirse diversos cambios en los campos visuales, la anormalidad clásica es la hemianopsia bitemporal. Debe realizarse examen de campos visuales a todos los pacientes con un macroadenoma, porque puede producirse compresión quiasmática con prolongación supraselar y que puede no ser apreciada por medio del TAC o la RNM.
Tratamiento
Antes de emprender el manejo del paciente, debemos responder a la siguiente pregunta: ¿estamos frente a un paciente con un prolactinoma verdadero o un seudoprolactinoma?; dependiendo de la respuesta nos orientaremos hacia un tipo de terapéutica ya bien establecida para cada uno de estos casos; es así, como el tratamiento quirúrgico se considera como primera línea de manejo si la lesión es un seudoprolactinoma, mientras que el tratamiento médico debe ser considerado en todos los pacientes con verdaderos prolactinomas.
Deben considerarse tanto los síntomas relacionados con la hiperprolactinemia como los relativos a la masa y sus potenciales problemas.
En la actualidad hay cierta tendencia hacia un manejo más conservador como resultado del reconocimiento de la evolución natural benigna de la hiperprolactinemia patológica.
Objetivos del tratamiento
Normalizar el nivel sérico de PRL: esto puede no ser necesario en todos los casos; para lograr ciclos regulares (mejorar la fertilidad), sí se requieren niveles de prolactina normales.
Reducir la masa tumoral: sobre todo cuando el agrandamiento tumoral produce síntomas como anormalidades de los campos visuales.
Restablecer la función gonadal: para normalizar los esteroides sexuales y/o revertir la infertilidad.
Evitar cualquier daño como el hipopituitarismo: es muy importante tomar en cuenta la preferencia personal de cada paciente en cuanto a la toma de decisiones. Prevenir recaídas.
Todo enfoque terapéutico debe caracterizarse por tasas de morbilidad y mortalidad más bajas que las de la condición patológica benigna. Las decisiones terapéuticas dependen de objetivos médicos, cumplimiento y tolerancia por parte del paciente al cual se le deben explicar todas las formas potenciales de tratamiento.
Tratamiento médico
Muchos prolactinomas conservan sus receptores de dopamina, motivo por el cual podemos iniciar tratamiento con medicamentos agonistas de dopamina, logrando disminuir los niveles séricos de prolactina hasta un rango normal en el 80% de los casos aproximadamente.
Los objetivos planteados anteriormente pueden lograrse en su mayoría (75%) con estos medicamentos.
Agonistas de la dopamina
1. Derivados del cornezuelo de centeno.
a. Derivados del ácido lisérgico: bromocriptina, metergolina.
b. Derivados de la clavina: pergolida.
c. 8-a-amino-ergolina: lisurida, tergurida, CU 32085, CQP 201-403, cabergolina.
2. No derivados del cornezuelo de centeno: quinagolida (CV 205 502).
a. Antagonista de la serotonina (metergolina).
b. Ácido gama-aminobutírico (GABA) potenciado: valproato de sodio.
3. Agonista de la dopamina no oral.
a. Bromocriptina de acción prolongada por vía intramuscular.
b. Bromocriptina intravaginal.
Bromocriptina
Se compone de un residuo de ácido lisérgico y una fracción tripeptídica, con una estructura similar a la dopamina.
Por vía oral se absorbe del 40 al 90% del fármaco y la concentración sanguínea pico ocurre en 2 a 3 horas; sólo el 6% de la bromocriptina llega a la circulación debido al metabolismo hepático de primer paso. El nivel sérico de la PRL disminuye después de una hora, es mínimo en siete horas y persiste disminuido durante 14 horas luego de la administración de una tableta del fármaco como resultado de la prolongada fijación en los receptores de la dopamina. El 90% está unido a proteínas plasmáticas. El 90% es excretado en heces. Dado que una sola dosis oral dura 14 horas, el fármaco se administra en dos o tres tomas/día.
Efectos colaterales
Los efectos colaterales incluyen:
Náuseas en el 50% de los pacientes y vómitos en aproximadamente el 5%, mareos ortostáticos, en el 20% de los casos, durante tres horas después de la administración; rara vez ocurren como un efecto severo de la primera dosis. Es beneficioso que las primeras dosis sean ingeridas en el momento de acostarse.
Congestión nasal (5%). Dos horas después de la administración, puede durar hasta seis horas; los antihistamínicos no son útiles, pero puede emplearse seudoefedrina.
Otros síntomas: cefalea, fatiga, calambres abdominales, constipación, somnolencia, visión borrosa, vasoespasmo digital y pesadillas y muy raro, edemas, ergotismo y sequedad de la boca con altas dosis.
Cabergolina
Es un agonista dopaminérgico de larga acción, derivado de la ergolina, se puede administrar una o dos veces por semana y ha demostrado mayor efectividad que la bromocriptina en la supresión de secreción de PRL en pacientes con hiperprolactinemia; es mejor tolerada (menos náusea y vómitos). Con relación a la suspensión de lactancia fisiológica es un poco menos efectiva que la bromocriptina.
Junto con la quinagolida se considera como una droga ideal de segunda línea en pacientes con intolerancia o resistencia a la bromocriptina.
Dosis: entre 0.2 y 3.5 mg dos veces por semana inducen disminución del tamaño tumoral en el 96% de pacientes tratadas11.
Duración del tratamiento: no se ha determinado. Ocurre recurrencia de la hiperprolactinemia y cambios en el volumen tumoral al suspender el medicamento, por lo cual debe tenerse precaución en pacientes con lesiones grandes. Se han descrito pacientes con reducciones estables en el tamaño del adenoma y el nivel de PRL después de suspender la medicación dopamino-agonista. Algunas pacientes requerirán terapia indefinida.
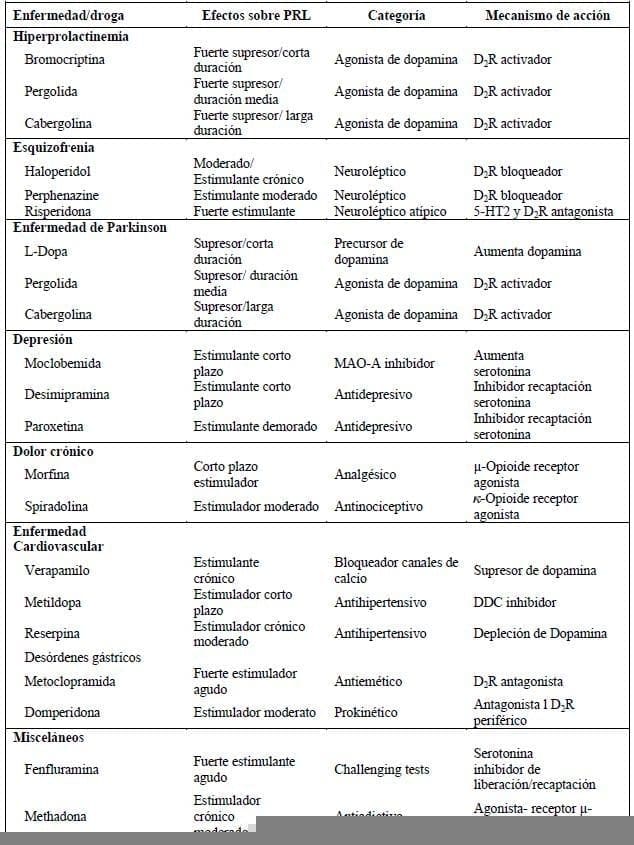
Medicamentos usados en la práctica clínica que afectan la secreción de PRL: varios medicamentos usados en la práctica médica que afectan los niveles de PRL, hecho a tener en cuenta para el diagnóstico y tratamiento de la HPRL. En la Tabla 1 tenemos una lista de ellos.
El autor declara haber recibido honorarios de Laboratorios Pfizer.
Tabla 1. Drogas usadas en la práctica clínica que afectan la secreción de PRL
Referencias
1. Blackwell RE. Hyperprolactinemia: evaluation and management. Reprod Endocrinol 1992; 21: 105-124.
2. Molitch ME. Prolactinomas. In: Horseman ND, ed. Prolactin. Boston: Kluwer; 2001; 81-100.
3. De Rosa M, Colao A, Di Sarno A.Effecto of hyperprolactinemia in men with prolactinomas. European Journal of Endocrinology, 1998; 138: 286-293.
4. Molicht ME. Medical treatment of prolactinomas. Endocrinol Metab Clin North Am 1999; 28: 143-169.
5. Sluijmer AV, Lappohn RE. Clinical history and outcome of 59 patients with idiopathic hyperprolactinemia. Fertil Steril 1992; 58: 72– 77 [Medline].
6. Sophie Vallette-Kasic, Isabelle Morange-Ramos, Adel Selim, et al. Macroprolactinemia Revisited: A Study on 106 Patients. JCEM 2002; 87: 581-588.
7. Blackwell RE. Hyperprolactinemia: evaluation and management. Reprod Endocrinol 1992; 21: 105-124.
8. Colao A, Lombardi G. Growth-hormone and prolactin excess. Lancet 1998; 352: 1455- 1461[CrossRef][Medline].
9. Gómez GT, Posada GE, Martínez CM. Prolactina y Prolactinomas. Una visión global. Rev Col Menop. 2000; 6: 244-269.
10. Espinós GJJ, Calaf J. Prolactina, Hiperprolactinemia. En Endocrinologia Reproductiva e Infertilidad. Ed Gómez GT. Editora Catorze. 1999. págs 245-264.
11. Pontikides N, Krassas GE, Nikopoulou E, Kaltsas T. Cabergoline as a first-line treatment in newly diagnosed macroprolactinomas. Pituitary 2000; 2: 277-281[CrossRef][Medline].
• Ginecólogo. Endocrinología Reproductiva, Profesor Titular Y Distinguido. Universidad Del Valle –Cali –Colombia.
