Actualidad Inmediata
Elizabeth Barrett-Connor, Lori Mosca, Peter Collins, Mary Jane Geiger,
Deborah Grady, Marcel Kornitzer, Michelle A. Mcnabb, Nanette K. Wenger
New Gmg J Med 2006; 355:125-137.
Resumen
Antecedentes: Los efectos del raloxifeno, un modulador selectivo de estrógenos sobre la enfermedad cardiaca coronaria ECC y el cáncer de mama, no han sido determinados aún. Métodos: asignamos de forma aleatorizada 10.101 mujeres posmenopáusicas (edad promedio: 67.5 años), con ECC o múltiples factores de riesgo para ECC, a 60 mg diarios de raloxifeno o a placebo y las seguimos por un tiempo promedio de 5.6 años.
Los dos objetivos primarios fueron eventos coronarios (es decir, muerte por causas coronarias, infarto del miocardio u hospitalización por un síndrome coronario agudo) y cáncer invasivo de mama. Resultados: comparado con el placebo, el raloxifeno no tiene efectos significantes sobre el riesgo de eventos coronarios primarios (533 frente a 553 eventos; RR, 0.95 IC 95%, 0.84-10,7) y el riesgo de cáncer invasivo de mama se reduce (40 frente a 70 eventos; RR 0.56; IC 95%, 0.38-0.83); riesgo absoluto de reducción: 1.2 cánceres invasivos por 1.000 mujeres tratadas por año; el beneficio fue primariamente debido a la reducción de riesgo en los cánceres invasivos RE positivos. No hubo diferencia significativa en las tasas de muerte por cualquier causa o ACV de acuerdo con el grupo asignado, pero el raloxifeno fue asociado a un aumento de riesgo de ACV fatal (59 eventos frente a 39; RR 1.49; IC 95%, 1.00-2.24; riesgo absoluto aumenta 0.7 por 100 mujeres-año) y tromboembolismo venoso (103 frente a 71 eventos; RR, 1.44; IC 95% 1.06-1.95); riesgo absoluto aumentado de 1.2 por 200 mujeres-año. El raloxifeno reduce el riesgo de fracturas vertebrales (64 eventos frente a 97; RR, 0.65; IC 95%, 0.47-0.89; riesgo absoluto de reducción: 1.3 por 1.000).
Conclusiones: el raloxifeno no afecta de manera significante el riesgo de ECC. Los beneficios del raloxifeno en la reducción del riesgo de cáncer y fracturas vertebrales debe sopesarse contra el aumento de riesgo de tromboembolismos venosos y ACV fatal.
Abstract
Background: the effect of raloxifene, a selective estrogen-receptor modulator, on coronary heart disease (CHD) and breast cancer is not established.
Methods: We randomly assigned 10,101 postmenopausal women (mean age, 67.5 years) with CHD or multiple risk factors for CHD to 60 mg of raloxifene daily or placebo and followed them for a median of 5.6 years. The two primary outcomes were coronary events (i.e., death from coronary causes, myocardial infarction, or hospitalization for an acute coronary syndrome) and invasive breast cancer.
Results: as compared with placebo, raloxifene had no significant effect on the risk of primary coronary events (533 vs. 553 events; hazard ratio, 0.95; 95 percent confidence interval, 0.84 to 1.07), and it reduced the risk of invasive breast cancer (40 vs. 70 events; hazard ratio, 0.56; 95 percent confidence interval, 0.38 to 0.83; absolute risk reduction, 1.2 invasive breast cancers per 1000 women treated for one year); the benefit was primarily due to a reduced risk of estrogen-receptor–positive invasive breast cancers. There was no significant difference in the rates of death from any cause or total stroke according to group assignment, but raloxifene was associated with an increased risk of fatal stroke (59 vs. 39 events; hazard ratio, 1.49; 95 percent confidence interval, 1.00 to 2.24; absolute risk increase, 0.7 per 1000 woman-years) and venous thromboembolism (103 vs. 71 events; hazard ratio, 1.44; 95 percent confidence interval, 1.06 to 1.95; absolute risk increase, 1.2 per 1000 woman-years).
Raloxifene reduced the risk of clinical vertebral fractures (64 vs. 97 events; hazard ratio, 0.65; 95 percent confidence interval, 0.47 to 0.89; absolute risk reduction, 1.3 per 1.000).
Conclusions: raloxifene did not significantly affect the risk of CHD. The benefits of raloxifene in reducing the risks of invasive breast cancer and vertebral fracture should be weighed against the increased risks of venous thromboembolism and fatal stroke.
El raloxifeno es un modulador selectivo de los receptores estrogenitos (SERM) que se unen al receptor de estrógenos, teniendo efecto antagonista de estrógenos en algunos tejidos y efecto antagonista de estrógenos en otros 1. La terapia con raloxifeno ha sido asociada con mejoría de los niveles las lipoproteínas séricas de colesterol 2, 3, fibrinógeno 3, y homocisteín 4.
El efecto favorable del raloxifeno sobre marcadores del riesgo cardiovascular, junto con la evidencia de estudios observacionales de que el tratamiento con estrógenos estaba asociado con una reducción del riesgo de enfermedad cardiaca coronaria (ECC) en mujeres posmenopáusicas 5, 6, llevaron a diseñar el estudio Raloxifene Use for The Heart (RUTH) para determinar los efectos del raloxifeno en eventos coronarios clínicos. Después del comienzo del RUTH en 1998, los resultados de los estudios clínicos Heart and Estrogen/ Progestin Replacement Study (HERS) and the Women’s Health Initiative (WHI)7-9 no mostraron reducción de la ECC después del tratamiento con estrógenos o estrógenos-progestinas. Un
análisis secundario de los datos del estudio Múltiple Outcomes of Raloxifene Evaluation (MORE) (un estudio de tratamiento de osteoporosis) no mostró efectos significativos en los efectos del raloxifeno sobre los eventos cardiovasculares pero sugirió una reducción del riesgo entre las mujeres que estaban en un riesgo aumentado de eventos cardiovasculares10.
El raloxifeno tiene un efecto antiestrogénico en la mama, bloqueando competitivamente la transcripción de DNA inducida por los estrógenos11 e inhibiendo el crecimiento de los cánceres estimulados por los estrógenos en los animales12. Después de que el estudio RUTH comenzó, un segundo análisis de los datos del MORE mostró que el raloxifeno reducía el riesgo de cáncer invasivo de mama en el 2%13.
Hicimos el RUTH para medir los riesgos y beneficios del tratamiento con raloxifeno en mujeres con EEC o a un riesgo aumentado de ECC, con el objetivo primario de determinar los efectos sobre objetivos coronarios y cáncer de mama.
Métodos
El RUTH fue un estudio internacional, multicéntrico randomizado, doble ciego. Una descripción detallada del diseño y estudio de la población ha sido publicada en otro sitio 14, 15. Los dos objetivos primarios fueron determinar el efecto del raloxifeno comparado con el placebo sobre la incidencia de eventos coronarios (p. ej., muerte por causas coronarias, infarto de miocardio [incluso silencioso], u hospitalización (por un síndrome coronario diferente al infarto del miocardio) y cáncer invasivo de mama.
El comité ejecutivo desarrolló el protocolo en colaboración con el financiador. Un comité independiente de datos y seguridad con soporte estadístico independiente realizó un análisis interno de seguridad y eficacia. Los datos fueron analizados por el financiador de acuerdo al plan de análisis especificado. El comité ejecutivo tenía solicitud sin restricción de acceso a los datos según rendimiento, los cuales fueron retenidos por el financiador. Todos los autores estuvieron involucrados en la interpretación de los datos y preparación del manuscrito, y en verificar la exactitud y totalidad de los datos reportados. Los datos reportados fueron los que estaban disponibles en febrero 2 de 2006.
El protocolo fue aprobado por los comités de ética en cada sitio de la investigación. Todas las mujeres dieron consentimiento informado por escrito para su participación de acuerdo con los principios de la declaración de Helsinki.
Población de Estudio
Entre junio de 1998 y agosto del 2000, 10.101 mujeres posmenopáusicas fueron asignadas por randomización a tratamiento o placebo en 177 sitios en 26 países. Las mujeres elegibles fueron de 55 años de edad o mayores, un año o más posmenopáusicas, y tenían ECC establecida o estaban en un mayor riesgo de ECC14. Las participantes veían tener un riesgo cardiaco mayor de 4, de acuerdo con el sistema de puntaje que toma en cuenta la presencia de lo siguiente14: ECC establecida (4 puntos), enfermedad arterial de las piernas (4 puntos) y edad al menos de 70 años (2 puntos), diabetes mellitus (3 puntos), fumadora de cigarrillo (1 punto), hipertensión (1 punto) e hiperlipidemia (1 punto).
Los criterios de exclusión fueron: infarto del miocardio, “bypass” coronario o intervención coronaria percutánea dentro de los tres meses anteriores a la randomización, historia de cáncer o tromboembolismo venoso, una expectativa de vida de menos de cinco años, sangrado uterino sin explicación dentro los seis meses anteriores a la randomización, falla cardiaca clase II o IV según la New York Heart Association, enfermedad renal o hepática crónica, uso de estrógenos orales o transdérmicos dentro de los seis meses anteriores a la randomización, o uso actual de otras hormonas sexuales o SERMs.
Tratamientos y Procedimientos
Las mujeres elegibles fueron asignadas aleatoriamente a 60 mg/día orales de raloxifeno (Evista Eli Lilly) o a un placebo de apariencia idéntica (Tabla 1). La aleatorización fue realizada con el uso de sistema telefónico de voz de respuesta interactiva, estratificado de acuerdo al estudio.
En cada visita anual o contacto telefónico, se averiguaron eventos adversos, resultados y adherencia a la medicación. Se hizo un electrocardiograma de entrada y otros al año 2, al año 4 y en la visita final. Se realizaron mamografía y examen clínico del seno aleatoriamente cada dos años después. Los niveles de lípidos en el suero se midieron después de ayuno nocturno de base al año 1, al año 5 y en la visita final.
Los investigadores, participantes, personal de laboratorio y el financiador (Eli Lilly) no supieron la asignación de las participantes al tratamiento (ciegos).La asignación se reveló a los investigadores solo por razones de seguridad de las participantes.
La droga del estudio fue permanentemente descontinuada cuando el tratamiento asignado fue revelado a las participantes (26 mujeres) o cuando se diagnosticaba cáncer de mama o tromboembolismo.
La medicación del estudio fue temporalmente descontinuada durante períodos prolongados de inmovilización o si la participante tomaba medicaciones que contuvieran estrógenos, otros agentes hormonales o SERM s.
Objetivos
Los reportes de los resultados de eventos coronarios, cáncer de mama, tromboembolismos venosos y muerte fueron adjudicados por el comité de expertos quienes no conocían el tratamiento asignado a los participantes y que no eran empleados del financiador. Empleados del financiador, que no conocían la asignación de tratamiento, adjudicaron los resultados secundarios de fracturas, revascularización miocárdica, revascularización no coronaria, amputación de una pierna, y hospitalización por cualquier causa.
Eventos Coronarios
Los objetivos coronarios primarios se definieron como el primero de cualquiera de los siguientes eventos: muerte por causas coronarias (p. ej., infarto agudo del miocardio, muerte sin explicación, falla cardíaca o muerte relacionada con un procedimiento coronario arterial), infarto del miocardio, u hospitalización por un síndrome coronario agudo diferente a un infarto del miocardio (IM)14.
El IM fue diagnosticado si al menos uno de los siguientes eventos estuvo presente: síntomas isquémicos y niveles anormales de enzimas cardíacas, con o sin cambios nuevos e inequívocos del ECG; una nueva onda Q o antológica, con o sin síntomas isquémicos o niveles anormales de enzimas cardiacas; y nueva onda Q patológica o niveles anormales de enzimas cardíacas después de un procedimiento invasivo coronario.
Hospitalización por un síndrome coronario agudo se definió como hospitalización por o el desarrollo durante la hospitalización de síntomas cardíacos con nuevos cambios en el segmento S-T del ECG o niveles anormales de enzimas cardiacas o troponin.
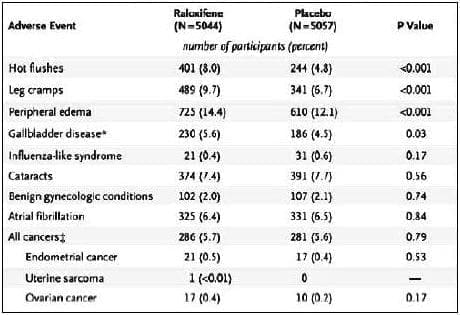
Tabla 1. Eventos Adversos
Cáncer de mama
Los cánceres de mama fueron confirmados por reporte de patología. Se clasificaron en invasivos y no invasivos y de acuerdo a estatus de receptores de estrógenos.
Objetivos Secundarios
Los objetivos de mortalidad secundaria fueron muertes por causas coronarias, muertes por causas cardiovasculares (muerte por causas coronarias y muertes por causas cardiovasculares no coronarias tales como cerebrovasculares, tromboembolismo venoso; enfermedad coronaria arteriosclerótica, y otras causas cardiovasculares, y muertes por cualquier causa (muerte por cusas cardiovasculares y causas no cardiovasculares tales como cáncer, accidente, suicidio, homicidio, o cualquier otra causa).
La causa de muerte fue asignada sobre la base de información clínica disponible, el certificado de defunción o la autopsia. ACV fue definido como el inicio rápido de un déficit neurológico de más de 24 horas de duración, en la mayoría de los casos apoyado por estudio de imágenes. Un evento tromboembólico requirió síntomas clínicos apoyados por estudios de diagnóstico relevantes.
La revascularización incluye revascularización arterial coronaria y no coronaria; las amputaciones no traumáticas de las piernas incluyeron aquellas de por encima o por debajo de la rodilla. Todas las fracturas clínicas reportadas fueron validadas por revisión del reporte del radiólogo. La hospitalización por cualquier causa se definió como hospitalización de al menos 24 horas.
Eventos Adversos
Los eventos adversos fueron registrados por el investigador en cada visita sobre la base de un reporte no solicitado por la participante. Todos los eventos adversos fueron clasificados de acuerdo a Medical Dictionary for Regulatory Activities (MedDRA, una marca registrada de la International Federation of Pharmaceutical Manufacturers and Associations), desarrollado bajo los auspicios de la International Conference on Harmonization of Technical Requirements for Registration of Pharmaceuticals for Human Use.
Los eventos adversos comunes se definieron como eventos en el término de la MedDRA que ocurrían al menos en el 2% de las mujeres asignadas a raloxifeno.
Se establecieron categorías especiales de búsqueda con el uso de los términos del MedDRA para describir comprensivamente los eventos adversos de potencial relevancia a los SERMs o terapia hormonal. Eventos adversos serios fueron definidos como eventos que atentaron contra la vida, severos o incapacidad permanente, cáncer, o clínicamente significante para cualquier otra causa. Se identificaron como objetivos primarios o secundarios o, en el caso de cáncer, como una categoría especial establecida con el uso de los términos del MedDRA.
Análisis Estadístico
Las comparaciones de las características basales entre los grupos de tratamiento se realizaron con el uso de análisis de crianza de una vía para variables continuas y test de chi-cuadrado para categorías variables. El análisis primario usó el método de tiempo al evento sobre la base del principio de intento de tratar. Lo datos sobre mujeres que no habían tenido un evento fueron censados en la fecha cuando la información del estudio fue colectada o en la fecha de la muerte.
Las incidencias relativas de los objetivos primarios de eventos coronarios y cáncer invasivo de mama se compararon con el uso del test logrank. Modelos de peligrosos proporcionales de Cox se usaron para estimar los radios de peligro (RR) con el 95% de intervalos de confidencia para los objetivos primarios y secundarios.
Los eventos adversos se analizaron con el test de Cochran-Mantel-Haenszel estratificado de acuerdo al país. Si ocurrieron menos de cinco eventos, no se realizó ningún test estadístico. Los valores basales de laboratorio y los porcentajes de cambio sobre la línea de base a un año se analizaron con el uso de análisis de varianza no ajustado de una vía.
Se realizaron análisis secundarios para los objetivos primarios en una población “como tratada”, definida como mujeres que al menos eran 70% adherentes al tratamiento del estudio sobre la base del conteo de las píldoras. El objetivo primario de eventos coronarios fue determinado separadamente para aquellas con ECC y para aquellas en un riesgo aumentado para ECC con el uso de modelo de riesgos proporcionales de Cox.
Todos los análisis fueron especificados, excepto el test de interacción de objetivo primario de eventos coronarios en mujeres con ECC establecida comparada con aquellas en un riesgo aumentado para ECC. El valor reportado de p es de dos lados. El análisis estadístico fue realizado con el uso del programa SAS, versión 8.2 (SAS Institute).
El cálculo del poder se basó en la asunción de un porcentaje del 20.0% de reducción relativa en el riesgo de eventos coronarios y un 58.5 de reducción relativa en el riesgo de cáncer de mama con raloxifeno, dando un poder estadístico del 80% y nivel a doble lado de 0.0423 para eventos coronarios y 0.008 para cáncer invasivo de mama.
Otros objetivos fueron medidos a un nivel de significancia del 0.05, excepto efectos de interacción, los cuales fueron medidos a un nivel de significancia del 0.10. No se hicieron ajustes para comparaciones múltiples.
Resultados
Para ambos grupos de tratamiento, la duración promedio del seguimiento fue de 5.56 años (rango: 0.01 a 7.06) y la mediana de exposición a la droga del estudio fue de 5-05 años. El estudio fue completado en el 79% de las mujeres en el grupo placebo y en el 80% en el grupo de raloxifeno (p=0.02). En total, el 71% de las mujeres en el grupo placebo y el 70% en el grupo de raloxifeno tomó al menos el 70% de la medicación asignada y fueron clasificadas como adherentes al tratamiento (p=0.62).
Los grupos de tratamiento fueron similares con respecto a las característicasbasales, excepto el grupo de raloxifeno que tenía ligeramente mayor riesgo cardiovascular y una mayor proporción de mujeres que reportaron bypass coronario. Durante el estudio, tanto el placebo como el grupo de raloxifeno tuvieron un aumento del uso de estatinas (21% y 19%, respectivamente), agentes antihipertensivos (6% y 7%), y aspirina (13% y 15%) (p>0.05 para cada comparación).
Objetivos Primarios
No hubo una diferencia significativa entre el grupo de raloxifeno y el de placebo en la incidencia de objetivo primario de muerte por causas coronarias, infarto no fatal, u hospitalización por síndrome coronario agudo (RR, 0.95; IC 95%, 0.84-1.07) (Tabla 2) o por muerte de causas coronarias, infarto no fatal u hospitalización por un síndrome coronario agudo individualmente.
Los efectos del tratamiento de objetivo primario de eventos coronarios no difieren significativamente entre las mujeres con ECC establecido (RR, 0.97; IC 95%, 0.83-1.12) o mujeres con un aumento del riesgo para ECC (RR, 0.91; IC 95, 0.74-1.1) (valor p para la interacción: 0.64). Hubo otros 18 análisis de subgrupos preespecificados para los objetivos coronarios primarios (incluyendo la edad y la presencia o ausencia de factores de riesgo para ECC); no hubo interacciones significantes en los grupos de tratamiento para ningún otro subgrupo (p>0.10).
Los resultados del análisis como tratadas fueron similares a los de intención de tratar para los objetivos primarios (RR de comparación del grupo de raloxifeno con el grupo placebo: 0.96; IC 95%, 0.83-1.12; P=0.61) y sus componentes individuales (p>0.05 para cada comparación).
El raloxifeno redujo la incidencia de cáncer de mama invasivo (RR, 0.56; IC 95%, 0.38,-0.83) (Figura 1), primariamente debido a la reducción de cánceres de mama RE positivos. La reducción absoluta por 1.000 mujeres tratadas con raloxifeno por un año fue de 1.2 casos de cáncer de mama invasivo y 1.2 casos de cánceres RE positivos. Los resultados del análisis como tratados para cáncer invasivo de mama fueron similares (RR para comparación del grupo de raloxifeno con el grupo placebo, 0.65; IC 95%, 0.39-0.95; p=0.03). No hubo diferencia significante entre los grupos de tratamiento en la incidencia de cánceres de mama. RE negativos.
Los efectos del tratamiento sobre el cáncer invasivo de mama no difieren significantemente entre las mujeres con un riesgo estimado para cáncer de mama de cinco años de menos de 1-88 por ciento en la escala de Gail14 (RR, 0.49; IC 95%, 0.28-0.88) o 1.66 por ciento o más (RR, 0.65; IC 95%, 0.38-1.09; valor de interacción p=0.50). Hubo otros análisis de ocho subgrupos preespecificados para cáncer invasivo de mama; no hubo interacciones significativas en los grupos para ninguno de los subgrupos (p>0.1) excepto el análisis del grupo de ooforectomía (p=0.007).
Objetivos Secundarios
La incidencia global de ACV no difiere significativamente entre los grupos, pero la incidencia de ACV fatal fue un 49 por ciento más alto en el grupo de raloxifeno que en el grupo placebo (aumentó el riesgo absoluto 1.2 por 1.000 mujeres-año). Hubo un 33% menos de incidencia de todos los cánceres de mama (reducción del riesgo absoluto, 0.9 por 1000 mujeres-año) y un 35% menos incidencia de fracturas vertebrales clínicas (reducción del riesgo absoluto 1.3 por 1000 mujeres año) en el grupo de raloxifeno.
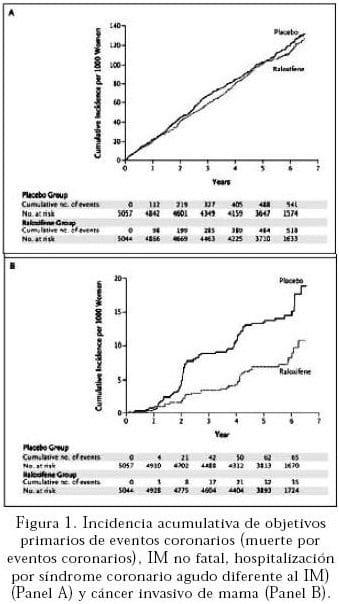
Tabla 2. Incidencia de Riesgos de Peligro (RR) para objetivos de Enfermedad Coronaria combinada y cancer de mama
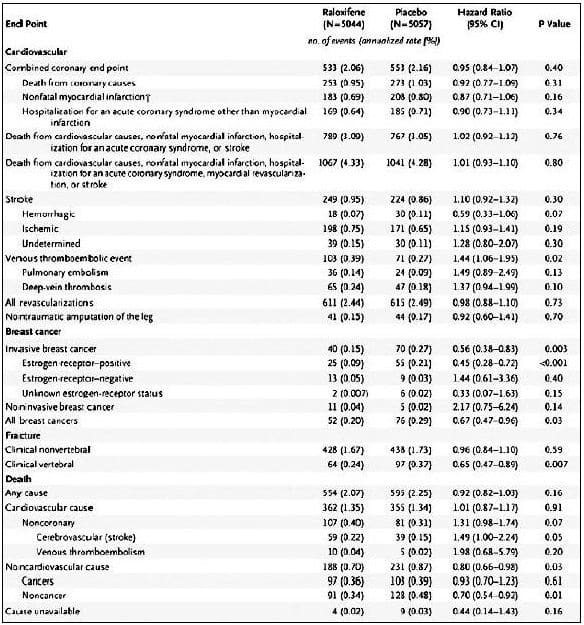
No hubo diferencia significante entre los grupos de tratamiento en las tasas de muerte por cualquier causa o muerte general por causas cardiovasculares. La incidencia de muertes por causas no cardiovasculares fue menor en el grupo de raloxifeno que en el grupo placebo (reducción de riesgo absoluto 1.7 por 1.000 mujeres-año); no hubo una categoría de enfermedad específica que explicara estos hallazgos.
Menos mujeres en el grupo de raloxifeno en el grupo de placebo tenían una o más hospitalizaciones por cualquier causa (52% frente a 54%; RR, 0.91; IC 95%, 0.87-0.96; p=0.001).
Efectos Adversos
No hubo diferencia significante en los grupos de tratamiento en el número de mujeres con uno o más eventos adversos posibles (93 % en ambos grupos, p=0.71). Más mujeres en el grupo de raloxifeno que en el grupo de placebo que descontinuaron permanentemente el uso de la medicación del estudio por un evento adverso (22% frente a 20%, p=0.01).
Cuatro eventos adversos comunes (un síndrome coronario agudo, ansiedad, constipación y osteoporosis) se reportaron más frecuentemente en el grupo placebo que en el de raloxifeno, y siete (artritis, colelitiasis, dispepsia, fogajes, claudicación intermitente, espasmo muscular y edema periférico) se reportaron más frecuentemente en el grupo de raloxifeno que en el grupo placebo (p<0.05). Fogajes, calambres en las piernas, edema periférico, y cálculos biliares, todas las categorías especiales fueron más comunes en las mujeres asignadas a raloxifeno que en las asignadas a placebo. Las tasas de colecistectomia no difieren significantemente entre los grupos de tratamiento (p=0.25). Las incidencias de cáncer endometrial de todos los cánceres diferentes al cáncer de mama no difieren significantemente entre los grupos de tratamiento.
Cambios en los Niveles de Lipoproteínas
De la línea de base al año, hubo un aumento del 3.6% en los niveles de lipoproteínas de baja densidad LDL en el grupo placebo comparado con una disminución del 4.4% en los niveles en el grupo de raloxifeno (p<0.001) y un porcentaje de 0.9 de aumento en los niveles de lipoproteínas de alta densidad (HDL) en el grupo placebo comparado con un 2.3% de aumento en los niveles en el grupo de raloxifeno (p<0.001).
Discusión
El tratamiento con raloxifeno durante un promedio de 5.6 años no afecta de manera significativa el riesgo de eventos coronarios. Tal tratamiento disminuye el riesgo de cáncer invasivo de mama y fracturas vertebrales clínicas y aumenta el riesgo de eventos tromboembólicos y ACV fatal. Cuando el RUTH fue diseñado, evidencias compiladas de muchos estudios observacionales sugirieron que la terapia estrogénica posmenopáusica era cardioprotectora 5, 6. Sin embargo, tres grandes estudios de tratamiento posmenopáusico con hormonas 7-9 fallaron subsecuentemente en mostrar los efectos cardioprotectores de los estrógenos, y los estudios de estrógenos progestágenos 7, 8 mostraron un aumento temprano del riesgo.
Encontramos que el tratamiento con raloxifeno no afectó significativamente el riesgo de eventos coronarios entre mujeres con ECC o entre mujeres en alto riesgo de ECC, ni causó un aumento temprano en el riesgo de ECC.
Estos resultados confirman los resultados del MORE, en el cual el raloxifeno tenía un efecto nulo sobre la enfermedad coronaria en las mujeres posmenopáusicas con osteoporosis, pero no proveyó soporte para el efecto cardioprotector observado en un análisis post hoc de mujeres en el estudio MORE quienes estaban a alto riesgo cardiovascular10. El estrecho intervalo del índice de confidencia del 95% para los efectos del raloxifeno en el objetivo primario coronario sugiere que el raloxifeno no reduzca el riesgo posiblemente por debajo del 16% o que aumente el riesgo coronario más del 7%.
El raloxifeno tuvo un efecto moderado sobre los niveles de colesterol LDL y HDL que fue de magnitud menor que los cambios alcanzados por otras medicaciones que muestran ser protectoras 17. El uso de medicaciones que bajan los lípidos, agentes antihipertensivos, y agentes antiplaquetarios fue fomentado en el RUTH y aumentó durante el estudio. El uso de medicamentos cardioprotectores no difiere significantemente entre los grupos de tratamiento y no parece explicar los efectos nulos. Sin embargo, la tasa más baja que la esperada de eventos coronarios puede reflejar el uso sustancial de estos medicamentos.
La mujeres en el grupo de raloxifeno tenían un 55% menor de riesgo de cáncer invasivo RE positivo que las mujeres en el grupo placebo (riesgo absoluto de reducción de 1.2 cánceres invasivos de mama RE positivos por 1.000 mujeres tratadas en un año). Esta reducción es consistente con la observada en mujeres posmenopáusicas en el estudio MORE13. La reducción relativa en el riesgo de cáncer invasivo de mama fue también similar a la vista entre mujeres en un riesgo aumentado de cáncer invasivo de mama tratadas con tamoxifeno en el Breast Cáncer Prevention Trial 18.
El efecto del tratamiento con raloxifeno en el estudio RUTH fue similar, sin importar el riesgo predecible a cinco años de cáncer invasivo de mama, con base en el puntaje de Gil 16.
Aunque las participantes en el RUTH no se seleccionaron en un aumento del riesgo de cáncer de mama, el 41% tenía un riesgo predecible del 1.66% o más16. Este riesgo estimado podría haberlas hecho elegibles para el estudio Breast Cancer Ptrevention Trial y el estudio de Tamoxifen y Raloxifene (STAR) 18, 19. Los resultados del STAR indican que el raloxifeno es tan efectivo como el tamoxifeno en la reducción del riesgo de cáncer invasivo de mama entre mujeres en un riesgo aumentado de cáncer invasivo de mama; además está asociado con menos cánceres uterinos y eventos tromboembólicos 19.
Los resultados del RUTH y estudios previos13-20 muestran que el raloxifeno no reduce el riesgo de cánceres invasivos de mama ER negativos. El mecanismo por el cual el raloxifeno reduce el riesgo de cánceres de mama estrógenos positivos no es claro, pero probablemente está relacionado con el antagonismo a los estrógenos en la regresión de cánceres subclínicos con RE positivos.
El raloxifeno no aumenta el riesgo total de ACV pero se asoció con el 49% de aumento en la incidencia de ACV fatal. El raloxifeno no tiene efecto significativo en el riesgo total de muerte por causas cardiovasculares o por muerte de cualquier otra causa. No hubo efecto del raloxifeno en el riesgo de ACV en el estudio MORE10. El tamoxifeno aumentó el riesgo de ACV en la mayoría18, 21-23, pero no en todos24 los estudios.
En el STAR19, la incidencia de ACV fue similar en los grupos de tamoxifeno y raloxifeno. En el estudio WHI, los estrógenos solos o con una progestina aumentaron el riesgo de ACV en aproximadamente el 40% en mujeres jóvenes posmenopáusicas 8,9. Entre las mujeres con una historia reciente de ACV o ataque isquémico transitorio, los estrógenos no afectaron el riesgo de ACV no fatal pero aumentaron el riesgo de ACV fatal25.
Consistente con los hallazgos de estudios previos de estrógenos y SERMs 1, 8, 9, 18, 26, se encontró que el uso de raloxifeno se asoció con un aumento del riesgo de eventos de tromboembolismo venoso. Hubo un 35 por ciento de reducción en el riesgo de fracturas vertebrales clínicas, pero no una reducción significante de fracturas no vertebrales en el grupo de raloxifeno, consistente con los resultados del estudio MORE 27.
Los fogajes, calambres en las piernas y edema periférico, todos se saben asociados al uso de raloxifeno 20, 28; se reportó más frecuentemente en mujeres asignadas a raloxifeno. El raloxifeno no aumentó el riesgo de cánceres diferentes al de mama, incluyendo cáncer de endometrio. Las incidencias mayores de cálculos biliares reportadas no se observaron en el estudio de Grady y colaboradores26, pero son una reconocida complicación de la terapia hormonal oral29. Las tasas de colecistectomía no se relacionaron con la asignación a tratamiento.
En conclusión, en mujeres posmenopáusicas con ECV o en un riesgo aumentado para ECV, el tratamiento con raloxifeno por un promedio de 5.6 años reduce el riesgo de cáncer invasivo de mama y no cambia la incidencia de eventos coronarios. En estas mujeres, la diferencia en las tasas absolutas de eventos que estaban disminuidas (p. ej., cáncer de mama y fracturas vertebrales clínicas) fueron similares a la diferencia en las tasas absolutas de eventos que estaban aumentadas (p. ej., eventos tromboembólicos venosos y ACVs fatales). Cuando se considere el uso de raloxifeno en una mujer posmenopáusica, el clínico debe tener en cuenta el riesgo individual de enfermedad de la mujer y sus preferencias personales y pensar en los beneficios potenciales contra los riesgos y contra la disponibilidad de alternativas individuales.
El Dr. Barrett-Connor reporta haber recibido salario de Eli Lilly por trabajar como investigador principal y como un investigador del sitio de la clínica del estudio RUTH; ha servido con pago en los comités supervisores para Merck, Eli Lilly, Procter & Gamble y Amgen; y ha recibido donaciones para investigación de Amgen. El Dr. Mosca reportó haber recibido pago como consultante de Eli Lilly y Organon. El Dr. Collins reporta haber recibido pago como consultor de Eli Lilly, Berlex, Merk, Pantarhei, y Pfizer; y pagos por conferencias de Berlex, Merck, Pfizer, Novo Nordisk y Organon; y haber recibido donaciones por investigación de Eli Lilly, Organon, y Merck.
El Dr. Grady reporta haber recibido salario por medio de contratos con la Universidad de California, San Francisco, de Berlex, Eli Lilly, Merck, Pfizer y Wyeth-Ayerst, y pagos como consultor y por presidir comités de datos y seguridad de Organon. El Dr. Kornitzer reporta haber recibido donación de investigación y pagos de conferencias de Eli Lilly, Merck, Bristol-Meyers Squibb, Sandoz, y Astra Zeneca.
El Dr. Wenger reporta haber recibido salario de Eli Lilly por trabajar como coinvestigador y como principal investigador en el sitio de la clínica del estudio RUTH; y ha recibido pagos como consultor de Eli Lilly, CV Therapeutics, NitroMed, Schering-Plough, y el consejo de liderazgo para mejorar el cuidado cardiovascular y ha recibido pago como conferenciante de Pfizer, Novartis, Merck, Eli Lilly, y NitroMed; y ha recibido donaciones para investigación o contratos o ha trabajado en comités de estudios de Eli Lilly, Astra-Zeneca, y Pfizer.
El Dr. Geiger y Ms. McNabb son empleados de tiempo completo de Eli Lilly.
Estamos muy agradecidos con las 10.101 mujeres, los investigadores, y los directivos por su dedicación y compromiso con el estudio RUTH; con Lisa Houterloot y Steve Zheng por la programación estadística; con Jingli Song y Messan Amewou-Atisso por el análisis estadístico; y con Mindy Rance por la asistencia con las figuras y la preparación del manuscrito; y con Sherie Dowsett por su participación en el contenido científico.
Los participantes en el estudio RUTH se listan al principio del artículo.
Referencias
1. Fuchs-Young R, Glasebrook AL, Short LL, et al. Raloxifene is a tissue-selective agonist/ antagonist that functions through the estrogen receptor. Ann N Y Acad Sci 1995; 761: 355-360.
2. Delmas PD, Bjarnason NH, Mitlak BH, et al. Effects of raloxifene on bone mineral density, serum cholesterol concentrations, and uterine endometrium in postmenopausal women. N Engl J Med 1997; 337: 1641- 1647.
3. Walsh BW, Kuller LH, Wild RA, et al. Effects of raloxifene on serum lipids and coagulation factors in healthy postmenopausal women. JAMA 1998; 279: 1445-1451.
4. Walsh BW, Paul S, Wild RA, et al. The effects of hormone replacement therapy and raloxifene on C-reactive protein and homocysteine in healthy postmenopausal women: a randomized, controlled trial. J Clin Endocrinol Metab 2000; 85: 214-218.
5. Stampfer MJ, Colditz GA. Estrogen replacement therapy and coronary heart disease: a quantitative assessment of the epidemiologic evidence. Prev Med 1991; 20: 47-63.
6. Grady D, Rubin SM, Petitti DB, et al. Hormone therapy to prevent disease and prolong life in postmenopausal women. Ann Intern Med 1992; 117: 1016-1037.
7. Hulley S, Grady D, Bush T, et al. Randomized trial of estrogen plus progestin for secondary prevention of coronary heart disease in postmenopausal women. JAMA 1998; 280: 605-613.
8. Writing Group for the Women’s Health Initiative Investigators. Risks and benefits of estrogen plus progestin in healthy postmenopausal women: principal results from the Women’s Health Initiative randomized controlled trial. JAMA 2002; 288: 321-333.
9. Anderson GL, Limacher M, Assaf AR, et al. Effects of conjugated equine estrogen in postmenopausal women with hysterectomy: the Women’s Health Initiative randomized controlled trial. JAMA 2004; 291: 701-712.
10. Barrett-Connor E, Grady D, Sashegyi A, et al. Raloxifene and cardiovascular events in osteoporotic postmenopausal women: fouryear results from the MORE (Multiple Outcomes of Raloxifene Evaluation) randomized trial. JAMA 2002; 287: 847-857.
11. Brzozowski AM, Pike ACW, Dauter Z, et al. Molecular basis of agonism and antagonism in the oestrogen receptor. Nature 1997; 389: 753-758.
12. Anzano MA, Peer CW, Smith JM, et al. Chemoprevention of mammary carcinogenesis in the rat: combined use of raloxifene and 9-cis-retinoic acid. J Natl Cancer Inst 1996; 88: 123-125.
13. Cauley JA, Norton L, Lippman ME, et al. Continued breast cancer risk reduction in postmenopausal women treated with raloxifene: 4-year results from the MORE trial. Breast Cancer Res Treat 2001; 67: 191.
14. Mosca L, Barrett-Connor E, Wenger NK, et al. Design and methods of the Raloxifene Use for The Heart (RUTH) study. Am J Cardiol 2001; 88: 392-395.
15. Wenger NK, Barrett-Connor E, Collins P, et al. Baseline characteristics of participants in the Raloxifene Use for The Heart (RUTH) trial. Am J Cardiol 2002; 90: 1204-1210.
16. Costantino JP, Gail MH, Pee D, et al. Validation studies for models projecting the risk of invasive and total breast cancer incidence. J Natl Cancer Inst 1999; 91: 1541-1548.
17. Pasternak RC. The ALLHAT lipid lowering trial — less is less. JAMA 2002; 288: 3042- 3044.
18. Fisher B, Costantino JP, Wickerham DL, et al. Tamoxifen for prevention of breast cancer: report of the National Surgical Adjuvant Breast and Bowel Project P-1 Study. J Natl Cancer Inst 1998; 90: 1371-1388.
19. Vogel VG, Costantino JP, Wickerham DL, et al. Effects of tamoxifen vs. raloxifene on the risk of developing invasive breast cancer and other disease outcomes: the NSABP Study of Tamoxifen and Raloxifene (STAR) P-2 trial. JAMA 2006; 295: 2727-2741.
20. Martino S, Cauley JA, Barrett-Connor E, et al. Continuing outcomes relevant to Evista: breast cancer incidence in postmenopausal osteoporotic women in a randomized trial of raloxifene. J Natl Cancer Inst 2004; 96: 1751-1761.
21. Braithwaite RS, Col NF, Wong JB. Estimating hip fracture morbidity, mortality and costs. J Am Geriatr Soc 2003; 51: 364-370. 22. Bushnell CD, Goldstein LB. Risk of ischemic stroke with tamoxifen treatment for breast cancer: a meta-analysis. Neurology 2004; 63: 1230-1233.
22. Dignam JJ, Fisher B. Occurrence of stroke with tamoxifen in NSABP B-24. Lancet 2000; 355: 848-849.
23. Geiger AM, Fischberg GM, Chen W, Bernstein L. Stroke risk and tamoxifen therapy for breast cancer. J Natl Cancer Inst 2004; 96: 1528-1536.
24. Viscoli CM, Brass LM, Kernan WN, Sarrel PM, Suissa S, Horwitz RI. A clinical trial of estrogen-replacement therapy after ischemic stroke. N Engl J Med 2001; 345: 1243-1249.
25. Grady D, Ettinger B, Moscarelli E, et al. Safety and adverse effects associated with raloxifene: multiple outcomes of raloxifene evaluation. Obstet Gynecol 2004; 104: 837-844.
26. Delmas PD, Ensrud KE, Adachi JD, et al. Efficacy of raloxifene on vertebral fracture risk reduction in postmenopausal women with osteoporosis: four-year results from a randomized clinical trial. J Clin Endocrinol Metab 2002; 87: 3609-3617.
27. Ettinger B, Black DM, Mitlak BH, et al. Reduction of vertebral fracture risk in postmenopausal women with osteoporosis treated with raloxifene: results from a 3-year randomized clinical trial. JAMA 1999; 282: 2124.
28. Cirillo DJ, Wallace RB, Rodabough RJ, et al. Effect of estrogen therapy on gallbladder disease. JAMA 2005; 293: 330-339.
