Doctor MARIO SANCHEZ MEDINA; Director Científico
*Asociación Colombiana de Diabetes; Presentado en sesión
especial de la Academia Nacional de Medicina y reproducido
con permiso de la revista Medicina de la Academia.
La diabetes 1 es una enfermedad incurable, devastadora por sus complicaciones locales y sistémicas que no tienen tratamiento electivo hasta el presente. Sino el riguroso control, mediante múltiples dosis diarias de insulina o bombas infusión, no sin riesgos, que detienen el progreso de las lesiones vasculares y neurológicas.
Se considera un proceso órgano específico1, 2, 3, 4, 5 en el cual las células β se destruyen. Por mecanismos mediados por autoanticuerpos y por productos de células T auto reactivas que desencadenan inflamación y alteraciones anatómicas y funcionales en el órgano afectado.
Así mismo, debe cumplir con los criterios6 para definir a una enfermedad auto inmune que son:
- Ser transferible por anticuerpos o células T del paciente
- Su curso debe demorarse o prevenirse mediante inmunosupresores
- Estar asociada a signos de autoinmunidad humoral o mediada por la célula, dirigidas contra el órgano blanco
- La enfermedad debe ser experimentalmente inducida por sensibilización contra un antígeno presente en el órgano blanco
Inmunológicamente hasta hoy, en la diabetes 1 hay una susceptibilidad hereditaria y se ha encontrado una asociación con los alelos HLA – DR3 – DR4 del complejo mayor de histocompatibilidad (MHC)7.
Además cada día aparecen nuevos locis8, que se asocian con predisposición a la enfermedad.
Basados en la tasa de concordancia, 35 – 50%, en gemelos homocigóticos9 y por los estudios epidemiológicos,10. Factores ambientales11, infecciosos,12 químicos13 y nutricionales,14 inician o precipitan el progreso de la diabetes 1.
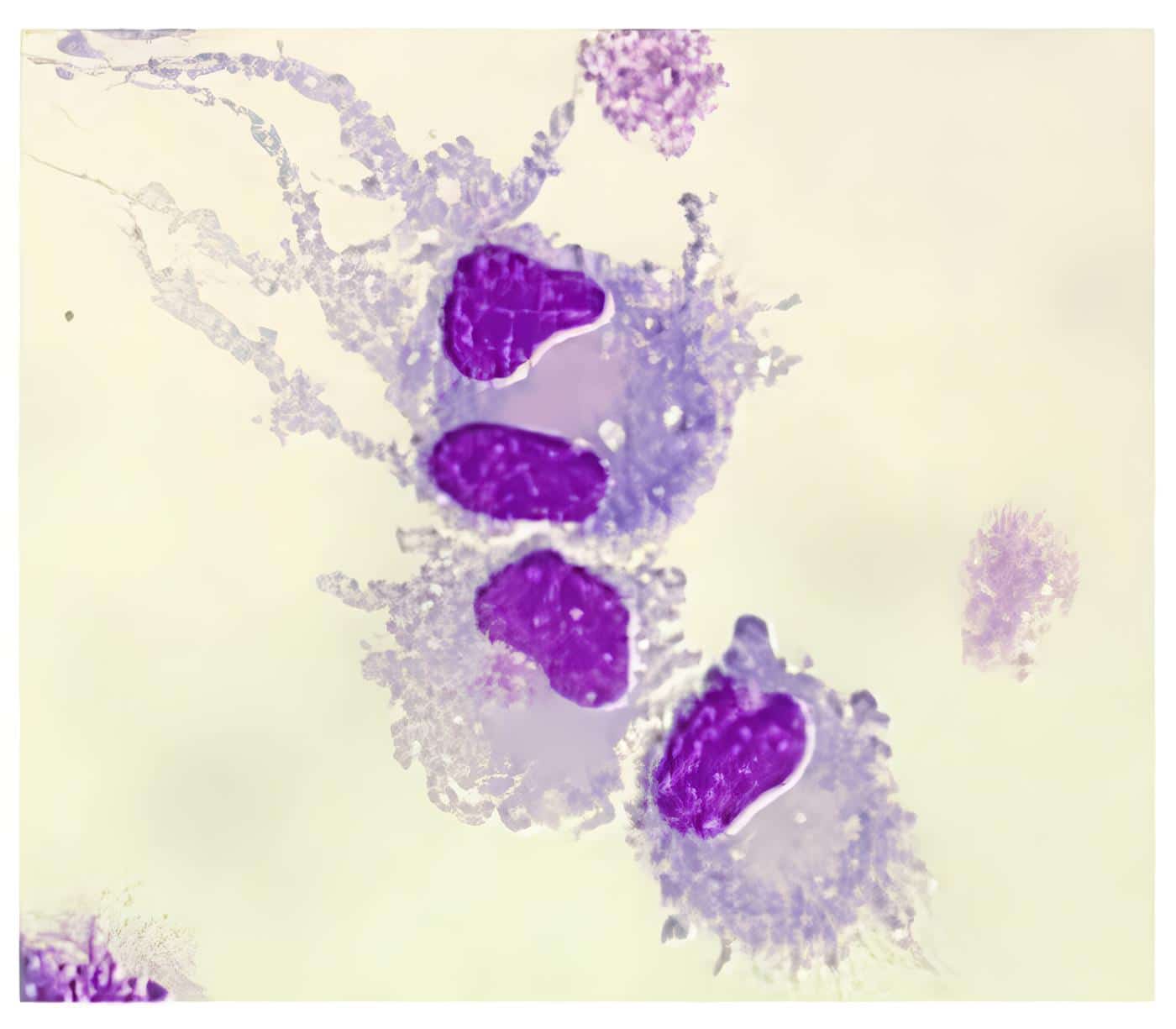
Tiene como base una falla central y periférica en la tolerancia de la β célula a moléculas específicas como ocurre en diversos procesos autoinmunes,4. En que hay sobreproducción de citoquinas,15 en el caso de la diabetes el interferon γ (IFN-γ),16. El factor de necrosis tumoral (TNF-α),17 cuya fuente son los macrófagos y las células dendríticas3, 18 localizados en el infiltrado del islote. Y la interleuquina-1β (IL-β)19 también elaborada por la célula presentadora del antígeno (APC). Además hay un desequilibrio en la respuesta inmune, entre los linfocitos Th-1/Th-2 presentes en el momento de la insulitis20, 21.
Mecanismos del Proceso Autoinmune Coestimulación Celular en la Diabetes 1
Inmuno Regulación de las Citoquinas
Tanto los ratones NOD y BB como el hombre, inmunopatológicamente, desarrollan igual tipo de diabetes 1.
La autoinmunidad se inicia22 con una gran invasión de linfocitos Th, específicamente los que llevan en sus receptores los anticuerpos o CD4 y CD8.23 Los primeros se ligan a la parte invariable de las moléculas clase II del MHC. Y del MHC24 y son citotóxicas.
Son las moléculas clase II del MHC las que dan la señal a los linfocitos25 para inducir la expresión de citoquinas proinflamatorias.
El primer grupo, Th1CD4, induce la expresión de las moléculas IL1β e IFNγ que tienen acciones pleiotrópicas sobre diversos tipos de células26 entre ellas la célula β.
El segundo grupo Th2, secretan IL-4, 5, 6 y 10. Las citoquinas producidas por el grupo Th1 facilita la inmunidad mediada por la célula que incluye la activación de los macrófagos y la citotoxicidad está mediada por el grupo Th2. Moléculas que a su vez pueden insertar perforinas27 en la membrana de la célula blanco y por los poros que originan entran las caspasas28 que inducen la apoptosis de la célula β .
Dos formas de óxido nítrico sintetasas participan en la formación del NO dentro de la βcélula. Una es la forma constitutiva (cNOS), la segunda la forma inducible (iNOS) que libera el NO29.
Las funciones del NO son de una molécula de señal, de acción citotóxica según el tipo de células en donde actúe y la cantidad de NO producido.
Las Th1 promueven la expresión y refuerzan la actividad de la forma inducible iNOS, con la correspondiente elevación del NO30
La IL-1β fue la primera citoquina19 que incubada en islotes, produjo inhibición de la secreción de insulina por el estímulo de la glucosa.
Las moléculas como el IFN-γ elaborado por los monononucleares durante la insulitis y el TNF-α elaborado por el macrófago y las células dendríticas, son citoquinas proinflamatorias que producen quimiotaxis. Activación de los leucocitos, sobre- regulación de las molécula de adhesión en las células endoteliales y maduración y migración de las células dendríticas31.
Estas citoquinas actúan sobre el macrófago residente en el islote, para producir IL-1β que luego se liga al tipo de receptor de señal 1 IL-1 que es expresado en las células β 32 y media en la señal de producción de IL-1β33.
La inducción en la producción de NO por la IL-1β, en la superficie de la célula β es simultánea con la expresión de una molécula de transmembrana 34que pertenece a la familia de de los receptores del TNF y del factor de crecimiento del nervio (NGF),35. El antígeno APO1 denominado Fas, proteína de superficie que tiene actividad de inducir la apoptosis36 de la célula β y que no la expresa la célula normal.
Este hecho se demuestra37en células β de ratón NOD, que expresan el Fas y se ligan con anticuerpos humanos que actúan como antagonistas de la proteína Fas. Su estructura sugiere que puede ser un receptor para una citoquina aún no establecida38.
El proceso de identificar cómo se liga el Fas a su anticuerpo monoclonal,39 se ha hecho en linfocitos citotóxicos (CTL) en un hibridoma generado por unión de un línea de CTL (d10S) con un linfoma de rata que pudiera matar las células Fas positivas pero no las células Fas negativas.
Lo interesante de este modelo es que se emplearon formas solubles de Fas (Fas-Fc) y del receptor TNF (TNF-Fc) creadas por fusión de las regiones extracelulares de estas moléculas con las moléculas de la fracción constante (Fc) de la IgG.
Así se llegó a demostrar36 que lo que se puede llamar Fas-Fc, pero no el TNFR-Fc, inhibió la actividad de la línea original de células d10S. Lo cual dejó en claro que estas células expresaban un “ligando” para el Fas, denominado FasL
Esta molécula humana es 77% similar a la murina en la identidad de los aminoácidos que la componen40.
Tampoco tiene señal de secuencia en el N-terminal, pero tiene un dominio de amino ácidos hidrofóbicos en el centro de la molécula40, lo cual significa que es una proteína de membrana con el C-terminal del lado extracelular de la misma.
Finalmente el FasL recombinante expresado en la superficie de celulas COS41 línea como fibroblastos derivada del riñón. Induce la apoptosis en las células que expresen el Fas indicando que el FasL es un factor de muerte y el Fas es su receptor.
Estas dos moléculas son indispensables para la homeostasis y autotolerancia de los linfocitos humanos y murinos.
Lea También: Inmuno Patogénesis de la Diabetes 1, Células Dendríticas
Terapia Génica y Prevención del Daño del Islote en la Diabetes 1
Inducción de la Tolerancia
Es un primer sistema para preservar el daño del islote en ratones NOD y BB, en los cuales la inmunopatología de la diabetes es similar a la humana.
En el NOD la expresión de los transgenes de proinsulina, controlados por el promotor del MHC moléculas clase II, expresaron en el timo la insulina y se previno la diabetes42.
Si la inducción de la tolerancia y la supresión de la inmunidad ocurre en el timo por eliminación de los timocitos43, que reconocen antígenos, antiislotes o anticélula beta, es posible plantear la transferencia en individuos de alto riesgo, la transferencia en el timo de genes que codifiquen autoantígenos.
Así se obtendrían la tolerancia a la inducción y supresión de la autoinmunidad.
Modificación en la Presentación del Antígeno
Las células APC que están presentes en la mayoría de los tejidos del organismo que están en reposo e inactivas, toman el antígeno y producen moléculas inflamatorias, quimioquinas, etc. que migran y activan los linfocitos.
Entonces son candidatos para transferir genes, sea al macrófago o a la célula dendrítica, para prevenir la activación, el procesamiento del antígeno, limitar la producción de moléculas de adhesión y promover la muerte del linfocito.
La inhibición tanto de la ligadura de la IL-1β al receptor en la célula β44, como también de la producción de NO en los islotes, pueden prevenir la destrucción celular y la insulitis, por transferencia del gen del receptor antagonista de la IL-1β, una molécula soluble de transmembrana45, la proteína antagonista del receptor de l IL-1 (IRAP), que va expresar la βcélula y actúa come señuelo para bloquear un grupo importante de citoquinas proinflamatorias, entre ellas, el TNF-α potente regulador de la actividad de la APC.
Esto se ha comprobado33 en islotes humanos cultivados en los cuales no se presentaron: El bloqueo de la producción de insulina por el estímulo con la glucosa, la apoptosis inducida por el Fas y la inducción en la producción del NO29.
Interferencia en la Coestimulación
La coestimulación entre los linfocitos Th y las moléculas clase II del MHC requiere una segunda señal46, resultante de la unión de la molécula CD28 presente en la superficie de las células T con las moléculas CD80 y CD86, denominadas B7 – 1 y B7 – 2 respectivamente, que expresan en su superficie las células dendríticas (APC).
La unión CD28 – B7, es apoptóica.
Para impedir esta coestimulación se logró fusionar una proteína de dominio extracelular derivada de los linfocitos citotóxicos47 (CTL) con otra proteína asociada al mismo CTL que se denominó A4.
Para estabilizarla se la unió a una porción (Fc) de IgG1 y se la llamó IgG1-Fc. Así se logró la molécula asociada al linfocito citotóxico, denominada CTLA4 – Ig. Que actúa como señuelo para las moléculas B7 y previene la interacción apoptóica de la molécula CD28-B7.
La administración de esta molécula recombinante CTLA4 – Ig previene el rechazo de los islotes humanos en el roedor y prolonga en el timo la supervivencia de xenoinjertos microencapsulados porcinos y de conejo48.
Citoquinas Inmunoreguladoras
Las interleuquinas son potentes mediadores del sistema inmune al nivel de la presentación del antígeno por la APC.
La IL-4 y la IL-10 son citoquinas inmnosupresoras así como también las que se clonan a través del virus Epstein-Barr. Lo que ha llevado a usar formas recombinantes de estas citoquinas para prevenir la diabetes 1 en el ratón NOD. Así como también para prolongar la supervivencia y prevenir la insulitis de los injertos49.
La IL-10 previene la producción de IFN γ por las células Th1 y previene la producción de IL-12 por la APC.50. Estas y nuevas investigaciones sugieren que la aplicación de la ingeniería genética con células T islotes reactivas. Que expresen citoquinas inmunosupresoras, puede ser un método de prevención para el desarrollo de la insulitis.
Sin embargo para su factibilidad en el hombre, todo depende de la identificación del auto- antígeno específico y de los receptores que expresen específicamente las células T comprometidas en la insulitis.