Isabel Cristina Ávila, Julio César Bueno,
Hernán Darío Vergara, Ángela P. Cadavid
Programa Reproducción, Facultad de Medicina,
Universidad de Antioquia.
Este es un artículo de revisión donde se hace énfasis en el papel del metabolismo del triptófano en la regulación del sistema inmune principalmente por inhibición de la proliferación de los linfocitos T, tanto en la respuesta inmune sistémica como en la de la interfase maternofetal.
El triptófano es metabolizado por dos vías: la vía de la serotonina y la vía de la quinurenina, participando en esta última las enzimas triptófano 2-3 dioxigenasa (TDO) y la indolamina 2-3 dioxigenasa (IDO). El interferón gama estimula la producción de IDO por una subpoblación de macrófagos diferenciados por el factor estimulante de colonias 1 y por las células dendríticas. Otros activadores del sistema inmune como las interleuquinas 1 y 2, el lipopolisacárido bacteriano y el virus de la inmunodeficiencia humana, pueden aumentar los niveles de IDO.
En el caso particular de la gestación, se ha planteado que la IDO expresada por el sincitiotrofoblasto disminuye el triptófano disponible para la proliferación de los linfocitos T en la interfase materno fetal que serían los mediadores del rechazo del aloinjerto fetal.
La inhibición de la IDO con el 1-metil-triptófano, competidor específico de la enzima, disminuye la reabsorción embrionaria. En nuestro grupo estamos planteando que los macrófagos deciduales expresan IDO en respuesta al IFN-g producido por las células NK, y que ésta al metabolizar el triptófano, modula la activación de las células NK
Palabras claves: triptófano, tolerancia, indolamina 2-3 dioxigenasa, maternofetal
El L-triptófano es uno de los diez aminoácidos esenciales conocidos y fue en 1901 por Hopkin y Col (1). Es un aminoácido aromático, apolar y presenta un anillo indólico en su cadena lateral con capacidad de establecer enlaces débiles con estructuras semejantes, por lo cual se clasifica como un aminoácido hidrofóbico (2). Es necesario para la biosíntesis de proteínas estructurales y funcionales y es el principal precursor del neurotransmisor serotonina, de la hormona melatonina secretada por la glándula pineal y de la vitamina niacina (3).
Los requerimientos diarios mínimos de triptófano en los adultos están en el rango de 175-250 mg/día. La dieta típica occidental suministra 600-1200 mg de triptófano en las proteínas, cantidad suficiente para satisfacer tales requerimientos.
Una deficiencia de triptófano en la dieta conlleva a un balance negativo de nitrógeno en el organismo, además de una reducción en los niveles de los metabolitos finales de la degradación del triptófano como son la serotonina, el ácido picolínico y la niacina (4). La deficiencia de niacina trae como consecuencia
la enfermedad conocida como pelagra cuyos síntomas y manifestaciones clásicas son diarrea, dermatitis y demencia; sin un tratamiento adecuado y oportuno la
pelagra puede ocasionar la muerte (2).
Rutas metabólicas del triptófano
En los mamíferos, el triptófano es catabolizado por dos vías: la vía de la serotonina y la vía de la quinurenina. La primera vía implica la oxidación del triptófano a 5-hidroxitriptófano por la enzima triptófano-hidroxilasa, seguida por una descarboxilación a 5-hidroxitriptamina (serotonina).
Posteriormente, la enzima hidroxi-indol-0-metil-transferasa acetila la serotonina para formar la melatonina (Figura 1) (1).
La serotonina es un potente neurotransmisor producido por neuronas cuyos cuerpos celulares se encuentran principalmente en el hipotálamo y en el bulbo cerebral y, al parecer, participa en las rutas que se relacionan con el sueño, la depresión, el humor y la percepción sensorial. Aproximadamente el 3% del triptófano de la dieta es metabolizado por esta vía (3).
La otra vía metabólica es la de la quinurenina, la cual comienza con una oxidación del triptófano a N-formilquinurenina y rápidamente es hidrolizada a quinurenina, siendo ésta el producto inicial que conduce a varias vías de degradación y cuyos productos finales son el ácido quinureico, el ácido picolínico y los metabolitos de niacina (Figura 1) (5).
Triptófano THP Serotonina Melatonina xiantranilico Ácido picolínico xiantranilico Ácido picolínico |
Figura 1. Rutas metabólicas del triptófano: (1) ruta de la serotonina en la cual actúa la enzima TPH; (2) ruta de la quinurenina, donde pueden actuar las enzimas IDO o TDO dependiendo del tejido.
La oxidación del triptófano a N-formilquinurenina es catabolizada por la enzima triptófano 2,3-dioxigenasa (TDO), también conocida como triptófano pirrolasa o triptófano oxigenasa.
Esta enzima se localiza principalmente en el tejido hepático y ha sido muy estudiada en los mamíferos. La administración de grandes cantidades de triptófano provoca un incremento, hasta de 10 veces, en los niveles de TDO.
Un efecto similar es provocado por los niveles elevados de los glucocorticoides adrenales: cortisona, dihidrocortisona y análogos sintéticos, que actúan induciendo la síntesis de la enzima (3).
Una segunda enzima, la indolamina 2,3-dioxigenasa (IDO), cataboliza también el triptófano por la vía de la quinurenina.
La IDO ha sido encontrada en los tejidos extrahepáticos tales como el intestino, el pulmón, la placenta y el cerebro; y en las células del sistema inmune como los macrófagos y las células dendríticas (6).
Esta enzima, a diferencia de la TDO, presenta una actividad enzimática muy baja, pero sus niveles pueden aumentar hasta 1000 veces cuando es inducida por factores que activan el sistema inmune como: las interleuquinas 1 y 2, los interferones gama y beta, el lipopolisacárido bacteriano (LPS) y algunos virus como el virus de la inmunodeficiencia humana (7).
La IDO además posee un Km muy bajo (20 mM), por lo que la afinidad de la enzima por el triptófano es mayor, comparada con la TDO (4, 8, 9).
Los productos de la degradación del triptófano participan en la activación y en la supresión del sistema inmune.
El ácido picolínico, por ejemplo, actúa como un coestimulador del interferón gama (INFg) en la activación de los macrófagos (10), mientras que la serotonina inhibe la expresión de las moléculas del Complejo Mayor de Histocompatibilidad clase II murinas inducida por esta citoquina (11).
El INFg es un potente inmunomodulador con efectos antiproliferativos y antineoplásicos:
Capaz de inducir la expresión de la IDO en diferentes célula como macrófagos, células dendríticas, líneas de células tumorales, fibroblastos de piel y de tejido conectivo sinovial (1). Los efectos antiproliferativos del INFg se han observado en líneas celulares de tumores debido a la disminución de triptófano en el medio de cultivo (4).
Recientemente se demostró que la expresión de la IDO en las células dendríticas humanas inducida por el INFg, el LPS o a través del ligando CD40, es capaz de metabolizar grandes cantidades de triptófano e inhibir la proliferación de linfocitos T.
En cocultivos de células dendríticas con linfocitos T, el INFg fue el más potente inductor en la síntesis de la IDO (12). Otro estudio se demostró que el factor de necrosis tumoral alfa participa en la inducción de la IDO en respuesta al estímulo con LPS (7).
En pacientes con cáncer, tratados con interferones tipo I y II se observó una disminución en los niveles séricos de triptófano (20-50% de los observados antes del tratamiento), acompañado de un incremento de hasta 500 veces en los metabolitos urinarios producidos en la vía de la quinurenina. También se ha reportado esta relación inversa entre los niveles del INFg y los del triptófano en pacientes con escleroderma, lupus eritematoso sistémico, artritis reumatoidea y en algunos pacientes con SIDA (4, 13).
Algunas de las manifestaciones clínicas en el SIDA como:
La demencia, la caquexia, los problemas dermatológicos e inclusive la inmunosupresión pueden ser el resultado de una deficiencia crónica de triptófano, debida probablemente al aumento de la actividad de la IDO por la infección del virus de inmunodeficiencia humana (VIH) (2).
En trabajos realizados con macrófagos infectados por diferentes cepas de VIH neurotrópico, se demostró que algunos de los macrófagos eran capaces de expresar IDO y por tanto de metabolizar el triptófano; además observaron que sólo algunas cepas de VIH fueron capaces de estimular la de esta enzima.
Adicionalmente, la demencia que acompaña al SIDA podría ser explicada por los bajos niveles de serotonina o por los niveles elevados de ácido quinolínico que es conocido como una potente neurotoxina y se encuentra aumentado en estos pacientes (14).
Por todo lo anterior se ha propuesto que la actividad de la IDO, y en general el metabolismo del triptófano, juegan un papel importante en la regulación en la respuesta inmune, pero no queda claro si esta actividad es benéfica o perjudicial para el organismo por los efectos de los metabolitos (7).
El proceso por el cual el sistema inmune inhibe las respuestas específicas de los linfocitos T y B frente a los antígenos propios se ha denominado tolerancia.
Las clonas de células T que no son eliminadas en el timo son reguladas posteriormente en la periferia de dos maneras: una por apoptosis, la cual se define como la muerte celular que ocurre normalmente en la homeostasis tisular; y la otra por anergia, fenómeno que consiste en la pérdida de la capacidad de respuesta de los linfocitos T a los antígenos (15).
La forma como se da la tolerancia periférica aún no es clara, sin embargo, se ha demostrado que algunas subpoblaciones de macrófagos y de células dendríticas pueden inducir anergia en los linfocitos T. Munn y colaboradores observaron que los linfocitos T preactivados, cocultivados con macrófagos diferenciados por el factor estimulante de colonias 1 (CSF-1), entraban en un estado de anergia e incluso, después de un período de tiempo, podían llegar a sufrir apoptosis, por lo que propusieron que los macrófagos participaban en la tolerancia periférica y que este fenómeno se explicaba por la expresión inducida de la IDO (16).
Para demostrarlo, cocultivaron macrófagos diferenciados por el CSF-1 con linfocitos T previamente activados y se determinó la actividad enzimática de la IDO, cuantificando la quinurenina como producto estable de esa vía metabólica.
En estos ensayos la depleción del triptófano en el medio de cultivo se correlacionó con la disminución en la proliferación de los linfocitos T; estos efectos se revirtieron al utilizar 1-metil triptófano, inhibidor competitivo específico de la enzima IDO (Figura 2) (6).
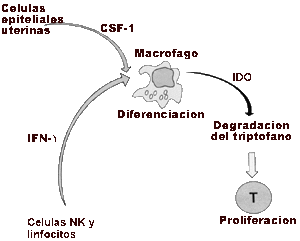
Figura 2. Proceso por el cual el macrófago puede inhibir la proliferación de los linfocitos T.
Las primeras aproximaciones sobre la tolerancia en la interfase maternofetal estuvieron enmarcadas en el desarrollo de la inmunología de los trasplantes durante la década de los 50. Peter Medawar, pionero en este campo de la investigación, propuso por primera vez al feto como el único aloinjerto natural exitoso, tolerado por el sistema inmune de la madre, pese a la expresión de antígenos de origen paterno.
Se conocía desde ese entonces que en la gestación humana ocurría la invasión de los tejidos placentarios de origen fetal (trofoblasto) al endometrio que ha sufrido una reacción inflamatoria mediada por la progesterona (decidua), y en la cual los antígenos fetales están expuestos a la circulación materna.
Los mecanismos que inducen la tolerancia de las células del sistema inmune de la madre a los antígenos del feto no han sido totalmente dilucidados. Con los linfocitos T, en particular, se demostró que en el embarazo alogénico murino, éstos eran capaces de reconocer aloantígenos paternos, pero su número era reducido si se comparaba con el embarazo singénico.
Este fenómeno se revertía luego del parto y la cantidad de linfocitos T reactivos par aloantígenos paternos era semejante a la encontrada antes del embarazo (17).
Papel del metabolismo del triptófano
A la luz de los hallazgos que proponen un papel del metabolismo del triptófano en la tolerancia inmune, Se ha postulado éste como un mecanismo que podría explicar la anergia de los linfocitos T en la decidua.
Munn y cols, encontraron transcriptos de la enzima IDO alrededor del día 7.5 a 9.5 postcoito en todo el conceptus murino; en la gestación más tardía (10.5 a 13.5), los transcriptos se detectaron en la placenta pero no en el útero materno o en los tejidos embrionarios; al inyectar 1 metil-triptófano a las ratonas gestantes aumentaron las reabsorciones embrionarias por activación y proliferación de linfocitos T (18).
Suzuki y cols, observaron la expresión de la proteína IDO a partir del día 9.5 hasta el día 12.5, pero no la encontraron en la gestación más temprana. El hallazgo más importante en este estudio fue la actividad aumentada de la degradación del triptófano desde el día 5.5 a 10-5 que no era inhibida por el 1 metil-triptófano y que fue demostrado se debía a la expresión de la TDO.
Con esto se plantea que además de la IDO, la enzima TDO, puede estar contribuyendo a la tolerancia en la intertase maternofetal (19).
El modelo propuesto por Munn y colaboradores para explicar la tolerancia materna mediada por la expresión de la enzima IDO, se basa en que el rechazo del aloinjerto fetal es dependiente de la activación de linfocitos T y que éste se acompaña de depósitos extensos de complemento en la interfase maternofetal que finalmente conducen a inflamación, necrosis hemorrágica e infiltración celular.
Para la demostración experimental utilizaron la inhibición farmacológica de la IDO, in vivo, con el 1 metil-triptófano, y observaron que mientras en los embarazos alogénicos había reabsorción embrionaria, los embarazos singénicos no se afectaban con este tratamiento (20).
Otra tendencia en la investigación de la tolerancia materna al feto:
Propone que son las células asesinas naturales (NK), y no los linfocitos T, las que estarían determinado el no rechazo del feto. La población de células del sistema inmune más abundante en la decidua es la de células NK (70%), por lo cual se ha tratado de establecer cuál es la función que éstas están ejerciendo en la implantación y el desarrollo embrionario.
Las células NK uterinas tienen toda la maquinaria citolítica pero su actividad citotóxica es más baja que la de las células NK en sangre periférica, por lo que es válido considerar que estén siendo moduladas por otras células en la interfase maternofetal (21, 22).
Los macrófagos se encuentran también en decidua y constituyen el 15-20% de la población celular.
La expresión de la IDO aún no ha sido determinada en los macrófagos deciduales, sin embargo, la evidencia indirecta demuestra que éstos se diferencian en la interfase materno fetal bajo el influjo de los estrógenos y la progesterona y son estimulados por el CSF-1; se observa así mismo una relación directa entre la producción del CSF-1 y la densidad de los macrófagos en la decidua a partir del día 8 postcoito (23, 24).
El inductor más conocido de la IDO, el IFN-g, se secreta en la decidua murina por las células NK y otros tipos celulares, y sus niveles se elevan también a partir del día 8 (25); ya que se ha demostrado un incremento de hasta 1000 veces en la concentración de CSF-1 en el útero de ratones gestantes, podría existir una expresión de la IDO, inducida por el IFN-g, en estos macrófagos.
En nuestro grupo estamos desarrollando un proyecto de investigación para tratar de esclarecer si la inhibición de la capacidad citotóxica de las células NK, observada naturalmente en la interfase materno fetal, es debida al catabolismo del triptófano, y particularmente, a la expresión de IDO en los macrófagos.
Abstract
This is a review where the role of tryptophan metabolism in the regulation of the immune system is discussed. This regulation is mediated by inhibition of T cells in systemic immunity and at the maternofetal interface.
The catabolism of tryptophan flows by serotonine and kinurenine pathways. In the latter, two enzymes participate: tryptophan 2-3 dyoxigenase (TDO) and indolamine 2-3 indolamine (IDO). Gamma-interferon stimulates the IDO production by CSF-1 stimulated-macrophages and dendritic cells.
Other immune activators such as interleukins 1 and 2, lipopolysaccharides and human immunodeficiency virus can increase the IDO levels.
In gestation, it has been proposed that the IDO enzyme expressed by syncitiotrophoblast decreased the available tryptophan for T cell proliferation which would be responsible of the fetal allograft rejection. Pharmacological inhibition of IDO with 1-methyl-tryptophan decreased embryo resorption. In our group, we are proposing that decidual macrophages express IDO in response to IFNg produced by NK cells and this results in tryptophan decline to modulate NK cell activation.
Key words: Tryptophan, tolerance, indolamine 2-3 dioxigenase, maternofetal
Referencias bibliográficas
- 1. Brown RR. Tryptophan metabolism: A review. En: Kochen W, Steinhart H. L-Tryptophan Current Prospects in Medicine and Drug Safety. New York: Warter de Gruyter, 1994; 17-30.
- 2. Brown RR, Ozaki Y, Datta SP, Borden EC, Sondel PM, Malone DG. Implications of interferon-induced tryptophan catabolism in cancer, auto-immune disease and AIDS. Adv Exp Med Biol 1991; 294: 425 – 435.
- 3. RodweII Víctor W. Catabolismo de los esqueletos de carbono de aminoácidos. En: RodweII V, Martín D, Mayes P. Bioquímica de Harper. México D.F: El Manual Moderno, S.A. de C.V, 1992; 286-309.
- 4. Brown RR, Fissette PL, Ared RA, Ozaki Y. Tryptophan metabolism and immune markers in eosinophilia-myalgia syndrome associated with tryptophan ingestión. Advances in Tryptophan Research 1992; 337-346.
- 5. Widner B, Ledochowski M, Fuchs D. Interferon g-induced tryptophan degradation: Neuropsychiatric and immunological consequence. Curr Drug Metab 2000; 1:193-204.
- 6. Munn D, Shafizdeh E, Affwood J, Bondarey I, Pashine A, Mellor A. Inhibition of T cell proliferation by macrophages tryptophan catabolism. J Exp Med 1999; 189:1363-1372.
- 7. Fujigaki S, Saito K, Sekikawa K, et al. Lipopolysaccharide induction of indoleamine 2,3 dioxigenase is mediated dominantly by an IFN-g independent mechanism. Eur J Immunol 2000; 31:2313-2318.
- 8. Brown RR, Lee CM, Kohler PC, Hank JA, Storer BE, Sondel PM. Altered tryptophan and neopterin metabolism in cancer patients treated with recombinant interleukin – 2. Cancer Res 1989; 49:4941 – 4944.
- 9. Musso T, Gusella GL, Brooks A, Longo DL, Varesio L. Interleukin—4 inhibits indoleamine 2,3-dioxigenase expression in human monocytes. Blood 1994; 83, 5:1408 – 1411.
Fuentes bibliográficas
- 10. Varesio L, Clayton M, Blasi E, Ruffman R, Radzioch D. Picolonic acid, a catabolite of tryptophan, an the second signal in the activation of IFN-g- primed macrophages. J Immunol 1990; 145:4265-4271.
- 11. Sternberg EM, Trial J, Parker CW. Effect of serotonin on murine macrophages: suppression of I-A expression by serotonin and its reversal by 5-HT2 serotonergic receptor antagonists. J Immunol 1986; 137:276- 282.
- 12. Hwu P, Du M, Lapointe R, Do M, Taylor MW, Young H. Indoleamine 2,3- dioxygenase production by human dendritic cells results in the inhibition of T cell proliferation. J Immunol 2000; 164:3596 – 3599.
- 13. Banchereau J, Stenman RM. Dendritic cells and the control of immunity. Nature 1998; 392:245-252.
- 14. Grant R, Nait H, thuruthyil S. Induction of indoleamine 2-3 dioxigenase in primary human macrophages by human immunodeficiency virus type 1 is strain dependent. J Virol 2000; 4110- 4115.
- 15. Schwartz R. Modeis of T cell anergy: is there a common molecular
- mechanism?. J Exp Med 1996; 184:1 -8.
- 16. Munn DH, Pressey J, Beall AC, Mudes R, Alderson MR. Selective activation-induced apoptosis of peripheral T cells imposed by macrophages: a potential mechanism of antigen-specific peripheral lymphocyte deletion. J Immunol 1996; 156:523-532.
- 17. Tafuri A, Alferink J, Moller P, Hammerling GJ, Arnold B. T cell awareness of paternal alloantigens during pregnancy. Science 1995; 270:630-632.
- 18. Munn DH, Zhou M, Attwood JT, Bondarev I, Conway SJ, Marshall B, Brown C, Mellor A. Prevention of allogenic fetal rejection by tryptophan catabolism. Science 1998; 281:1191 – 1193,
- 19. Suzuki S, Tone S, Takikawa O, Kubos T, Kohno I, Minatogawa Y. Expression of indoleamine 2,3-dioxygenase and tryptophan 2,3- dioxygenase in early concepti. Biochem J 2001; 355 :425-429.
Lecturas Recomendadas
- 20. Mellor AL, Munn DH. Tryptophan catabolism prevents maternal T cells from activating letal anti-fetal immune responsos. J Reprod Immunol 2001:52:5-13.
- 21. King A, Burrows T, Loke YW. Human uterine natural killer cells. Nat Immunol 1996; 15:41-52.
- 22. Higuchi K, Aoki K, Kimbara T, Hosoi N, Yamamoto T, Okada H. Suppression on natural killer cell activity by monocytes following immunotherapy for recurrent spontaneous aborters. Am J Reprod Immunol 1995:33:221-227.
- 23. Kyaw Y, Hasegawa G, Takatsuka H, et al. Expression of macrophage colony-stimulating factor, scavenger receptor, and macrophage proliferation in the mouse uterus. Arch Histol Cytol 1998; 61, 5:383 – 393.
- 24. De Mamata, Wood GW. Analysis of the number and distribution of macrophages, lymphocytes and granulocytes in the mouse uterus from implantation through parturition. J Leukoc Biol 1991; 50:381-392.
- 25. Croy A, Ashkar A. Interferon y contributes to the normalcy of murine pregnancy. Biol Reprod 1999; 61:493-502.





Gracias por sus artículos, intentaré aprovecharlos al máximo