Zuluaga M. 2,Trujillo C.M. 1,2, Vélez I.D. 2, Patiño P.J. 1, Robledo S.M. 2
1 Grupo de Inmunodeficiencias Primarias. 2 Programa de Estudio y Control de Enfermedades Tropicales-PECET.
Universidad de Antioquia, Medellín, Colombia Correo electrónico: milenazul@latinmail.com
Introducción
El papel de las moléculas coestimuladoras en la diferenciación de las células Th1/ Th2 y en la regulación de la respuesta inmune específica durante la infección por Leishmania en humanos permanece por definirse.
Objetivo
Caracterizar la expresión de moléculas coestimuladoras expresadas tanto en el linfocito T como en la célula presentadora de antígeno. Durante la exposición a Leishmania (Viannia) panamensis en humanos.
Materiales y métodos
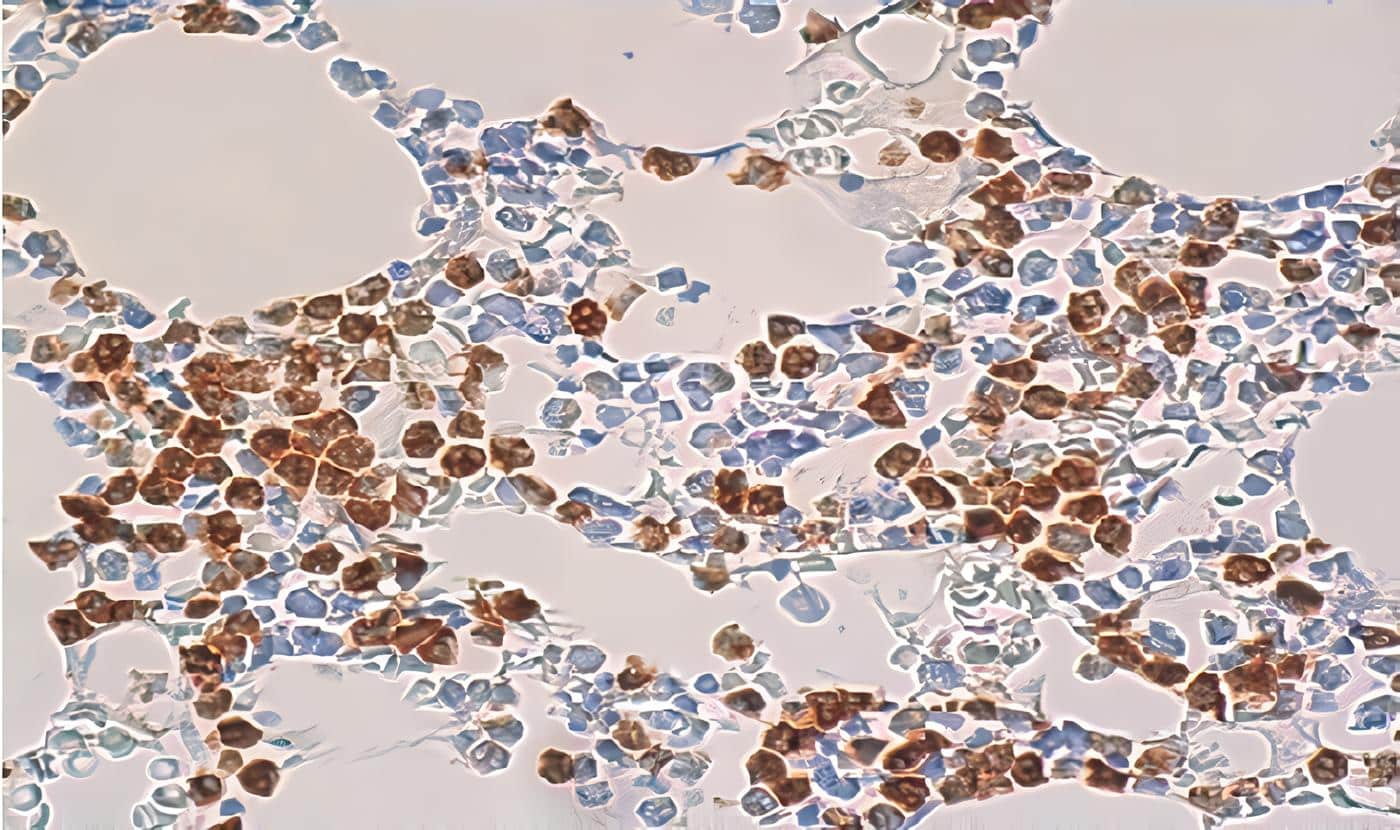
Células mononucleares de sangre periférica de individuos susceptibles, resistentes y controles sanos se estimularon in vitro con promastigotes de L (V) panamensis durante 24, 48 ó 72 horas. La expresión de las moléculas se evaluó por citometría de flujo.
Resultados
Se encontraron diferencias en la expresión de CD80 con respecto a la exposición al parásito y al grupo de individuos; CD86 mostró un aumento en su expresión luego de 48 horas en los individuos controles, aunque su expresión fue mayor en las células activadas de individuos susceptibles.
La expresión de CD152 aumentó luego de 72 horas, con diferencias entre los grupos de individuos. CD40 mostró diferencias en la expresión entre los individuos resistentes y los controles sanos luego de 48 horas y entre las células activadas de los individuos susceptibles y los resistentes.
La expresión basal de CD154 fue mayor en los controles sanos y disminuyó luego de 48 horas. A su vez, CD28 no mostró variaciones en su expresión con respecto al tiempo ni al grupo de individuos.
Conclusión
Las diferencias de expresión de estas moléculas entre los individuos que habían estado en contacto previo con el parásito y aquellos que no. Sugieren que existe una modulación en las moléculas presentes en la célula hospedera con el fin de controlar la infección.
Esta característica podría constituir un mecanismo inmunoterapéutico para inducir una respuesta de células T asociada con resistencia a la enfermedad.
Inmunogenicidad de Péptidos Derivados de la Proteína cs de Plasmodium Vivax en Ratones Transgénicos HLA-A*0201/Kb
Arévalo-Herrera M.1,2, Bonelo A.2, Valencia AZ.2, Herrera S.2
1 Escuela de Bacteriología y Laboratorio Clínico, Universidad del Valle. 2 Instituto de Inmunología, Universidad del Valle.
Una de las proteínas más estudiadas como candidato a vacuna contra la malaria ha sido la proteína circumesporozoito (CS) que se localiza en la superficie de los esporozoitos. Se ha sugerido que la protección a nivel de la fase hepática está mediada principalmente por la activación de linfocitos CD8+ que producen IFN-g. Y dispara la producción de óxido nítrico por parte de la célula hepática causando la muerte del parásito.
Para que un epítope sea reconocido por las células CD8+ deben presentarse en el contexto de las moléculas de clase I del Complejo Mayor de Histocompatibilidad.
El objetivo de este trabajo es evaluar la influencia del tamaño de los epitopes (9aa ó 10aa) derivados de la proteína CS de P. vivax en la unión a la molécula HLA-A*0201y el reconocimiento por parte de los linfocitos CD8+.
Se sintetizaron 3 péptidos de 9 residuos (Pv3n, Pv6n y Pv7n) y 3 de 10 residuos de longitud (Pv3d, Pv6d y Pv7d) que se evaluaron en su capacidad de unión in vitro a la molécula HLA-A*0201 y la estabilidad de los complejos péptido/HLA. Ratones transgénicos HLA-A*0201/Kb fueron inmunizados con los péptidos Pv3n y Pv3d. Los resultados demostraron que la afinidad en la unión a la molécula HLA-A*0201 y la estabilidad es mejor con los epitopes de 9 residuos que con los decapéptidos.
Los ratones inmunizados con el Pv3n presentaron una lisis del 20 y 30% y producción de IFN-g en linfocitos provenientes de ganglios linfáticos y bazo respectivamente comparados con los valores negativos con el decapéptido.
En conclusión se demostró que el tamaño de los epítopes influencia la unión, la estabilidad y el reconocimiento por parte de los linfocitos CD8+.
Estos resultados son de gran importancia para el diseño de vacunas porque se confirma la presencia de epítopes CD8+ productores de IFN-g y con capacidad citolítica.